文档内容
第 12 讲 氮及其化合物
1.氨气溶于水得到氨水,氯气溶于水得到氯水,下列关于新制的氨水、氯水的描述正确的是( )
A.“两水”都是混合物,溶液中含有的粒子种类、数目相同
B.“两水”都有刺激性气味,都能漂白有机色素
C.“两水”中都存在可逆反应的化学平衡和弱电解质的电离平衡
D.“两水”放置时间较久后都会因为相同的原理而变质
2.清代《本草纲目拾遗》中关于“鼻冲水(氨水)”的记载明确指出:“鼻冲水,……贮以玻璃瓶,紧
塞其口,勿使泄气,则药方不减……唯以此水瓶口对鼻吸其气,即遍身麻颤出汗而愈,虚弱者忌之。宜外
用,勿服。”下列有关“鼻冲水”的推断不正确的是( )
A.鼻冲水是弱电解质
B.鼻冲水滴入酚酞溶液中,溶液变红色
C.鼻冲水中含有分子和离子的种类为6种
D.存在平衡:NH +HONH·H ONH+OH-
3 2 3 2
3.汽车排放的尾气中含有NO ,NO 是城市大气污染的主要污染物之一,在日光照射下,NO 发生一
2 2 2
系列光化学烟雾的循环反应,从而不断产生O,加重空气污染。反应过程为①2NO ―→2NO+2O,
3 2
②2NO+O―→2NO ,③O+O―→O。下列对该反应过程及生成物叙述正确的是( )
2 2 2 3
A.NO 起催化剂作用 B.NO只起催化剂作用
2
C.NO 只起氧化剂作用 D.O 与O 为同分异构体
2 3 2
4.将相同质量的铜分别与足量的浓硝酸、稀硝酸反应,下列叙述正确的是( )
A.硝酸浓度越大消耗的硝酸越少,产生的有毒气体也越少
B.反应中转移的电子总数稀硝酸少
C.试管内壁上的铜用浓硝酸除去最好,因反应速率快
D.两者用排水法收集的气体的体积相同
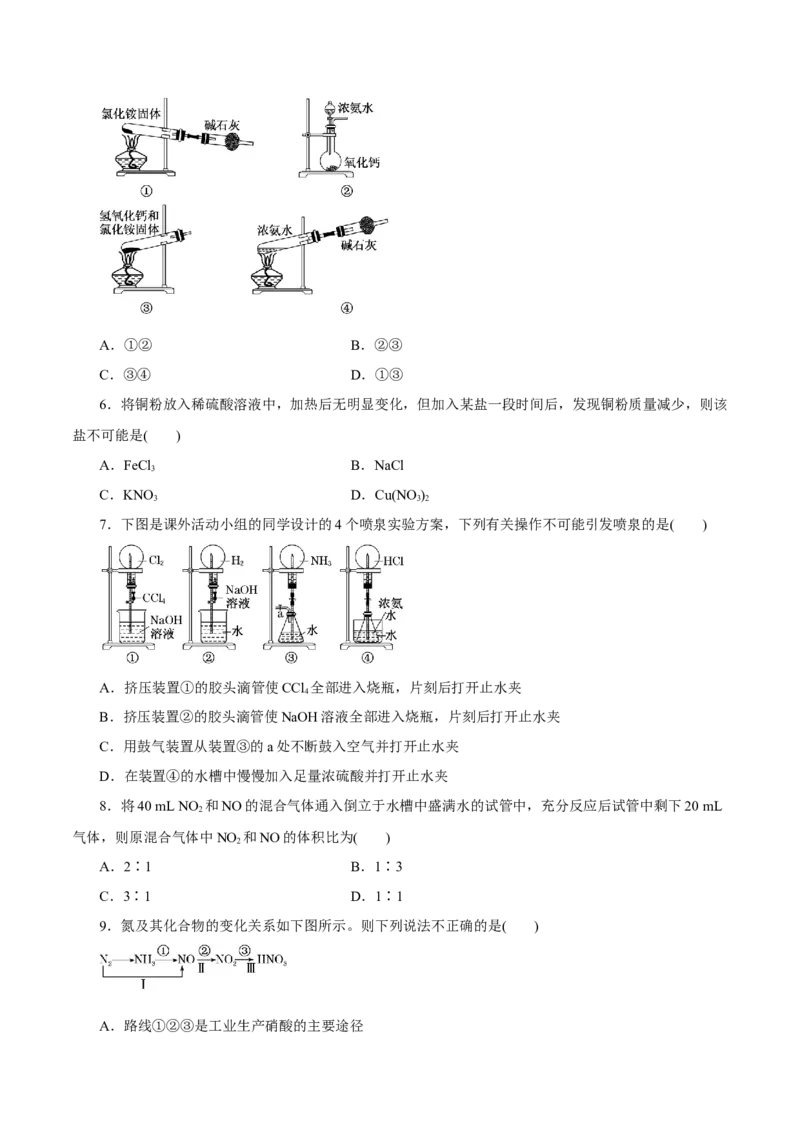
5.下面是实验室制取氨气的装置和选用的试剂,其中错误的是( )A.①② B.②③
C.③④ D.①③
6.将铜粉放入稀硫酸溶液中,加热后无明显变化,但加入某盐一段时间后,发现铜粉质量减少,则该
盐不可能是( )
A.FeCl B.NaCl
3
C.KNO D.Cu(NO )
3 3 2
7.下图是课外活动小组的同学设计的4个喷泉实验方案,下列有关操作不可能引发喷泉的是( )
A.挤压装置①的胶头滴管使CCl 全部进入烧瓶,片刻后打开止水夹
4
B.挤压装置②的胶头滴管使NaOH溶液全部进入烧瓶,片刻后打开止水夹
C.用鼓气装置从装置③的a处不断鼓入空气并打开止水夹
D.在装置④的水槽中慢慢加入足量浓硫酸并打开止水夹
8.将40 mL NO 和NO的混合气体通入倒立于水槽中盛满水的试管中,充分反应后试管中剩下20 mL
2
气体,则原混合气体中NO 和NO的体积比为( )
2
A.2∶1 B.1∶3
C.3∶1 D.1∶1
9.氮及其化合物的变化关系如下图所示。则下列说法不正确的是( )
A.路线①②③是工业生产硝酸的主要途径B.路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径
C.上述所有反应都是氧化还原反应
D.氮气可在足量的氧气中通过一步反应生成NO
2
10.利用如图所示的装置,可以验证NH 和HCl的有关性质。实验前a、b、c活塞均关闭。
3
(1)若要在烧瓶Ⅱ中产生“喷泉”现象,烧瓶Ⅰ中不产生“喷泉”现象,其操作方法是
____________________________________________________________________________。
(2)若先打开a、c活塞,再挤压胶头滴管,在烧瓶中可观察到的现象是
____________________________________________________________________________。
(3)通过挤压胶头滴管和控制活塞的开关,在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现
象,其操作方法是_____________________________________________;若要在该装置中产生双喷泉现象,
其操作方法是__________________________________。
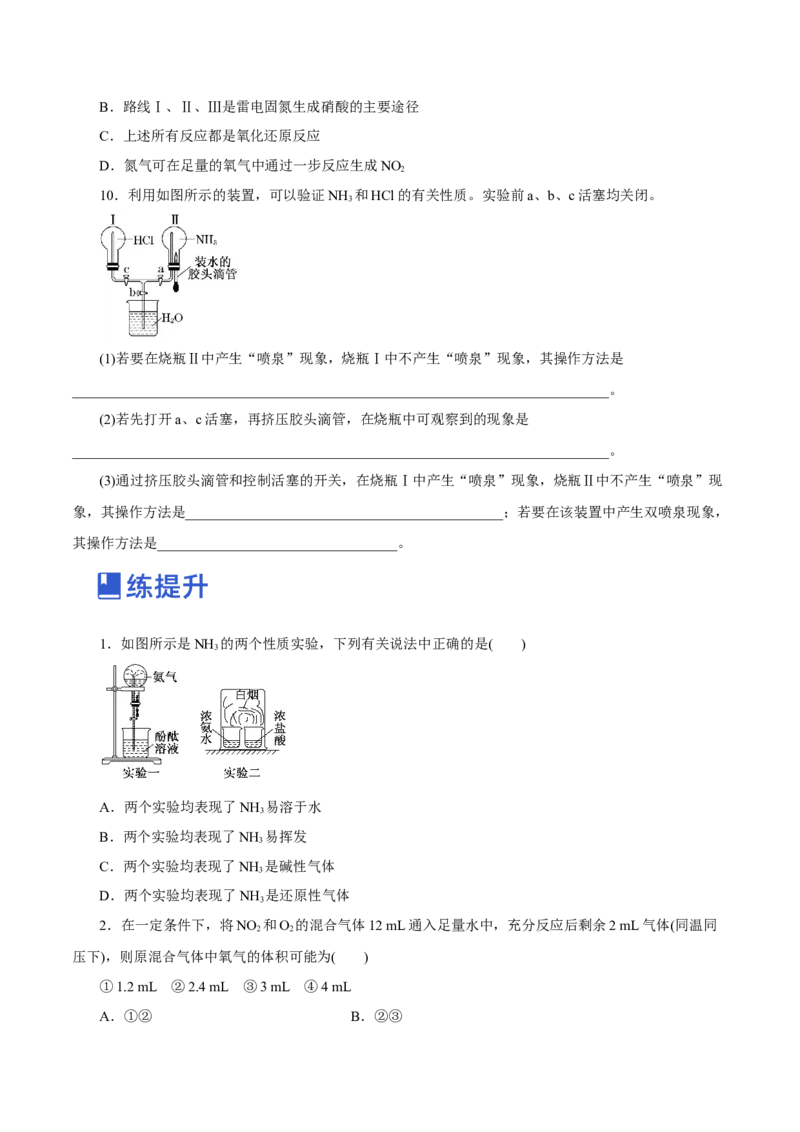
1.如图所示是NH 的两个性质实验,下列有关说法中正确的是( )
3
A.两个实验均表现了NH 易溶于水
3
B.两个实验均表现了NH 易挥发
3
C.两个实验均表现了NH 是碱性气体
3
D.两个实验均表现了NH 是还原性气体
3
2.在一定条件下,将NO 和O 的混合气体12 mL通入足量水中,充分反应后剩余2 mL气体(同温同
2 2
压下),则原混合气体中氧气的体积可能为( )
①1.2 mL ②2.4 mL ③3 mL ④4 mL
A.①② B.②③C.③④ D.①④
3.在标准状况下将1.92 g铜粉投入一定量浓HNO 中,随着铜粉的溶解,反应生成的气体颜色逐渐变
3
浅,当铜粉完全溶解后共收集到由NO 和NO组成的混合气体1.12 L,则混合气体中NO的体积为( )
2
A.112 mL B.1 008 mL
C.224 mL D.448 mL
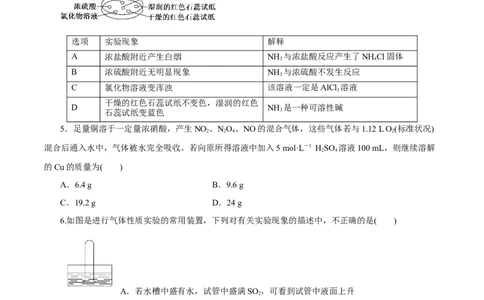
4.如图,利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在
上面。下表中对实验现象所做的解释正确的是( )
选项 实验现象 解释
A 浓盐酸附近产生白烟 NH 与浓盐酸反应产生了NH Cl固体
3 4
B 浓硫酸附近无明显现象 NH 与浓硫酸不发生反应
3
C 氯化物溶液变浑浊 该溶液一定是AlCl 溶液
3
干燥的红色石蕊试纸不变色,湿润的红色
D NH 是一种可溶性碱
石蕊试纸变蓝色 3
5.足量铜溶于一定量浓硝酸,产生NO 、NO、NO的混合气体,这些气体若与1.12 L O (标准状况)
2 2 4 2
混合后通入水中,气体被水完全吸收。若向原所得溶液中加入5 mol·L-1 HSO 溶液100 mL,则继续溶解
2 4
的Cu的质量为( )
A.6.4 g B.9.6 g
C.19.2 g D.24 g
6.如图是进行气体性质实验的常用装置,下列对有关实验现象的描述中,不正确的是( )
A.若水槽中盛有水,试管中盛满SO ,可看到试管中液面上升
2
B.若水槽中盛有水,试管中盛满NO ,可看到试管中液面上升并充满试管
2
C.若水槽中盛有水(滴有酚酞),试管中是NH ,可看到试管内液面上升并呈红色
3
D.若水槽中盛有NaOH溶液,试管中是Cl,可看到试管内液面上升,黄绿色褪去
2
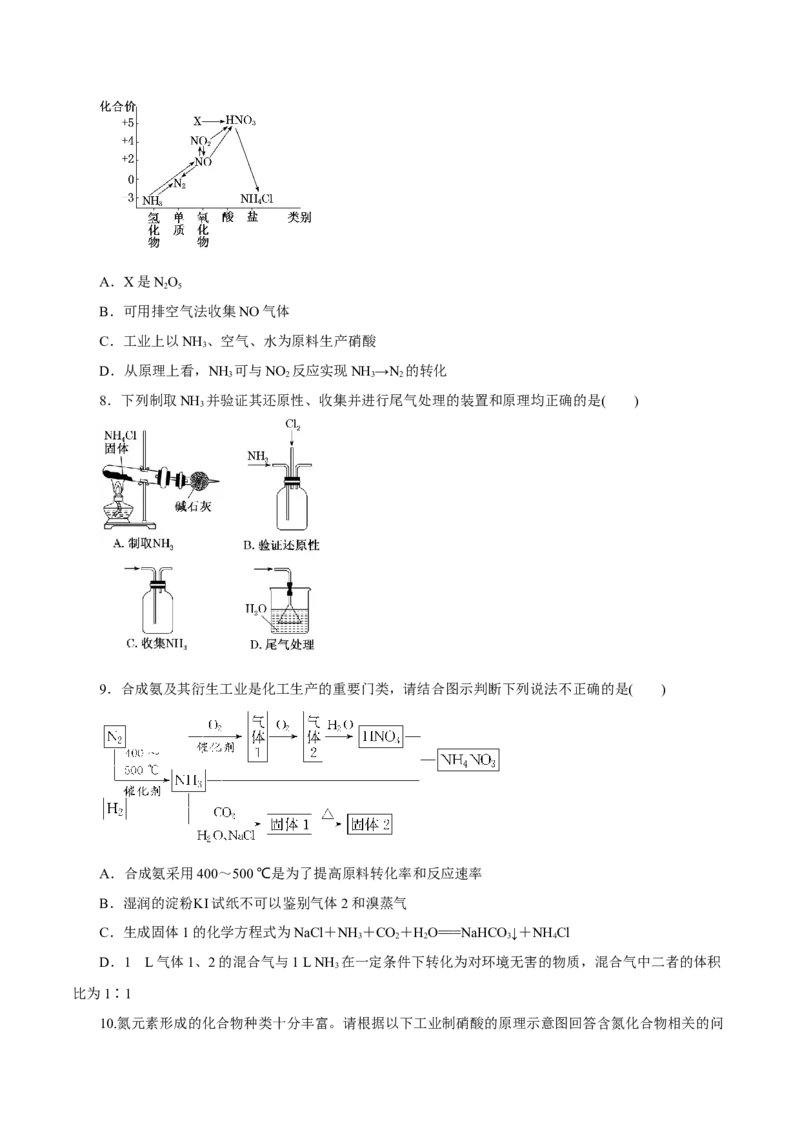
7.依据下图中氮元素及其化合物的转化关系,判断下列说法中不正确的是( )A.X是NO
2 5
B.可用排空气法收集NO气体
C.工业上以NH 、空气、水为原料生产硝酸
3
D.从原理上看,NH 可与NO 反应实现NH →N 的转化
3 2 3 2
8.下列制取NH 并验证其还原性、收集并进行尾气处理的装置和原理均正确的是( )
3
9.合成氨及其衍生工业是化工生产的重要门类,请结合图示判断下列说法不正确的是( )
A.合成氨采用400~500 ℃是为了提高原料转化率和反应速率
B.湿润的淀粉KI试纸不可以鉴别气体2和溴蒸气
C.生成固体1的化学方程式为NaCl+NH +CO+HO===NaHCO↓+NH Cl
3 2 2 3 4
D.1 L气体1、2的混合气与1 L NH 在一定条件下转化为对环境无害的物质,混合气中二者的体积
3
比为1∶1
10.氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:
(1)下列有关NH 的说法中,不正确的是________(填字母)。
3
A.工业合成NH 需要在高温、高压、催化剂下进行
3
B.NH 可用来生产碳铵和尿素等化肥
3
C.NH 可用浓硫酸或无水氯化钙干燥
3
D.NH 受热易分解,须置于冷暗处保存
3
(2)NH 易溶于水,标准状况下,用充满NH 的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质
3 3
的量浓度为________mol·L-1。
(3)氨气燃烧的化学方程式为_________________________________________________。
(4)HNO 是一种重要的化工原料,工厂生产出的浓硝酸可用铝槽车或铁槽车来运输。在常温下能使铝、
3
铁钝化,说明浓硝酸具有很强的__________性。
(5)“吸收塔” 尾部会有含NO、NO 等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用
2
以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO 反应的原理为
2
NaCO+2NO ===NaNO +________+CO(请填写完成化学方程式)。
2 3 2 3 2
②氨转化法。已知7 mol氨恰好能将含NO和NO 共6 mol 的混合气体完全转化为N,则混合气体中
2 2
NO和NO 的物质的量之比为________,若用通式NO 表示氮氧化物,则每摩尔氨可将________mol的NO
2 x x
转化为N。
2
1.(2021·河北卷)硫和氮及其化合物对人类生存和社会发展意义重大,但硫氧化物和氮氧化物造成的
环境问题也日益受到关注。下列说法正确的是( )
A.NO 和SO 均为红棕色且有刺激性气味的气体,是酸雨的主要成因
2 2
B.汽车尾气中的主要大气污染物为NO、SO 和PM
2 2.5
C.植物直接吸收利用空气中的NO和NO 作为肥料,实现氮的固定
2
D.工业废气中的SO 可采用石灰法进行脱除
2
2.(2021·广东卷)部分含氮物质的分类与相应氮元素的化合价关系如图所示。下列说法错误的是( )A.a可经催化氧化生成b
B.b为红棕色,可转化为c
C.密闭体系中,c存在2NO NO
2 2 4
D.d的溶液与Cu反应可生成b或c
3.(2021·河北卷)关于非金属含氧酸及其盐的性质,下列说法正确的是( )
A.浓HSO 具有强吸水性,能吸收糖类化合物中的水分并使其炭化
2 4
B.NaClO、KClO 等氯的含氧酸盐的氧化性会随溶液的pH减小而增强
3
C.加热NaI与浓HPO 混合物可制备HI,说明HPO 比HI酸性强
3 4 3 4
D.浓HNO 和稀HNO 与Cu反应的还原产物分别为NO 和NO,故稀HNO 氧化性更强
3 3 2 3