文档内容
第五章 物质结构 元素周期律
第16讲 元素周期律和元素周期表(精练)
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
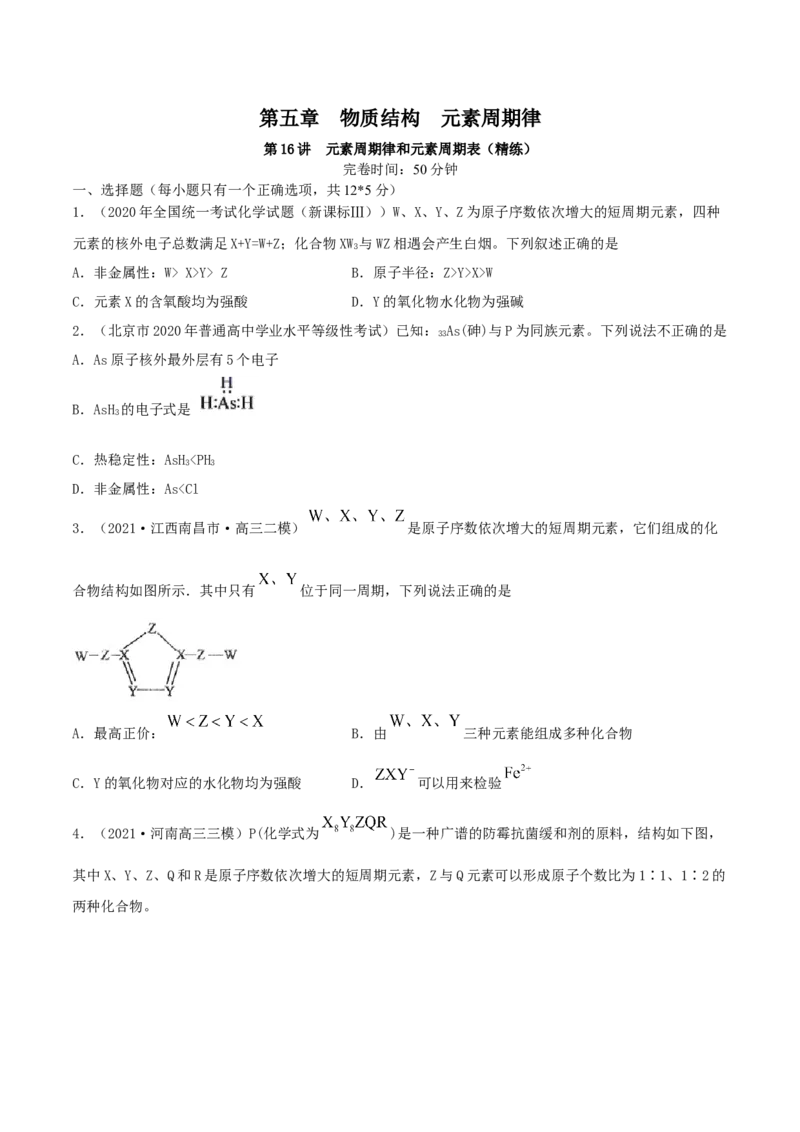
1.(2020年全国统一考试化学试题(新课标Ⅲ))W、X、Y、Z为原子序数依次增大的短周期元素,四种
元素的核外电子总数满足X+Y=W+Z;化合物XW 与WZ相遇会产生白烟。下列叙述正确的是
3
A.非金属性:W> X>Y> Z B.原子半径:Z>Y>X>W
C.元素X的含氧酸均为强酸 D.Y的氧化物水化物为强碱
2.(北京市2020年普通高中学业水平等级性考试)已知: As(砷)与P为同族元素。下列说法不正确的是
33
A.As原子核外最外层有5个电子
B.AsH 的电子式是
3
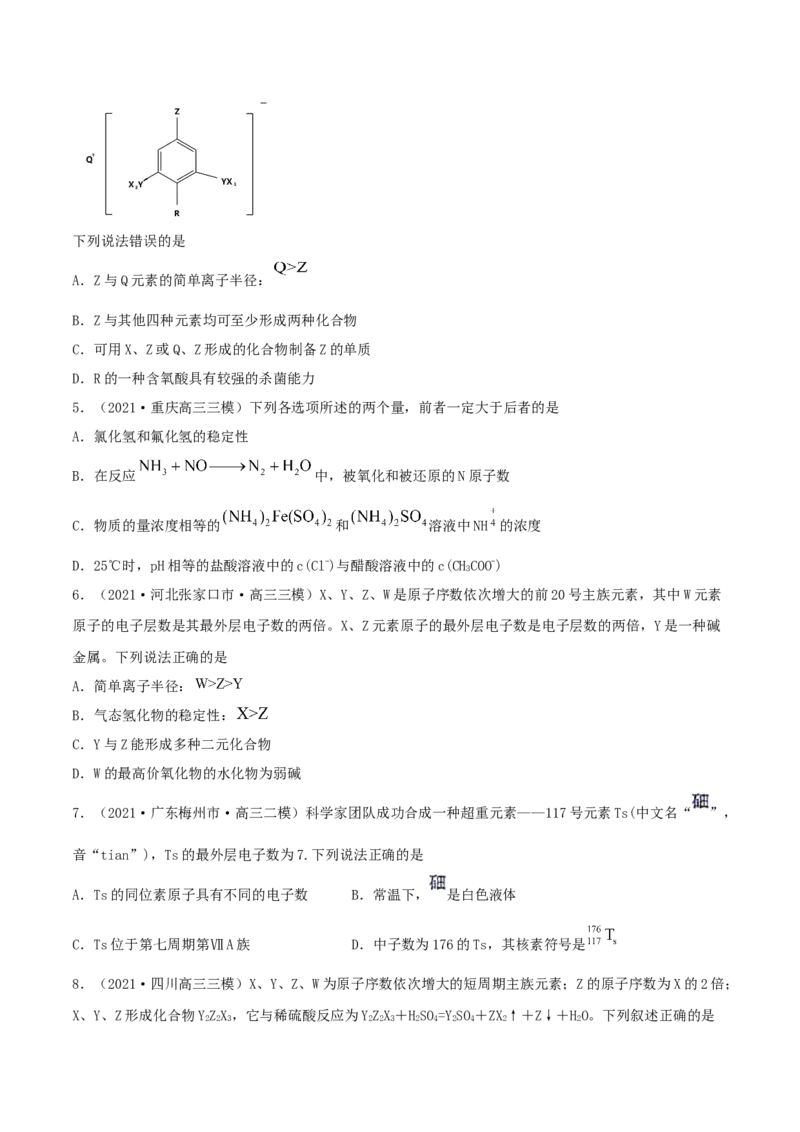
C.热稳定性:AsHC>D>A
D.简单氢化物的沸点:C>E
10.(2021·天津高三三模)下列排序正确的是
A.酸性: B.碱性:
C.熔点: (金刚石) D.沸点:
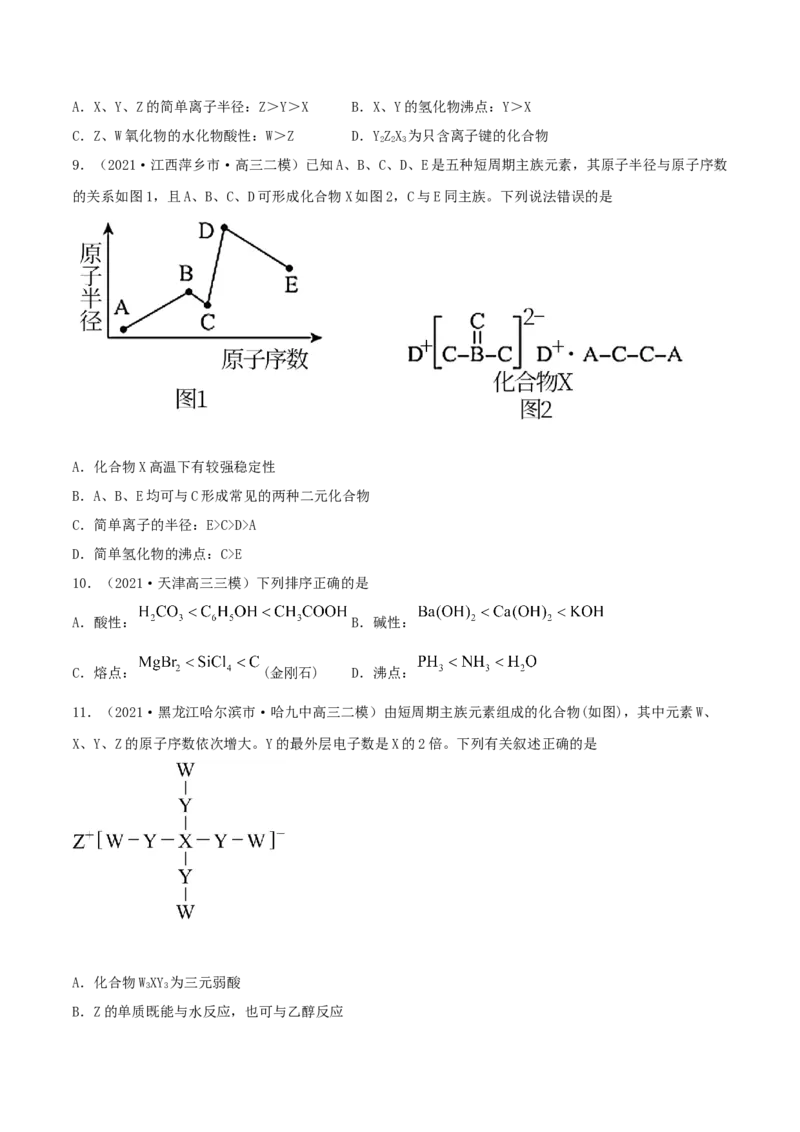
11.(2021·黑龙江哈尔滨市·哈九中高三二模)由短周期主族元素组成的化合物(如图),其中元素W、
X、Y、Z的原子序数依次增大。Y的最外层电子数是X的2倍。下列有关叙述正确的是
A.化合物WXY 为三元弱酸
3 3
B.Z的单质既能与水反应,也可与乙醇反应C.W分别与X、Y、Z形成的化合物化学键类型相同
D.X的氯化物XCl 中原子均为8电子稳定结构
3
12.(2020·浙江高三月考)短周期主族元素 X、Y、Z、W 原子序数依次增大, Y 在同周期主族元素中
原子半径最大,Y分别与 X、Z、W 形成二元化合物甲、乙、丙,其 0.1mol·L-1 水溶液近似 pH(常温)如
下表:
甲 乙 丙
近似 pH 值 8 12 7
下列说法不正确的是
A.甲、丙的晶体类型相同,且熔点:甲>丙
B.由 Y 和 Z 组成的二元化合物中不可能含共价键
C.原子半径:r(Y) > r(Z) > r(W) > r(X)
D.X 的简单气态氢化物的热稳定性比 W 的强
二、主观题(共3小题,共40分)
13.(2021·上海高三二模)(20分)氧、碳等非金属元素形成的物质种类繁多、性状各异。
(1)氧、氟、氮三种元素都可形成简单离子,它们的离子半径最小的是___________(填离子符号),硅元素
在元素周期表中的位置是___________。CO 和SiO 是同一主族元素的最高正价氧化物,常温下CO 为气体,
2 2 2
SiO 为高熔点固体。请分析原因:___________。
2
(2)比较硫和氯性质的强弱。热稳定性HS___________HCl(选填“<”、“>”或“=”,下同);酸性:
2
HClO___________HSO 用一个离子方程式说明氯元素和硫元素非金属性的相对强弱:___________。
4 2 4。
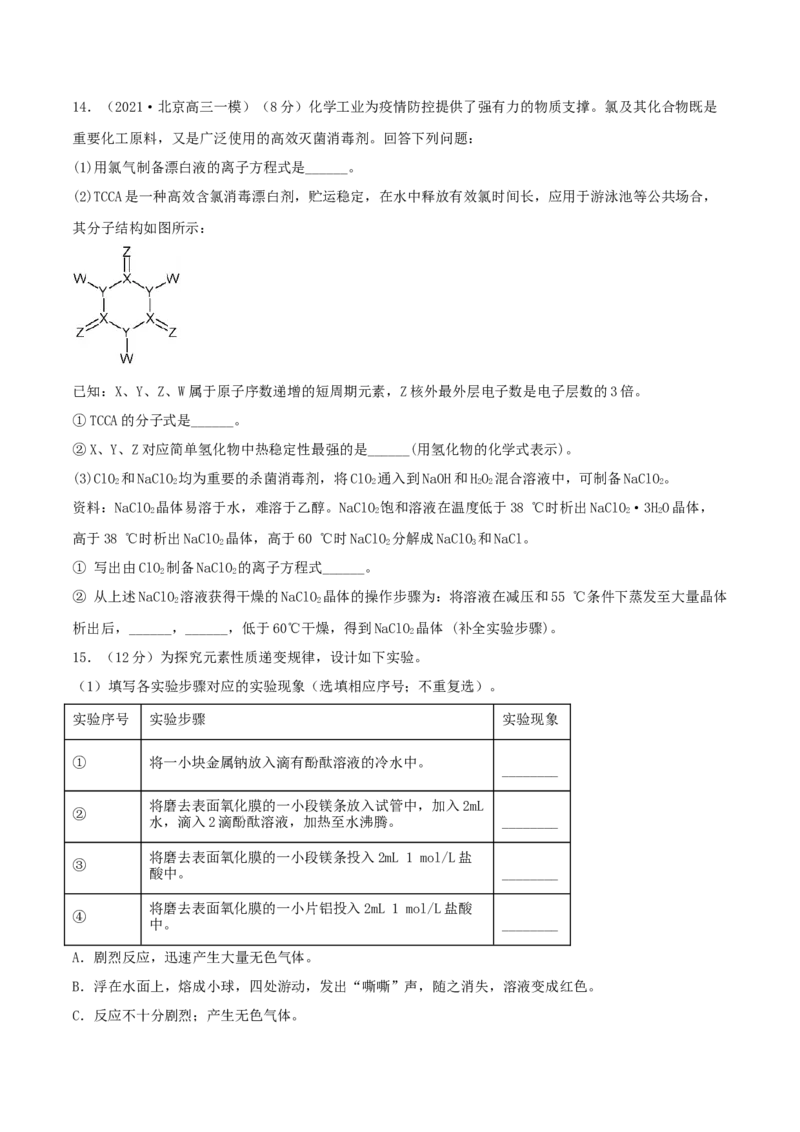
(3)红酒中添加一定量的SO 可以防止酒液氧化,这利用了SO 的___________性。若将SO 气体通入HS水
2 2 2 2
溶液中直至过量,下列表示溶液的pH随通入SO 气体体积变化的示意图正确的是___________(填序号)。
2
已知NaHSO 溶液呈酸性,而HSO 既能电离又能水解。则在NaHSO 溶液中c(HSO)___________c(SO )(选
3 3 2 3
填“<”、“>”或“=”) 。
(4)亚硫酸钠和碘酸钾在酸性条件下反应生成硫酸钠、硫酸钾、碘和水,写该反应方程式
________________。14.(2021·北京高三一模)(8分)化学工业为疫情防控提供了强有力的物质支撑。氯及其化合物既是
重要化工原料,又是广泛使用的高效灭菌消毒剂。回答下列问题:
(1)用氯气制备漂白液的离子方程式是______。
(2)TCCA是一种高效含氯消毒漂白剂,贮运稳定,在水中释放有效氯时间长,应用于游泳池等公共场合,
其分子结构如图所示:
已知:X、Y、Z、W属于原子序数递增的短周期元素,Z核外最外层电子数是电子层数的3倍。
①TCCA的分子式是______。
②X、Y、Z对应简单氢化物中热稳定性最强的是______(用氢化物的化学式表示)。
(3)ClO 和NaClO 均为重要的杀菌消毒剂,将ClO 通入到NaOH和HO 混合溶液中,可制备NaClO。
2 2 2 2 2 2
资料:NaClO 晶体易溶于水,难溶于乙醇。NaClO 饱和溶液在温度低于38 ℃时析出NaClO·3HO晶体,
2 2 2 2
高于38 ℃时析出NaClO 晶体,高于60 ℃时NaClO 分解成NaClO 和NaCl。
2 2 3
① 写出由ClO 制备NaClO 的离子方程式______。
2 2
② 从上述NaClO 溶液获得干燥的NaClO 晶体的操作步骤为:将溶液在减压和55 ℃条件下蒸发至大量晶体
2 2
析出后,______,______,低于60℃干燥,得到NaClO 晶体 (补全实验步骤)。
2
15.(12分)为探究元素性质递变规律,设计如下实验。
(1)填写各实验步骤对应的实验现象(选填相应序号;不重复选)。
实验序号 实验步骤 实验现象
① 将一小块金属钠放入滴有酚酞溶液的冷水中。
________
将磨去表面氧化膜的一小段镁条放入试管中,加入2mL
②
水,滴入2滴酚酞溶液,加热至水沸腾。 ________
将磨去表面氧化膜的一小段镁条投入2mL 1 mol/L盐
③
酸中。 ________
将磨去表面氧化膜的一小片铝投入2mL 1 mol/L盐酸
④
中。 ________
A.剧烈反应,迅速产生大量无色气体。
B.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。
C.反应不十分剧烈;产生无色气体。D.有气体产生,溶液变成浅红色。
(2)实验④:向1mL 1 mol/L AlCl 溶液中滴加2 mol/L NaOH溶液至过量,观察生成白色胶状沉淀,继
3
而沉淀消失。
请用离子方程式解释该实验现象: ________ 、 ________ 。
(3)实验⑤:在试管中加入3~5 mL NaSiO 溶液,逐滴加入稀硫酸,边加边振荡。观察试管中出现白色凝
2 3
胶。相应化学方程式: ________ ,证明酸性:________﹥ (用化学式表示)。
(4)实验⑥:向新制得的NaS溶液中滴加新制的氯水。观察试管中出现黄色沉淀。相应离子方程式:
2
________ ,证明氧化性:________﹥ (用化学式表示)。
通过以上实验和讨论,推断钠、镁、铝的金属性逐渐 ________ (选填“增强”或“减弱”),硅、硫、
氯的非金属性逐渐 ________ (选填“增强”或“减弱”)。