文档内容
第六章 化学反应与能量
第18讲 原电池 化学电源(精练)
完卷时间:50分钟
可能用到的相对分子质量:Li7 Zn65
一、选择题(每小题只有一个正确选项,共12*5分)
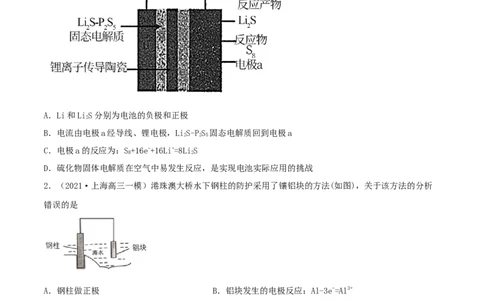
1.(2021·安徽淮南市·高三二模)全固态锂电池能量密度大,安全性能高引起大量研究者的兴趣。一
种以硫化物固体电解质的锂-硫电池的工作示意图如下。下列说法错误的是
A.Li和LiS分别为电池的负极和正极
2
B.电流由电极a经导线、锂电极,LiS-PS 固态电解质回到电极a
2 2 5
C.电极a的反应为:S+16e-+16Li+=8LiS
8 2
D.硫化物固体电解质在空气中易发生反应,是实现电池实际应用的挑战
2.(2021·上海高三一模)港珠澳大桥水下钢柱的防护采用了镶铝块的方法(如图),关于该方法的分析
错误的是
A.钢柱做正极 B.铝块发生的电极反应:Al-3e-=Al3+
C.可使化学能转变为电能 D.电子由钢柱经导线流向铝块
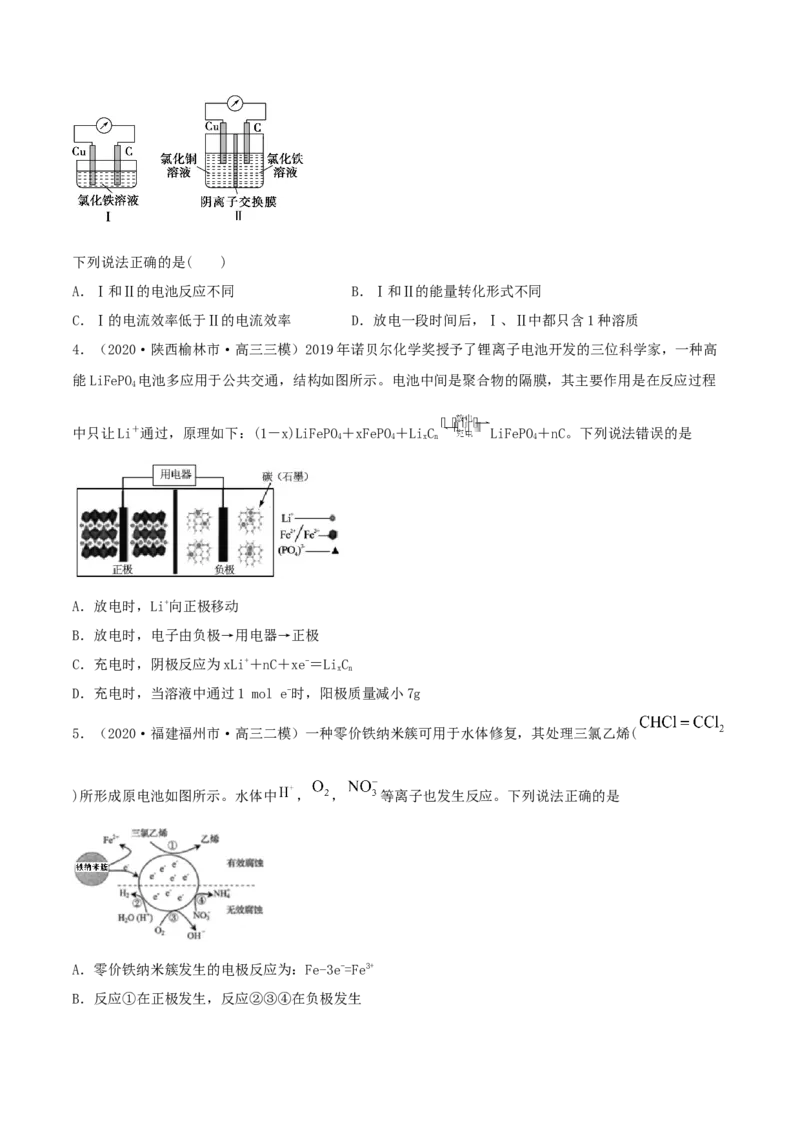
3.(2021·广东潮州市·高三二模)已知:电流效率=电路中通过的电子数与消耗负极失去电子总数之
比。现有两个电池Ⅰ、Ⅱ,装置如图所示。下列说法正确的是( )
A.Ⅰ和Ⅱ的电池反应不同 B.Ⅰ和Ⅱ的能量转化形式不同
C.Ⅰ的电流效率低于Ⅱ的电流效率 D.放电一段时间后,Ⅰ、Ⅱ中都只含1种溶质
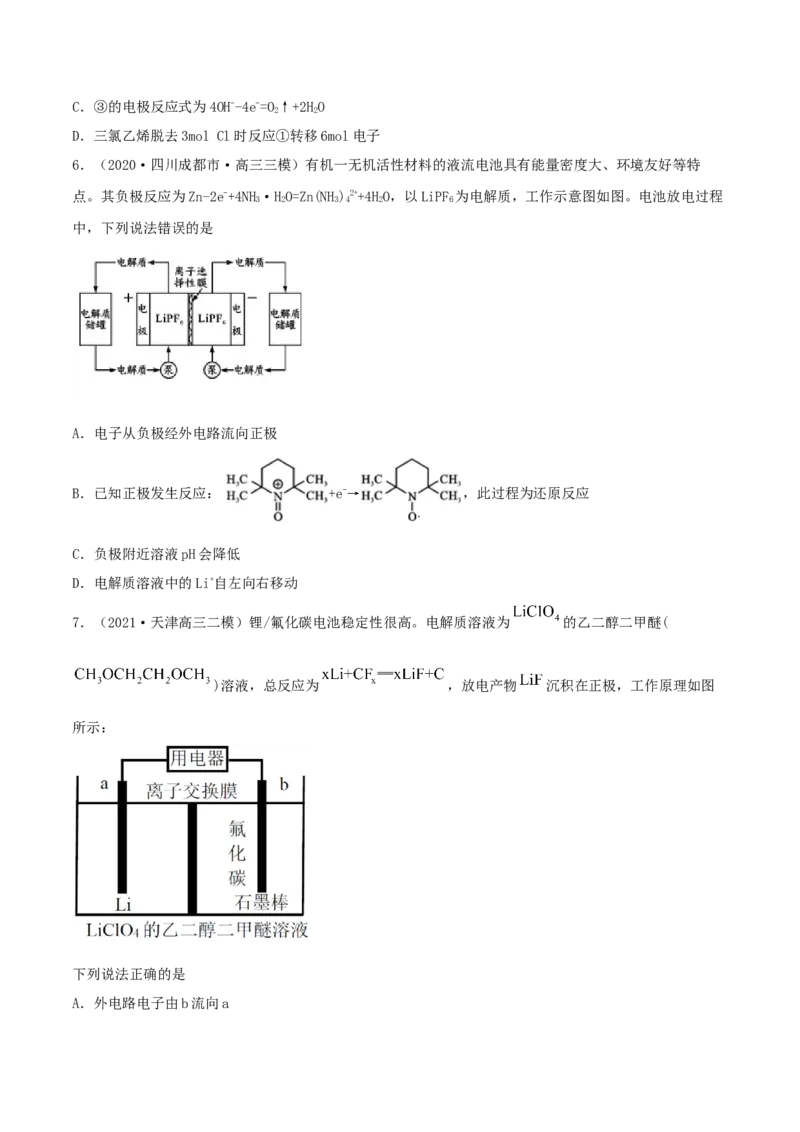
4.(2020·陕西榆林市·高三三模)2019年诺贝尔化学奖授予了锂离子电池开发的三位科学家,一种高
能LiFePO 电池多应用于公共交通,结构如图所示。电池中间是聚合物的隔膜,其主要作用是在反应过程
4
中只让Li+通过,原理如下:(1-x)LiFePO+xFePO+LiC LiFePO+nC。下列说法错误的是
4 4 x n 4
A.放电时,Li+向正极移动
B.放电时,电子由负极→用电器→正极
C.充电时,阴极反应为xLi++nC+xe-=LiC
x n
D.充电时,当溶液中通过1 mol e-时,阳极质量减小7g
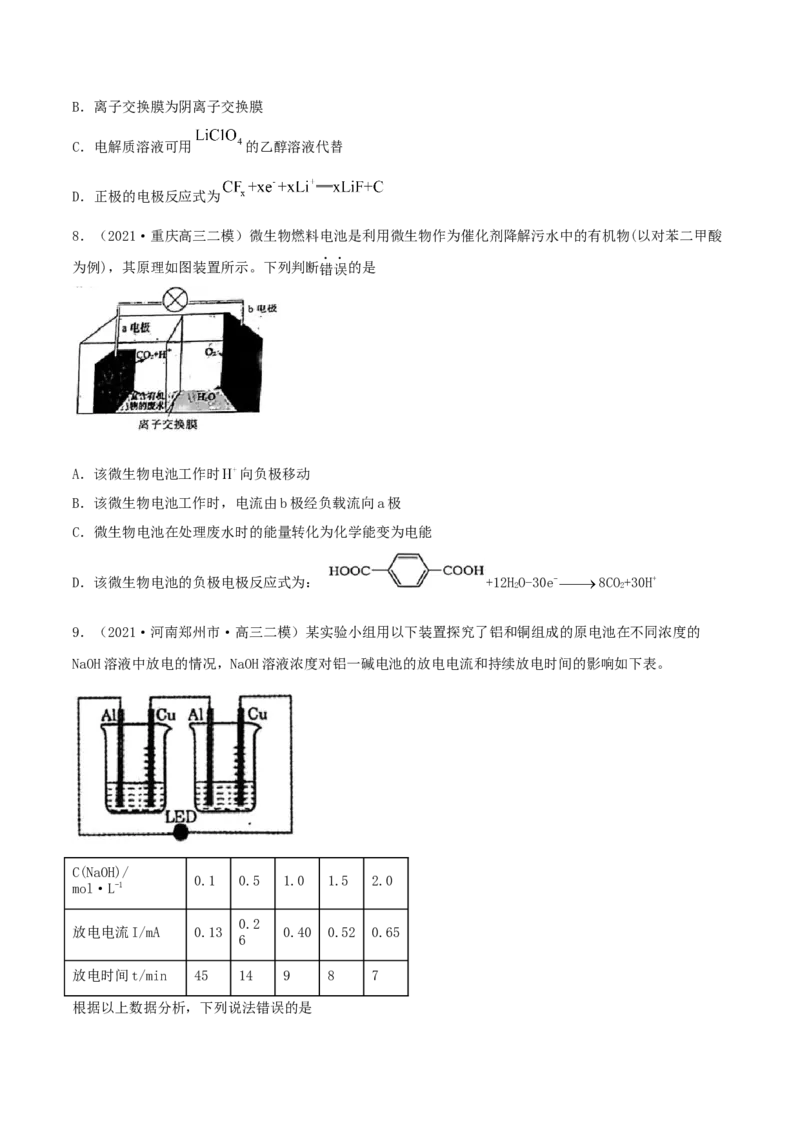
5.(2020·福建福州市·高三二模)一种零价铁纳米簇可用于水体修复,其处理三氯乙烯(
)所形成原电池如图所示。水体中 , , 等离子也发生反应。下列说法正确的是
A.零价铁纳米簇发生的电极反应为:Fe-3e-=Fe3+
B.反应①在正极发生,反应②③④在负极发生C.③的电极反应式为4OH--4e-=O↑+2HO
2 2
D.三氯乙烯脱去3mol Cl时反应①转移6mol电子
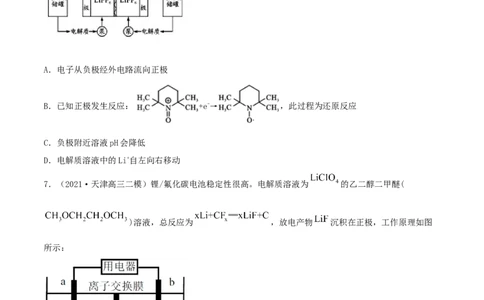
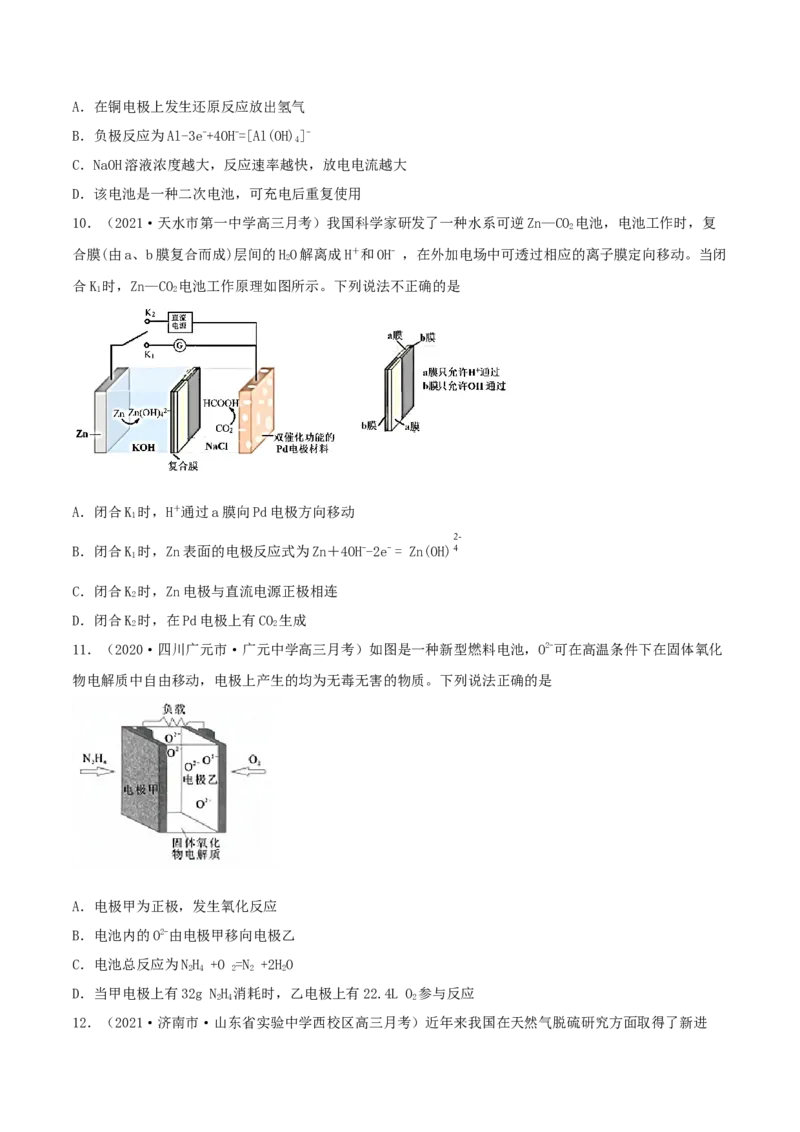
6.(2020·四川成都市·高三三模)有机一无机活性材料的液流电池具有能量密度大、环境友好等特
点。其负极反应为Zn-2e-+4NH·HO=Zn(NH)2++4HO,以LiPF 为电解质,工作示意图如图。电池放电过程
3 2 3 4 2 6
中,下列说法错误的是
A.电子从负极经外电路流向正极
B.已知正极发生反应: +e-→ ,此过程为还原反应
C.负极附近溶液pH会降低
D.电解质溶液中的Li+自左向右移动
7.(2021·天津高三二模)锂/氟化碳电池稳定性很高。电解质溶液为 的乙二醇二甲醚(
)溶液,总反应为 ,放电产物 沉积在正极,工作原理如图
所示:
下列说法正确的是
A.外电路电子由b流向aB.离子交换膜为阴离子交换膜
C.电解质溶液可用 的乙醇溶液代替
D.正极的电极反应式为
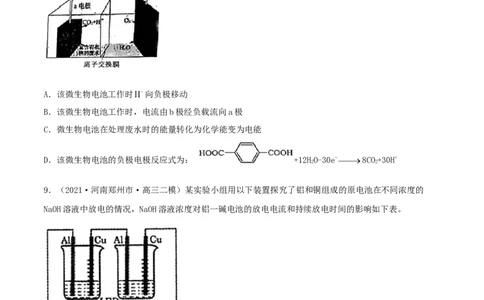
8.(2021·重庆高三二模)微生物燃料电池是利用微生物作为催化剂降解污水中的有机物(以对苯二甲酸
为例),其原理如图装置所示。下列判断错误的是
A.该微生物电池工作时 向负极移动
B.该微生物电池工作时,电流由b极经负载流向a极
C.微生物电池在处理废水时的能量转化为化学能变为电能
D.该微生物电池的负极电极反应式为: +12HO-30e- 8CO+30H+
2 2
9.(2021·河南郑州市·高三二模)某实验小组用以下装置探究了铝和铜组成的原电池在不同浓度的
NaOH溶液中放电的情况,NaOH溶液浓度对铝一碱电池的放电电流和持续放电时间的影响如下表。
C(NaOH)/
0.1 0.5 1.0 1.5 2.0
mol·L-1
0.2
放电电流I/mA 0.13 0.40 0.52 0.65
6
放电时间t/min 45 14 9 8 7
根据以上数据分析,下列说法错误的是A.在铜电极上发生还原反应放出氢气
B.负极反应为Al-3e-+4OH-=[Al(OH)]-
4
C.NaOH溶液浓度越大,反应速率越快,放电电流越大
D.该电池是一种二次电池,可充电后重复使用
10.(2021·天水市第一中学高三月考)我国科学家研发了一种水系可逆Zn—CO 电池,电池工作时,复
2
合膜(由a、b膜复合而成)层间的HO解离成H+和OH- ,在外加电场中可透过相应的离子膜定向移动。当闭
2
合K 时,Zn—CO 电池工作原理如图所示。下列说法不正确的是
1 2
A.闭合K 时,H+通过a膜向Pd电极方向移动
1
B.闭合K 时,Zn表面的电极反应式为Zn+4OH--2e- = Zn(OH)
1
C.闭合K 时,Zn电极与直流电源正极相连
2
D.闭合K 时,在Pd电极上有CO 生成
2 2
11.(2020·四川广元市·广元中学高三月考)如图是一种新型燃料电池,O2-可在高温条件下在固体氧化
物电解质中自由移动,电极上产生的均为无毒无害的物质。下列说法正确的是
A.电极甲为正极,发生氧化反应
B.电池内的O2-由电极甲移向电极乙
C.电池总反应为NH +O =N +2HO
2 4 2 2 2
D.当甲电极上有32g NH 消耗时,乙电极上有22.4L O 参与反应
2 4 2
12.(2021·济南市·山东省实验中学西校区高三月考)近年来我国在天然气脱硫研究方面取得了新进展,利用如图1装置可完成天然气脱硫,甲池中发生反应如图2所示。
下列关于该装置工作原理的说法中,正确的是( )
A.碳棒为该脱硫装置的负极
B.乙池中发生的反应为:HS+2e-=S+2H+
2
C.AQ与HAQ间的转化属于非氧化还原反应
2
D.除I /I-外,Fe3+/Fe2+也能实现如图所示循环过程
二、主观题(共3小题,共40分)
13.(2021·四川高三期中)(10分)铅蓄电池、镍镉碱性充电电池都是重要的二次电池。已知:
①铅蓄电池总的化学方程式为: ,使用(放电)段时间后,其
内阻明显增大,电压却几乎不变,此时只有充电才能继续使用;
②镍镉碱性充电电池放电时,正极反应为: ,负极反应式:
,使用(放电)到后期,当电压明显下降时,其内阻却几乎不变,此时充电后也
能继续使用;
回答下列问题:
(1)铅蓄电池负极板上覆盖的物质是_______(填名称),充电时,PbSO 在________(填“阳极”、“阴极”
4
或“两个电极”)上________(填“生成或除去”)。
(2)镍镉碱性充电电池在充电时的总反应的化学方程式为_________________。
(3)铅蓄电池和镍镉碱性充电电池使用一段时间后,一个内阻明显增大,而另一个内阻却几乎不变的主要
原因可能是_____________________。
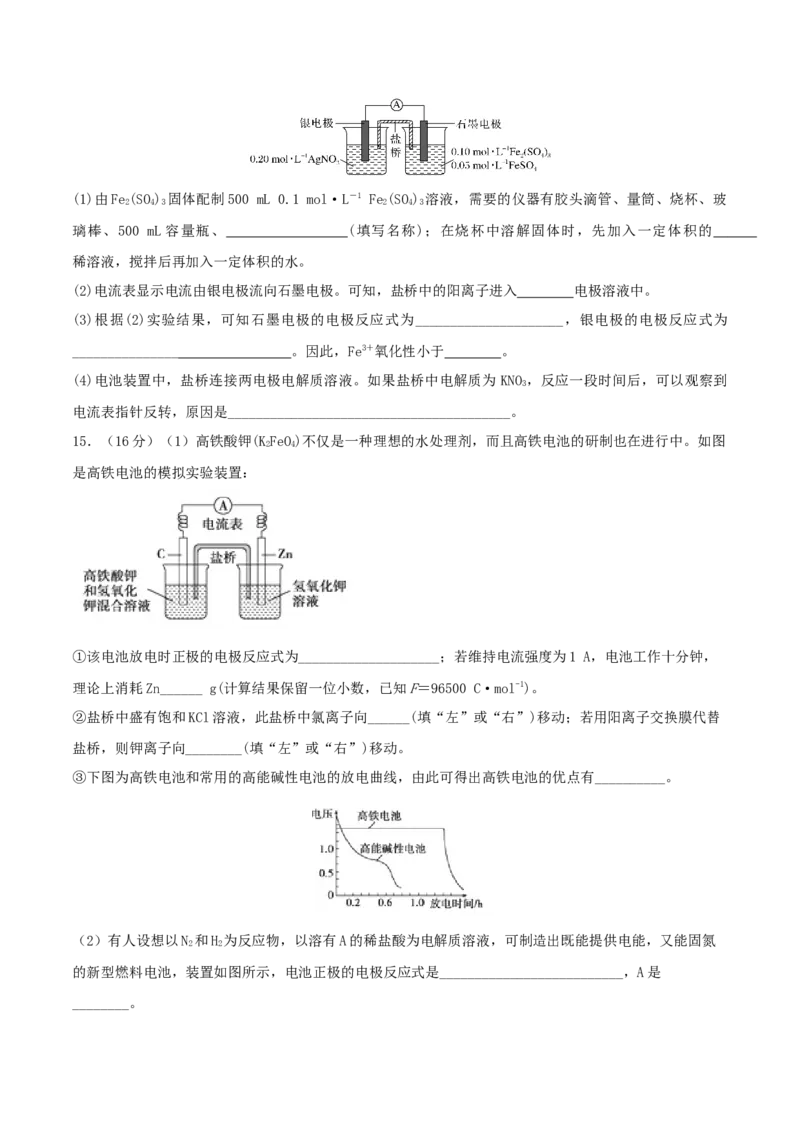
14.(2021·江西南昌高三摸底)(14分)为验证反应Fe3++Ag Fe2++Ag+,利用如图电池装置进行实
验。(1)由Fe(SO) 固体配制500 mL 0.1 mol·L-1 Fe(SO) 溶液,需要的仪器有胶头滴管、量筒、烧杯、玻
2 4 3 2 4 3
璃棒、500 mL容量瓶、 (填写名称);在烧杯中溶解固体时,先加入一定体积的
稀溶液,搅拌后再加入一定体积的水。
(2)电流表显示电流由银电极流向石墨电极。可知,盐桥中的阳离子进入 电极溶液中。
(3)根据(2)实验结果,可知石墨电极的电极反应式为_____________________,银电极的电极反应式为
_______________ 。因此,Fe3+氧化性小于 。
(4)电池装置中,盐桥连接两电极电解质溶液。如果盐桥中电解质为 KNO ,反应一段时间后,可以观察到
3
电流表指针反转,原因是________________________________________。
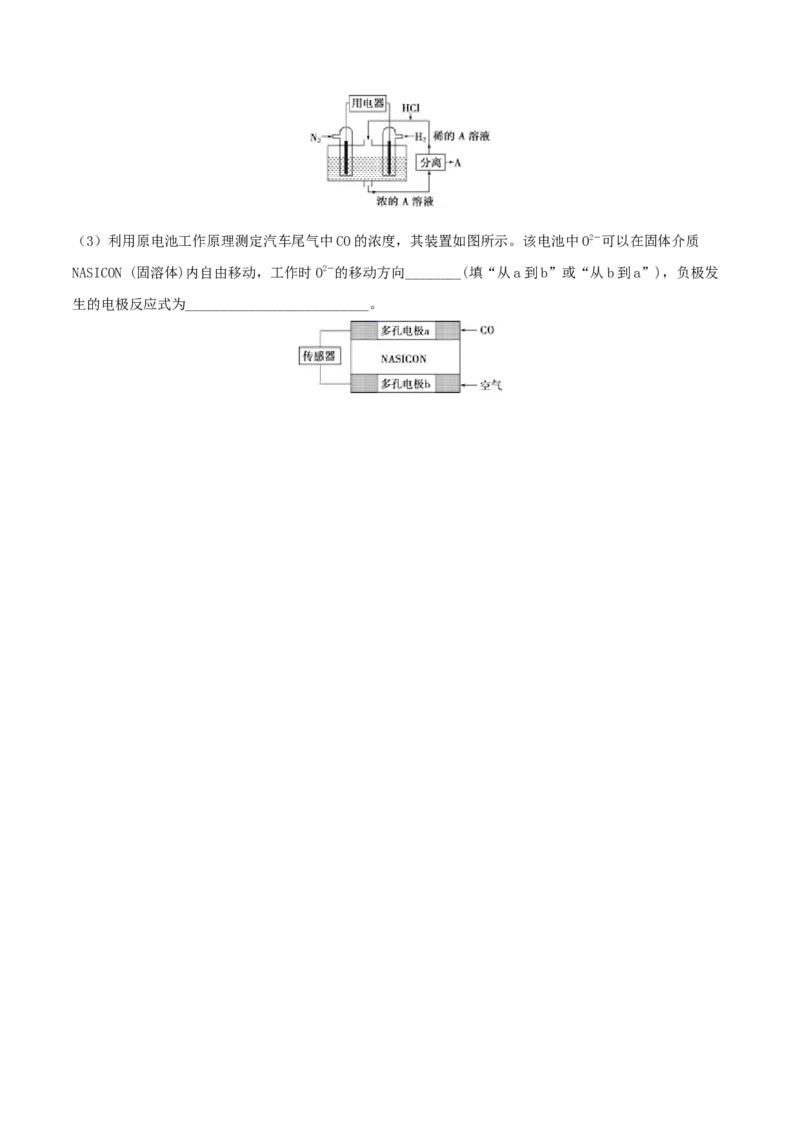
15.(16分)(1)高铁酸钾(KFeO)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图
2 4
是高铁电池的模拟实验装置:
①该电池放电时正极的电极反应式为____________________;若维持电流强度为1 A,电池工作十分钟,
理论上消耗Zn______ g(计算结果保留一位小数,已知F=96500 C·mol-1)。
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向______(填“左”或“右”)移动;若用阳离子交换膜代替
盐桥,则钾离子向________(填“左”或“右”)移动。
③下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有__________。
(2)有人设想以N 和H 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮
2 2
的新型燃料电池,装置如图所示,电池正极的电极反应式是__________________________,A是
________。(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质
NASICON (固溶体)内自由移动,工作时O2-的移动方向________(填“从a到b”或“从b到a”),负极发
生的电极反应式为__________________________。