文档内容
物质结构与性质 元素周期律
第 1 讲 原子结构 原子核外电子排布
课 程 标 准 知 识 建 构
1.知道原子核外电子的能级高低顺
序,了解原子核外电子排布的构造
原理。
2.能说明微观粒子的运动状态与宏
观物体运动特点的差异。
3.能结合能量最低原理、泡利不相
容原理、洪特规则书写1~36号元
素基态原子的核外电子排布和轨道
表示式,并说明含义。
一、原子结构与核素、同位素
1.原子的构成
(1)构成原子的微粒
(2)微粒之间的等式关系
质量关系:质量数(A)=质子数(Z)+中子数(N);
电性关系:
①原子中:质子数(Z)=核电荷数=核外电子数;
②阳离子的核外电子数=质子数-阳离子所带的电荷数;
③阴离子的核外电子数=质子数+阴离子所带的电荷数。
(3)微粒符号周围数字的含义2.元素、核素、同位素
(1)元素、核素、同位素的概念及相互关系
(2)同位素的特征
①同一元素的各种核素的中子数不同,质子数相同,化学性质几乎完全相同,
物理性质不同;
②同一元素的各种稳定核素在自然界中所占的原子百分数(丰度)不变。
(3)氢元素的三种核素
H:名称为氕,不含中子;
H:用字母D 表示,名称为氘或重氢;
H:用字母T 表示,名称为氚或超重氢。
(4)几种重要核素的用途
核素 U C H H O
用途 核燃料 用于考古断代 制氢弹 示踪原子
3.相对原子质量
(1)原子(即核素)的相对原子质量:一个原子(即核素)的质量与一个12C质量的
的比值。一种元素有几种同位素,就有几种不同核素的相对原子质量。
(2)元素的相对原子质量:是按该元素各种天然同位素原子所占的原子百分比
算出的平均值。如:Ar(Cl)=Ar(35Cl)×a%+Ar(37Cl)×b%。
(3)核素的近似相对原子质量=该核素的质量数。
【诊断1】 判断下列说法是否正确,正确的打√,错误的打×。
(1)任何原子的原子核均有质子和中子,任何离子均有电子( )
(2)一种元素可以有多种核素,也可能只有一种核素,有多少种核素就有多少
种原子( )
(3)核聚变如H+H―→He+n,因为有新微粒生成,所以该变化是化学变化(
)(4)Cl与Cl得电子能力几乎相同( )
(5)一种核素只有一种质量数( )
(6)H 、D 、HD均为氢元素的不同单质,三者属于同素异形体( )
2 2
答案 (1)× (2)√ (3)× (4)√ (5)√ (6)×
二、基态原子核外电子排布及表示方法
1.能层、能级与原子轨道
(1)能层(n)
①在多电子原子中,核外电子的能量不同。
②按电子的能量差异从内到外分成不同能层,通常用K、L、M、N……表示,
能量依次升高。
(2)能级
①同一能层电子的能量也可能不同,分成不同的能级,通常用 s 、 p 、 d 、 f 等表
示。
②同一能层里,各能级的能量按 s 、 p 、 d 、 f 的顺序依次升高。
(3)原子轨道
电子云轮廓图给出了电子在核外经常出现的区域,称为原子轨道。
(4)能层、能级与原子轨道的关系
①能级与原子轨道
能级 原子轨道 轨道形状 轨道个数
s s 球形 1
p p 、p 、p 哑铃形 3
x y z
②能层、能级与原子轨道的数量关系
第n层,有n 个能级, n 2 条原子轨道,最多容纳 2 n 2 个电子。
2.基态原子的核外电子排布
(1)能量最低原理:电子尽可能地先占有能量低的轨道,然后进入能量高的轨
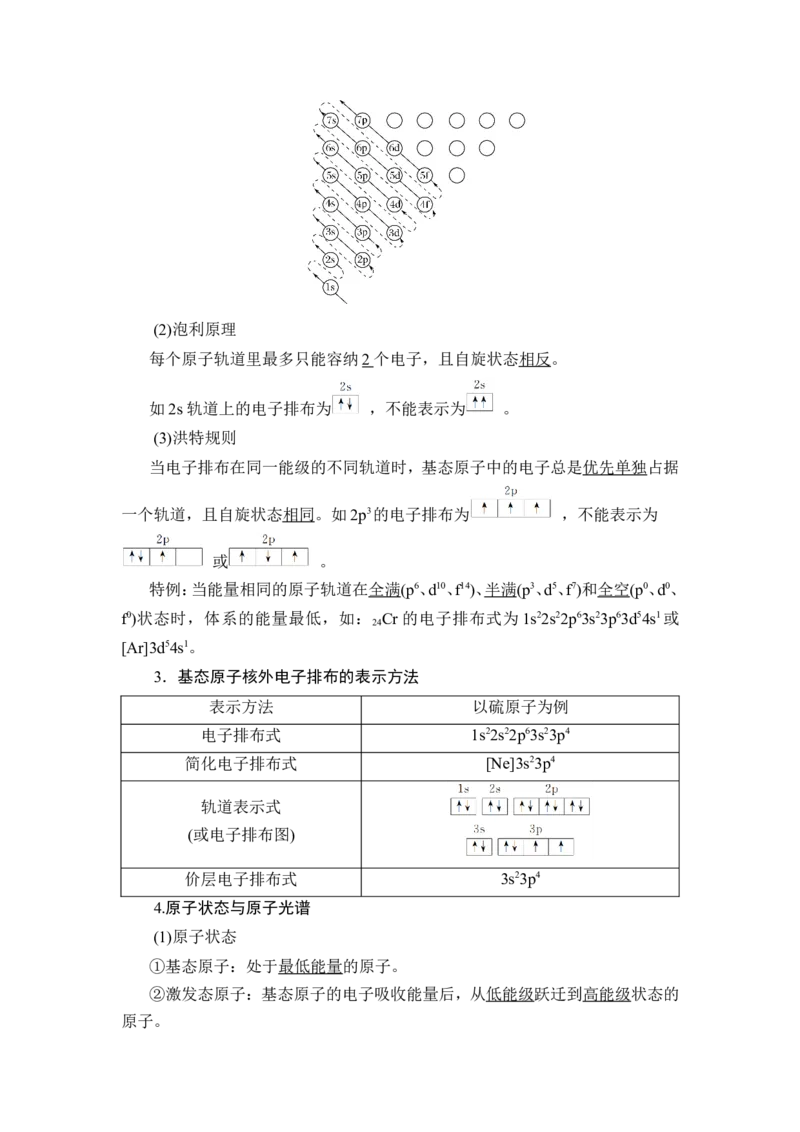
道,使整个原子的能量处于最低状态。(2)泡利原理
每个原子轨道里最多只能容纳2 个电子,且自旋状态相反。
如2s轨道上的电子排布为 ,不能表示为 。
(3)洪特规则
当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据
一个轨道,且自旋状态相同。如2p3的电子排布为 ,不能表示为
或 。
特例:当能量相同的原子轨道在全满(p6、d10、f14)、半满(p3、d5、f7)和全空(p0、d0、
f0)状态时,体系的能量最低,如: Cr的电子排布式为1s22s22p63s23p63d54s1或
24
[Ar]3d54s1。
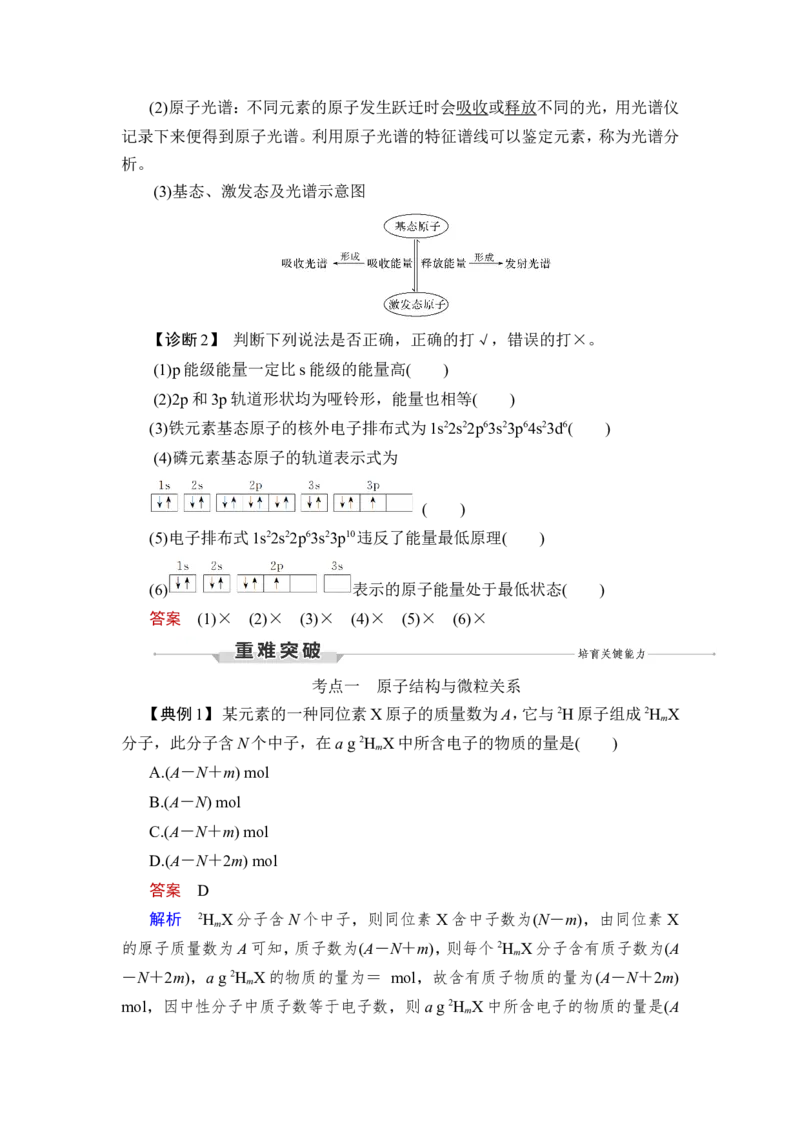
3.基态原子核外电子排布的表示方法
表示方法 以硫原子为例
电子排布式 1s22s22p63s23p4
简化电子排布式 [Ne]3s23p4
轨道表示式
(或电子排布图)
价层电子排布式 3s23p4
4.原子状态与原子光谱
(1)原子状态
①基态原子:处于最低能量的原子。
②激发态原子:基态原子的电子吸收能量后,从低能级跃迁到高能级状态的
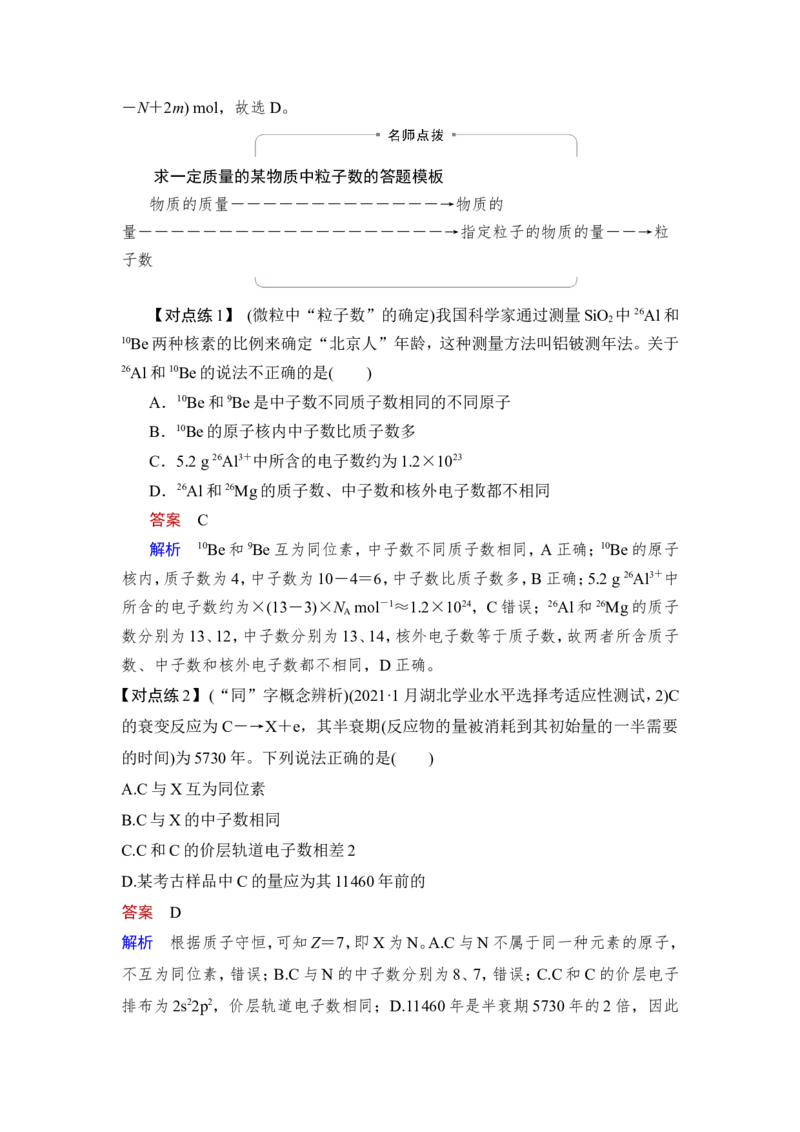
原子。(2)原子光谱:不同元素的原子发生跃迁时会吸收或释放不同的光,用光谱仪
记录下来便得到原子光谱。利用原子光谱的特征谱线可以鉴定元素,称为光谱分
析。
(3)基态、激发态及光谱示意图
【诊断2】 判断下列说法是否正确,正确的打√,错误的打×。
(1)p能级能量一定比s能级的能量高( )
(2)2p和3p轨道形状均为哑铃形,能量也相等( )
(3)铁元素基态原子的核外电子排布式为1s22s22p63s23p64s23d6( )
(4)磷元素基态原子的轨道表示式为
( )
(5)电子排布式1s22s22p63s23p10违反了能量最低原理( )
(6) 表示的原子能量处于最低状态( )
答案 (1)× (2)× (3)× (4)× (5)× (6)×
考点一 原子结构与微粒关系
【典例1】 某元素的一种同位素X原子的质量数为A,它与2H原子组成2H X
m
分子,此分子含N个中子,在a g 2H X中所含电子的物质的量是( )
m
A.(A-N+m) mol
B.(A-N) mol
C.(A-N+m) mol
D.(A-N+2m) mol
答案 D
解析 2H X分子含N个中子,则同位素X含中子数为(N-m),由同位素X
m
的原子质量数为A可知,质子数为(A-N+m),则每个2H X分子含有质子数为(A
m
-N+2m),a g 2H X的物质的量为= mol,故含有质子物质的量为(A-N+2m)
m
mol,因中性分子中质子数等于电子数,则a g 2H X中所含电子的物质的量是(A
m-N+2m) mol,故选D。
求一定质量的某物质中粒子数的答题模板
物质的质量―――――――――――――→物质的
量―――――――――――――――――――→指定粒子的物质的量――→粒
子数
【对点练1】 (微粒中“粒子数”的确定)我国科学家通过测量SiO 中26Al和
2
10Be两种核素的比例来确定“北京人”年龄,这种测量方法叫铝铍测年法。关于
26Al和10Be的说法不正确的是( )
A.10Be和9Be是中子数不同质子数相同的不同原子
B.10Be的原子核内中子数比质子数多
C.5.2 g 26Al3+中所含的电子数约为1.2×1023
D.26Al和26Mg的质子数、中子数和核外电子数都不相同
答案 C
解析 10Be和9Be互为同位素,中子数不同质子数相同,A正确;10Be的原子
核内,质子数为4,中子数为10-4=6,中子数比质子数多,B正确;5.2 g 26Al3+中
所含的电子数约为×(13-3)×N mol-1≈1.2×1024,C错误;26Al和26Mg的质子
A
数分别为13、12,中子数分别为13、14,核外电子数等于质子数,故两者所含质子
数、中子数和核外电子数都不相同,D正确。
【对点练2】 (“同”字概念辨析)(2021·1月湖北学业水平选择考适应性测试,2)C
的衰变反应为C―→X+e,其半衰期(反应物的量被消耗到其初始量的一半需要
的时间)为5730年。下列说法正确的是( )
A.C与X互为同位素
B.C与X的中子数相同
C.C和C的价层轨道电子数相差2
D.某考古样品中C的量应为其11460年前的
答案 D
解析 根据质子守恒,可知Z=7,即X为N。A.C与N不属于同一种元素的原子,
不互为同位素,错误;B.C与N的中子数分别为8、7,错误;C.C和C的价层电子
排布为2s22p2,价层轨道电子数相同;D.11460年是半衰期5730年的2倍,因此11460年后变为原来的×=倍,正确。
【对点练3】 (“10电子”微粒和“18电子”微粒)已知A、B、C、D是中学化
学中常见的四种不同粒子,它们之间存在如图所示的转化关系(反应条件已经略
去):
(1)如果 A、B、C、D 均是 10 电子的粒子,请写出 A、D 的电子式:
A________________;D_______________________________________。
(2)如果A和C是18电子的粒子,B和D是10电子的粒子,请写出:
①A 与 B 在 溶 液 中 反 应 的 离 子 方 程 式 为
___________________________________________________________________。
②根据上述离子方程式,可以判断 C 与 B 结合质子的能力大小是
________(用化学式或离子符号表示)。
答案 (1)
(2)①HS-+OH-===S2-+H O ②OH->S2-
2
寻找“10电子”微粒和“18电子”微粒的方法
(1)“10电子”微粒
(2)“18电子”微粒
考点二 原子核外电子排布原理【典例2】 有四种短周期元素,它们的结构、性质等信息如下表所述:
元素 结构、性质等信息
是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金
A
是原子反应堆的导热剂
B B与A同周期,其最高价氧化物的水化物呈两性
C 元素的气态氢化物极易溶于水,可用作制冷剂
是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来
D
水生产过程中常用的消毒杀菌剂
请根据表中信息填写:
(1)A原子的核外电子排布式______________________________________。
(2)B元素在周期表中的位置________________;离子半径:B________(填
“大于”或“小于”)A。
(3)C原子的轨道表示式是_________________________________________,
其原子核外有________个未成对电子,能量最高的电子为________轨道上的
电子,其轨道呈________形。
(4)D原子的电子排布式为________________________________________,
D-的结构示意图是________________。
(5)B的最高价氧化物对应的水化物与 A的最高价氧化物对应的水化物反应
的化学方程式为_____________________________________________________,
与D的氢化物的水溶液反应的化学方程式为______________________________
___________________________________________________________________。
答案 (1)1s22s22p63s1 (2)第三周期ⅢA族 小于
(3)
3 2p 哑铃
(4)1s22s22p63s23p5(或[Ne]3s23p5)
(5)NaOH+Al(OH) ===NaAlO +2H O
3 2 2
3HCl+Al(OH) ===AlCl +3H O
3 3 2
解析 根据题中信息可推出:A为Na,B为Al,C为N,D为Cl。
核外电子排布常见错误(1)在写基态原子的轨道表示式时,常出现以下错误:
① (违反能量最低原理)
② (违反泡利原理)
③ (违反洪特规则)
④ (违反洪特规则)
(2)当出现d轨道时,虽然电子按ns、(n-1)d、np的顺序填充,但在书写电子排
布式时,仍把(n-1)d放在ns前,如Fe:1s22s22p63s23p63d64s2,而失电子时,却先失
4s轨道上的电子,如Fe3+:1s22s22p63s23p63d5。
(3)注意比较原子核外电子排布式、简化电子排布式、价层电子排布式的区别
与联系。如Cu的电子排布式:1s22s22p63s23p63d104s1;简化电子排布式:
[Ar]3d104s1;价层电子排布式:3d104s1。
【对点练4】 (原子核外电子排布规律)(2020·四川威远中学校月考)已知锰的
核电荷数为25,下列有关基态锰原子核外电子排布正确的是( )
A.价层电子轨道表示式为
B.核外电子排布时,先排满4s轨道,再排3d轨道
C.锰原子失去电子形成Mn2+时应失去 3d 轨道上的电子
D.锰原子的 2p 和 3p 轨道的形状、能量均相同
答案 B
解析 按洪特规则知,基态锰原子核外电子排布时,5个3d轨道上各有1个
电子且自旋状态相同,价层电子轨道表示式为 ,A错误;
4s轨道能量比3d轨道低,故核外电子排布时,先排满4s轨道,再排3d轨道,B正
确;锰原子失去电子形成 Mn2+时应先失去4s轨道上的电子,C错误;锰原子的
2p和3p轨道的形状均为哑铃形、能量高低则不同,2p轨道能量低于3p轨道,D
错误。
【对点练5】 (化学用语的规范使用)(2020·四川雅安中学月考)下列关于化学
用语的表示错误的是( )
A.Na+的轨道表示式:B.氯离子的结构示意图:
C.甲基的电子式:
D.硫离子的核外电子排布式:1s22s22p63s23p6
答案 A
解 析 Na + 核 外 电 子 排 布 式 为 1s22s22p6 , 因 此 其 轨 道 表 示 式 为
,故A项错误;氯离子质子数为17,核外电子数为18,其结
构示意图为 ,故B项正确;甲基为—CH ,其电子式为 ,故C项正
3
确;硫离子核外有 18 个电子,根据构造原理可知,其核外电子排布式为
1s22s22p63s23p6,故D正确。
【对点练6】 (电子排布式、轨道表示式的书写)按要求书写电子排布式或轨道
表示式。
(1)基态C原子的核外电子排布式为________。
(2)基态Ni原子的核外电子排布式为________。
(3)基态Cr3+的核外电子排布式为________________。
(4)基态Mn2+的核外电子排布式为________________。
(5)基态钒原子的价层电子轨道表示式为____________________________。
(6)基态镓(Ga)原子的电子排布式为________。
(7)基态Ni2+的价层电子轨道表示式为_______________________________。
答案 (1)1s22s22p2 (2)[Ar]3d84s2 (3)[Ar]3d3
(4)[Ar]3d5 (5)
(6)[Ar]3d104s24p1 (7)
原子(离子)核外电子排布式(图)的书写
(1)核外电子排布式:按电子排入各能层中各能级的先后顺序,用数字在能级
符号右上角标明该能级上排布的电子数的式子。如Cu:1s22s22p63s23p63d104s1,其简化电子排布式为[Ar]3d104s1。
(2)价层电子排布式:如Fe原子的电子排布式为1s22s22p63s23p63d64s2,价层电
子排布式为3d64s2。价层电子排布式能反映基态原子的能层数和参与成键的电子
数以及最外层电子数。
(3)轨道表示式(电子排布图):用方框表示原子轨道,用“↑”或“↓”表示
自旋状态不同的电子,按排入各能层中各能级的先后顺序和在轨道中的排布情况
书写。如:S:
。核外电子排布图能直观地反映出原
子的核外电子的自旋情况以及成对的电子对数和未成对电子数。
1.(2020·课标全国Ⅰ,11)1934年约里奥-居里夫妇在核反应中用α粒子(即
氦核He)轰击金属原子X,得到核素Y,开创了人造放射性核素的先河:
X+He―→Y+n
其中元素X、Y的最外层电子数之和为8。下列叙述正确的是( )
A.X的相对原子质量为26 B.X、Y均可形成三氯化物
C.X的原子半径小于Y的 D.Y仅有一种含氧酸
答案 B
解析 由X+He―→Y+n可得W+4=30+1,则W=27,设X的最外层电子
数为x,结合题给信息可知,x+x+2=8,解得x=3,又X为金属原子,可得Z=
13,X为Al,Y为P。Al的质量数为27,A项错误;X(Al)、Y(P)均可形成三氯化物,
分别为AlCl 、PCl ,B项正确;根据同一周期主族元素从左到右原子半径依次减
3 3
小知,X(Al)的原子半径大于Y(P)的,C项错误;Y(P)有多种含氧酸,如H PO 和
3 3
H PO 等,D项错误。
3 4
2.(2021·1月辽宁普高校招生考试适应性测试,4)下列说法错误的是( )
A.CH 分子球棍模型: INCLUDEPICTURE "G:\\2021 课件\\D2.TIF" \*
4
MERGEFORMATINET INCLUDEPICTURE "G:\\2021 课 件 \\D2.TIF" \*
MERGEFORMATINETB.基态Si原子价电子排布图:
C.第一电离能:N>O>C
D.石墨质软的原因是其层间作用力微弱
答案 A
解析 C 原子的半径大于 H 原子,因此 CH 分子的球棍模型:
4
INCLUDEPICTURE "G:\\2021 课 件 \\D20.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021 课 件 \\D20.TIF" \* MERGEFORMATINET
,A 错误;基态 Si 原子价电子排布式为 3s23p2,价电子排布图为
,B正确;N原子的2p轨道处于半满状态,因此其第一电离
能比其左右的元素大,则第一电离能:N>O>C,C正确;在石墨中,同层的C原子
以共价键结合,而每层之间以范德华力结合,其层间作用力微弱,层与层之间可
以滑动,因此较为松软,D正确。
3.(高考组合题)电子排布式和轨道表示式的书写。
(1)(2020·全国Ⅱ)基态Ti原子的核外电子排布式为____________________。
(2)(2020·天津卷)Fe、Co、Ni在周期表中的位置为____________________,基
态Fe原子的电子排布式为___________________________________________。
(3)(2019·全国卷Ⅱ)Fe成为阳离子时首先失去________轨道电子,Sm的价层
电子排布式4f66s2,Sm3+价层电子排布式为________。
(4)(2019·全国卷Ⅰ)下列状态的镁中,电离最外层一个电子所需能量最大的是
________(填标号)。
(5)(2018·全国卷Ⅱ)基态 Fe 原子价层电子的轨道表达式(电子排布图)为
___________________________________________________________________。
答案 (1) 1s22s22p63s23p63d24s2或[Ar]3d24s2
(2)第四周期第Ⅷ族 1s22s22p63s23p63d64s2或[Ar]3d64s2
(3)4s 4f5 (4)A (5)
4.(高考组合题)原子核外未成对电子数的判断。(1)(2020·全国Ⅰ)基态Fe2+与Fe3+离子中未成对的电子数之比为________。
(2)(2020·上海等级考)碳原子核外电子中未成对电子数是________。
(3)(2017·全国卷Ⅲ)元素Mn与O中,基态原子核外未成对电子数较多的是
________。
(4)(2016·全国卷Ⅰ)基态Ge原子有________个未成对电子。
(5)(2016·全国卷Ⅱ)镍元素基态原子的3d能级上的未成对电子数为________。
答案 (1)4∶5 (2)2 (3)Mn (4)2 (5)2
5.(高考组合题)电子云图形和电子运动状态的判断。
(1)(2018·全国卷Ⅱ)基态 S 原子电子占据最高能级的电子云轮廓图为
________形。
(2)(2017·全国卷Ⅰ)基态 K 原子中,核外电子占据的最高能层的符号是
________,占据该能层电子的电子云轮廓图形状为________。
(3)(2015·全国卷Ⅰ)处于一定空间运动状态的电子在原子核外出现的概率密
度分布可用________形象化描述。在基态14C原子中,核外存在________对自旋
相反的电子。
答案 (1)哑铃(纺锤) (2)N 球形 (3)电子云 2
一、选择题(每小题只有一个选项符合题意)
1.下列各离子的电子排布式错误的是( )
A.Na+ 1s22s22p6 B.F- 1s22s22p6
C.N3+ 1s22s22p6 D.O2- 1s22s22p6
答案 C
解析 Na+核外电子数为10,其电子排布式为: 1s22s22p6,故A正确;F-,核
外电子总数为10,电子排布式为:1s22s22p6,故B正确; N3+核外含有4个电子,
其电子排布式为:1s22s2,故C错误;O2-电子排布式为: 1s22s22p6,故D正确。
2.(2020·陕西省咸阳市实验中学月考)下列描述原子结构的化学用语正确的
是( )
A.碳原子结构示意图:
B.基态铜原子( Cu)的价层电子排布式:3d94s2
29
C.氧原子核外能量最高的电子云的形状:D.碳原子核外电子的轨道表示式:
答案 C
解析 碳原子结构示意图应该为: ,A错误;基态铜原子( Cu)的价层
29
电子排布式应该为:3d104s1,B错误;氧原子核外能量最高的电子是2p4,p能级电
子云形状为哑铃形,C 正确;碳原子核外电子的轨道表示式应该为:
,D错误。
3.科学家成功合成了一种拥有117个质子的新元素。科学家用Ca轰击Bk,
生成了6个拥有117个质子的新原子,其中的5个原子有176个中子,1个原子有
177个中子。下列有关说法正确的是( )
A.第117号元素是副族元素
B.Bk的质量数为97
C.Ca的中子数为48
D.Ca2+的中子数比核外电子数多10
答案 D
解析 A.第117号元素在元素周期表中的第17列即ⅦA族,为主族元素,A
错误;B.Bk的质子数为97,质量数为249,B错误;C.Ca的质子数为20,质量数为
48,中子数=48-20=28,C错误;D.Ca2+的质子数为20,质量数为48,中子数=
48-20=28,核外电子数=20-2=18,中子数比核外电子数多10,D正确。
4.(2020·山东等级考模拟卷)某元素基态原子4s轨道上有1个电子,则该基
态原子价电子排布不可能是( )
A.3p64s1 B.4s1
C.3d54s1 D.3d104s1
答案 A
解析 A项为 K,核外电子排布式为1s22s22p63s23p64s1,主族元素的价电子
19
是最外层电子,应为4s1,A项错误;B项为 K的价层电子排布式,正确;C项为
19
Cr,副族元素的价电子是最外层电子与次外层的部分电子,核外电子为
24
[Ar]3d54s1,即价电子为3d54s1;D项为 Cu,价电子为3d104s1,3d轨道上的电子处
29
于全充满状态,整个体系的能量最低。
5.(2020·山东模拟)近日,温州大学王舜教授课题组与美国北德克萨斯大学
ZhenhaiXia教授合作在杂原子掺杂碳的超级电容领域取得了新突破。下列C原子轨道表示式表示的状态中能量关系正确的是( )
A.①=②=③=④ B.③>④>①>②
C.②>①>④>③ D.④>③>①=②
答案 C
解析 电子能量为1s<2s<2p,则2p轨道上电子越多、1s、2s轨道上电子越
少,其能量越高,则能量由高到低的顺序是②>①>④>③。
6.工业上通常利用反应2Al O (熔融)=====4Al+3O ↑来获得单质铝,该反应
2 3 2
还需要添加Na [AlF ](冰晶石)以降低氧化铝的熔化温度。下列表示相关微粒的化
3 6
学用语错误的是( )
A.质子数与中子数相等的氟原子:F
B.[AlF ]-的中心离子的结构示意图:
6
C.基态钠原子外围电子排布式:3s1
D.基态氧原子的轨道表示式:
答案 D
解析 A.氟原子质子数为9,则质子数与中子数相等的氟原子质量数为18,
原子符号表示为:F,故A正确;B.铝离子的核外电子数为10,有2个电子层,各层
电子数分别为2、8,铝离子结构示意图为 ,故B正确;C.根据构造原理的能
级顺序,电子大多是按能级顺序填充的,填满一个能级再填一个新能级;11号钠
基态原子的电子排布式为:1s22s22p63s1,其外围电子排布式为:3s1,此状态能量最
低,故C正确;D.由于简并轨道(能级相同的轨道)中电子优先单独占据1个轨道,
且自旋方向相同,原子的能量最低,O原子能量最低排布图为: ,
故D错误。
7.下列各项叙述中,正确的是( )
A.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发
态B.价层电子排布式为6s26p3的元素位于第六周期第ⅢA族,是s区元素
C.所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同
D. Cr原子的电子排布式是1s22s22p63s23p63d44s2
24
答案 C
解析 A 项镁原子由基态转化为激发态时吸收能量;B 项价电子排布为
6s26p3的元素位于第六周期ⅤA族,是p区元素;D项原子轨道处于全空、全满或
半 充 满 状 态 时 , 能 量 最 低 , 故 Cr 原 子 的 核 外 电 子 排 布 式 应 是
24
1s22s22p63s23p63d54s1。
8.(2020·银川一中月考)周期表中27号元素钴的方格中注明“3d74s2”,由此
可以推断( )
A.它位于周期表的第四周期ⅡA族
B.它的基态核外电子排布式可简写为[Ar]4s2
C.Co2+的核外价层电子排布式为3d54s2
D.Co位于周期表中第9列
答案 D
解析 3d74s2为价层电子排布式,可知其位于d区,为过渡元素,A项错误;
“3d74s2”为Co的价电子排布,其简写式中,也要注明3d轨道,B项错误;失电子
时,应失去最外层的电子,即先失4s上的电子,Co2+的价电子排布为3d7,C项错
误;“7+2=9”,说明它位于周期表的第9列,D项正确。
9.下列关于化学用语表示不正确的是( )
A.氮原子的轨道表示式是:
B.镁原子由1s22s22p63s2→ls22s22p63p2时,原子吸收能量,由基态转化成激发
态
C.钾原子的电子排布式是1s22s22p63s23p64s1
D.F元素的电负性小于O元素
答案 D
解析 A.基态氮原子核外电子总数为7,2p轨道3个电子各占据1个轨道,并
且自旋方向相同,故A正确;B.基态Mg的电子排布式为1s22s22p63s2,能量处于最
低状态,当变为ls22s22p63p2时,电子发生跃迁,需要吸收能量,变为激发态,故B
正确;C.钾元素核外有19个电子,根据构造原理书写出基态原子简化电子排布式
为:1s2s22p63s23p64s1,故C正确;D.同周期自左而右电负性增大,故F元素的电负性大于O元素,故D错误。
10.(2020·临沂一模)下列状态的铝元素中,电离最外层的一个电子所需能量
最小的是( )
A.
B.
C.[Ne]
D.
答案 D
解析 AB为基态,其中A失去最外层1个电子,为第三电离能,B失去最外
层1个电子,为第二电离能;C为铝离子,稳定结构,失去最外层1个电子所需能
量最大;D为铝原子的核外电子排布的激发态,易失去最外层的一个电子;所以
电离最外层的一个电子所需能量最小的是D。
11.具有如下电子层结构的原子,其相应元素一定属于同一主族的是( )
A.3p能级上有2个未成对电子的原子和4p能级上有2个未成对电子的原
子
B.3p能级上只有1个空轨道的原子和4p能级上只有1个空轨道的原子
C.最外层电子排布为1s2的原子和最外层电子排布为2s22p6的原子
D.最外层电子排布为1s2的原子和最外层电子排布为2s2的原子
答案 B
解析 当p能级上有2个或者4个电子时,p能级上都有2个未成对电子,所
以相应元素可能是第ⅣA族,也可能是第ⅥA族,故A项不符合题意;p能级上
有3个轨道,当p能级有1个空轨道时,另两个轨道各容纳了1个电子,加上s能
级上的2个电子,最外层为4个电子,所以不管处于哪个能层,只要最外层为4个
电子,就属于第ⅣA族,故B项符合题意;最外层电子排布为1s2的原子是He,最
外层电子排布为2s22p6的原子是Ne,两者均属于0族元素,题干中要求属于同一
主族元素,故C项不符合题意;最外层电子排布为2s2的原子是Be,属于第ⅡA
族,而最外层电子排布为1s2的原子是He,属于0族,故D项也是错误的。
12.原子序数依次增大的X、Y、Z、W四种元素,其中X是形成化合物种类最
多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p
原子轨道上有3个未成对的电子,W的原子序数为29。下列说法正确的是( )A.Y X 分子中Y原子轨道的杂化类型为sp2杂化
2 2
B.化合物YX 的沸点比化合物ZX 的沸点高
4 3
C.W的价层电子排布式为3d94s2
D.Y元素的电负性小于Z元素的电负性
答案 D
解析 由题目条件可以推知这四种元素分别是H、C、N、Cu。Y X 分子根据
2 2
推测出的元素应该是C H 分子,而C H 分子中的C原子的轨道的杂化类型为sp
2 2 2 2
杂化,故A项错误;化合物YX 应该是CH ,化合物ZX 应该是NH 由于NH 分
4 4 3 3 3
子间存在氢键,导致NH 的沸点高于CH 所以化合物YX 的沸点比ZX 低,故B
3 4 4 3
项错误; W是29号铜元素,其价层电子排布式为3d104s1,故C项错误; Y元素
是C元素,Z元素是N元素,电负性:C