文档内容
训练(二十七) 化学能与热能
1.(2020·四川成都期末)下列变化过程,属于放热反应的是( )
①NaOH固体溶于水 ②黑火药的爆炸 ③食物因氧化而腐败 ④铝热反应 ⑤酸碱
中和反应 ⑥煅烧石灰石制生石灰 ⑦盐酸溶液中插入打磨过的铝片
A.②③④⑤⑦ B.①②④⑤
C.②③④⑥ D.①②③⑥⑦
A [NaOH固体溶于水放热,为物理过程,不是放热反应,①错误;黑火药的爆炸为放热
反应,②正确;食物因氧化而腐败,为放热反应,③正确;铝热反应为放热反应,④正确;酸碱
中和反应为放热反应,⑤正确;煅烧石灰石制生石灰为吸热反应,⑥错误;盐酸溶液中插入打
磨过的铝片为放热反应,⑦正确。]
2.(2021·河北秦皇岛检测)下列说法正确的是( )
A.在101 kPa时,1 mol S(s)和2 mol S(s)的燃烧热相等
B.需要加热才能发生的反应一定是吸热反应
C.已知H+(aq)+OH-(aq)===H O(l) ΔH=-57.3 kJ·mol-1,则稀HSO 溶液和稀
2 2 4
Ba(OH) 溶液反应的反应热ΔH>2×(-57.3)kJ·mol-1
2
D.已知2C(s)+2O(g)===2CO (g) ΔH=a kJ·mol-1,2C(s)+O(g)===2CO(g) ΔH=b
2 2 2
kJ·mol-1,则b>0>a
A [燃烧热与物质的物质的量多少无关,所以在25 ℃、101 kPa下,1 mol 硫和2 mol硫
燃烧热相等, A项正确;反应热与反应条件无关,如铝热反应为放热反应,但需在高温下进
行,B项错误;稀HSO 溶液和稀Ba(OH) 溶液反应生成水和BaSO 沉淀,生成硫酸钡沉淀会
2 4 2 4
放出热量,则ΔH<2×(-57.3)kJ·mol-1,C项错误;C的燃烧为放热反应,完全燃烧放出的能
量多,则0>b>a,D项错误。]
3.(2021·河南焦作检测)等物质的量的CH===CHCH===CH 与HBr加成生成两种主要
2 2
产物X、Y的能量与反应进程如下图所示:
下列说法正确的是( )
A.产物Y比产物X更稳定
B.CH===CHCH===CH +HBr―→W的过程放出能量
2 2
C.W→X正反应的活化能比W→Y正反应的活化能大D.CH===CHCH===CH +HBr―→W的速率比W→X(或Y)的快
2 2
A [物质的能量越低越稳定,则产物 Y 比产物 X 更稳定,A 项正确;
CH===CHCH===CH 与HBr的总能量比W的总能量低,为吸热反应,B项错误;由图可知
2 2
W→X正反应的活化能小,W→Y正反应的活化能大,C项错误;活化能越小,反应速率越快,
则CH===CHCH===CH +HBr→W的速率比W→X(或Y)的慢,D项错误。]
2 2
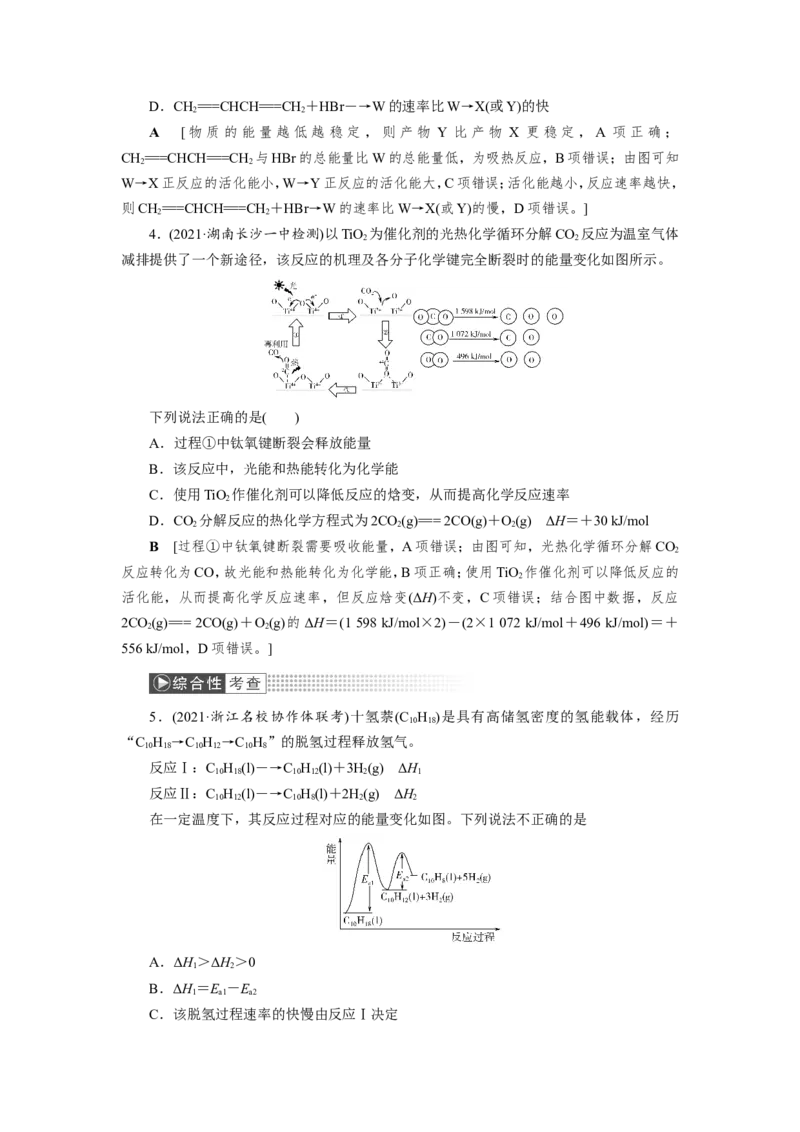
4.(2021·湖南长沙一中检测)以TiO 为催化剂的光热化学循环分解CO 反应为温室气体
2 2
减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
下列说法正确的是( )
A.过程①中钛氧键断裂会释放能量
B.该反应中,光能和热能转化为化学能
C.使用TiO 作催化剂可以降低反应的焓变,从而提高化学反应速率
2
D.CO 分解反应的热化学方程式为2CO(g)=== 2CO(g)+O(g) ΔH=+30 kJ/mol
2 2 2
B [过程①中钛氧键断裂需要吸收能量,A项错误;由图可知,光热化学循环分解CO
2
反应转化为CO,故光能和热能转化为化学能,B项正确;使用TiO 作催化剂可以降低反应的
2
活化能,从而提高化学反应速率,但反应焓变(ΔH)不变,C项错误;结合图中数据,反应
2CO(g)=== 2CO(g)+O(g)的ΔH=(1 598 kJ/mol×2)-(2×1 072 kJ/mol+496 kJ/mol)=+
2 2
556 kJ/mol,D项错误。]
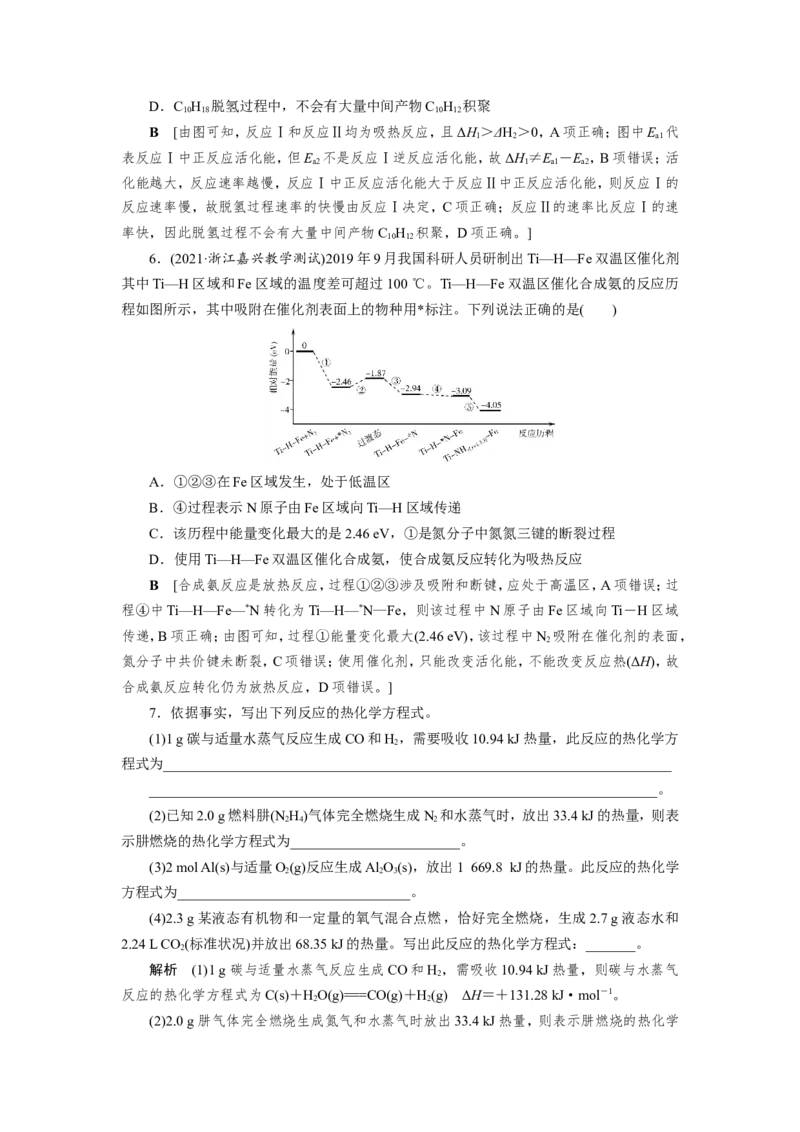
5.(2021·浙江名校协作体联考)十氢萘(C H )是具有高储氢密度的氢能载体,经历
10 18
“C H →C H →C H”的脱氢过程释放氢气。
10 18 10 12 10 8
反应Ⅰ:C H (l)―→C H (l)+3H(g) ΔH
10 18 10 12 2 1
反应Ⅱ:C H (l)―→C H(l)+2H(g) ΔH
10 12 10 8 2 2
在一定温度下,其反应过程对应的能量变化如图。下列说法不正确的是
A.ΔH>ΔH>0
1 2
B.ΔH=E -E
1 a1 a2
C.该脱氢过程速率的快慢由反应Ⅰ决定D.C H 脱氢过程中,不会有大量中间产物C H 积聚
10 18 10 12
B [由图可知,反应Ⅰ和反应Ⅱ均为吸热反应,且ΔH>ΔH>0,A项正确;图中E 代
1 2 a1
表反应Ⅰ中正反应活化能,但E 不是反应Ⅰ逆反应活化能,故ΔH≠E -E ,B项错误;活
a2 1 a1 a2
化能越大,反应速率越慢,反应Ⅰ中正反应活化能大于反应Ⅱ中正反应活化能,则反应Ⅰ的
反应速率慢,故脱氢过程速率的快慢由反应Ⅰ决定,C项正确;反应Ⅱ的速率比反应Ⅰ的速
率快,因此脱氢过程不会有大量中间产物C H 积聚,D项正确。]
10 12
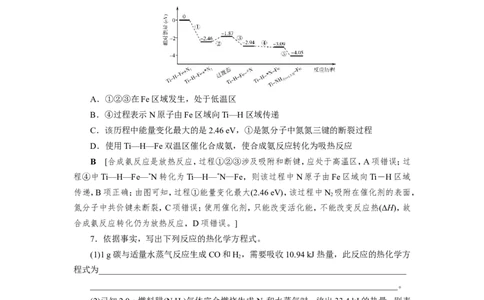
6.(2021·浙江嘉兴教学测试)2019年9月我国科研人员研制出Ti—H—Fe双温区催化剂
其中Ti—H区域和Fe区域的温度差可超过100 ℃。Ti—H—Fe双温区催化合成氨的反应历
程如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是( )
A.①②③在Fe区域发生,处于低温区
B.④过程表示N原子由Fe区域向Ti—H区域传递
C.该历程中能量变化最大的是2.46 eV,①是氮分子中氮氮三键的断裂过程
D.使用Ti—H—Fe双温区催化合成氨,使合成氨反应转化为吸热反应
B [合成氨反应是放热反应,过程①②③涉及吸附和断键,应处于高温区,A项错误;过
程④中Ti—H—Fe—*N转化为Ti—H—*N—Fe,则该过程中N原子由Fe区域向Ti-H区域
传递,B项正确;由图可知,过程①能量变化最大(2.46 eV),该过程中N 吸附在催化剂的表面,
2
氮分子中共价键未断裂,C项错误;使用催化剂,只能改变活化能,不能改变反应热(ΔH),故
合成氨反应转化仍为放热反应,D项错误。]
7.依据事实,写出下列反应的热化学方程式。
(1)1 g碳与适量水蒸气反应生成CO和H,需要吸收10.94 kJ 热量,此反应的热化学方
2
程式为________________________________________________________________________
________________________________________________________________________。
(2)已知2.0 g燃料肼(N H)气体完全燃烧生成N 和水蒸气时,放出33.4 kJ的热量,则表
2 4 2
示肼燃烧的热化学方程式为________________________。
(3)2 mol Al(s)与适量O(g)反应生成Al O(s),放出1 669.8 kJ的热量。此反应的热化学
2 2 3
方程式为_________________________________。
(4)2.3 g某液态有机物和一定量的氧气混合点燃,恰好完全燃烧,生成2.7 g液态水和
2.24 L CO(标准状况)并放出68.35 kJ的热量。写出此反应的热化学方程式:_______。
2
解析 (1)1 g 碳与适量水蒸气反应生成CO和H,需吸收10.94 kJ热量,则碳与水蒸气
2
反应的热化学方程式为C(s)+HO(g)===CO(g)+H(g) ΔH=+131.28 kJ·mol-1。
2 2
(2)2.0 g 肼气体完全燃烧生成氮气和水蒸气时放出33.4 kJ热量,则表示肼燃烧的热化学方程式为NH(g)+O(g)===N (g)+2HO(g) ΔH=-534.4 kJ·mol-1。
2 4 2 2 2
(3)2 mol Al(s)与适量O(g)反应生成Al O(s),放出1 669.8 kJ的热量,则此反应的热化
2 2 3
学方程式为4Al(s)+3O(g)===2AlO(s) ΔH=-1 669.8 kJ·mol-1×2=-3 339.6 kJ·mol-1。
2 2 3
(4)通过燃烧的产物可知该有机物中肯定含有碳元素和氢元素,可能含有氧元素。n(H O)
2
==0.15 mol,n(H)=0.3 mol,m(H)=0.3 g,n(CO)==0.1 mol,n(C)=0.1 mol,m(C)=1.2 g,
2
则碳元素和氢元素的质量之和是0.3 g+1.2 g=1.5 g<2.3 g,故该有机物中还含有氧元素,氧
元素的质量是2.3 g-1.5 g=0.8 g,n(O)=0.05 mol,从而可确定该有机物的分子式为C HO,
2 6
该液态有机物为 C HOH,故该反应的热化学方程式为 C HOH(l)+3O(g)===2CO (g)+
2 5 2 5 2 2
3HO(l) ΔH=-1 367 kJ·mol-1。
2
答案 (1)C(s)+HO(g)===CO(g)+H(g)ΔH=+131.28 kJ·mol-1
2 2
(2)N H(g)+O(g)===N (g)+2HO(g)ΔH=-534.4 kJ·mol-1
2 4 2 2 2
(3)4Al(s)+3O(g)===2AlO(s)ΔH=-3 339.6 kJ·mol-1
2 2 3
(4)C HOH(l)+3O(g)===2CO (g)+3HO(l)ΔH=-1 367 kJ·mol-1
2 5 2 2 2