文档内容
训练(十二) 钠及其重要化合物
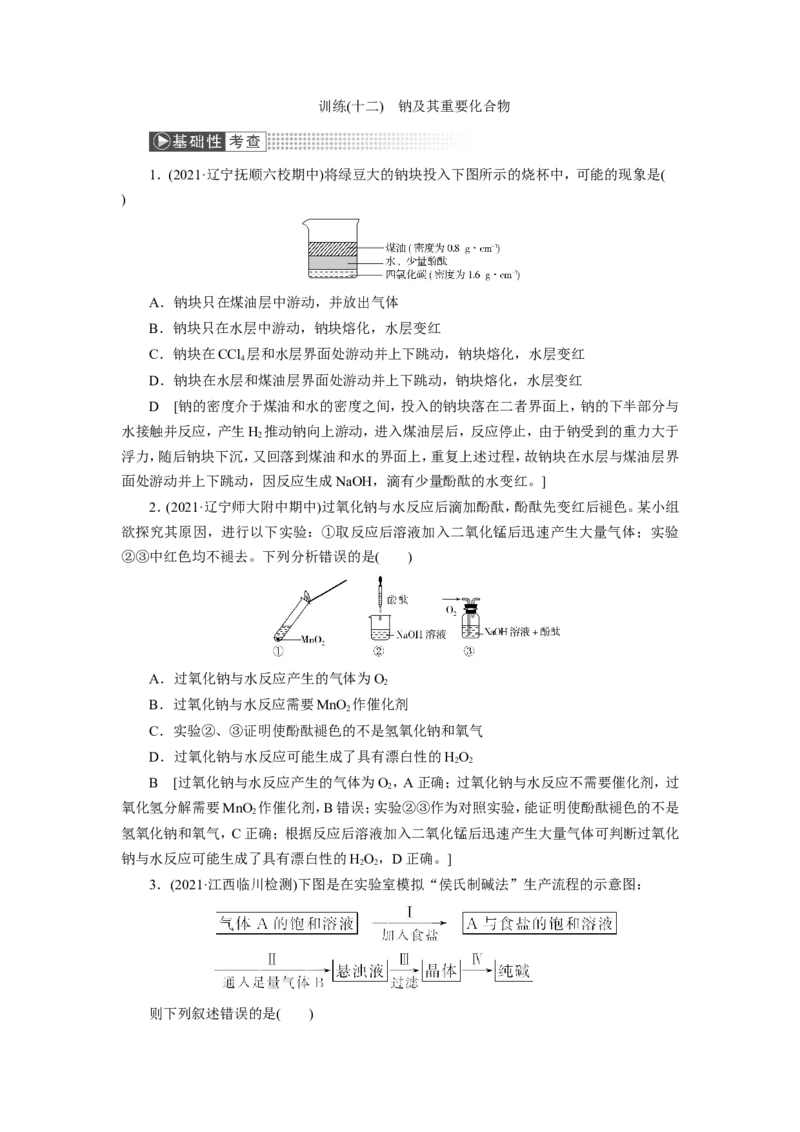
1.(2021·辽宁抚顺六校期中)将绿豆大的钠块投入下图所示的烧杯中,可能的现象是(
)
A.钠块只在煤油层中游动,并放出气体
B.钠块只在水层中游动,钠块熔化,水层变红
C.钠块在CCl 层和水层界面处游动并上下跳动,钠块熔化,水层变红
4
D.钠块在水层和煤油层界面处游动并上下跳动,钠块熔化,水层变红
D [钠的密度介于煤油和水的密度之间,投入的钠块落在二者界面上,钠的下半部分与
水接触并反应,产生H 推动钠向上游动,进入煤油层后,反应停止,由于钠受到的重力大于
2
浮力,随后钠块下沉,又回落到煤油和水的界面上,重复上述过程,故钠块在水层与煤油层界
面处游动并上下跳动,因反应生成NaOH,滴有少量酚酞的水变红。]
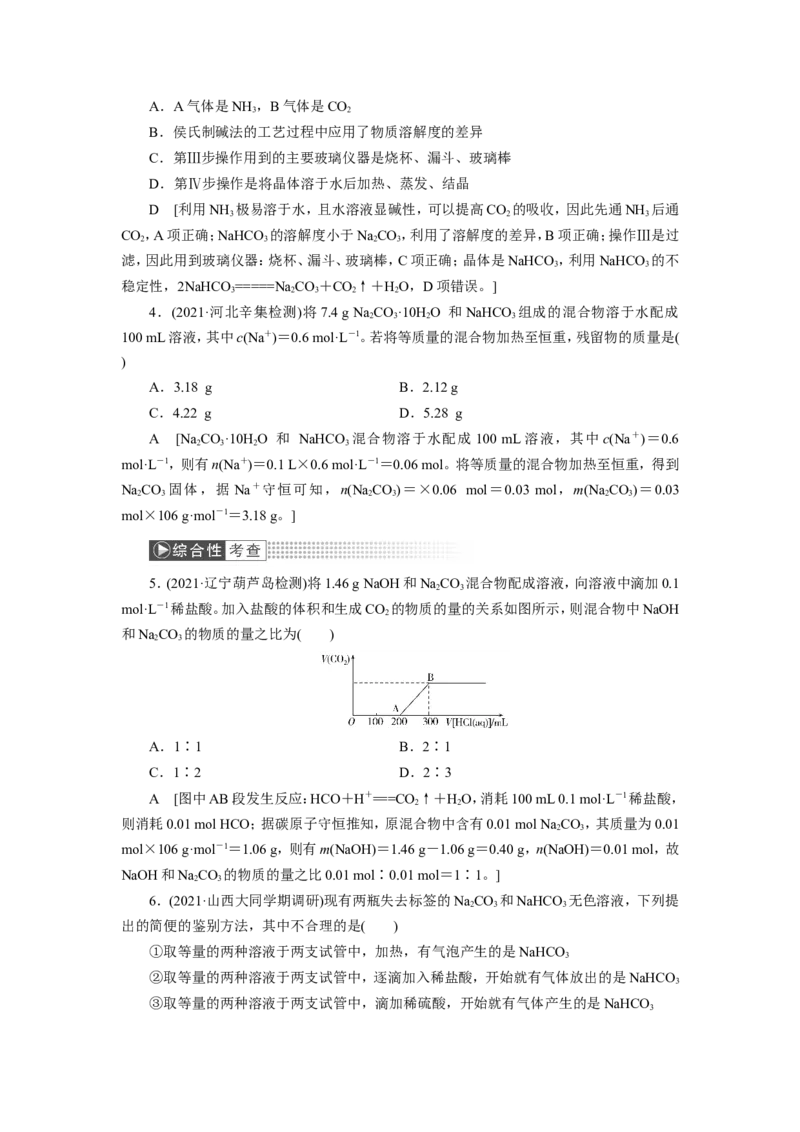
2.(2021·辽宁师大附中期中)过氧化钠与水反应后滴加酚酞,酚酞先变红后褪色。某小组
欲探究其原因,进行以下实验:①取反应后溶液加入二氧化锰后迅速产生大量气体;实验
②③中红色均不褪去。下列分析错误的是( )
A.过氧化钠与水反应产生的气体为O
2
B.过氧化钠与水反应需要MnO 作催化剂
2
C.实验②、③证明使酚酞褪色的不是氢氧化钠和氧气
D.过氧化钠与水反应可能生成了具有漂白性的HO
2 2
B [过氧化钠与水反应产生的气体为O,A正确;过氧化钠与水反应不需要催化剂,过
2
氧化氢分解需要MnO 作催化剂,B错误;实验②③作为对照实验,能证明使酚酞褪色的不是
2
氢氧化钠和氧气,C正确;根据反应后溶液加入二氧化锰后迅速产生大量气体可判断过氧化
钠与水反应可能生成了具有漂白性的HO,D正确。]
2 2
3.(2021·江西临川检测)下图是在实验室模拟“侯氏制碱法”生产流程的示意图:
则下列叙述错误的是( )A.A气体是NH ,B气体是CO
3 2
B.侯氏制碱法的工艺过程中应用了物质溶解度的差异
C.第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D.第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶
D [利用NH 极易溶于水,且水溶液显碱性,可以提高CO 的吸收,因此先通NH 后通
3 2 3
CO,A项正确;NaHCO 的溶解度小于NaCO,利用了溶解度的差异,B项正确;操作Ⅲ是过
2 3 2 3
滤,因此用到玻璃仪器:烧杯、漏斗、玻璃棒,C项正确;晶体是NaHCO ,利用NaHCO 的不
3 3
稳定性,2NaHCO =====NaCO+CO↑+HO,D项错误。]
3 2 3 2 2
4.(2021·河北辛集检测)将7.4 g Na CO·10H O 和NaHCO 组成的混合物溶于水配成
2 3 2 3
100 mL溶液,其中c(Na+)=0.6 mol·L-1。若将等质量的混合物加热至恒重,残留物的质量是(
)
A.3.18 g B.2.12 g
C.4.22 g D.5.28 g
A [Na CO·10H O 和 NaHCO 混合物溶于水配成 100 mL溶液,其中c(Na+)=0.6
2 3 2 3
mol·L-1,则有n(Na+)=0.1 L×0.6 mol·L-1=0.06 mol。将等质量的混合物加热至恒重,得到
NaCO 固体,据 Na+守恒可知,n(Na CO)=×0.06 mol=0.03 mol,m(Na CO)=0.03
2 3 2 3 2 3
mol×106 g·mol-1=3.18 g。]
5.(2021·辽宁葫芦岛检测)将1.46 g NaOH和NaCO 混合物配成溶液,向溶液中滴加0.1
2 3
mol·L-1稀盐酸。加入盐酸的体积和生成CO 的物质的量的关系如图所示,则混合物中NaOH
2
和NaCO 的物质的量之比为( )
2 3
A.1∶1 B.2∶1
C.1∶2 D.2∶3
A [图中AB段发生反应:HCO+H+===CO ↑+HO,消耗100 mL 0.1 mol·L-1稀盐酸,
2 2
则消耗0.01 mol HCO;据碳原子守恒推知,原混合物中含有0.01 mol Na CO,其质量为0.01
2 3
mol×106 g·mol-1=1.06 g,则有m(NaOH)=1.46 g-1.06 g=0.40 g,n(NaOH)=0.01 mol,故
NaOH和NaCO 的物质的量之比0.01 mol∶0.01 mol=1∶1。]
2 3
6.(2021·山西大同学期调研)现有两瓶失去标签的NaCO 和NaHCO 无色溶液,下列提
2 3 3
出的简便的鉴别方法,其中不合理的是( )
①取等量的两种溶液于两支试管中,加热,有气泡产生的是NaHCO
3
②取等量的两种溶液于两支试管中,逐滴加入稀盐酸,开始就有气体放出的是NaHCO
3
③取等量的两种溶液于两支试管中,滴加稀硫酸,开始就有气体产生的是NaHCO
3④取等量的两种溶液于两支试管中,滴加Ba(OH) 溶液,生成白色沉淀是NaCO
2 2 3
A.①② B.②③
C.③④ D.①④
D [NaHCO 在水中受热不易分解,加热NaCO 和NaHCO 溶液,溶液中溶解的气体随
3 2 3 3
温度升高而逸出,均产生气泡,①错误;NaHCO 与盐酸反应生成NaCl、CO 和HO,而
3 2 2
NaCO 溶液中滴加盐酸,先生成NaHCO ,再与盐酸反应放出CO,故开始就有气体放出的
2 3 3 2
是NaHCO ,②正确;NaCO 和NaHCO 溶液与Ba(OH) 溶液反应,均产生白色沉淀BaCO ,
3 2 3 3 2 3
④错误。]
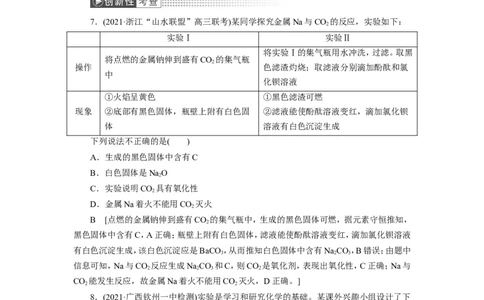
7.(2021·浙江“山水联盟”高三联考)某同学探究金属Na与CO 的反应,实验如下:
2
实验Ⅰ 实验Ⅱ
将实验Ⅰ的集气瓶用水冲洗,过滤。取黑
将点燃的金属钠伸到盛有CO 的集气瓶
2
操作 色滤渣灼烧;取滤液分别滴加酚酞和氯
中
化钡溶液
①火焰呈黄色 ①黑色滤渣可燃
现象 ②底部有黑色固体,瓶壁上附有白色固 ②滤液能使酚酞溶液变红,滴加氯化钡
体 溶液有白色沉淀生成
下列说法不正确的是( )
A.生成的黑色固体中含有C
B.白色固体是NaO
2
C.实验说明CO 具有氧化性
2
D.金属Na着火不能用CO 灭火
2
B [点燃的金属钠伸到盛有CO 的集气瓶中,生成的黑色固体可燃,据元素守恒推知,
2
黑色固体中含有C,A正确;瓶壁上附有白色固体,滤液能使酚酞溶液变红,滴加氯化钡溶液
有白色沉淀生成,该白色沉淀应是BaCO ,从而推知白色固体中含有NaCO,B错误;由题中
3 2 3
信息可知,Na与CO 反应生成NaCO 和C,则CO 是氧化剂,表现出氧化性,C正确;Na与
2 2 3 2
CO 能发生反应,故金属Na着火不能用CO 灭火,D正确。]
2 2
8.(2021·广西钦州一中检测)实验是学习和研究化学的基础。某课外兴趣小组设计了下
列装置,验证二氧化碳与过氧化钠反应时需要有水存在。
回答下列问题:
Ⅰ.二氧化碳的制备及纯化:(1)装置①中反应的离子方程式是_________________________________。
(2)装置②中的试剂是________________;装置③中的试剂是______________。
Ⅱ.实验验证:
步骤1:打开阀门K,关闭K,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
2 1
步骤2:打开阀门K,关闭K,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
1 2
(3)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是____________。
(4)过氧化钠与二氧化碳反应的化学方程式为__________________________________。
Ⅲ.实验反思:
(5)有同学提出质疑:“上述实验不足以证明有水存在时过氧化钠与二氧化碳发生了化
学反应,”其理由是_________________________________。
解析 (2)装置①中CaCO 与盐酸反应制备CO,混有HCl、HO(g)杂质,装置②中盛有
3 2 2
饱和NaHCO 溶液,用于除去HCl;装置③中盛有浓硫酸,用于除去HO(g)。
3 2
(3)步骤1中打开K,关闭K,CO 通过浓硫酸除去HO(g),干燥CO 进入④中NaO 中,
2 1 2 2 2 2 2
不发生反应,故a处带火星木条不复燃。步骤2中打开K,关闭K,CO 和HO(g)都能进入③
1 2 2 2
中NaO,发生反应生成O,过量CO 被⑥中碱石灰吸收,故a处带火星木条复燃。
2 2 2 2
(4)对比步骤1和步骤2中实验现象,HO(g)影响NaO 和CO 的反应,结合原子守恒写
2 2 2 2
出化学方程式:2NaO+2CO=====2NaCO+O。
2 2 2 2 3 2
(5)H O(g)与NaO 反应产生O,也能使带火星木条复燃,故不足以证明水存在下NaO
2 2 2 2 2 2
与CO 发生了反应。
2
答案 (1)CaCO+2H+===Ca2++HO+CO↑
3 2 2
(2)饱和NaHCO 溶液 浓硫酸
3
(3)步骤1中木条不复燃,步骤2中木条复燃
(4)2Na O+2CO=====2NaCO+O
2 2 2 2 3 2
(5)气体中的水可与NaO 反应产生O
2 2 2