文档内容
(一)溶液中粒子浓度关系
1.单一溶液
(1)Na S溶液
2
水解方程式:____________________________________________________________________;
离子浓度大小关系:_____________________________________________________________;
电荷守恒:_____________________________________________________________________;
物料守恒:__________________________________________________________________;
质子守恒:___________________________________________________________________。
(2)NaHS溶液
水解方程式:___________________________________________________________________;
离子浓度大小关系:______________________________________________________________;
电荷守恒:_____________________________________________________________________;
物料守恒:__________________________________________________________________;
质子守恒:___________________________________________________________________。
2.混合溶液
(1)1∶1的CHCOOH、CHCOONa溶液
3 3
水解方程式:___________________________________________________________________;
离子浓度大小关系:______________________________________________________________;
电荷守恒:______________________________________________________________________;
物料守恒:__________________________________________________________________;
质子守恒:____________________________________________________________________。
(2)CH COOH、CHCOONa混合呈中性溶液
3 3
离子浓度大小关系:______________________________________________________________;
电荷守恒:______________________________________________________________________;
物料守恒:________________________________________________________________。
(3)常温下pH=2的CHCOOH与pH=12的NaOH等体积混合的溶液
3
离子浓度大小关系:______________________________________________________________;
电荷守恒:___________________________________________________________________。
(二)滴定曲线的分析与应用
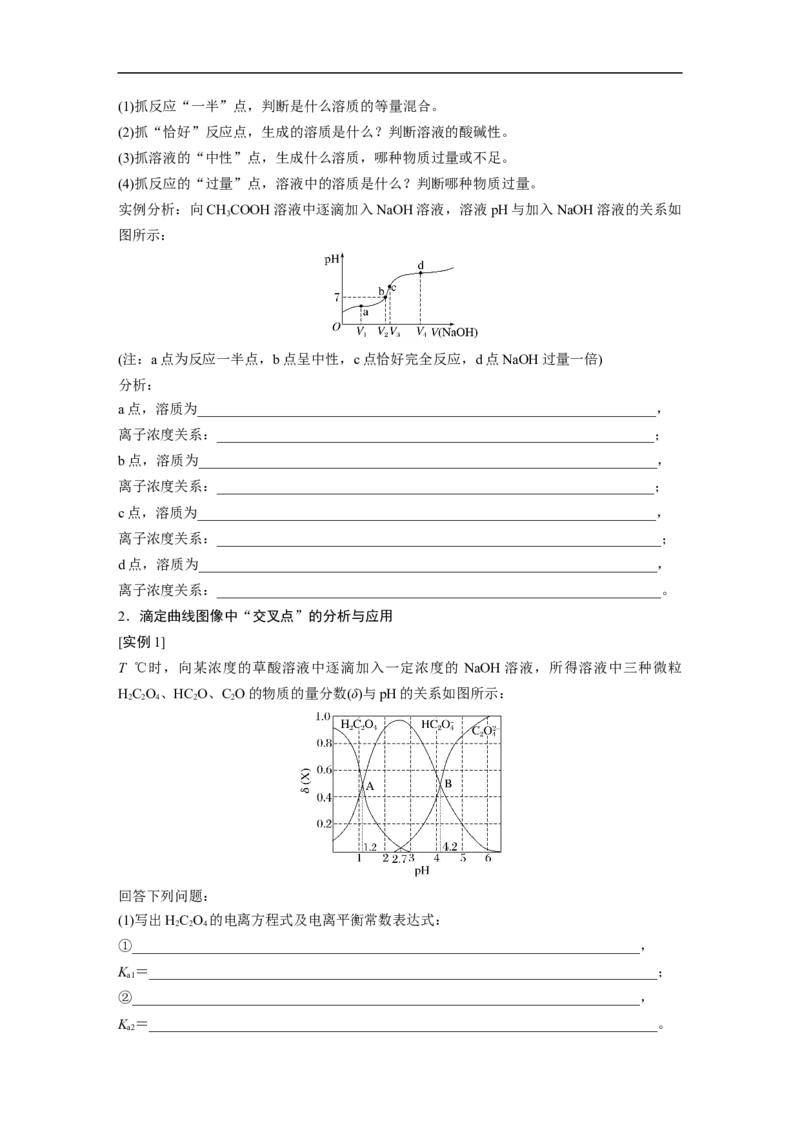
1.巧抓“四点”,突破溶液中的粒子浓度关系(1)抓反应“一半”点,判断是什么溶质的等量混合。
(2)抓“恰好”反应点,生成的溶质是什么?判断溶液的酸碱性。
(3)抓溶液的“中性”点,生成什么溶质,哪种物质过量或不足。
(4)抓反应的“过量”点,溶液中的溶质是什么?判断哪种物质过量。
实例分析:向CHCOOH溶液中逐滴加入NaOH溶液,溶液pH与加入NaOH溶液的关系如
3
图所示:
(注:a点为反应一半点,b点呈中性,c点恰好完全反应,d点NaOH过量一倍)
分析:
a点,溶质为_________________________________________________________________,
离子浓度关系:______________________________________________________________;
b点,溶质为_________________________________________________________________,
离子浓度关系:______________________________________________________________;
c点,溶质为_________________________________________________________________,
离子浓度关系:_______________________________________________________________;
d点,溶质为_________________________________________________________________,
离子浓度关系:_______________________________________________________________。
2.滴定曲线图像中“交叉点”的分析与应用
[实例1]
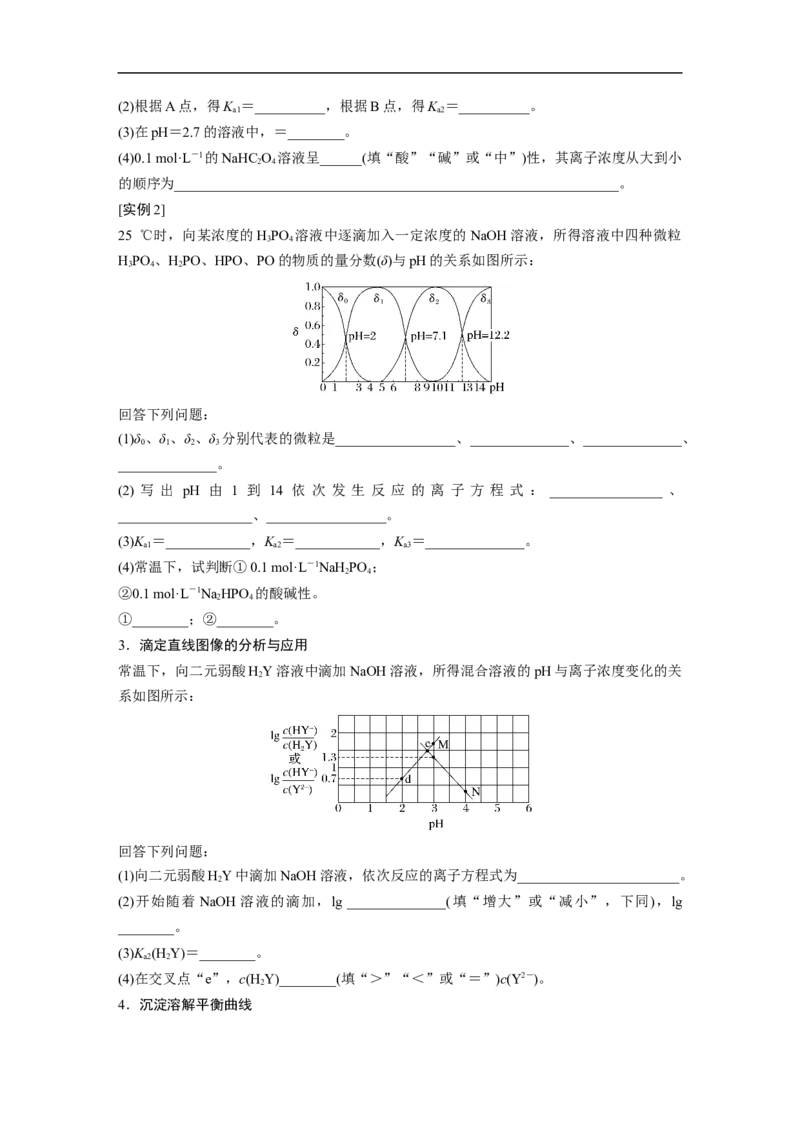
T ℃时,向某浓度的草酸溶液中逐滴加入一定浓度的 NaOH溶液,所得溶液中三种微粒
HC O、HC O、C O的物质的量分数(δ)与pH的关系如图所示:
2 2 4 2 2
回答下列问题:
(1)写出HC O 的电离方程式及电离平衡常数表达式:
2 2 4
①________________________________________________________________________,
K =________________________________________________________________________;
a1
②________________________________________________________________________,
K =________________________________________________________________________。
a2(2)根据A点,得K =__________,根据B点,得K =__________。
a1 a2
(3)在pH=2.7的溶液中,=________。
(4)0.1 mol·L-1的NaHC O 溶液呈______(填“酸”“碱”或“中”)性,其离子浓度从大到小
2 4
的顺序为_______________________________________________________________。
[实例2]
25 ℃时,向某浓度的HPO 溶液中逐滴加入一定浓度的NaOH溶液,所得溶液中四种微粒
3 4
HPO 、HPO、HPO、PO的物质的量分数(δ)与pH的关系如图所示:
3 4 2
回答下列问题:
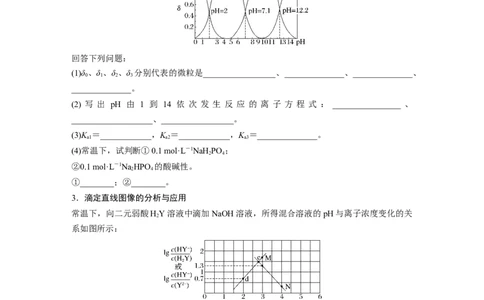
(1)δ 、δ 、δ 、δ 分别代表的微粒是_________________、______________、______________、
0 1 2 3
______________。
(2) 写 出 pH 由 1 到 14 依 次 发 生 反 应 的 离 子 方 程 式 : ________________ 、
___________________、_________________。
(3)K =____________,K =____________,K =______________。
a1 a2 a3
(4)常温下,试判断①0.1 mol·L-1NaH PO ;
2 4
②0.1 mol·L-1NaHPO 的酸碱性。
2 4
①________;②________。
3.滴定直线图像的分析与应用
常温下,向二元弱酸HY溶液中滴加NaOH溶液,所得混合溶液的pH与离子浓度变化的关
2
系如图所示:
回答下列问题:
(1)向二元弱酸HY中滴加NaOH溶液,依次反应的离子方程式为_______________________。
2
(2)开始随着NaOH溶液的滴加,lg ______________(填“增大”或“减小”,下同),lg
________。
(3)K (H Y)=________。
a2 2
(4)在交叉点“e”,c(H Y)________(填“>”“<”或“=”)c(Y2-)。
2
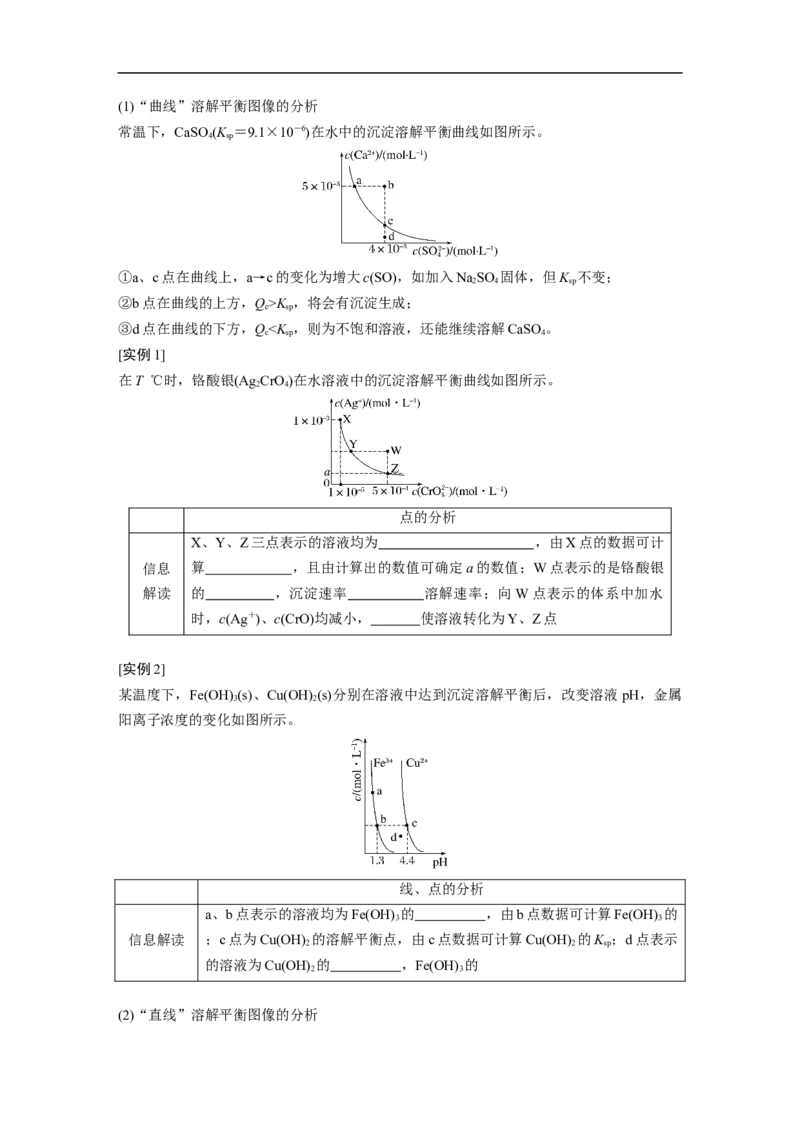
4.沉淀溶解平衡曲线(1)“曲线”溶解平衡图像的分析
常温下,CaSO(K =9.1×10-6)在水中的沉淀溶解平衡曲线如图所示。
4 sp
①a、c点在曲线上,a→c的变化为增大c(SO),如加入NaSO 固体,但K 不变;
2 4 sp
②b点在曲线的上方,Q>K ,将会有沉淀生成;
c sp
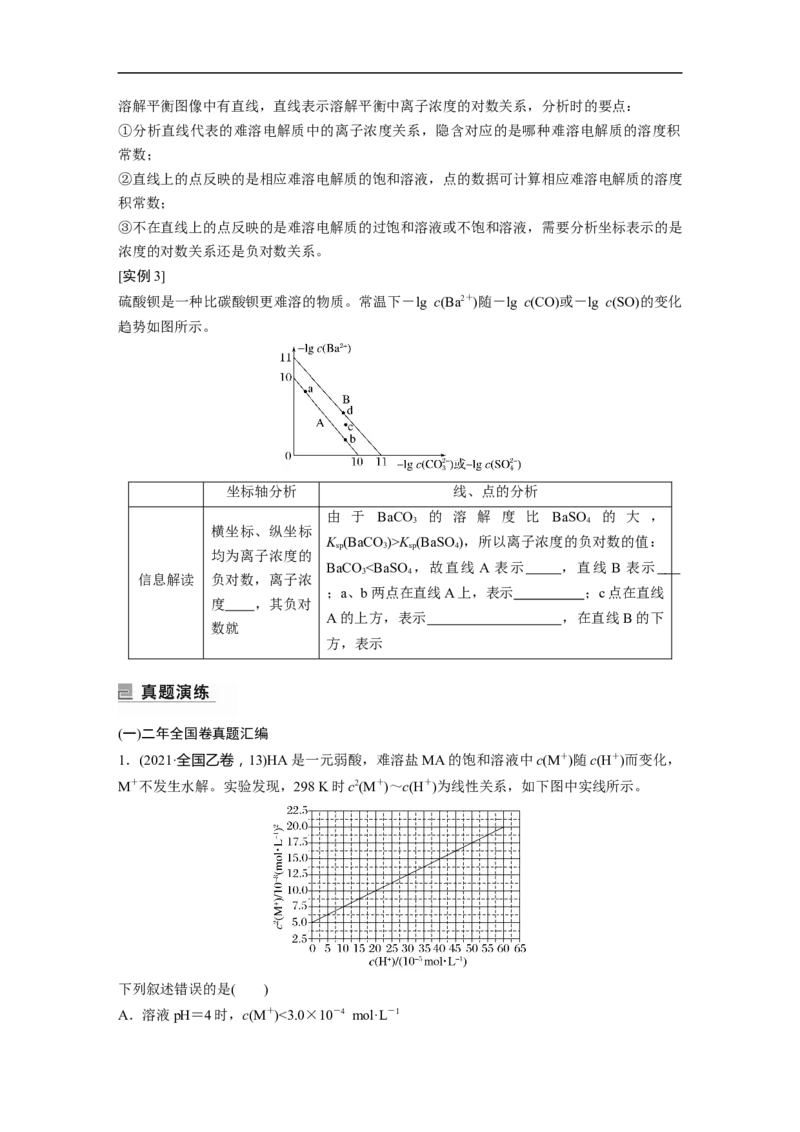
③d点在曲线的下方,QK (BaSO),所以离子浓度的负对数的值:
sp 3 sp 4
均为离子浓度的
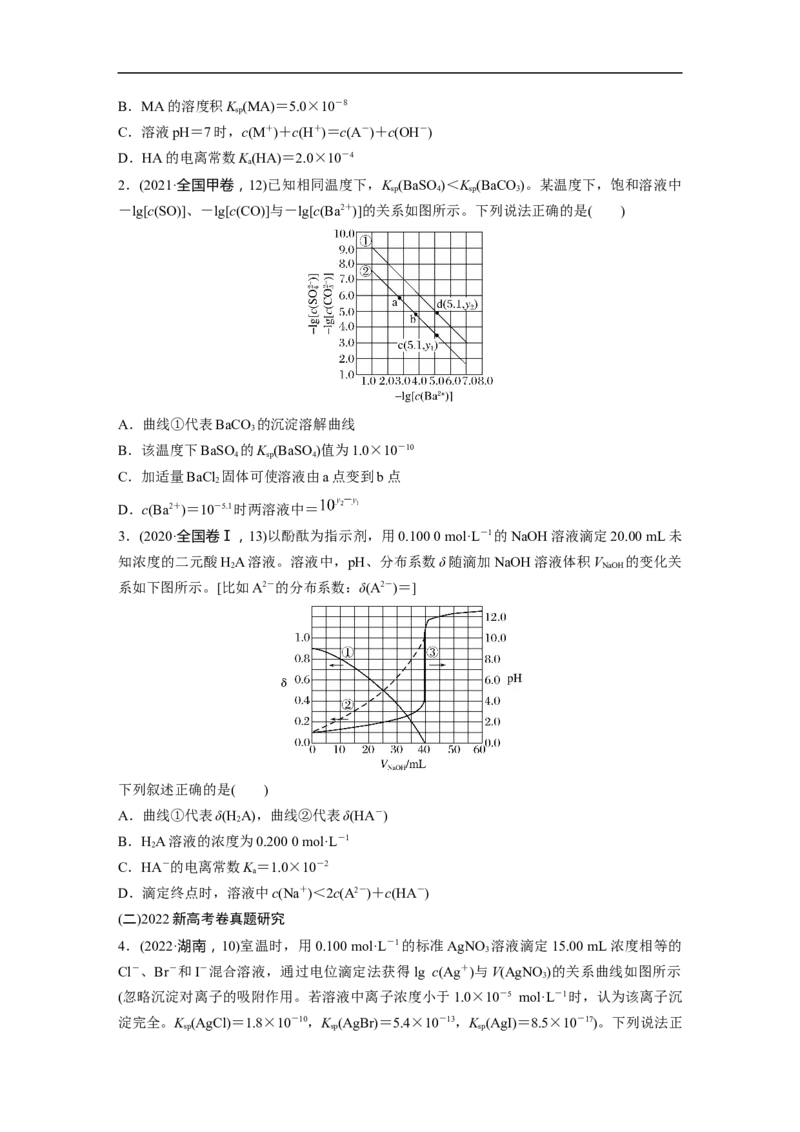
BaCO c(Br-)>c(I-)>c(Ag+)
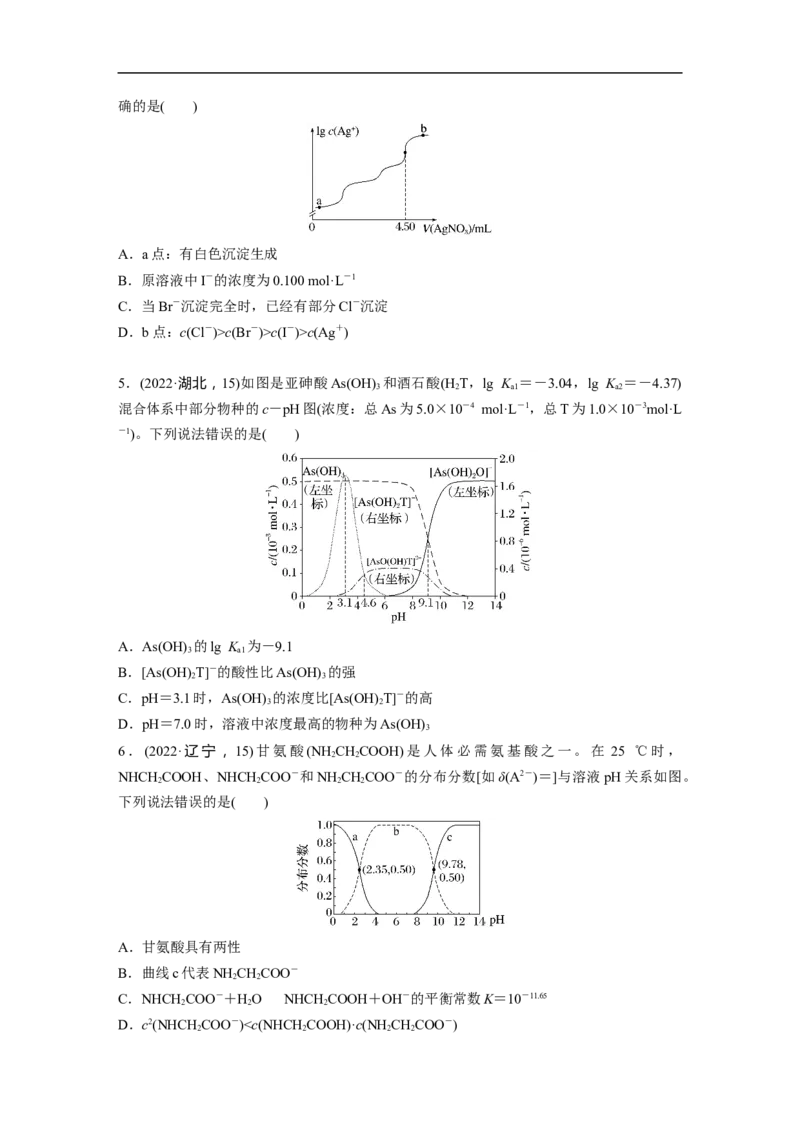
5.(2022·湖北,15)如图是亚砷酸As(OH) 和酒石酸(H T,lg K =-3.04,lg K =-4.37)
3 2 a1 a2
混合体系中部分物种的c-pH图(浓度:总As为5.0×10-4 mol·L-1,总T为1.0×10-3mol·L
-1)。下列说法错误的是( )
A.As(OH) 的lg K 为-9.1
3 a1
B.[As(OH) T]-的酸性比As(OH) 的强
2 3
C.pH=3.1时,As(OH) 的浓度比[As(OH) T]-的高
3 2
D.pH=7.0时,溶液中浓度最高的物种为As(OH)
3
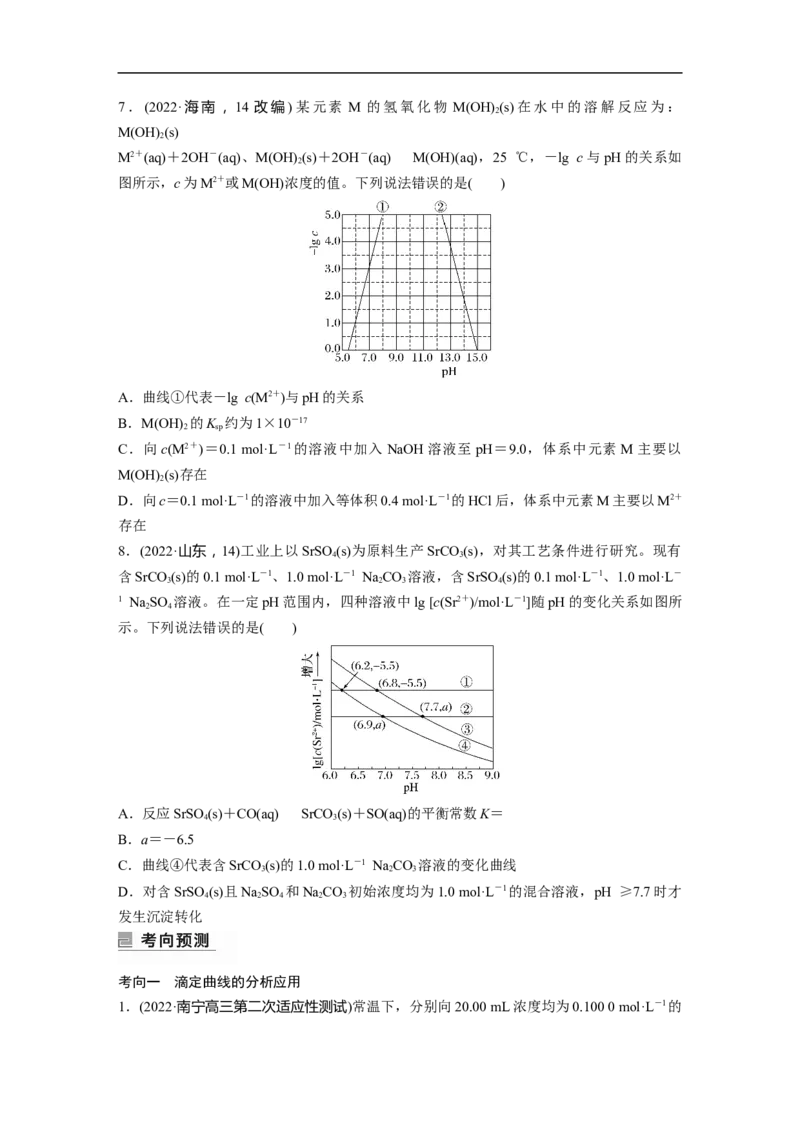
6.(2022·辽宁,15)甘氨酸(NH CHCOOH)是人体必需氨基酸之一。在 25 ℃时,
2 2
NHCH COOH、NHCH COO-和NH CHCOO-的分布分数[如δ(A2-)=]与溶液pH关系如图。
2 2 2 2
下列说法错误的是( )
A.甘氨酸具有两性
B.曲线c代表NH CHCOO-
2 2
C.NHCH COO-+HONHCH COOH+OH-的平衡常数K=10-11.65
2 2 2
D.c2(NHCHCOO-)