文档内容
第 22 讲 水的电离与溶液的 pH
1.认识水的电离,了解水的离子积常数,认识溶液的酸碱性及pH,掌握检测溶液pH的方法。
2.能进行溶液pH的简单计算,能正确测定溶液的pH,能调控溶液的酸、碱性。能选择实例说明溶
液pH的调控在工农业生产和科学研究中的重要作用。
【核心素养分析】
1.变化观念与平衡思想:认识水的电离有一定限度,是可以调控的。能多角度、动态地分析水的电离,
并运用平衡移动原理解决实际问题。
2.科学研究与创新意识:能发现并提出酸碱中和滴定中有探究价值的问题;能从问题和假设出发,确
定探究目的,设计探究方案,进行实验探究;在探究过程中学会合作,面对“异常”现象敢于提出自己的
见解,进行误差分析。
3.证据推理与模型认知:能从定性和定量上收集证据,能通过定性分析和定量计算推出合理的结论;
能运用pH计算模型进行pH的简单计算。
知识点一 水的电离与水的离子积常数
1.水的电离
水是极弱的电解质,水的电离方程式为HO+HO HO++OH-或HO H++OH-。
2 2 3 2
2.水的离子积常数
K =c(H+)·c(OH-)。
w
(1)室温下:K =1×10-14。
w
(2)影响因素:只与温度有关,升高温度,K 增大。
w
(3)适用范围:K 不仅适用于纯水,也适用于稀的电解质水溶液。
w
(4)K 揭示了在任何水溶液中均存在H+和OH-,只要温度不变,K 不变。
w w
3.影响水电离平衡的因素
体系变化
平衡移动方向 K 水的电离程度 c(OH-) c(H+)
w
条件
HCl 逆 不变 减小 减小 增大
NaOH 逆 不变 减小 增大 减小NaCO 正 不变 增大 增大 减小
2 3
可水解的盐
NH Cl 正 不变 增大 减小 增大
4
升温 正 增大 增大 增大 增大
温度
降温 逆 减小 减小 减小 减小
其他:如加入Na 正 不变 增大 增大 减小
知识点二 溶液的酸碱性和pH
1.溶液的酸碱性
溶液的酸碱性取决于溶液中c(H+)和c(OH-)的相对大小。
(1)酸性溶液:c(H+)>c(OH-),常温下,pH<7。
(2)中性溶液:c(H+)=c(OH-),常温下,pH=7。
(3)碱性溶液:c(H+)7。
2.pH及其测量
(1)计算公式:pH=-lg c(H+)。
(2)测量方法
①pH试纸法
用镊子夹取一小块试纸放在洁净的玻璃片或表面皿上,用玻璃棒蘸取待测液点在试纸的中央,变色后
与标准比色卡对照,即可确定溶液的pH。
②pH计测量法
(3)溶液的酸碱性与pH的关系
常温下:
3.溶液pH的计算
(1)单一溶液的pH计算
强酸溶液:如HA,设浓度为c mol·L-1,c(H+)=nc mol·L-1,pH=-lg c(H+)=-lg (nc)。
n
强碱溶液(25 ℃):如B(OH) ,设浓度为c mol·L-1,c(H+)= mol·L-1,pH=-lg c(H+)=14+lg
n
(nc)。
(2)混合溶液pH的计算类型
①两种强酸混合:直接求出c(H+) ,再据此求pH。c(H+) =。
混 混
②两种强碱混合:先求出c(OH-) ,再据K 求出c(H+) ,最后求pH。c(OH-) =。
混 w 混 混
③强酸、强碱混合:先判断哪种物质过量,再由下式求出溶液中H+或OH-的浓度,最后求pH。c(H+) 或c(OH-) =。
混 混
【方法规律】
1.稀释规律
酸、碱溶液稀释相同倍数时,强电解质溶液比弱电解质溶液的pH变化幅度大,但不管稀释多少倍,
最终都无限接近中性。
2.酸碱混合规律
(1)等浓度等体积一元酸与一元碱混合的溶液——“谁强显谁性,同强显中性”。
(2)25 ℃时,等体积pH之和等于14的一强一弱酸碱混合溶液——“谁弱谁过量,谁弱显谁性”。
(3)强酸、强碱等体积混合(25 ℃时)
①pH之和等于14呈中性;
②pH之和小于14呈酸性;
③pH之和大于14呈碱性。
知识点三 酸碱中和滴定
1.实验原理
利用酸碱中和反应,用已知浓度酸(或碱)来测定未知浓度的碱(或酸)的实验方法。以标准盐酸滴定待测
的NaOH溶液,待测的NaOH溶液的物质的量浓度为c(NaOH)=。
酸碱中和滴定的关键:
(1)准确测定标准液和待测液的体积;
(2)准确判断滴定终点。
2.实验用品
(1)仪器
图(A)是酸式滴定管、图(B)是碱式滴定管、滴定管夹、铁架台、锥形瓶。
(2)试剂:标准液、待测液、指示剂、蒸馏水。
(3)滴定管
①构造:“0”刻度线在上方,尖嘴部分无刻度。②精确度:读数可精确到0.01 mL。
③洗涤:先用蒸馏水洗涤,再用待装液润洗。
④排泡:酸、碱式滴定管中的液体在滴定前均要排出尖嘴中的气泡。
⑤使用注意事项:
试剂性质 滴定管 原因
酸性、氧化性 酸式滴定管 氧化性物质易腐蚀橡胶管
碱性 碱式滴定管 碱性物质易腐蚀玻璃,致使玻璃活塞无法打开
3.实验操作
以标准盐酸滴定待测NaOH溶液为例
(1)滴定前的准备
①滴定管:查漏→洗涤→润洗→装液→调液面→记录。
②锥形瓶:注碱液→记体积→加指示剂。
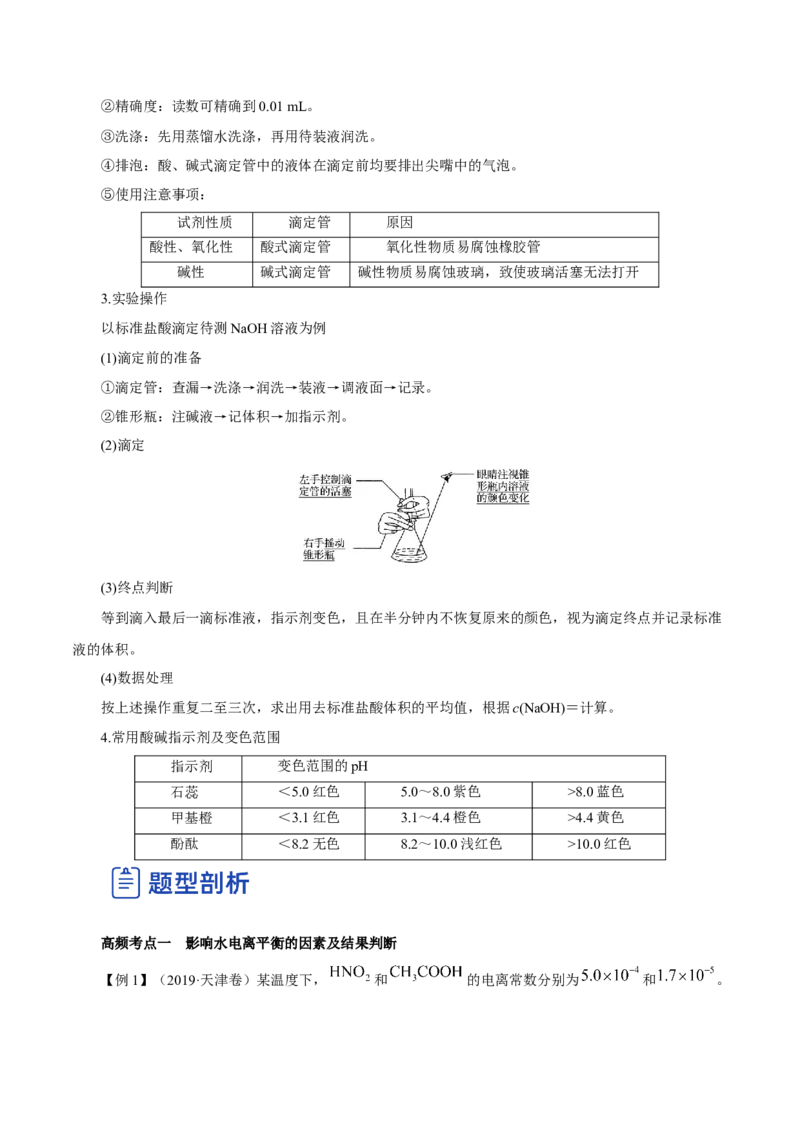
(2)滴定
(3)终点判断
等到滴入最后一滴标准液,指示剂变色,且在半分钟内不恢复原来的颜色,视为滴定终点并记录标准
液的体积。
(4)数据处理
按上述操作重复二至三次,求出用去标准盐酸体积的平均值,根据c(NaOH)=计算。
4.常用酸碱指示剂及变色范围
指示剂 变色范围的pH
石蕊 <5.0红色 5.0~8.0紫色 >8.0蓝色
甲基橙 <3.1红色 3.1~4.4橙色 >4.4黄色
酚酞 <8.2无色 8.2~10.0浅红色 >10.0红色
高频考点一 影响水电离平衡的因素及结果判断
【例1】(2019·天津卷)某温度下, 和 的电离常数分别为 和 。将 和体积均相同的两种酸溶液分别稀释,其 随加水体积的变化如图所示。下列叙述正确的是
A.曲线Ⅰ代表 溶液
B.溶液中水的电离程度:b点>c点
C.从c点到d点,溶液中 保持不变(其中 、 分别代表相应的酸和酸根离
子)
D.相同体积a点的两溶液分别与 恰好中和后,溶液中 相同
【答案】C
【解析】由图可知,稀释相同的倍数,Ⅱ的变化大,则Ⅱ的酸性比I的酸性强,Ⅱ代表HNO,I代表
2
CHCOOH,A错误;酸抑制水电离,b点pH小,酸性强,对水电离抑制程度大,B错误;Ⅱ代表HNO,
3 2
c(HNO )c(OH-)/c(NO-)=c(H+)·c(HNO)c(OH-)/[c(H+)·c(NO -)]=k /k(HNO ),k 为水的离子积常数,k(HNO)为
2 2 2 2 w 2 w 2
HNO 的电离常数,这些常数只与温度有关,温度不变,则不变,C正确;体积和pH均相同的HNO 和
2 2
CHCOOH溶液,c(CHCOOH)>c(HNO),分别滴加同浓度的NaOH溶液至恰好中和,CHCOOH消
3 3 2 3
耗的氢氧化钠溶液体积多,HNO 消耗的NaOH少,故D错误。
2
【方法技巧】正确理解水的电离平衡曲线
(1)曲线上任意点的K 都相同,即c(H+)·c(OH-)相同,温度相同。
w
(2)曲线外的任意点与曲线上任意点的K 不同,温度不同。
w
(3)实现曲线上点之间的转化需保持温度不变,改变酸碱性;实现曲线上点与曲线外点之间的转化一定
得改变温度。
【变式探究】下图三条曲线表示不同温度下水的离子积常数,下列说法不正确的是( )A.图中温度:T>T>T
3 2 1
B.图中pH关系:pH(B)=pH(D)=pH(E)
C.图中五点K 间的关系:E>D>A=B=C
w
D.C点可能是显酸性的盐溶液
【答案】D
【解析】水的电离吸热,升高温度促进电离,则水中c(H+)、c(OH-)及离子积常数均增大,根据图知,
离子积常数:T>T>T,所以温度:T>T>T,故A正确;水的离子积常数只与温度有关,温度越高,离子
3 2 1 3 2 1
积常数越大,同一曲线是相同温度,根据图知,温度高低点顺序是BD>A=B=C,故C正确;C点时,K =1×10-14,c(OH-)=1×10-6 mol·L
w w
-1,溶液的pH=8,显碱性,故D错误。
高频考点二 水电离出的c(H+)或c(OH-)的定量计算
【例2】在25 ℃时,某稀溶液中由水电离产生的H+浓度为1×10-13 mol·L-1,下列有关该溶液的叙述,
正确的是 ( )
A.该溶液可能呈酸性
B.该溶液一定呈碱性
C.该溶液的pH一定是1
D.该溶液的pH不可能为13
【答案】A
【解析】在25 ℃时,某稀溶液中由水电离产生的c(H+)=1×10-13 mol·L-1<1×10-7mol·L-1,说明溶液
中的溶质抑制水的电离,溶液可能呈酸性或碱性,A正确,B错误;如果该溶液呈酸性,则溶液的pH=
1,如果该溶液呈碱性,则溶液的pH=13,C、D错误。
【方法技巧】水电离的c(H+)或c(OH-)的计算技巧(25 ℃时)
(1)中性溶液:c(H+)=c(OH-)=1.0×10-7 mol·L-1。
(2)酸或碱抑制水的电离,水电离出的c(H+)=c(OH-)<10-7 mol·L-1,当溶液中的c(H+)<10-7 mol·L
-1时就是水电离出的c(H+);当溶液中的c(H+)>10-7 mol·L-1时,就用10-14除以这个浓度即得到水电离的c(H+)。
(3)可水解的盐促进水的电离,水电离的c(H+)或c(OH-)均大于10-7 mol·L-1。若给出的c(H+)>10-7
mol·L-1,即为水电离的c(H+);若给出的c(H+)<10-7 mol·L-1,就用10-14除以这个浓度即得水电离的c(H
+)。
【变式探究】下表是不同温度下水的离子积数据:
温度/℃ 25 t t
1 2
水的离子积常数 1×10-14 K 1×10-12
w
试回答下列问题:
(1)若 25<t <t ,则 K (填“>”“<”或“=”)1×10-14,做出此判断的理由是
1 2 w
。
(2)在t ℃时,测得纯水中的c(H+)=2.4×10-7 mol·L-1,则c(OH-)为 。该温度下,测得某
1
HSO 溶液中c(SO)=5×10-6 mol·L-1,该溶液中c(OH-)= mol·L-1。
2 4
【答案】(1)> 水的电离是吸热过程,升高温度,平衡向电离方向移动,c(H+)增大,c(OH-)增大,
K =c(H+)·c(OH-),K 增大
w w
(2)2.4×10-7 mol·L-1 5.76×10-9
【解析】(1)水是弱电解质,存在电离平衡,电离吸热,所以温度升高,水的电离程度增大,离子积增
大。(2)水电离出的氢离子浓度和氢氧根离子浓度相同,某温度下纯水中的 c(H+)=2.4×10-7 mol·L-1,则此
时纯水中的c(OH-)=2.4×10-7 mol·L-1,K =2.4×10-7×2.4×10-7=5.76×10-14。该温度下,某HSO 溶液中
w 2 4
c(SO)=5×10-6 mol·L-1,则溶液中氢离子浓度是1×10-5 mol·L-1,c(OH-)= mol·L-1=5.76×10-9 mol·L-
1。
高频考点三 pH的计算及其应用
【例3】(2022·浙江卷)已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说法正确的是
2 a1 a2
A.在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为0.013%
2 2
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
【答案】B
【解析】在等浓度的NaA、NaHA溶液中,A2-的水解程度大于HA-,水的电离程度前者大于后者,故
2
A错误;溶液中c(H+)=10-3mol/L,HA电离程度较小,溶液中c(HA)≈0.1mol/L,K =
2 2 a1,c(HA-)=1.3×10-5mol/L,c(HA-)≈c(HA) ,则HA的电离度
2 电离 2
0.013%,故B正确;向HA溶液中加入NaOH溶液至pH=11,
2
,则c(A2-)c(R+)>c(H+)>c(OH-)
C.c点溶液的pH=7,且所含溶质为ROH和RCl
D.碱性:MOH>ROH,且MOH是强碱,ROH是弱碱
【答案】B
【解析】A项,结合题图知,0.1 mol/L MOH溶液中,c(OH-)=0.1 mol/L,c(H+)=10-13 mol/L,OH-
来自碱电离,H+来自水电离,水电离出来的c(H+)和c(OH-)相等,乘积为1×10-26,正确;B项,b点加了
0.005 mol HCl,中和了一半的ROH,得到的溶液为等物质的量浓度的ROH和RCl混合溶液,lg =6,
c(OH-)=10-4 mol/L,溶液呈碱性,c(H+)V
X Y
D.若820mL,VmL时(a点、b点),没有二氧化碳产生,则所发生的反应为碳酸氢根离子与氢
1 1
离子结合生成碳酸,离子方程式表示为:HCO -+H+=H CO,B项错误;根据pH-V(HCl)图,滴定分析时,
3 2 3
c点的pH在9左右,符合酚酞的指示范围,可用酚酞作指示剂;d点的pH在4左右,符合甲基橙的指示范
围,可用甲基橙作指示剂指示滴定终点,C项正确;根据电荷守恒和物料守恒,则NaCO 中存在c(OH-)-
2 3
c(H+)=
2c(HCO)+c(HCO-),NaHCO 溶液中满足c(HCO)-c(CO2-)=c(OH-)-c(H+),D项错误;故选C。
2 3 3 3 2 3 3
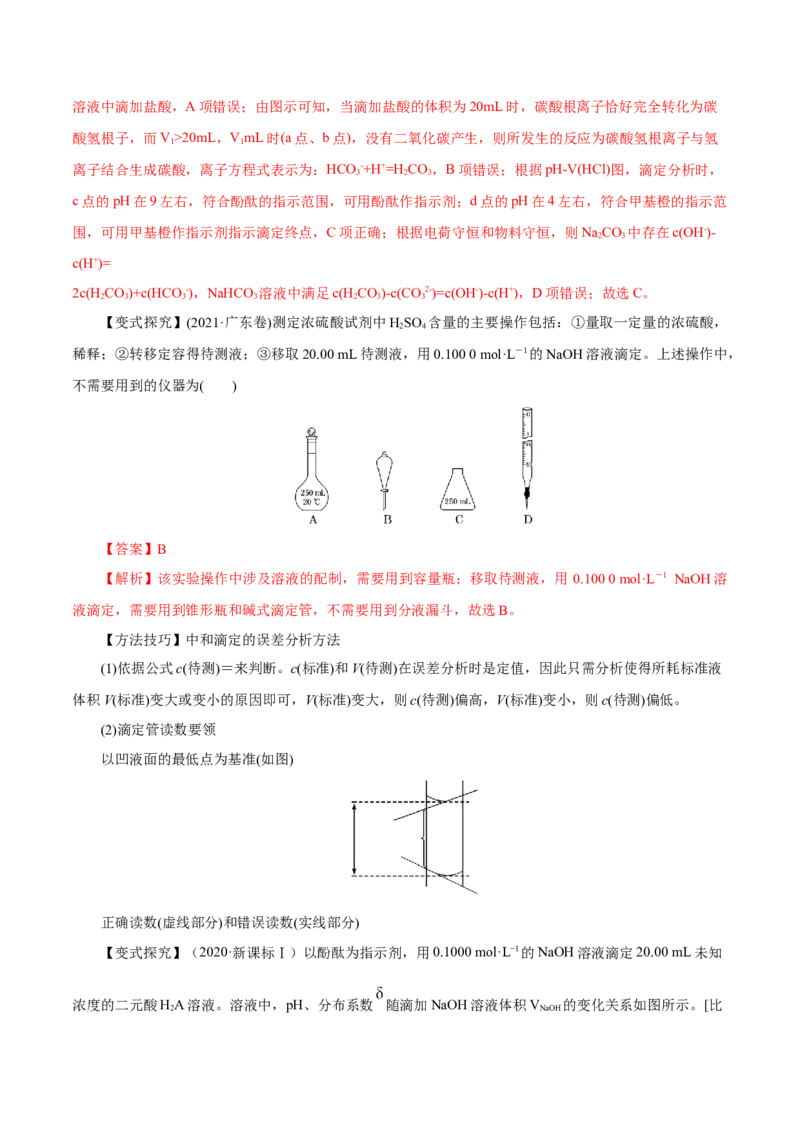
【变式探究】(2021·广东卷)测定浓硫酸试剂中HSO 含量的主要操作包括:①量取一定量的浓硫酸,
2 4
稀释;②转移定容得待测液;③移取20.00 mL待测液,用0.100 0 mol·L-1的NaOH溶液滴定。上述操作中,
不需要用到的仪器为( )
【答案】B
【解析】该实验操作中涉及溶液的配制,需要用到容量瓶;移取待测液,用 0.100 0 mol·L-1 NaOH溶
液滴定,需要用到锥形瓶和碱式滴定管,不需要用到分液漏斗,故选B。
【方法技巧】中和滴定的误差分析方法
(1)依据公式c(待测)=来判断。c(标准)和V(待测)在误差分析时是定值,因此只需分析使得所耗标准液
体积V(标准)变大或变小的原因即可,V(标准)变大,则c(待测)偏高,V(标准)变小,则c(待测)偏低。
(2)滴定管读数要领
以凹液面的最低点为基准(如图)
正确读数(虚线部分)和错误读数(实线部分)
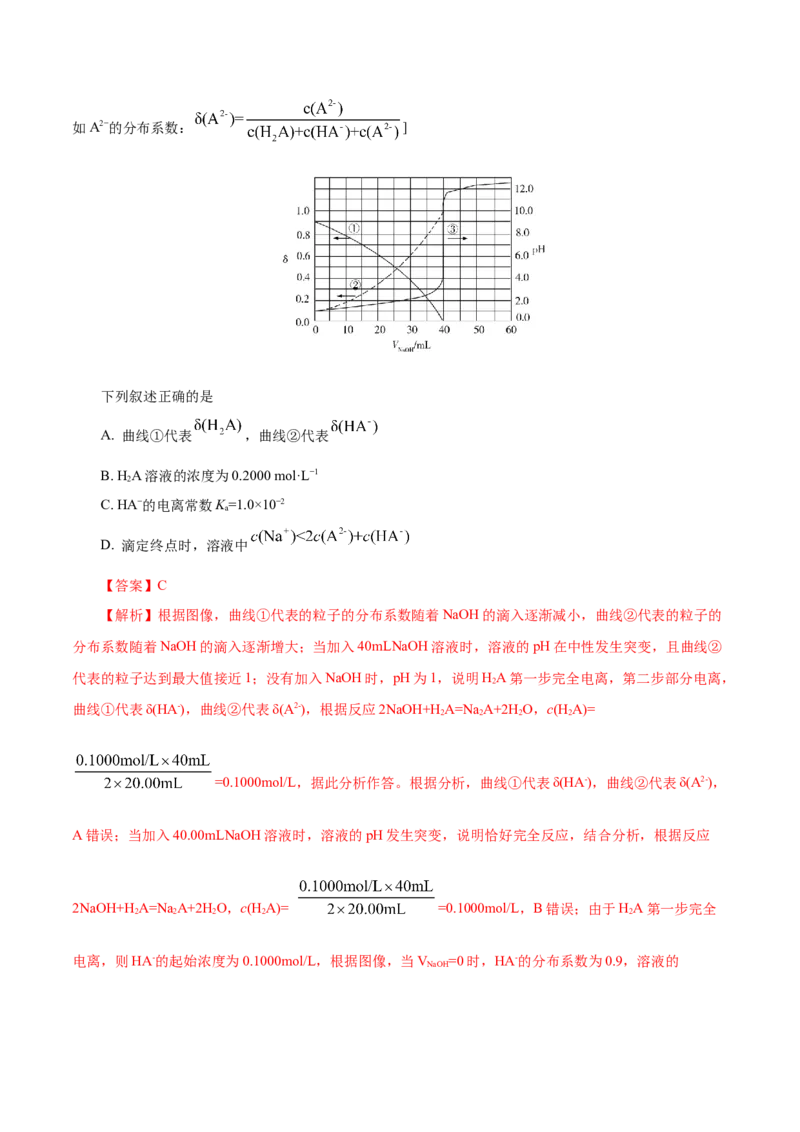
【变式探究】(2020·新课标Ⅰ)以酚酞为指示剂,用0.1000 mol·L−1的NaOH溶液滴定20.00 mL未知
浓度的二元酸HA溶液。溶液中,pH、分布系数 随滴加NaOH溶液体积V 的变化关系如图所示。[比
2 NaOH如A2−的分布系数: ]
下列叙述正确的是
A. 曲线①代表 ,曲线②代表
B. HA溶液的浓度为0.2000 mol·L−1
2
C. HA−的电离常数K=1.0×10−2
a
D. 滴定终点时,溶液中
【答案】C
【解析】根据图像,曲线①代表的粒子的分布系数随着NaOH的滴入逐渐减小,曲线②代表的粒子的
分布系数随着NaOH的滴入逐渐增大;当加入40mLNaOH溶液时,溶液的pH在中性发生突变,且曲线②
代表的粒子达到最大值接近1;没有加入NaOH时,pH为1,说明HA第一步完全电离,第二步部分电离,
2
曲线①代表δ(HA-),曲线②代表δ(A2-),根据反应2NaOH+H A=Na A+2HO,c(H A)=
2 2 2 2
=0.1000mol/L,据此分析作答。根据分析,曲线①代表δ(HA-),曲线②代表δ(A2-),
A错误;当加入40.00mLNaOH溶液时,溶液的pH发生突变,说明恰好完全反应,结合分析,根据反应
2NaOH+H A=Na A+2HO,c(H A)= =0.1000mol/L,B错误;由于HA第一步完全
2 2 2 2 2
电离,则HA-的起始浓度为0.1000mol/L,根据图像,当V =0时,HA-的分布系数为0.9,溶液的
NaOHpH=1,A2-的分布系数为0.1,则HA-的电离平衡常数K= =
a
≈1×10-2,C正确;用酚酞作指示剂,酚酞变色 p的H范围为8.2~10,终
点时溶液呈碱性,c(OH-)>c(H+),溶液中的电荷守恒为c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-),则c(Na+)>
2c(A2-)+c(HA-),D错误;答案选C。
【举一反三】(2019·浙江卷)室温下,取20 mL 0.1 mol·L−1某二元酸HA,滴加0.1 mol·L−1 NaOH溶
2
液。已知:HA H++HA−,HA− H++A2−。下列说法不正确的是( )
2
A.0.1 mol·L−1 HA溶液中有⇌c(H+)-c(OH−)-c(A2−)=0.1 mol·L−1
2
B.当滴加至中性时,溶液中c(Na+)=c(HA−)+2c(A2−),用去NaOH溶液的体积小于10 mL
C.当用去NaOH溶液体积10 mL时,溶液的pH<7,此时溶液中有c(A2−)=c(H+)-c(OH−)
D.当用去NaOH溶液体积20 mL时,此时溶液中有c(Na+)=2c(HA−)+2c(A2−)
【答案】B
【解析】0.1 mol·L−1HA溶液存在电荷守恒,其关系为c(H+)=c(OH−)+2c(A2−)+ c(HA−),因而c(H+)-
2
c(OH−)-c(A2−)= c(A2−)+c(HA−)=0.1mol·L−1,A正确;若NaOH用去10ml,反应得到NaHA溶液,由于
HA− H++A2−,溶液显酸性,因而滴加至中性时,需要加入超过10ml的NaOH溶液,B错误;当用去
NaO⇌H溶液体积10 mL时,得到NaHA溶液,溶液的pH<7,存在质子守恒,其关系为c(A2−)=c(H+)-
c(OH−),C正确;当用去NaOH溶液体积20 mL时,得到NaA溶液,根据物料守恒有:c(Na+)=2c(HA−)+
2
2c(A2−),D正确。
高频考点五 滴定曲线分析
【例5】 (2021·湖南卷)常温下,用0.1000mol·L-1的盐酸分别滴定20.00mL浓度均为0.1000mol·L-1
三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是( )
A. 该NaX溶液中:B. 三种一元弱酸的电离常数:
C. 当 时,三种溶液中:
D. 分别滴加20.00mL盐酸后,再将三种溶液混合:
【答案】C
【解析】由图可知,没有加入盐酸时,NaX、NaY、NaZ溶液的pH依次增大,则HX、HY、HZ三种
一元弱酸的酸性依次减弱。NaX为强碱弱酸盐,在溶液中水解使溶液呈碱性,则溶液中离子浓度的大小顺
序为c(Na+)>c(X-)>c(OH-)>c(H+),故A正确;弱酸的酸性越弱,电离常数越小,由分析可知,HX、
HY、HZ三种一元弱酸的酸性依次减弱,则三种一元弱酸的电离常数的大小顺序为K(HX)>K (HY)>
a a
K(HZ),故B正确;当溶液pH为7时,酸越弱,向盐溶液中加入盐酸的体积越大,酸根离子的浓度越小,
a
则三种盐溶液中酸根的浓度大小顺序为c(X-)>c(Y-)>c(Z-),故C错误;向三种盐溶液中分别滴加20.00mL
盐酸,三种盐都完全反应,溶液中钠离子浓度等于氯离子浓度,将三种溶液混合后溶液中存在电荷守恒关
系c(Na+)+ c(H+)= c(X-)+c(Y-)+c(Z-)+ c(Cl-)+ c(OH-),由c(Na+)= c(Cl-)可得:c(X-)+c(Y-)+c(Z-)= c(H+)—
c(OH-),故D正确;故选C。
【方法技巧】滴定曲线
1.强酸与强碱滴定过程中的pH曲线
(以0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1盐酸为例)
2.强酸(碱)滴定弱碱(酸)的pH曲线比较
氢氧化钠滴定等浓度、等体积的盐酸、醋酸 盐酸滴定等浓度、等体积的氢氧化钠、氨水
的滴定曲线 的滴定曲线曲线起点不同:强碱滴定强酸、弱酸的曲线,强酸起点低;强酸滴定强碱、弱碱的曲线,强
碱起点高
突跃点变化范围不同:强碱滴定强酸(强酸滴定强碱)的突跃点变化范围大于强碱滴定弱酸(强
酸滴定弱碱)的突跃点变化范围
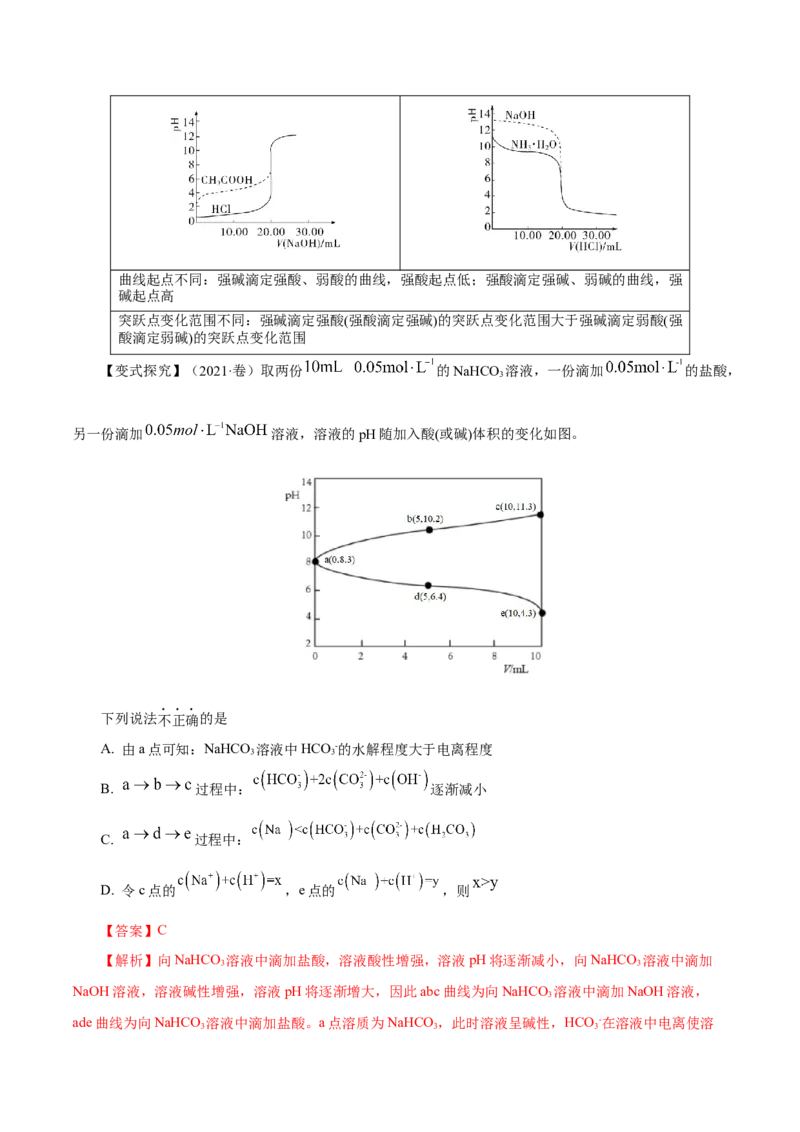
【变式探究】(2021·卷)取两份 的NaHCO 溶液,一份滴加 的盐酸,
3
另一份滴加 溶液,溶液的pH随加入酸(或碱)体积的变化如图。
下列说法不正确的是
A. 由a点可知:NaHCO 溶液中HCO -的水解程度大于电离程度
3 3
B. 过程中: 逐渐减小
C. 过程中:
D. 令c点的 ,e点的 ,则
【答案】C
【解析】向NaHCO 溶液中滴加盐酸,溶液酸性增强,溶液pH将逐渐减小,向NaHCO 溶液中滴加
3 3
NaOH溶液,溶液碱性增强,溶液pH将逐渐增大,因此abc曲线为向NaHCO 溶液中滴加NaOH溶液,
3
ade曲线为向NaHCO 溶液中滴加盐酸。a点溶质为NaHCO ,此时溶液呈碱性,HCO -在溶液中电离使溶
3 3 3液呈酸性,HCO -在溶液中水解使溶液呈碱性,由此可知,NaHCO 溶液中HCO -的水解程度大于电离程度,
3 3 3
故A正确;由电荷守恒可知, 过程溶液中 ,滴加
NaOH溶液的过程中 保持不变, 逐渐减小,因此 逐渐减小,故B正
确;由物料守恒可知,a点溶液中 ,向NaHCO 溶液中滴加盐酸过
3
程中有CO 逸出,因此 过程中 ,C错误;c点溶液中
2
=(0.05+10-11.3)mol/L,e点溶液体积增大1倍,此时溶液中 =(0.025+10-4)mol/L,因
此x>y,故D正确;故答案为C。
【变式探究】(2020·浙江卷)室温下,向20.00 mL 0.100 0 mol·L-1盐酸中滴加0.100 0 mol·L-1 NaOH溶
液,溶液的pH随NaOH溶液体积的变化如图。已知lg 5=0.7。下列说法不正确的是( )
A.NaOH与盐酸恰好完全反应时,pH=7
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.V(NaOH)=30.00 mL时,pH=12.3
【答案】C
【解析】氢氧化钠与盐酸恰好完全反应生成氯化钠和水,氯化钠属于强酸强碱盐,溶液呈中性,即室
温下pH=7,A正确;指示剂的变色范围在pH突变范围内,可减小实验误差,B正确;指示剂的变色范围
越接近反应的理论终点,实验误差越小,从题图可知,甲基红的变色范围更接近反应终点(pH=7),误差更
小,C错误;当加入NaOH溶液的体积为 30.00 mL时,盐酸不足,NaOH过量,则过量的n(NaOH)=
30.00×10-3 L×0.100 0 mol·L-1-20.00×10-3 L×0.100 0 mol·L-1=10-3 mol,所以溶液中c(NaOH)==0.02
mol·L-1,c(H+)= mol·L-1=5×10-13 mol·L-1,故pH=12.3,D正确。高频考点六 酸碱中和滴定的拓展应用
【例6】(2020·江苏卷)次氯酸钠溶液和二氯异氰尿酸钠(C NOClNa)都是常用的杀菌消毒剂。NaClO
3 3 3 2
可用于制备二氯异氰尿酸钠。
(1)NaClO 溶液可由低温下将 Cl 缓慢通入 NaOH 溶液中而制得。制备 NaClO 的离子方程式为
2
____________________________;用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时
间过长且见光,将会导致消毒作用减弱,其原因是__________________________________________。
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质
品标准。实验检测原理为
C NOCl+H++2HO===C HNO+2HClO
3 3 3 2 3 3 3 3
HClO+2I-+H+===I +Cl-+HO
2 2
I+2SO===S O+2I-
2 2 4
准确称取1.120 0 g样品,用容量瓶配成250.0 mL溶液;取25.00 mL上述溶液于碘量瓶中,加入适量
稀硫酸和过量KI溶液,密封在暗处静置5 min;用0.100 0 mol·L-1 Na SO 标准溶液滴定至溶液呈微黄色,
2 2 3
加入淀粉指示剂,继续滴定至终点,消耗NaSO 溶液20.00 mL。
2 2 3
①通过计算判断该样品是否为优质品。
(写出计算过程,该样品的有效氯=
×100%)
②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值________(填“偏高”或“偏低”)。
【解析】(1)Cl 与NaOH反应生成NaCl、NaClO和HO。HClO的酸性弱于HCO,则NaClO溶液露
2 2 2 3
置于空气中,与空气中CO 反应产生HClO,HClO见光易分解,故会导致消毒作用减弱。(2)①依据三个反
2
应得出关系式:C NOCl~2HClO~2I~4SO,根据NaSO 的消耗量,可以计算出测定中转化为HClO的
3 3 3 2 2 2 2 3
氯的物质的量,进而得出氯元素的质量,再由有效氯的计算公式×100%,可计算出有效氯。②加入的稀硫
酸的量过少,则生成的I 少,消耗NaSO 的量减少,则计算出的HClO的量偏少,导致样品的有效氯测定
2 2 2 3
值偏低。
【答案】(1)Cl +2OH-===ClO-+Cl-+HO NaClO溶液吸收空气中的CO 后产生HClO,HClO见光
2 2 2
分解
(2)①n(S O)=0.100 0 mol·L-1×0.020 00 L=2.000×10-3 mol
2
根据物质转换和电子得失守恒关系:C NOCl~2HClO~2I~4SO得n(Cl)=0.5n(S O)=1.000 ×10-3
3 3 3 2 2 2
mol
氯元素的质量:m(Cl)=1.000×10-3 mol×35.5 g·mol-1=0.035 50 g
该样品的有效氯为×2×100%≈63.39%该样品的有效氯大于60%,故该样品为优质品
②偏低
【方法技巧】
1.氧化还原滴定法
(1)原理:以氧化剂(或还原剂)为滴定剂,直接滴定一些具有还原性(或氧化性)的物质。
(2)实例
①酸性KMnO 溶液滴定HC O 溶液
4 2 2 4
原理 2MnO+6H++5HC O===10CO ↑+2Mn2++8HO
2 2 4 2 2
指示剂 酸性KMnO 溶液本身呈紫色,不用另外选择指示剂
4
当滴入最后一滴酸性KMnO 溶液后,溶液由无色变浅红色,且半分钟内不褪
终点判断 4
色,说明到达滴定终点
②NaSO 溶液滴定碘液
2 2 3
原理 2NaSO+I===Na SO+2NaI
2 2 3 2 2 4 6
指示剂 用淀粉作指示剂
当滴入最后一滴NaSO 溶液后,溶液的蓝色褪去,且半分钟内不恢复原色,
终点判断 2 2 3
说明到达滴定终点
2.沉淀滴定法
(1)概念:沉淀滴定法是利用沉淀反应进行滴定、测量分析的方法。生成沉淀的反应很多,但符合条件
的却很少,实际上应用最多的是银量法,即利用Ag+与卤素离子的反应来测定Cl-、Br-、I-浓度。
(2)原理:沉淀滴定所用的指示剂本身就是一种沉淀剂,滴定剂与被滴定物反应的生成物的溶解度要比
滴定剂与指示剂反应的生成物的溶解度小,否则不能用这种指示剂。如用AgNO 溶液滴定溶液中的Cl-的
3
含量时常以CrO为指示剂,这是因为AgCl比Ag CrO 更难溶。
2 4
【变式探究】用沉淀滴定法快速测定NaI等碘化物溶液中c(I-),实验过程包括准备标准溶液和滴定待
测溶液。
Ⅰ.准备标准溶液
a.准确称取AgNO 基准物4.246 8 g(0.025 0 mol)后,配制成250 mL标准溶液,放在棕色试剂瓶中避
3
光保存,备用。
b.配制并标定100 mL 0.100 0 mol·L-1NH SCN标准溶液,备用。
4
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00 mL于锥形瓶中。
b.加入25.00 mL 0.100 0 mol·L-1AgNO 溶液(过量),使I-完全转化为AgI沉淀。
3
c.加入NH Fe(SO ) 溶液作指示剂。
4 4 2
d.用0.100 0 mol·L-1NH SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现
4淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如下表:
实验序号 1 2 3
消耗NH SCN标准溶液体积/mL 10.24 10.02 9.98
4
f.数据处理。
回答下列问题:
(1)将称得的AgNO 配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有________。
3
(2)AgNO 标准溶液放在棕色试剂瓶中避光保存的原因是________________。
3
(3)滴定应在pH<0.5的条件下进行,其目的是________________。
(4)b和c两步操作是否可以颠倒________,说明理由______________________________________。
(5)所消耗的NH SCN标准溶液平均体积为________mL,测得c(I-)=________mol·L-1。
4
(6)在滴定管中装入NH SCN标准溶液的前一步,应进行的操作为________________。
4
(7)判断下列操作对c(I-)测定结果的影响(填“偏高”“偏低”或“无影响”)。
①若在配制AgNO 标准溶液时,烧杯中的溶液有少量溅出,则测定结果________。
3
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果________。
【解析】(1)配制一定物质的量浓度的标准溶液,除烧杯和玻璃棒外,还需用到的仪器有250 mL(棕色)
容量瓶、胶头滴管。(2)AgNO 见光容易分解,因此需要保存在棕色试剂瓶中。(3)滴定实验中用
3
NH Fe(SO ) 溶液作指示剂,Fe3+容易发生水解,影响滴定终点判断,因此控制pH<0.5,目的是抑制Fe3+
4 4 2
的水解。(4)Fe3+能与I-发生氧化还原反应:2Fe3++2I-===2Fe2++I ,因此b、c不能颠倒,否则指示剂耗
2
尽,无法判断滴定终点。(5)第1组数据误差较大,舍去,取第 2组、第3组实验数据的平均值,消耗
NH SCN标准溶液的体积为(10.02+9.98)mL×=10.00 mL。根据滴定原理,则n(Ag+)=n(I-)+n(SCN-),故
4
n(I-)=n(Ag+)-n(SCN-)=0.025 L×0.100 0 mol·L-1-0.01 L×0.100 0 mol·L-1=0.001 5 mol,则c(I-)==
0.060 0 mol·L-1。(6)在滴定管中装入NH SCN标准溶液之前,要先用NH SCN标准溶液润洗滴定管。(7)①
4 4
在配制AgNO 标准溶液时,若烧杯中溶液有少量溅出,配制的 AgNO 标准溶液的浓度偏低,则滴定时消
3 3
耗的NH SCN标准溶液的体积偏小,测得的c(I-)偏高。②滴定管“0”刻度在上,读数时从上往下读数,读
4
取体积偏小,计算所用NH SCN的物质的量偏低,测得的c(I-)偏高。
4
【答案】(1)250 mL(棕色)容量瓶、胶头滴管
(2)避免AgNO 见光分解
3
(3)防止因Fe3+的水解而影响滴定终点的判断(或抑制Fe3+的水解)
(4)否(或不能) 若颠倒,Fe3+与I-反应,指示剂耗尽,无法判断滴定终点
(5)10.00 0.060 0(6)用NH SCN标准溶液进行润洗
4
(7)偏高 偏高