文档内容
第 23 讲 盐类水解
1.下列盐的水溶液因水解而呈碱性的是
A. B. C. D.
2.判断下列盐类水解的叙述中正确的是
A.溶液呈中性的盐一定是强酸、强碱生成的盐
B.含有弱酸根盐的水溶液一定呈碱性
C.盐溶液的酸碱性主要决定于形成盐的酸和碱的相对强弱
D.碳酸溶液中氢离子物质的量浓度是碳酸根离子物质的量浓度的两倍
3.在一定条件下发生下列反应,其中属于盐类水解反应的是
A.NH +2H
2
O⇌NH
3
·H
2
O+H
3
O+ B.HCO +H
2
O⇌H
3
O++CO
C.HS-+H
3
O+=H
2
S+H
2
O D.Cl
2
+H
2
O⇌H++Cl-+HClO
4.要使0.01mol/LK CO 溶液中的c( )更接近0.01mol/L,可以采取的措施是
2 3
A.通入CO B.加入NaCO 固体
2 2 3
C.加热 D.加入适量KOH固体
5.下列关于盐类水解的说法正确的是
A.在NaS溶液中加入少量NaS固体,NaS的水解程度增大
2 2 2
B.将CuSO 溶液由20℃加热到60℃,溶液的pH增大
4
C.向CHCOONa溶液中加水,溶液中 的比值增大
3
D.常温下,0.1mol/L的NaB溶液的pH=8,溶液中c(Na+)=c(B-)+c(HB)=0.1mol/L
6.浓度均为0.1mol/L的NH Cl、(NH )SO 、NH HSO 、(NH )Fe(SO ) 四种溶液中,设NH 离子浓度分别
4 4 2 4 4 4 4 2 4 2
为amol/L、bmol/L和cmol/L,dmol/L则a、b、c、d关系为
A.b=d>a=c B.c<a<b<d C.a<c<b=d D.a<c<b<d
7.常温下,pH=10的 溶液1mL加水稀释至10mL,下列说法错误的是
A.稀释前溶液中B.稀释后溶液中
C.加水过程中使水解平衡正向移动
D.加水过程中 逐渐减小
8.下列措施能使NaClO溶液的水解平衡正向移动,水解程度反而减小的是
A.增大NaClO溶液浓度 B.加水稀释
C.升高温度 D.加入适量NaOH固体
9.下列说法不正确的是
A.水分解变成氢气和氧气属于不自发反应
B.用润湿的pH试纸测稀NaOH溶液的pH,测定值偏小
C.NaHCO 溶液加水稀释,水解程度增大,电离程度减小
3
D.将pH=3的醋酸溶液稀释1000倍得到pH<6醋酸溶液
10.室温下,对于1.0L0.1mol•L-1的醋酸钠溶液,下列判断正确的是
A.加入少量醋酸钠固体后,水解平衡正向移动,溶液的pH降低
B.加入少量的冰醋酸后,水解平衡逆向移动,水解平衡常数减小
C.升高温度,平衡正向移动,c(CHCOOH)与c(CHCOO-)的比值减小
3 3
D.滴加氢氧化钠溶液过程中,n(CHCOO-)与n(CHCOOH)之和始终为0.1mol
3 3
11.在 的平衡体系中,要抑制 的水解,可采取的措施为
A.升高温度 B.滴加少量盐酸
C.加入适量氢氧化钠溶液 D.加水稀释
12.两种溶液混合后的成分与溶液酸碱性的变化可能有关,下列说法正确的是
A. 的 溶液与 的NaOH溶液等体积混合后所得溶液中:
B.等体积、等物质的量浓度的 溶液和 溶液混合:
C.常温下, 的HA溶液与 的BOH溶液等体积混合,所得溶液pH>7,则D.向某 溶液中加入少量 晶体,所得溶液中 水解程度增大,pH增大
13.等物质的量浓度的下列溶液中, 的物质的量浓度最大的是
A.NH Cl B.NH HCO C.NH HSO D.NH NO
4 4 3 4 4 4 3
14.对于0.1mol·L NaSO 溶液,下列说法正确的是
2 3
A.升高温度,溶液pH降低(不考虑SO 的氧化)
B.c(Na+)=2c( )+c( )+c(H SO )
2 3
C.
D.
15.在Al3++3H O A1(OH) +3H+的平衡体系中,要促进Al3+的水解,可采取的措施
2 3
A.降低温度 B.滴加少量盐酸 C.加入适量氢氧化钠溶液 D.加少量氯化钠固体
16.已知 溶液中存在如下平衡: ,下列说法中正确的是
A.加入适量水后平衡向右移动, 增大
B.加热后平衡向左移动, 增大
C.加入 后有气泡产生,一段时间后可得到红褐色沉淀
D.加热蒸干溶液并灼烧可得
17.下列五种混合溶液,由分别为 的两种溶液等体积混合而成:
① 与 ② 与
③ 与 ④ 与
⑤ 与 , 由大到小排序正确的是
A.①>④>③>②>⑤ B.①>③>⑤>④>②C.②>④>③>⑤>① D.②>③>④>⑤>①
18.为了探究外界条件对氯化铵水解平衡的影响,某研究性学习小组设计实验方案,获得如下数据:
实
c(NH Cl)/mol·L−1 V(NHCl)/mL 温度/℃ pH
验 4 4
1 0.02 5 25 x
2 0.02 5 30 y
3 0.2 5 25 z
下列说法不正确的是
A.由 x>y可知:升高温度能促进氯化铵的水解
B.由x >z可知:增大盐的浓度,水解平衡正向移动,水解程度增大
C.由z < x < z +1可知:稀释氯化铵溶液,水解平衡正向移动
D.K(NH Cl)与K(NH ·H O)的关系为:K= (K 为水的离子积常数)
h 4 b 3 2 h w
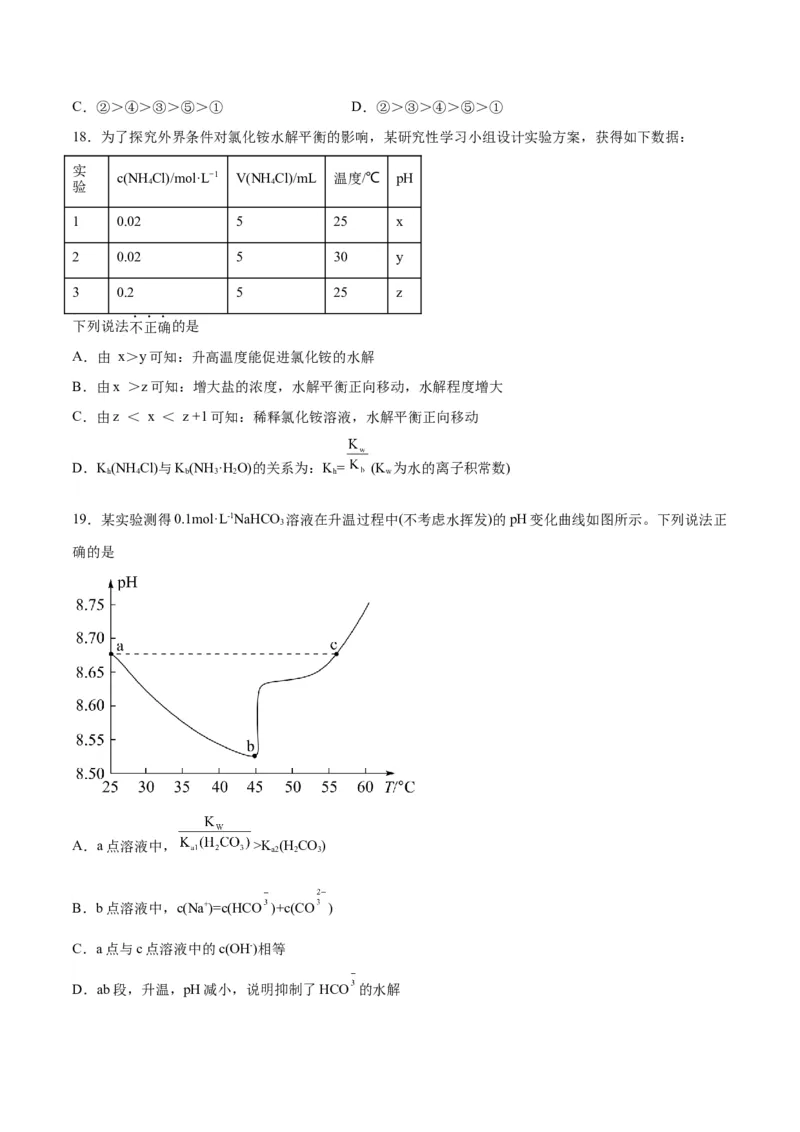
19.某实验测得0.1mol·L-1NaHCO 溶液在升温过程中(不考虑水挥发)的pH变化曲线如图所示。下列说法正
3
确的是
A.a点溶液中, >K (H CO)
a2 2 3
B.b点溶液中,c(Na+)=c(HCO )+c(CO )
C.a点与c点溶液中的c(OH-)相等
D.ab段,升温,pH减小,说明抑制了HCO 的水解20.25℃时,向高铁酸钾(K FeO)水溶液中加酸过程中,平衡体系中含Fe微粒的分布系数δ[如
2 4
]随pH的变化曲线如下图所示。下列说法正确的是
A.高铁酸为三元酸
B.pH=2时,
C.向KFeO 水溶液中加入KOH, 水解程度增大
2 4
D. 的平衡常数
21.实验探究反应条件对盐类水解程度的影响
已知FeCl
3
发生水解反应的离子方程式:Fe3++3H
2
O⇌Fe(OH)
3
+3H+,根据实验操作填写下表:
影响因
实验步骤 实验现象 解释
素
盐的浓 加入FeCl 固体,再 溶液颜色变 , 加入FeCl 固体,c(Fe3+)增大,水解平衡向
3 3
度 测溶液的pH 溶液的pH 方向移动
加盐酸后,测溶液 溶液颜色变 , 加入盐酸,c(H+)增大,水解平衡向 方
的pH 溶液的pH 向移动,但c(H+)仍比原平衡中c(H+)大
溶液的
酸碱度
加入少量NaOH溶 加入氢氧化钠后,OH-消耗H+,c(H+)减小,水
产生 色沉淀
液 解平衡向 方向移动
温度 升高温度 溶液颜色变深 升高温度,水解平衡正向移动
22.盐溶液呈现不同酸碱性的原因
醋酸钠溶液中微粒变 和 结合生成弱电解质 CHCOOH ,使水的电离平衡向电离方向移
3
化 动
平衡时酸碱性 使溶液中c(H+)<c(OH-),溶液呈碱性水解方程式 CHCOO-+HO
3 2
氯化铵溶液中微粒变 NH 和 结合生成弱电解质 ,使水的电离平衡向 的方向移
化
动
平衡时酸碱性 使溶液中c(H+)>c(OH-),溶液呈 性
水解方程式 NH +H
2
O⇌
氯化钠溶液 H
2
O⇌H++OH-,NaCl=Cl-+Na+
理论解释:溶液中不生成 ,水的电离平衡未受影响,溶液中c(H+)=c(OH-),溶液呈 性。