文档内容
第 24 讲 水的电离和溶液的 pH
第一部分:高考真题感悟
1.(2022·浙江·高考真题)已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说法正确的是
2 a1 a2
A.在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为0.013%
2 2
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
2.(2021·广东·高考真题)测定浓硫酸试剂中 含量的主要操作包括:
①量取一定量的浓硫酸,稀释;②转移定容得待测液;③移取 待测液,用 的
溶液滴定。
上述操作中,不需要用到的仪器为
A. B. C. D.
3.(2021·浙江·高考真题)某同学拟用 计测定溶液 以探究某酸HR是否为弱电解质。下列说法正确
的是
A.25℃时,若测得 溶液 ,则HR是弱酸
B.25℃时,若测得 溶液 且 ,则HR是弱酸
C.25℃时,若测得HR溶液 ,取该溶液 ,加蒸馏水稀释至 ,测得 ,则
HR是弱酸
D.25℃时,若测得NaR溶液 ,取该溶液 ,升温至50℃,测得 , ,则HR是弱酸
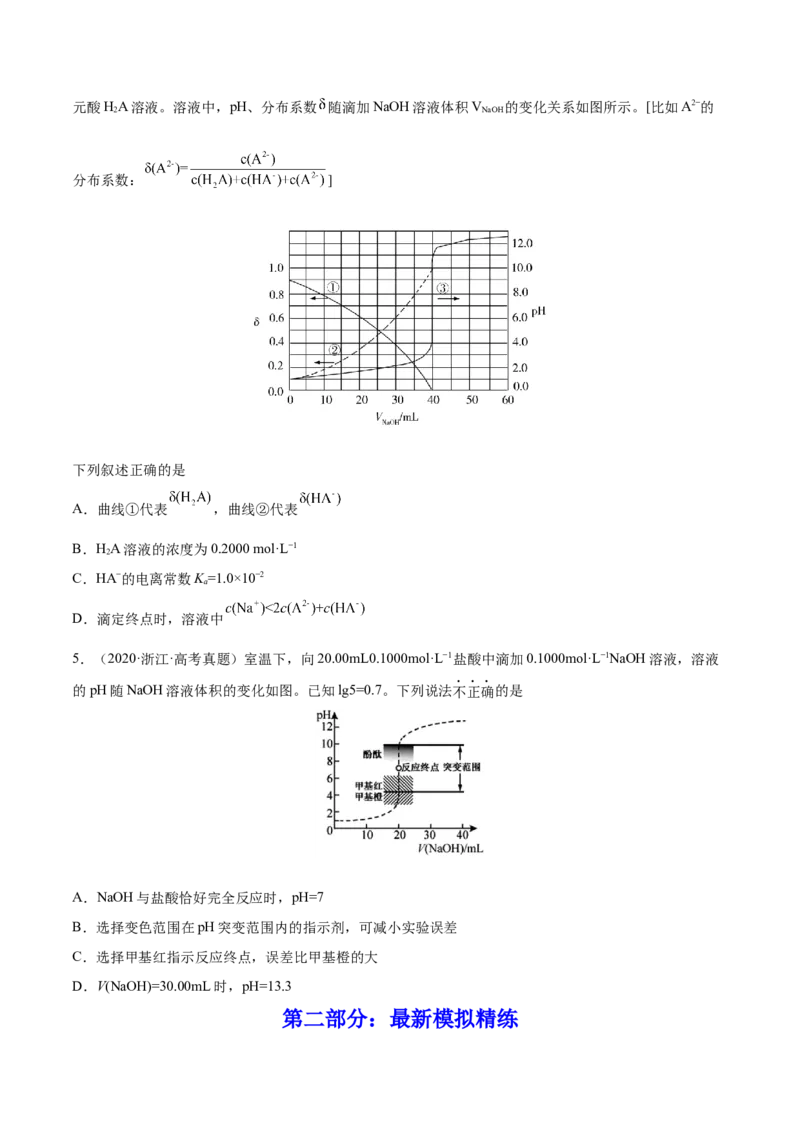
4.(2020·全国·高考真题)以酚酞为指示剂,用0.1000 mol·L−1的NaOH溶液滴定20.00 mL未知浓度的二元酸HA溶液。溶液中,pH、分布系数 随滴加NaOH溶液体积V 的变化关系如图所示。[比如A2−的
2 NaOH
分布系数: ]
下列叙述正确的是
A.曲线①代表 ,曲线②代表
B.HA溶液的浓度为0.2000 mol·L−1
2
C.HA−的电离常数K =1.0×10−2
a
D.滴定终点时,溶液中
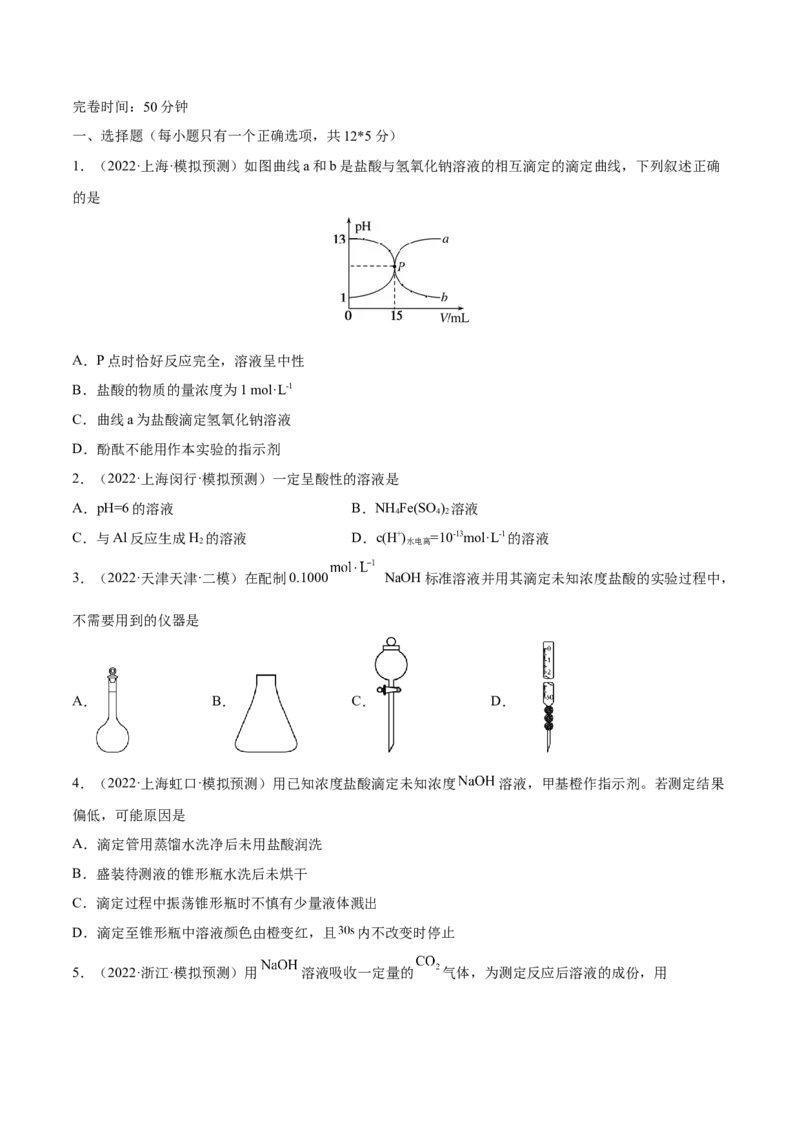
5.(2020·浙江·高考真题)室温下,向20.00mL0.1000mol·L−1盐酸中滴加0.1000mol·L−1NaOH溶液,溶液
的pH随NaOH溶液体积的变化如图。已知lg5=0.7。下列说法不正确的是
A.NaOH与盐酸恰好完全反应时,pH=7
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.V(NaOH)=30.00mL时,pH=13.3
第二部分:最新模拟精练完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·上海·模拟预测)如图曲线a和b是盐酸与氢氧化钠溶液的相互滴定的滴定曲线,下列叙述正确
的是
A.P点时恰好反应完全,溶液呈中性
B.盐酸的物质的量浓度为1 mol·L-1
C.曲线a为盐酸滴定氢氧化钠溶液
D.酚酞不能用作本实验的指示剂
2.(2022·上海闵行·模拟预测)一定呈酸性的溶液是
A.pH=6的溶液 B.NH Fe(SO ) 溶液
4 4 2
C.与Al反应生成H 的溶液 D.c(H+) =10-13mol·L-1的溶液
2 水电离
3.(2022·天津天津·二模)在配制0.1000 NaOH标准溶液并用其滴定未知浓度盐酸的实验过程中,
不需要用到的仪器是
A. B. C. D.
4.(2022·上海虹口·模拟预测)用已知浓度盐酸滴定未知浓度 溶液,甲基橙作指示剂。若测定结果
偏低,可能原因是
A.滴定管用蒸馏水洗净后未用盐酸润洗
B.盛装待测液的锥形瓶水洗后未烘干
C.滴定过程中振荡锥形瓶时不慎有少量液体溅出
D.滴定至锥形瓶中溶液颜色由橙变红,且 内不改变时停止
5.(2022·浙江·模拟预测)用 溶液吸收一定量的 气体,为测定反应后溶液的成份,用的 溶液滴定 待测液,先用酚酞作指示剂,消耗盐酸 ,再滴加甲基红为指示剂,
消耗盐酸为 ,下列说法不正确的是
A.当 时,溶液溶质为
B.当 , ,溶液中发生的反应为
C.当 , 时,待测液中,
D.当 , 时,待测液中, 的浓度为
6.(2022·天津市咸水沽第一中学模拟预测)常温下,下列说法错误的是
A. 均为5的稀硫酸和 溶液,由水电离的 浓度之比为
B.向水中加入少量 固体, 增大, 不变
C.等物质的量浓度的 和 溶液,前者 较大,则可发生反应:
D. 与 溶液等体积混合( 为二元弱酸):
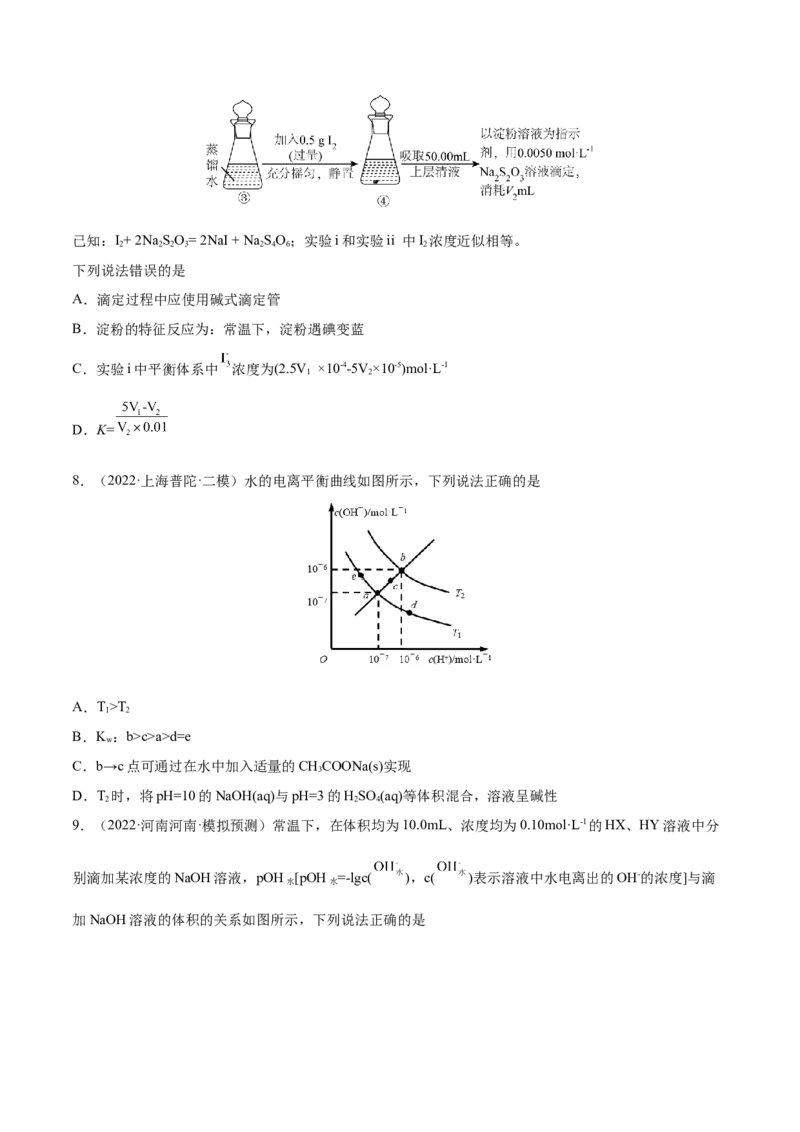
7.(2022·湖北·襄阳四中模拟预测)碘水中存在可逆反应: I(ag)+I- (aq) (aq),为测定该反应的平衡
2
常数K进行如下实验。
实验i测定平衡体系中 I 和 总浓度
2
实验ii测定饱和碘水中 I 浓度
2已知:I+ 2Na SO= 2NaI + Na SO;实验i和实验ii 中I 浓度近似相等。
2 2 2 3 2 4 6 2
下列说法错误的是
A.滴定过程中应使用碱式滴定管
B.淀粉的特征反应为:常温下,淀粉遇碘变蓝
C.实验i中平衡体系中 浓度为(2.5V ×10-4-5V ×10-5)mol·L-1
1 2
D.K=
8.(2022·上海普陀·二模)水的电离平衡曲线如图所示,下列说法正确的是
A.T>T
1 2
B.K :b>c>a>d=e
w
C.b→c点可通过在水中加入适量的CHCOONa(s)实现
3
D.T 时,将pH=10的NaOH(aq)与pH=3的HSO (aq)等体积混合,溶液呈碱性
2 2 4
9.(2022·河南河南·模拟预测)常温下,在体积均为10.0mL、浓度均为0.10mol·L-1的HX、HY溶液中分
别滴加某浓度的NaOH溶液,pOH [pOH =-lgc( ),c( )表示溶液中水电离出的OH-的浓度]与滴
水 水
加NaOH溶液的体积的关系如图所示,下列说法正确的是A.HX、HY均为弱酸,HY的酸性更强
B.NaOH溶液浓度c(NaOH)=0.1mol·L-1
C.M、N两点的溶液中:c(X-)与c(Y-)不相等
D.常温下HY的电离常数K≈5.4×10-6
a
10.(2022·黑龙江绥化·模拟预测)已知pOH=-lgc(OH-)。初始温度20℃时,向20mL0.1mol·L-1氨水中滴加
0.05mol·L-1的稀硫酸,测得混合溶液的温度T、pOH随加入稀硫酸体积V的变化如图所示。
下列说法正确的是
A.a、b、c三点对应NH 的水解平衡常数:K(c)>K (b)>K(a)
h h h
B.a点溶液中水电离产生的c <(OH-)=0.001mol·L-1
水
C.图中x=7,b点溶液中,c(NH )>2c(SO )
D.若V=40,则c点对应溶液中c(H+)=c(OH-)+c(NH )+2c(NH·H O)
3 3 2
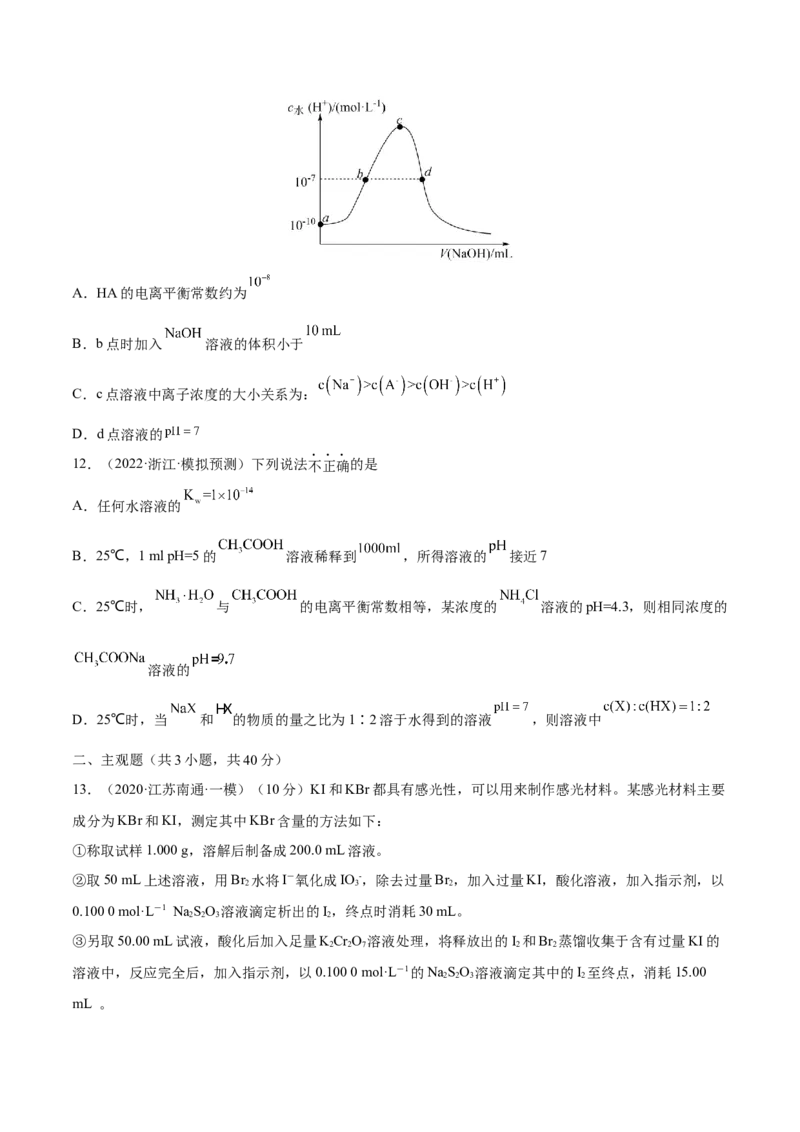
11.(2022·重庆南开中学模拟预测)常温下,向 溶液中逐滴加入 的
溶液,溶液中水电离出的 浓度随加入 溶液的体积变化如图所示,下列说法不正确的是A.HA的电离平衡常数约为
B.b点时加入 溶液的体积小于
C.c点溶液中离子浓度的大小关系为:
D.d点溶液的
12.(2022·浙江·模拟预测)下列说法不正确的是
A.任何水溶液的
B.25℃,1 ml pH=5的 溶液稀释到 ,所得溶液的 接近7
C.25℃时, 与 的电离平衡常数相等,某浓度的 溶液的pH=4.3,则相同浓度的
溶液的
D.25℃时,当 和 的物质的量之比为1∶2溶于水得到的溶液 ,则溶液中
二、主观题(共3小题,共40分)
13.(2020·江苏南通·一模)(10分)KI和KBr都具有感光性,可以用来制作感光材料。某感光材料主要
成分为KBr和KI,测定其中KBr含量的方法如下:
①称取试样1.000 g,溶解后制备成200.0 mL溶液。
②取50 mL上述溶液,用Br 水将I-氧化成IO -,除去过量Br ,加入过量KI,酸化溶液,加入指示剂,以
2 3 2
0.100 0 mol·L-1 Na SO 溶液滴定析出的I,终点时消耗30 mL。
2 2 3 2
③另取50.00 mL试液,酸化后加入足量KCr O 溶液处理,将释放出的I 和Br 蒸馏收集于含有过量KI的
2 2 7 2 2
溶液中,反应完全后,加入指示剂,以0.100 0 mol·L-1的NaSO 溶液滴定其中的I 至终点,消耗15.00
2 2 3 2
mL 。(1)写出第②步中用Br 水氧化I-的离子方程式:________。
2
(2)第②步除去过量Br 最简单的物理方法是________;若未除去过量的Br ,对KBr含量测定结果的影响是
2 2
________(填“偏大”“偏小”或“无影响”)。
(3)计算试样中KBr的质量分数_______ (写出计算过程)。
14.(2021·河南·模拟预测)(16分)草酸、KMnO 均是重要的化学分析试剂,某次实验中需要使用
4
480mL0.2000mol/L的草酸溶液,回答下列问题。
(1)实验中需要称取___________g草酸晶体(H C O•2H O),称量后___________(填“需要”或“不需要”)
2 2 4 2
加热除去相应的结晶水;配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管及___________。
(2)假设称取草酸时使用的是托盘天平,称量中试剂与砝码位置错放,则所配制溶液中c(HC O)0.2000
2 2 4
___________ (填“>”、“=”或“<”,下同);若定容时俯视刻度线,则所配溶液中
c(HC O)___________0.2000 。
2 2 4
(3)若配置溶液时所取草酸晶体不纯(杂质无还原性),为测定草酸的纯度,某同学量取20.00mL,上述所配
溶液放入锥形瓶中,然后用0.1000 的酸性KMnO 标准溶液滴定(氧化产物是CO),滴定终点时消耗
4 2
VmL标准溶液。
①标准溶液应使用___________(填“酸”或“碱”)式滴定管取用,合理的V值可能是___________。
A. 15.8 B. 16.20 C. 15.82 D. 16.18
②滴定终点时溶液颜色的变化为___________,样品中草酸品体的质量分数为___________(用含V的式子
表示)。
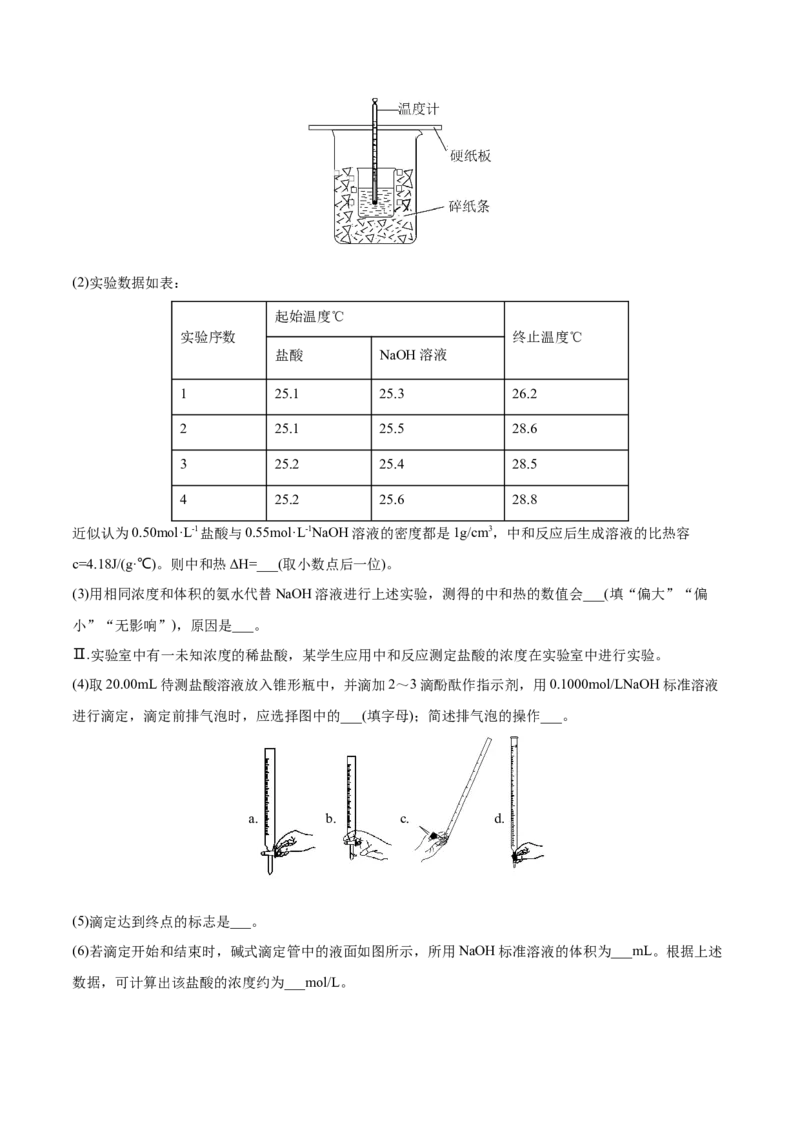
14.(2022·黑龙江实验中学高三阶段练习)(14分)酸与碱作用生成盐和水的反应叫做中和反应,它在
工农业生产和日常生活中有广泛应用。
Ⅰ.某实验小组用50mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在图示的装置中进行中和反应。通过
测定反应过程中所放出的热量可计算中和热。
(1)测定中和热实验。从实验装置上看,图中尚缺少的一种玻璃用品是___,烧杯间填满碎纸条的作用是___。(2)实验数据如表:
起始温度℃
实验序数 终止温度℃
盐酸 NaOH溶液
1 25.1 25.3 26.2
2 25.1 25.5 28.6
3 25.2 25.4 28.5
4 25.2 25.6 28.8
近似认为0.50mol·L-1盐酸与0.55mol·L-1NaOH溶液的密度都是1g/cm3,中和反应后生成溶液的比热容
c=4.18J/(g·℃)。则中和热ΔH=___(取小数点后一位)。
(3)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会___(填“偏大”“偏
小”“无影响”),原因是___。
Ⅱ.实验室中有一未知浓度的稀盐酸,某学生应用中和反应测定盐酸的浓度在实验室中进行实验。
(4)取20.00mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用0.1000mol/LNaOH标准溶液
进行滴定,滴定前排气泡时,应选择图中的___(填字母);简述排气泡的操作___。
a. b. c. d.
(5)滴定达到终点的标志是___。
(6)若滴定开始和结束时,碱式滴定管中的液面如图所示,所用NaOH标准溶液的体积为___mL。根据上述
数据,可计算出该盐酸的浓度约为___mol/L。(7)在上述实验中,下列操作(其他操作正确)会造成测定结果偏低的有___。A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C.锥形瓶水洗后未干燥
D.碱式滴定管尖嘴部分有气泡,滴定后消失