文档内容
第 25 讲 化学反应平衡
(模拟精练+真题演练)
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12×5分)
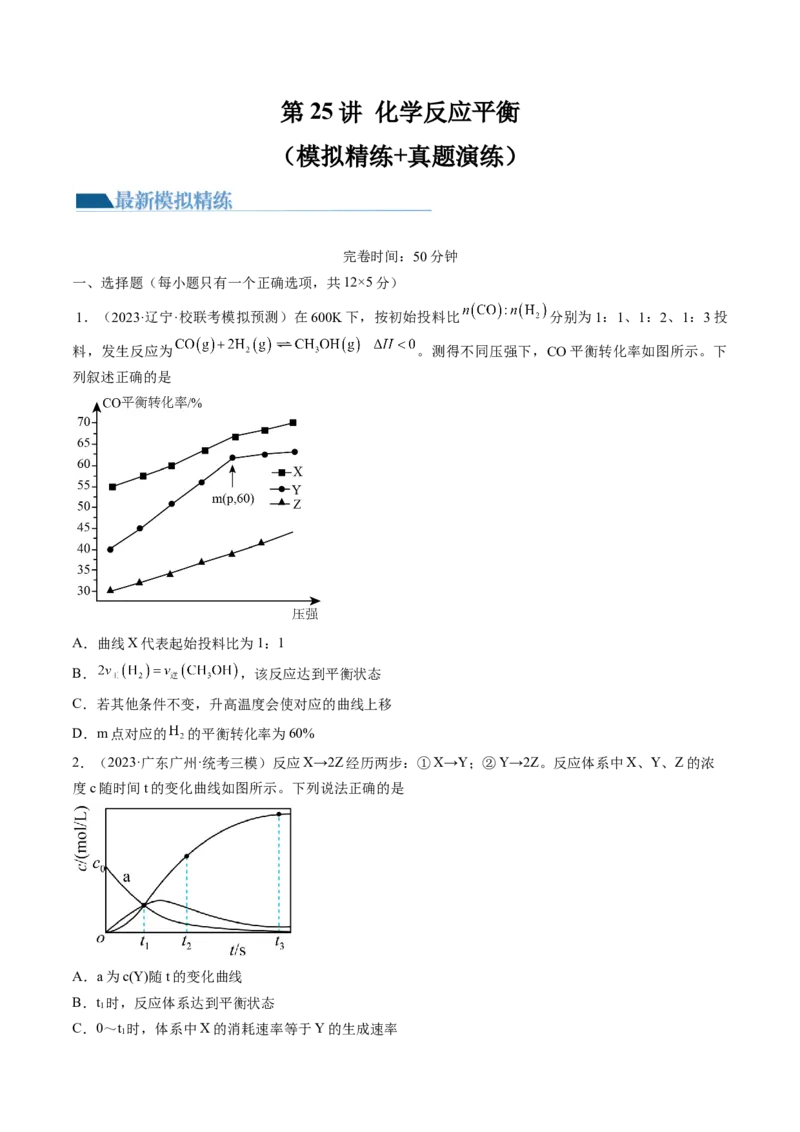
1.(2023·辽宁·校联考模拟预测)在600K下,按初始投料比 分别为1:1、1:2、1:3投
料,发生反应为 。测得不同压强下,CO平衡转化率如图所示。下
列叙述正确的是
A.曲线X代表起始投料比为1:1
B. ,该反应达到平衡状态
C.若其他条件不变,升高温度会使对应的曲线上移
D.m点对应的 的平衡转化率为60%
2.(2023·广东广州·统考三模)反应X→2Z经历两步:①X→Y;②Y→2Z。反应体系中X、Y、Z的浓
度c随时间t的变化曲线如图所示。下列说法正确的是
A.a为c(Y)随t的变化曲线
B.t 时,反应体系达到平衡状态
1
C.0~t 时,体系中X的消耗速率等于Y的生成速率
1D.反应体系中始终存在:c=c(X)+c(Y)+ c(Z)
0
3.(2023·江苏盐城·盐城市伍佑中学校考模拟预测)利用 和CO反应生成 的过程中主要涉及的反
应如下:
反应Ⅰ kJmol-1
反应Ⅱ kJm⋅ol-1
⋅
[ 的产率 , 的选择性 ]。保持温度一定,在固定容积
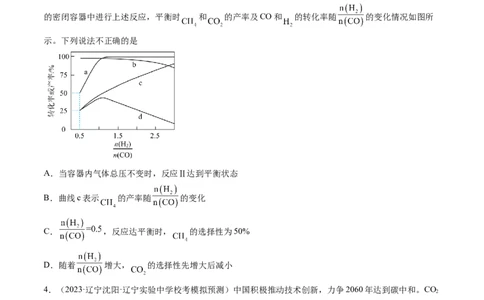
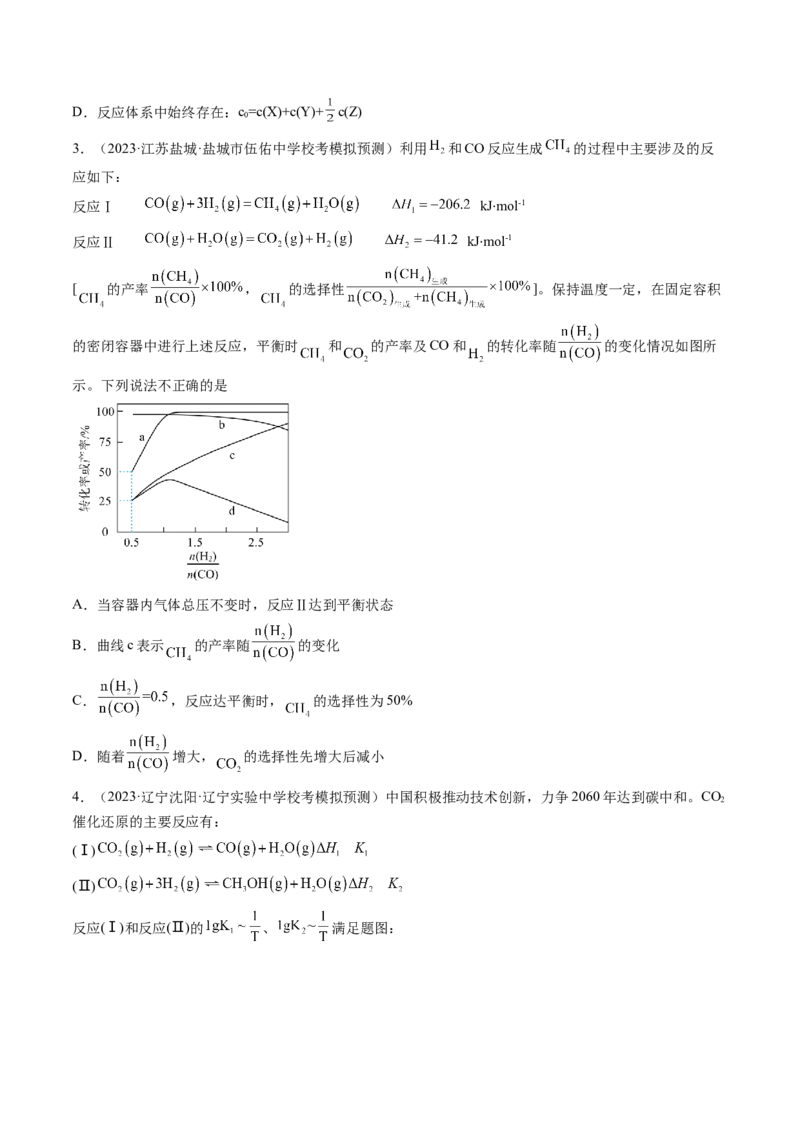
的密闭容器中进行上述反应,平衡时 和 的产率及CO和 的转化率随 的变化情况如图所
示。下列说法不正确的是
A.当容器内气体总压不变时,反应Ⅱ达到平衡状态
B.曲线c表示 的产率随 的变化
C. ,反应达平衡时, 的选择性为50%
D.随着 增大, 的选择性先增大后减小
4.(2023·辽宁沈阳·辽宁实验中学校考模拟预测)中国积极推动技术创新,力争2060年达到碳中和。CO
2
催化还原的主要反应有:
(Ⅰ)
(Ⅱ)
反应(Ⅰ)和反应(Ⅱ)的 、 满足题图:在恒温恒压条件下通入1molCO 和3molH 进行反应.下列说法错误的是
2 2
A.若反应体系密度不再变化,说明反应(Ⅰ)和(Ⅱ)都达到了平衡状态
B.使用催化剂可能在反应体系未达平衡前使甲醇产率提高
C.反应Ⅱ在高温条件下易自发进行
D.升高温度,CO 的转化率可能下降
2
5.(2023·江苏盐城·盐城市伍佑中学校考模拟预测)卤族元素单质及其化合物应用广泛。 具有与卤
素单质相似的化学性质。 在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的 反应生成
硫酰氟( )。 与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37. 通入
酸性溶液中可制得黄绿色气体 ,该气体常用作自来水消毒剂。工业用 制备 的热化学方
程式为 。下列关于反应
的说法不正确的是
A.保持其他条件不变,平衡时升高温度,
B.保持其他条件不变,平衡时通入 ,达到新平衡时 变小
C.反应生成1mol ,转移电子数目为
D.及时分离出CO,有利于 生成
6.(2023·重庆渝中·重庆巴蜀中学校考模拟预测)1,2-二甲基环丙烷的顺反异构体可相互转化:
(顺式) (反式) ,该反应的速率方程为: (顺)和 (反),
和 分别为正、逆反应速率常数。 ℃时,加入顺式异构体发生反应,两种异构体的质量分数w随时间t
的变化如图所示。下列说法正确的是A.反应速率: (正) (逆)
B.L点:转化率为50%,Q(浓度商)>K
C.升高温度, 、 增大倍数:
D. ℃时发生反应,测得 ,则
7.(2023·海南省直辖县级单位·嘉积中学校考模拟预测)在一定温度下, 和C在一密闭容器中进行
反应: ,CO的平衡浓度(mol/L)的对数 与温度的倒数 的
关系如图所示,下列说法中正确的是
A.Q点CO的消耗速率大于其生成速率
B.该反应的
C.温度是 时,反应的平衡常数为1
D.温度不变,将R点状态的容器体积扩大,重新达到平衡时,气体的压强减小
8.(2023·河北衡水·河北武邑中学校考模拟预测)已知阿仑尼乌斯公式是反应速率常数随温度变化关系的
经验公式,可写作 (k为反应速率常数, 为反应活化能,R和C为大于0的常数),为探究
m、n两种催化剂对某反应的催化效能,进行了实验探究,依据实验数据获得曲线如图所示。下列说法错
误的是A.在m催化剂作用下,该反应的活化能
B.对该反应催化效能较高的催化剂是m
C.不改变其他条件,只升高温度,k值增大
D.无法根据该图像判断升高温度时平衡移动的方向
9.(2023·辽宁·朝阳市第一高级中学校联考一模)氨气去除NO的反应原理为:
,反应速率与浓度之间存在如下关系:
, , 、 为速率常数,只受温度影响。350℃时,
在2L恒容密闭容器中,通入 和 发生反应,保持温度不变,5min后反应达平
衡,NO的转化率为50%。下列说法正确的是
A.用 表示的化学反应速率为
B.350℃时,该反应的平衡常数为0.5
C.其他条件不变,往反应后的容器中再通入 和 ,重新达平衡时NO的体积分
数减小
D.当温度改变为T℃时,若 ,则
10.(2023·上海·模拟预测)一定温度下,向1L密闭容器中充入2molX和1molY,发生反应2X(g)
+Y(g) 3Z(?)。达到平衡时,容器的压强从原来的P 变为0.4P 。下列说法错误的是
0 0
A.Z不可能为气体
⇌
B.达到平衡时容器内有1.8molZ
C.压缩体积,再次达到平衡,X的浓度不变
D.Y的体积分数不变说明反应达到平衡状态
11.(2023·重庆·校联考模拟预测)一定温度下,在三个容积均为2.0L的恒容密闭容器中仅发生反应:
CHCOOH(g) CHOH(g)+CO(g) ΔH>0。下列说法正确的是
3 3
物质的起始浓度/mol·L-1 物质的平衡浓度/mol·L-1
容器编号 温度/K
c(CHOH) c(CO) c(CHCOOH) c(CHCOOH)
3 3 3
I 230 0.60 0.60 0 0.40
II 230 0.30 0.30 0.40
III 210 0 0 0.60
A.达平衡时,容器I与容器II中的总压强之比为6∶7
B.达平衡时,容器II中 比容器I中的大
C.达平衡时,容器III与容器I中的正反应速率相等
D.达平衡时,容器I中CHOH转化率与容器III中CHCOOH转化率之和大于1
3 312.(2023·重庆沙坪坝·重庆一中校考模拟预测)在催化剂的作用下,氢气还原 的过程中可同时发生
反应①②。
①
②
在恒温恒容密闭容器中,充入一定量的 及 ,起始及达到平衡时,容器内各气体的物质的量及总压的
部分数据如下表所示。
总压
起始 0.5 0.9 0 0 0 1.4p
平衡 m 0.3 p
下列说法正确的是
A.反应①任意温度下均能自发进行
B.恒温恒容下,再充入 和 ,反应①平衡右移,反应②平衡不移动
C.
D.反应②的平衡常数
二、主观题(共3小题,共40分)
13.(14分)(2023·上海·模拟预测)Ⅰ.H S与CH 重整,不但可以消除污染,还可以制氢。主要反应如
2 4
下:①CH(g)+2HS(g) CS(g)+4H(g)+Q(Q<0)
4 2 2 2
(1)在恒温恒容条件下,可作为反应①达到平衡状态的判断依据是___________(选填编号)。
A.混合气体密度不变 B.容器内压强不变
C.2v (H S)=v (CS) D.CH 与H 的物质的量分数之比保持不变
正 2 逆 2 4 2
Ⅱ.在恒压条件下,以n(CH)∶n(H S)=1∶2的组成的混合气体发生反应①,达到平衡状态时,四种组分物
4 2
质的量分数随温度的变化如图所示。
(2)如图中表示CH、CS 变化的曲线分别是 、 (选填编号)。
4 2
(3)M点对应温度下,HS的转化率是 。
2Ⅲ.在研究反应发生的适宜条件时发现:过多的CH 会导致Al O 催化剂失活;Co助剂有稳定催化剂的作用。
4 2 3
如图表示800℃,Al O 催化剂条件下投入等量HS,投料比[n(CH )∶n(H S)]分别为1∶1、1∶3、12∶1,
2 3 2 4 2
达平衡时HS转化率、平均反应速率。
2
(4)投料比n(CH)∶n(H S)=1∶1为对应图中 组图像(选填“A”“B”或“C”);在三组图像中,C
4 2
组图像中平均反应速率最低的可能原因是 。
(5)未添加Co助剂时,无积碳,随着Co添加量的变化,积碳量变化如图所示,Co助剂可能催化原料气发
生反应的化学方程式为 。
14.(12分)(2023·上海静安·统考二模)聚丙烯腈纤维俗名人造羊毛,由丙烯腈聚合而得。用丙烯合成
丙烯腈的反应如下: 2C H(g)+2NH (g)+3O(g) 2C HN(g)+6HO(g)+1030kJ
3 6 3 2 3 3 2
(1)某密闭容器中发生上述反应,生成丙烯腈的反应速率与反应时间的关系如下图所示。
t 时刻表示体系改变的反应条件为 ; t 时刻表示体系改变了另一反应条件,此时平衡 移动
1 2
(填“正向”、“逆向”或“不”)。
丙烯的转化率与反应温度的关系如图示:(2)有利于提高丙烯平衡转化率的反应条件有 ;
(3)最大转化率所对应的温度为460℃。当温度低于460℃时,丙烯的转化率 (填“是”或“不是”)
所对应温度下的平衡转化率,理由是 。
(4)一定条件下,在2L恒容密闭容器中,通入84g C H、34g NH、96g O ,若该反应5 min到达a点,则0
3 6 3 2
~5min内丙烯的平均反应速率为 mol∙L−1∙min−1。
15.(14分)(2023·上海黄浦·统考二模)NO 的排放主要来自于汽车尾气,包含NO 和NO。若用活性炭
x 2
对NO进行吸附,可发生C(s)+2NO(g) N(g)+CO (g),在T℃时,借助传感器测得反应在不同时间点上
2 2 1
各物质的浓度如表:
时间(min)
浓度(mol•L-1)
0 10 20 30 40 50
NO 1.00 0.58 0.40 0.40 0.48 0.48
N 0 0.21 0.30 0.30 0.36 0.36
2
(1)关于该反应说法错误的是 。
a.该反应体现了NO的氧化性
b.降低NO浓度能够减慢反应速率
c.加入足量的炭粉可以使NO100%转化
d.合适的催化剂可以加快反应速率
(2)表中0~10min内,NO的平均反应速率v(NO)= ;当升高反应温度,该反应的平衡常数K减小,说
明正反应为 反应(填“吸热”或“放热”).
(3)30min后,只改变某一条件,反应重新达到平衡;根据表中的数据判断改变的条件可能是 (填字
母)。
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
某实验室模拟该反应,在恒压密闭容器中加入足量的活性炭和一定量的NO气体,测得NO的转化率随温
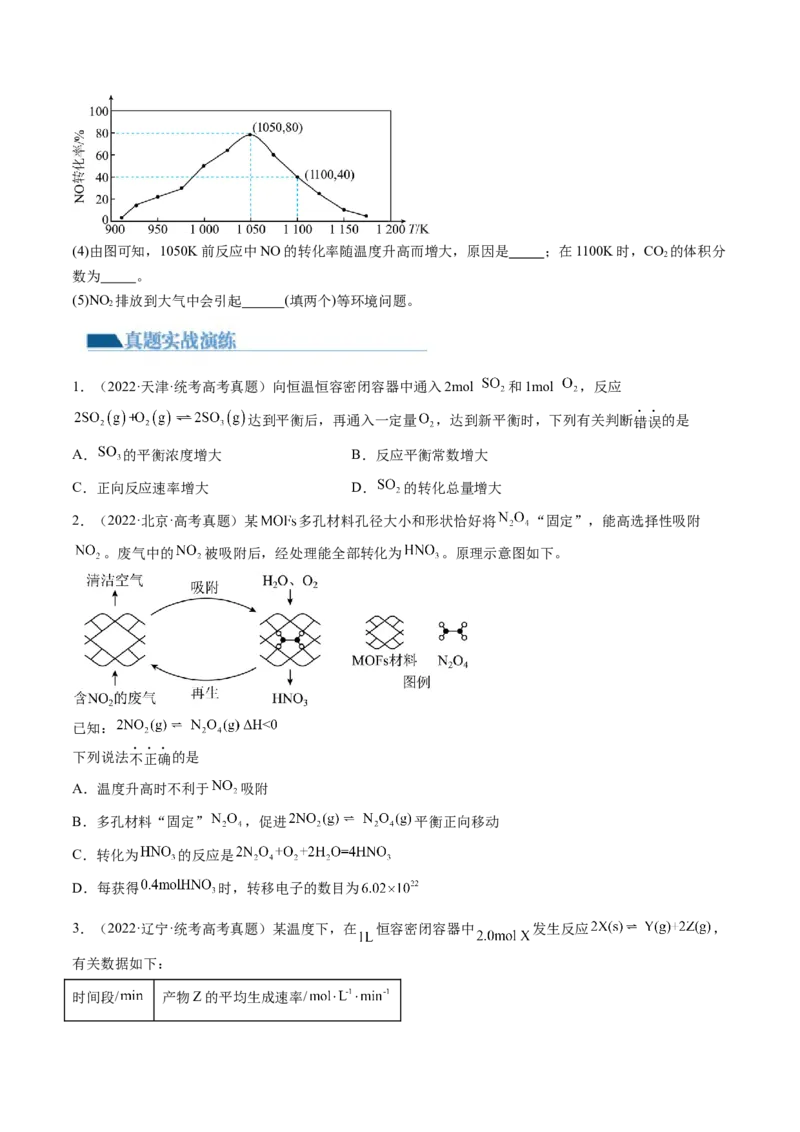
度的变化如图所示:(4)由图可知,1050K前反应中NO的转化率随温度升高而增大,原因是 ;在1100K时,CO 的体积分
2
数为 。
(5)NO 排放到大气中会引起 (填两个)等环境问题。
2
1.(2022·天津·统考高考真题)向恒温恒容密闭容器中通入2mol 和1mol ,反应
达到平衡后,再通入一定量 ,达到新平衡时,下列有关判断错误的是
A. 的平衡浓度增大 B.反应平衡常数增大
C.正向反应速率增大 D. 的转化总量增大
2.(2022·北京·高考真题)某 多孔材料孔径大小和形状恰好将 “固定”,能高选择性吸附
。废气中的 被吸附后,经处理能全部转化为 。原理示意图如下。
已知:
下列说法不正确的是
A.温度升高时不利于 吸附
B.多孔材料“固定” ,促进 平衡正向移动
C.转化为 的反应是
D.每获得 时,转移电子的数目为
3.(2022·辽宁·统考高考真题)某温度下,在 恒容密闭容器中 发生反应 ,
有关数据如下:
时间段/ 产物Z的平均生成速率/0~2 0.20
0~4 0.15
0~6 0.10
下列说法错误的是
A. 时,Z的浓度大于
B. 时,加入 ,此时
C. 时,Y的体积分数约为33.3%
D. 时,X的物质的量为
4.(2022·海南·统考高考真题)某温度下,反应CH=CH (g)+HO(g) CHCHOH(g)在密闭容器中达到平
2 2 2 3 2
衡,下列说法正确的是
A.增大压强, ,平衡常数增大
B.加入催化剂,平衡时 的浓度增大
C.恒容下,充入一定量的 ,平衡向正反应方向移动
D.恒容下,充入一定量的 , 的平衡转化率增大
5.(2022·浙江·统考高考真题)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下
列说法不正确的是
A.实验①, ,
B.实验②, 时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
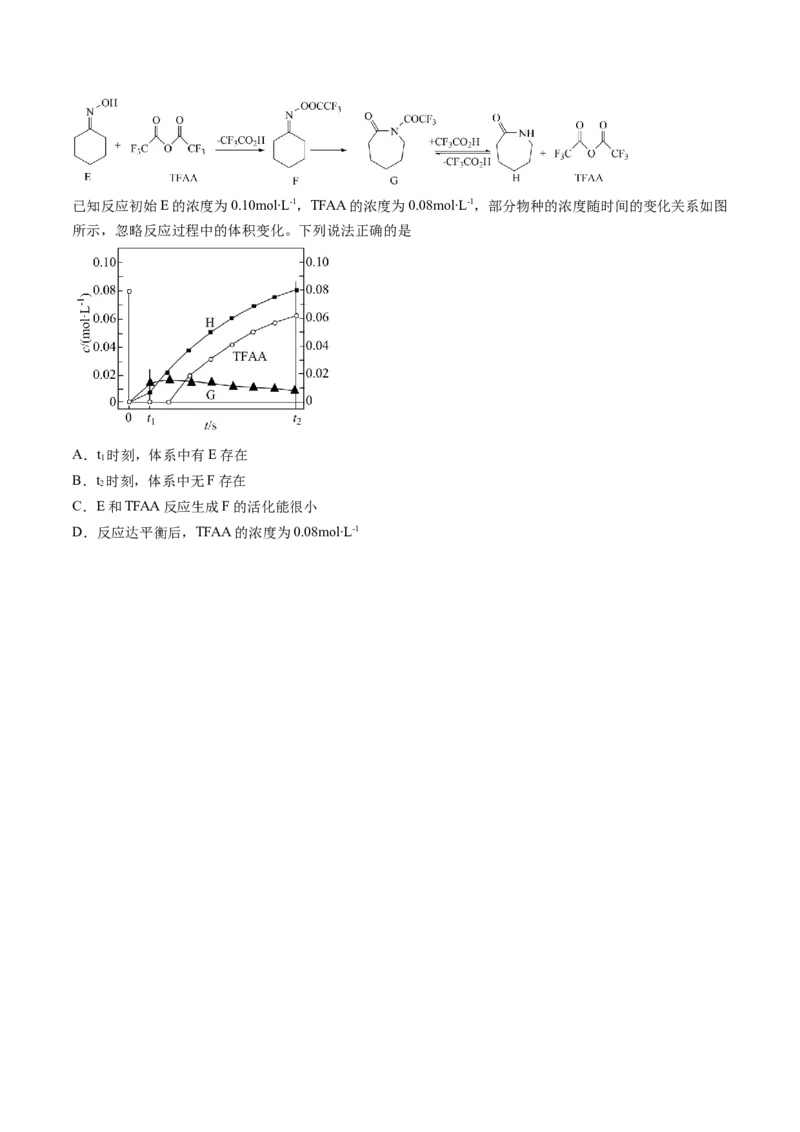
6.(2023·山东·统考高考真题)一定条件下,化合物E和TFAA合成H的反应路径如下:已知反应初始E的浓度为0.10mol∙L-1,TFAA的浓度为0.08mol∙L-1,部分物种的浓度随时间的变化关系如图
所示,忽略反应过程中的体积变化。下列说法正确的是
A.t 时刻,体系中有E存在
1
B.t 时刻,体系中无F存在
2
C.E和TFAA反应生成F的活化能很小
D.反应达平衡后,TFAA的浓度为0.08mol∙L-1