文档内容
第 25 讲 盐类水解
第一部分:高考真题感悟
1.(2022·浙江·高考真题)水溶液呈酸性的盐是
A.NH Cl B.BaCl C.HSO D.Ca(OH)
4 2 2 4 2
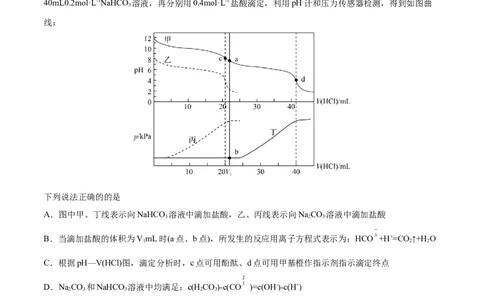
2.(2022·浙江·高考真题)某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1NaCO 溶液和
2 3
40mL0.2mol·L-1NaHCO 溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲
3
线:
下列说法正确的的是
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐酸
3 2 3
B.当滴加盐酸的体积为VmL时(a点、b点),所发生的反应用离子方程式表示为:HCO +H+=CO ↑+H O
1 2 2
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.NaCO 和NaHCO 溶液中均满足:c(HCO)-c(CO )=c(OH-)-c(H+)
2 3 3 2 3
3.(2020·浙江·高考真题)某固体混合物X,含有Al (SO )、FeCl 、NaCO 和CuSO 中的几种,进行如
2 4 3 3 2 3 4
下实验:
①X与水作用有气泡冒出,得到有色沉淀Y和弱碱性溶液Z;②沉淀Y与NaOH溶液作用,无变化。
下列说法不正确的是
A.混合物X中必定含有NaCO,不含Al (SO )
2 3 2 4 3
B.溶液Z中溶质主要是钠盐,且必含NaHCO
3
C.灼烧沉淀Y,可能得到黑色物质D.往溶液Z中加入Cu粉,若不溶解,说明X中不含FeCl
3
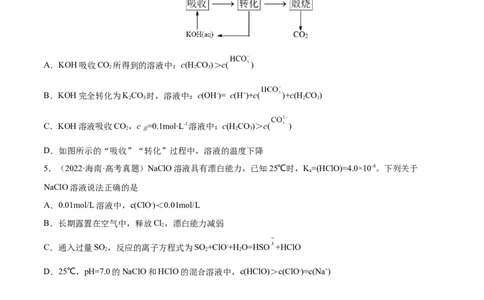
4.(2022·江苏·高考真题)一种捕集烟气中CO 的过程如图所示。室温下以0.1mol∙L-1KOH溶液吸收
2
CO,若通入CO 所引起的溶液体积变化和HO挥发可忽略,溶液中含碳物种的浓度c =c(H CO)+c(
2 2 2 总 2 3
)+c( )。HCO 电离常数分别为K =4.4×10-7、K =4.4×10-11。下列说法正确的是
2 3 a1 a2
A.KOH吸收CO 所得到的溶液中:c(H CO)>c( )
2 2 3
B.KOH完全转化为KCO 时,溶液中:c(OH-)= c(H+)+c( )+c(H CO)
2 3 2 3
C.KOH溶液吸收CO,c =0.1mol∙L-1溶液中:c(H CO)>c( )
2 总 2 3
D.如图所示的“吸收”“转化”过程中,溶液的温度下降
5.(2022·海南·高考真题)NaClO溶液具有漂白能力,已知25℃时,K=(HClO)=4.0×10-8。下列关于
a
NaClO溶液说法正确的是
A.0.01mol/L溶液中,c(ClO-)<0.01mol/L
B.长期露置在空气中,释放Cl,漂白能力减弱
2
C.通入过量SO ,反应的离子方程式为SO +ClO-+H O=HSO +HClO
2 2 2
D.25℃,pH=7.0的NaClO和HClO的混合溶液中,c(HClO)>c(ClO-)=c(Na+)
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·浙江绍兴·模拟预测)下列物质的水溶液因水解而呈酸性的是
A. B. C. D.
2.(2022·上海嘉定·二模)氯化铵溶液中放入镁粉能放出H 和NH ,产生这种现象的原因是
2 3A.金属镁能把NH 置换出来
3
B.镁具有强还原性,NH 具有氧化性,发生氧化还原反应
C.因为NH 水解溶液显酸性,Mg与H+反应放出H,平衡向正反应方向移动
2
D.因为Mg与HO反应,生成Mg(OH) 与NH Cl反应
2 2 4
3.(2022·江苏泰州·模拟预测)下列有关物质的性质与用途不具有对应关系的是
A.硫酸亚铁水溶液呈弱酸性,可用作食品抗氧化剂
B.小苏打水溶液呈弱碱性,可用作制药中的抗酸剂
C.氨气具有还原性,可用作烟气中NO 脱除
x
D.漂白粉具有强氧化性,可用作游泳池的杀菌消毒剂
4.(2022·河南河南·模拟预测)《本草图经》有“白矾多入药用”。白矾[KAl(SO)·12H O]又称明矾、钾
4 2 2
明矾等,是一种重要的化学试剂。下列说法正确的是
A.白矾可用于自来水杀菌消毒
B.白矾溶液中n(K+):n(Al3+)=1:1
C.白矾溶液可清洗铜镜表面铜锈
D.灼烧白矾时可直接观察焰色呈紫色
5.(2022·河南·模拟预测)“天宫课堂”中王亚平老师在空间站“变”出奥运五环,在透明的五环模型中
第一次、第二次分别加入的溶液如下表所示[已知溴百里酚蓝变色的pH范围:6.0(黄)~7.6(蓝)]。下列叙述
正确的是
1号环 2号环 3号环 4号环 5号环
第一次加 乙酸溶
NaCO 溶液 KI和KIO 溶液 NaCO 溶液 NaCO 溶液
入 2 3 3 液 2 3 2 3
第二次加
溴百里酚蓝 淀粉溶液,乙酸 甲基橙 甲基橙 甲基橙、溴百里酚蓝
入
A.1号环中 水解的离子方程式为 +2HO=HCO+2OH-
2 2 3B.2号环中发生的离子反应为5I-+ +6H+=3I +3HO
2 2
C.3号环中溶液的pH若为a,将其稀释10倍则pH变为a+1
D.5号环最后溶液呈现的绿色是黄色与蓝色的混合色
6.(2022·重庆南开中学模拟预测)劳动创造美好未来。下列叙述正确的是
A.施加适量石膏可降低盐碱地的碱性 B.铵态氮肥和草木灰混合施用可提高肥效
C.用稀硫酸清洗锅炉中的水垢 D.84消毒液和洁厕剂混合使用效果更好
7.(2022·江苏省平潮高级中学模拟预测)室温下,通过下列实验探究NaCO 溶液的性质。用K 、K 分
2 3 a1 a2
别表示HCO 的第一步和第二步电离常数。
2 3
实验 实验操作和现象
1 用pH试纸测定0.1mol·L-1NaCO 溶液的pH,测得pH约为12
2 3
2 向0.1mol·L-1NaCO 溶液中加入过量0.2mol·L-1CaCl 溶液,产生白色沉淀
2 3 2
3 向0.1mol·L-1NaCO 溶液中通入过量CO,测得溶液pH约为8
2 3 2
4 向含有酚酞的0.1mol·L-1NaCO 中滴加几滴0.2mol·L-1NaOH,红色加深
2 3
下列有关说法不正确的是
A.0.1mol·L-1NaCO 溶液中存在c(OH-)=c(H+)+2c(H CO)+c(HCO )
2 3 2 3
B.实验2反应静置后的上层清液中有c(Ca2+)·c(CO )=K (CaCO)
sp 3
C.实验3得到的溶液中有c(HCO )>c(HCO)>c(CO ),且K K <K
2 3 a1 a2 w
D.实验4中滴加的NaOH抑制了CO 的水解, 的值变小
8.(2022·安徽省广德中学模拟预测)二元酸HA在水中的电离方程式为:HA=H++HA-,HA- H++A2-。
2 2
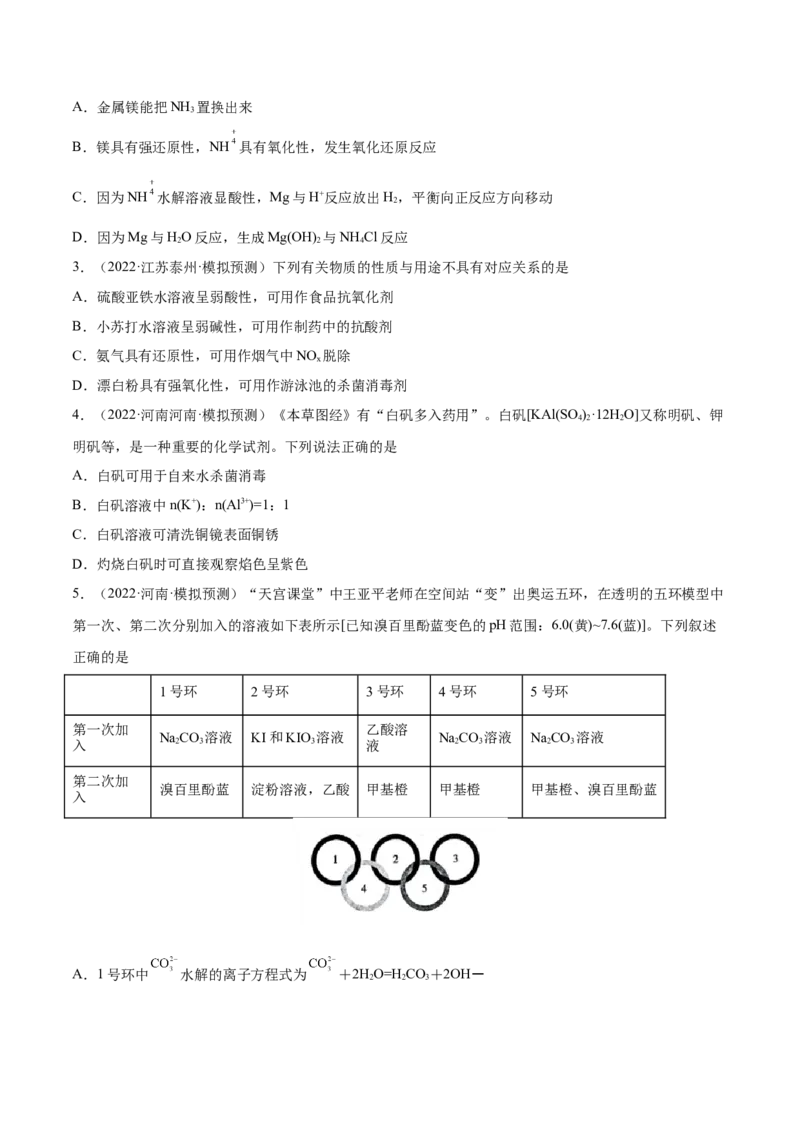
25°C时,向20.00mL 0.1mol/L H A溶液中加入NaOH溶液,pOH 与所加NaOH溶液体积的关系如图所示。
2 水
已知:pOH 表示溶液中由水电离出的c (OH- )的负对数[-lgc (OH-)]。下列说法中不正确的是(忽略过程
水 水 水
中溶液的体积变化)A.A点溶液,c(H+ )=1 × 10-0.9 mol/L
B.B点溶液呈酸性,原因是NaHA电离程度比水解程度大
C.C点至D点变化过程中 逐渐减小
D.D点溶液中:c(Na+)+c(HA-)+c(A2-)=0.1mol/L
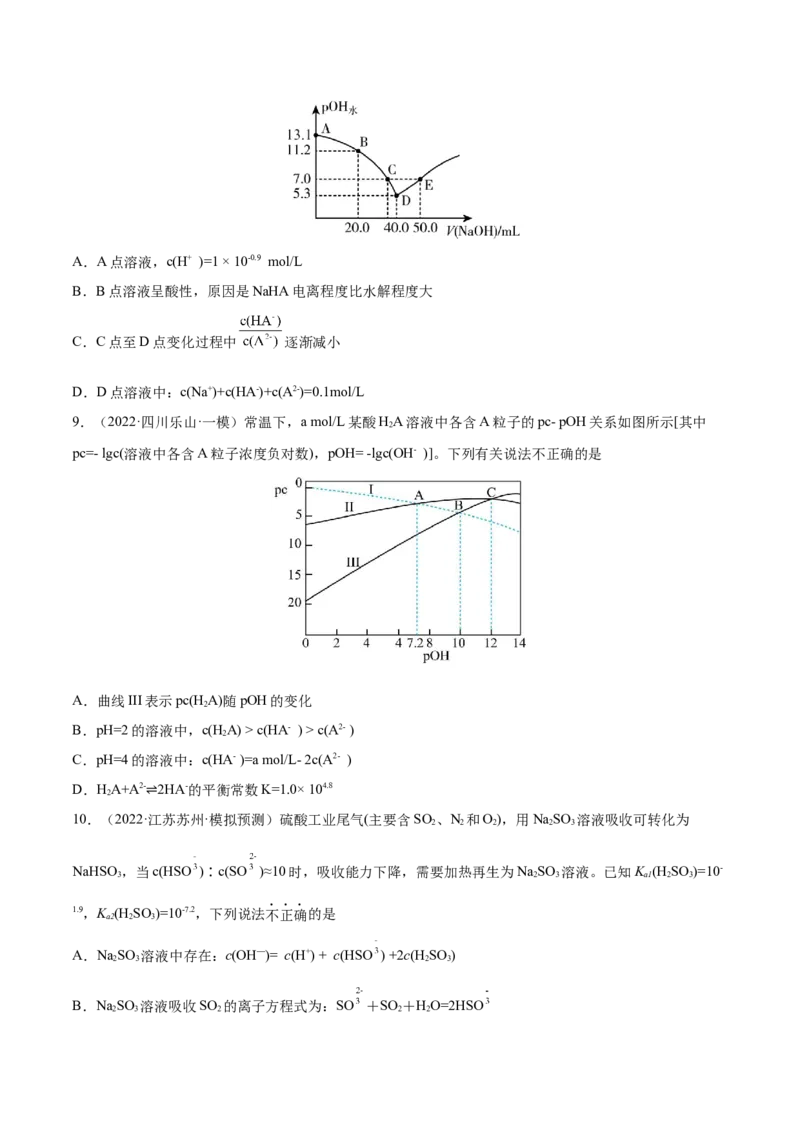
9.(2022·四川乐山·一模)常温下,a mol/L某酸HA溶液中各含A粒子的pc- pOH关系如图所示[其中
2
pc=- lgc(溶液中各含A粒子浓度负对数),pOH= -lgc(OH- )]。下列有关说法不正确的是
A.曲线III表示pc(HA)随pOH的变化
2
B.pH=2的溶液中,c(HA) > c(HA- ) > c(A2- )
2
C.pH=4的溶液中:c(HA- )=a mol/L- 2c(A2- )
D.HA+A2- 2HA-的平衡常数K=1.0× 104.8
2
10.(2022·⇌江苏苏州·模拟预测)硫酸工业尾气(主要含SO
2
、N
2
和O
2
),用Na
2
SO
3
溶液吸收可转化为
NaHSO,当c(HSO )∶c(SO )≈10时,吸收能力下降,需要加热再生为NaSO 溶液。已知K (H SO )=10-
3 2 3 a1 2 3
1.9,K (H SO )=10-7.2,下列说法不正确的是
a2 2 3
A.NaSO 溶液中存在:c(OH—)= c(H+) + c(HSO ) +2c(H SO )
2 3 2 3
B.NaSO 溶液吸收SO 的离子方程式为:SO +SO +HO=2HSO
2 3 2 2 2C.当c(HSO ):c(SO )=10时,此时吸收液的pH=6.2
D.与原NaSO 溶液相比,吸收液充分分解放出SO 再生后吸收SO 能力几乎不变
2 3 2 2
11.(2022·广东广州·模拟预测)50℃时,下列各溶液中,离子的物质的量浓度关系正确的是
A. 的 溶液中,
B. 和 的酸性混合溶液中,
C. 溶液中,
D. 的 溶液中:
12.(2022·广东实验中学三模)室温下,用0.1 mol/L 的盐酸滴定相同浓度的25 mL溴化肼(N HBr)溶液,
2 5
已知肼(N H)是二元弱碱,NH+H O NH +OH﹣ K =1.0×10﹣6,NH +H O +OH﹣ K =1.3×10﹣
2 4 2 4 2 2 b1 2 2 b2
⇌ ⇌
15,滴定过程中混合溶液的相对导电能力变化曲线如图所示。下列叙述错误的是
A.NH 与硫酸反应形成的酸式盐的化学式为NH(HSO )
2 4 2 6 4 2
B.b点表示盐酸与溴化肼恰好完全反应:c(Cl﹣)=c(Br﹣)>c( )
C.a点对应的溶液中:c(Br﹣)+c(OH﹣)=c(N H )+2c( )+c(H+)
2
D.c点的混合溶液中:c(Cl﹣)>c(Br﹣)>c(H+)>c( )>c(NH )>c(OH﹣)
2
二、主观题(共3小题,共40分)
13.(2021·福建省福州第一中学模拟预测)(12分)人体内尿酸(HUr)含量偏高,关节滑液中产生尿酸钠
晶体(NaUr)会引发痛风,NaUr(s) Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研
究,回答下列问题:已知:①37℃时,K(HUr) = 4×10−6,K = 2.4×10−14,K (NaUr) = 6.4×10−5
a w sp
②37℃时,模拟关节滑液pH =7.4,c(Ur-) =4.6×10−4 mol∙L−1
(1)尿酸电离方程式为_______
(2)K 为盐的水解常数,37℃时,K(Ur−)=_______。
h h
(3)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中c(Na+)_______c(Ur−) (填“>”、
“<”或“=”)。
(4)37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+) = 0.2 mol∙L−1时,通过计算判断是否有NaUr晶体析
出,请写出判断过程_______
(5)对于尿酸偏高的人群,下列建议正确的是_______。
a.加强锻炼,注意关节保暖 b.多饮酒,利用乙醇杀菌消毒
c.多喝水,饮食宜少盐、少脂 d.减少摄入易代谢出尿酸的食物
14.(2021·新疆·一模)(14分)化学上把外加少量酸、碱,而pH基本不变的溶液,称为缓冲溶液。
I.现有25℃时,浓度均为 的 和 的缓冲溶液,pH=4.76,回答下列问题:
[25℃时 , 为盐的水解常数]
(1)25℃时 _______(写表达式),计算 _______(保留三位有效数字)。
(2)该缓冲溶液中离子浓度由大到小的顺序是_______。
(3)用1.0L上述缓冲溶液中滴加几滴NaOH稀溶液(忽略溶液体积的变化),反应后溶液中
c(H+)_______mol/L。
(4)改变下列条件,能使 稀溶液中 保持增大的是_______。
a.升温 b.加入NaOH固体 c.稀释 d.加入CHCOONa固体
3
II.人体血液里主要通过碳酸氢盐缓冲体系( )维持pH稳定。已知正常人体血液在正常体温时,
的一级电离常数 , , 。由题给数据可算得正常人体血液的pH约为_____,当过量的酸进入血液中时,血液缓冲体系中 的值将___(填“变大”“变小”或“不
变”)。
15.(2022·安徽·模拟预测)(14分)某小组从反应速率和产物角度探究Mg与NaHCO 溶液反应。
3
实验I、25°C, 相同镁条分别与下列试剂反应
序 浓度 体积
试剂 pH 现象
号 (mol·L-1) (mL)
i HO —— 7.5 7 镁条表面有微量气泡附着
2
ii 1.0 7.5 8.4
NaHCO 溶 镁条表面持续产生大量气泡,溶液略显浑浊,点燃气
3
液 泡有爆鸣声
(1)已知: Mg(OH) 固体致密,易包裹在金属表面成膜。根据上述现象,推测在实验ii中。
2
①Mg可以提高 的电离程度,原因是___________;
②浑浊的主要原因是产生了___________(填化学式) ;
③实验ii中产生气泡的速率快于实验i的原因可能是___________。
(2)补充实验II,证实(1)的推测:
序号 试剂 浓度(mol·L-1) 体积(mL) pH 现象
iii NaNO 溶液 1.0 7.5 7 镁条表面有微量气泡附着
3
iv NaCO 溶液 0.5 7.5 11.8 持续产生少量气泡,溶液显浑浊
2 3
①小组设计实验iii 的目的是___________ ; 甲同学结合实验iv的现象认为可以不必进行实验iii,他的理
由是___________;
②实验ii生成气体的速率快于实验iv,原因可能是___________ ;
③查资料知 +Mg2+[Mg(HCO)]+,请从平衡移动的角度解释实验ii产生气体速率更快的原因
3
___________。