文档内容
第 28 讲 定性、定量实验
1.某小组同学欲通过实验探究影响金属与酸反应速率的因素,进行下列实验。
实验装置:
序号 实验操作 实验现象
钠浮在液面上并来回移动,表面出现白色固体;白
取下胶塞,放入一小片金
实验1 色固体逐渐沉到烧杯底部,液体不沸腾;气球迅速
属钠,迅速塞上胶塞
鼓起,15 s时测量气球直径约为3 cm
取下胶塞,放入与钠表面 镁条开始时下沉,很快上浮至液面,片刻后液体呈
实验2 积基本相同的镁条,迅速 沸腾状,同时产生大量白雾;气球迅速鼓起,15 s时
塞上胶塞 测量气球直径约为5 cm
下列说法不正确的是( )
A.实验1获得的白色小颗粒可用焰色试验检验其中的Na元素
B.对比实验1与实验2,不能说明钠比镁的金属活动性强
C.对比实验1与实验2,能说明同温下NaCl的溶解度比MgCl 的小
2
D.金属钠、镁与盐酸反应的速率与生成物状态等因素有关
2.高纯碘化钠晶体是核医学、大型安防设备、暗物质探测等领域的核心材料。某研究小组在实验室制
备高纯NaI的简化流程如图:
已知:①I(s)+I-(aq)I(aq)。
2
②水合肼(N H·H O)具有强还原性,可将各种价态的碘还原为I-,氧化产物为N。
2 4 2 2
③NaI易被氧化,易溶于水、酒精,在酒精中的溶解度随温度的升高增加不大。
回答下列问题:(1)①步骤Ⅰ,I 与NaCO 溶液同时发生两个反应,生成物除NaI外,还分别生成NaIO和NaIO ,一
2 2 3 3
个反应为 I +NaCO===NaI+NaIO+CO↑,另一个反应为___________________________(填化学方程
2 2 3 2
式)。
②I 与 NaCO 溶液的反应很慢,加入 NaI 固体能使开始反应时的速率明显加快,原因可能是
2 2 3
___________________________________________________________________________________。
(2)步骤Ⅱ,水合肼与IO反应的离子方程式为___________________________________。
(3)步骤Ⅲ,多步操作为:
①将步骤Ⅱ得到的pH为6.5~7的溶液调整pH至9~10,在100 ℃下保温8 h,得到溶液A;
②将溶液A的pH调整至3~4,在70~80 ℃下保温4 h,得溶液B;
③将溶液B的pH调整至6.5~7,得溶液C;
④在溶液C中加入活性炭,混合均匀后煮沸,静置10~24 h后,过滤除杂得粗NaI溶液。
上述①②③操作中,调整pH时依次加入的试剂为__________、___________、___________(填字母)。
A.NaOH B.HI
C.NH ·H O D.高纯水
3 2
(4)步骤Ⅳ,蒸发操作为减压蒸发。
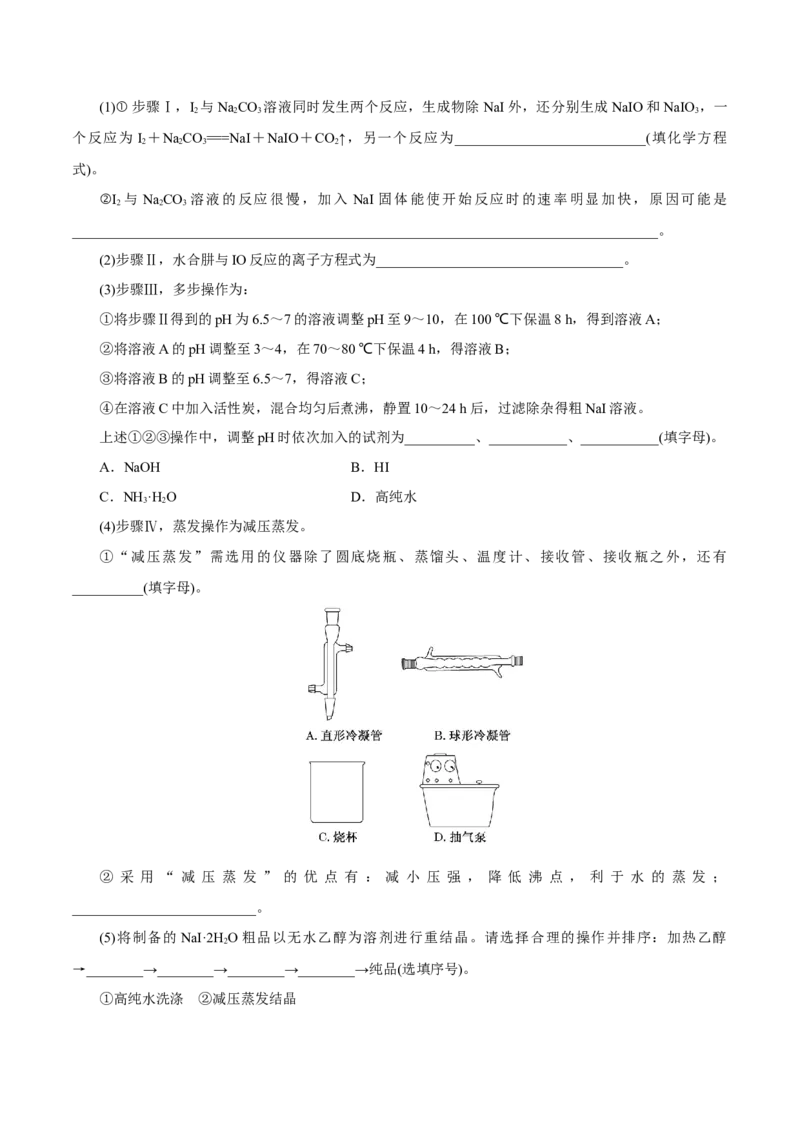
①“减压蒸发”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管、接收瓶之外,还有
__________(填字母)。
② 采 用 “ 减 压 蒸 发 ” 的 优 点 有 : 减 小 压 强 , 降 低 沸 点 , 利 于 水 的 蒸 发 ;
__________________________。
(5)将制备的 NaI·2H O粗品以无水乙醇为溶剂进行重结晶。请选择合理的操作并排序:加热乙醇
2
→________→________→________→________→纯品(选填序号)。
①高纯水洗涤 ②减压蒸发结晶③真空干燥 ④NaI·2H O粗品溶解
2
⑤趁热过滤 ⑥降温结晶
3.实验小组制备高铁酸钾(K FeO)并探究其性质。
2 4
资料:KFeO 为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O ,在
2 4 2
碱性溶液中较稳定。
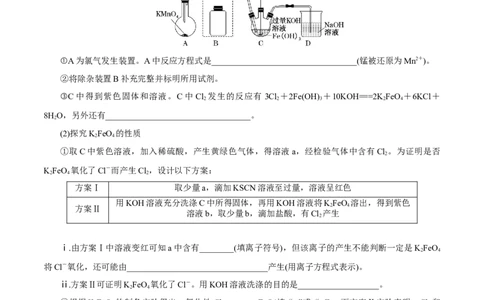
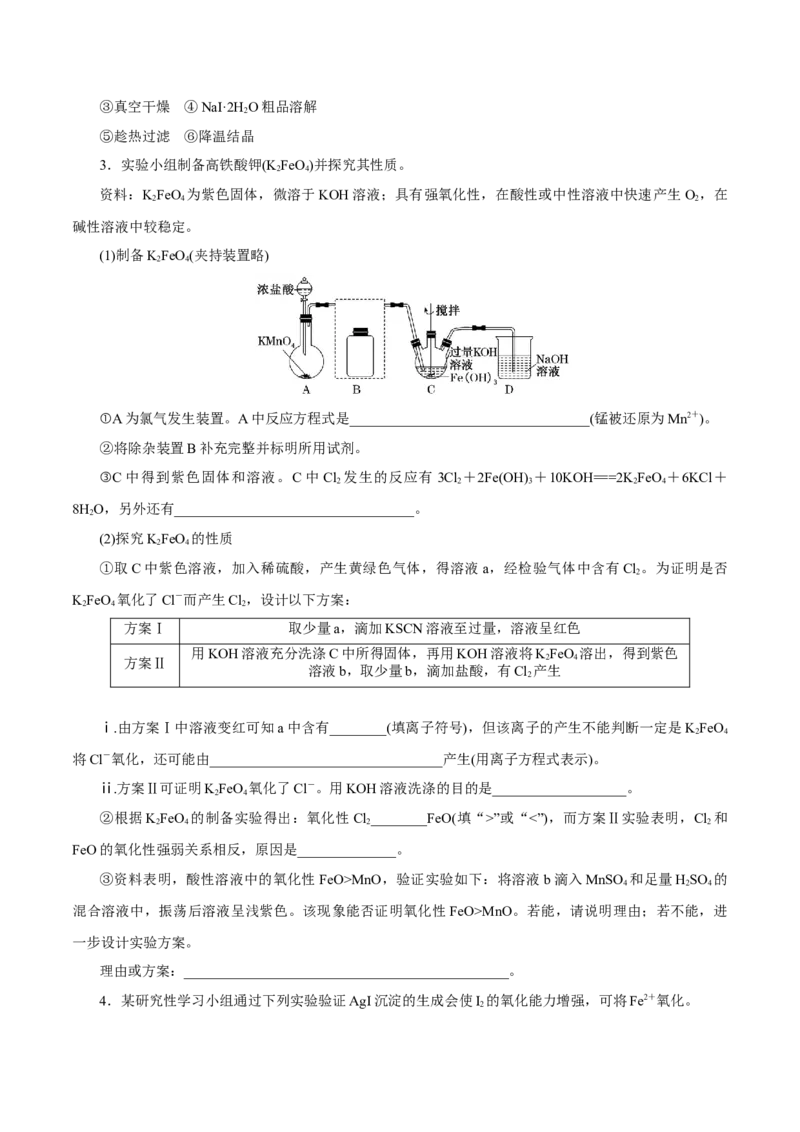
(1)制备KFeO(夹持装置略)
2 4
①A为氯气发生装置。A中反应方程式是__________________________________(锰被还原为Mn2+)。
②将除杂装置B补充完整并标明所用试剂。
③C中得到紫色固体和溶液。C中Cl 发生的反应有 3Cl +2Fe(OH) +10KOH===2K FeO +6KCl+
2 2 3 2 4
8HO,另外还有__________________________________。
2
(2)探究KFeO 的性质
2 4
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl 。为证明是否
2
KFeO 氧化了Cl-而产生Cl,设计以下方案:
2 4 2
方案Ⅰ 取少量a,滴加KSCN溶液至过量,溶液呈红色
用KOH溶液充分洗涤C中所得固体,再用KOH溶液将KFeO 溶出,得到紫色
方案Ⅱ 2 4
溶液b,取少量b,滴加盐酸,有Cl 产生
2
ⅰ.由方案Ⅰ中溶液变红可知a中含有________(填离子符号),但该离子的产生不能判断一定是KFeO
2 4
将Cl-氧化,还可能由_________________________________产生(用离子方程式表示)。
ⅱ.方案Ⅱ可证明KFeO 氧化了Cl-。用KOH溶液洗涤的目的是___________________。
2 4
②根据KFeO 的制备实验得出:氧化性Cl________FeO(填“>”或“<”),而方案Ⅱ实验表明,Cl 和
2 4 2 2
FeO的氧化性强弱关系相反,原因是______________。
③资料表明,酸性溶液中的氧化性FeO>MnO,验证实验如下:将溶液b滴入MnSO 和足量HSO 的
4 2 4
混合溶液中,振荡后溶液呈浅紫色。该现象能否证明氧化性FeO>MnO。若能,请说明理由;若不能,进
一步设计实验方案。
理由或方案:______________________________________________。
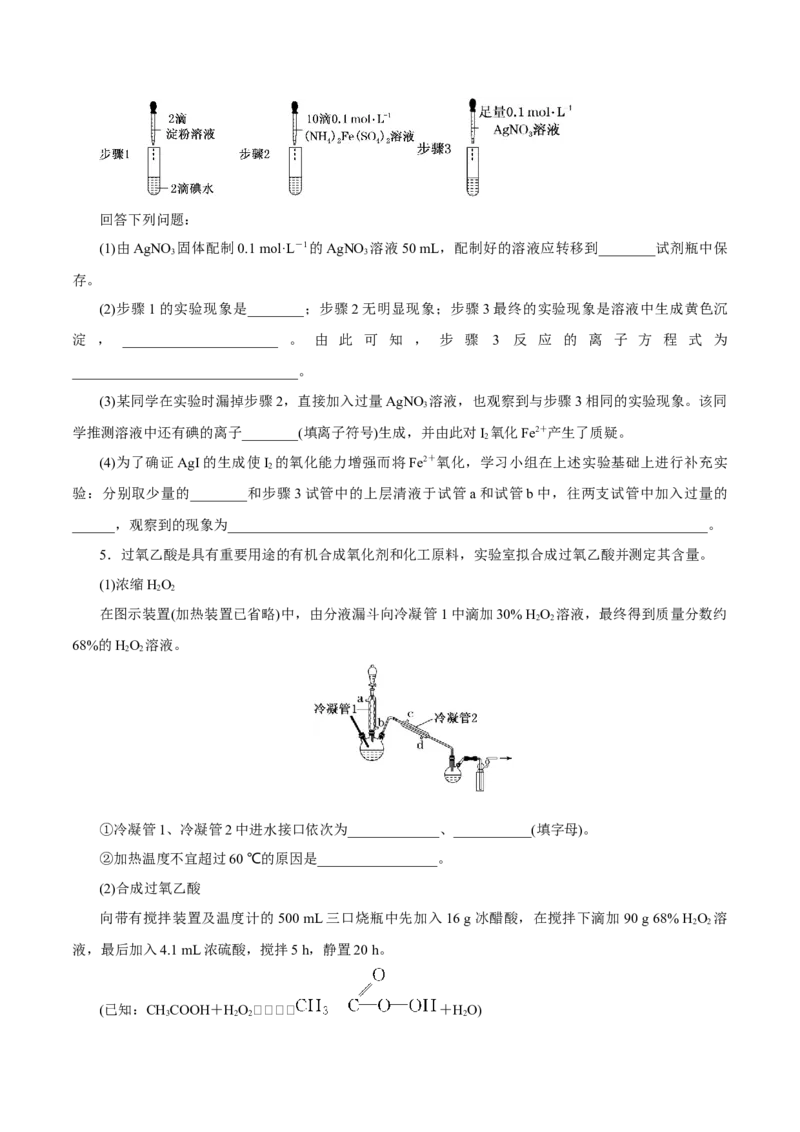
4.某研究性学习小组通过下列实验验证AgI沉淀的生成会使I 的氧化能力增强,可将Fe2+氧化。
2回答下列问题:
(1)由AgNO 固体配制0.1 mol·L-1的AgNO 溶液50 mL,配制好的溶液应转移到________试剂瓶中保
3 3
存。
(2)步骤1的实验现象是________;步骤2无明显现象;步骤3最终的实验现象是溶液中生成黄色沉
淀 , ______________________ 。 由 此 可 知 , 步 骤 3 反 应 的 离 子 方 程 式 为
________________________________。
(3)某同学在实验时漏掉步骤2,直接加入过量AgNO 溶液,也观察到与步骤3相同的实验现象。该同
3
学推测溶液中还有碘的离子________(填离子符号)生成,并由此对I 氧化Fe2+产生了质疑。
2
(4)为了确证AgI的生成使I 的氧化能力增强而将Fe2+氧化,学习小组在上述实验基础上进行补充实
2
验:分别取少量的________和步骤3试管中的上层清液于试管a和试管b中,往两支试管中加入过量的
______,观察到的现象为____________________________________________________________________。
5.过氧乙酸是具有重要用途的有机合成氧化剂和化工原料,实验室拟合成过氧乙酸并测定其含量。
(1)浓缩HO
2 2
在图示装置(加热装置已省略)中,由分液漏斗向冷凝管1中滴加30% H O 溶液,最终得到质量分数约
2 2
68%的HO 溶液。
2 2
①冷凝管1、冷凝管2中进水接口依次为_____________、___________(填字母)。
②加热温度不宜超过60 ℃的原因是_________________。
(2)合成过氧乙酸
向带有搅拌装置及温度计的500 mL三口烧瓶中先加入16 g冰醋酸,在搅拌下滴加90 g 68% H O 溶
2 2
液,最后加入4.1 mL浓硫酸,搅拌5 h,静置20 h。
(已知:CHCOOH+HO +HO)
3 2 2 2①用浓缩的68% H O 溶液代替常见的30% H O 溶液的目的是_______________。
2 2 2 2
②充分搅拌的目的是______________________________。
(3)过氧乙酸含量的测定
步骤a:称取5.0 g过氧乙酸试样(液体),配制成100 mL溶液A。
步骤b:在碘量瓶中加入5.0 mL H SO 溶液、3滴MnSO 溶液、5.0 mL溶液A,摇匀,用0.01 mol·L-
2 4 4
1的KMnO 溶液滴定至溶液呈微红色。
4
步骤c:向滴定后的溶液中再加1.0 g KI(CH COOOH+2H++2I-===I +CHCOOH+HO),摇匀,置
3 2 3 2
于暗处5 min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂 20 mL,摇匀,用淀粉溶液作指示剂,用0.05
mol·L-1的NaSO 标准溶液滴定至蓝色刚好褪去(I+2SO===2I-+SO)。
2 2 3 2 2 4
重复步骤b、步骤c三次,测得平均消耗NaSO 标准溶液的体积为20.00 mL。
2 2 3
①步骤a中配制溶液A时,需要用到的玻璃仪器除烧杯、100 mL容量瓶,玻璃棒和量筒外,还需要
____________。
②设计步骤b的目的是__________________。
③过氧乙酸的质量分数为__________%。
6.某小组对木炭与浓硝酸的反应进行探究。
已知:2NaOH+2NO ===NaNO +NaNO +HO,2NaOH+NO +NO===2NaNO +HO。
2 3 2 2 2 2 2
请回答下列问题:
Ⅰ.甲同学设计如图所示装置制备并收集NO(夹持装置省略)。
(1)木炭与浓硝酸反应的化学方程式为_____________________________。
(2)装置C的作用为_____________________________________________________。
(3)乙同学认为用装置F代替装置B更合理,理由为_____________________________。
Ⅱ.探究NO与NaO 的反应
2 2
已知:NaNO 既有氧化性,又有还原性;J处硬质玻璃管中制得的NaNO 中含有少量NaNO 。
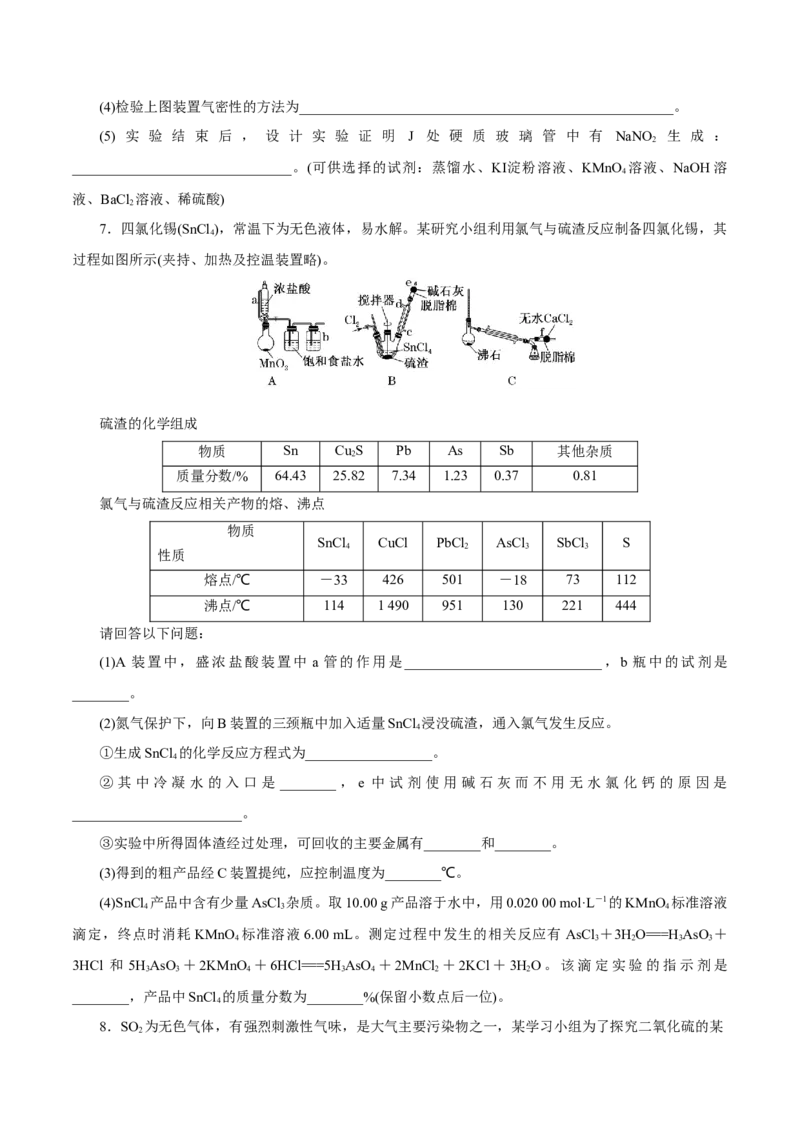
2 2 3(4)检验上图装置气密性的方法为_____________________________________________________。
(5) 实 验 结 束 后 , 设 计 实 验 证 明 J 处 硬 质 玻 璃 管 中 有 NaNO 生 成 :
2
_______________________________。(可供选择的试剂:蒸馏水、KI淀粉溶液、KMnO 溶液、NaOH溶
4
液、BaCl 溶液、稀硫酸)
2
7.四氯化锡(SnCl ),常温下为无色液体,易水解。某研究小组利用氯气与硫渣反应制备四氯化锡,其
4
过程如图所示(夹持、加热及控温装置略)。
硫渣的化学组成
物质 Sn Cu S Pb As Sb 其他杂质
2
质量分数/% 64.43 25.82 7.34 1.23 0.37 0.81
氯气与硫渣反应相关产物的熔、沸点
物质
SnCl CuCl PbCl AsCl SbCl S
4 2 3 3
性质
熔点/℃ -33 426 501 -18 73 112
沸点/℃ 114 1 490 951 130 221 444
请回答以下问题:
(1)A 装置中,盛浓盐酸装置中 a 管的作用是____________________________,b 瓶中的试剂是
________。
(2)氮气保护下,向B装置的三颈瓶中加入适量SnCl 浸没硫渣,通入氯气发生反应。
4
①生成SnCl 的化学反应方程式为__________________。
4
②其中冷凝水的入口是 ________,e 中试剂使用碱石灰而不用无水氯化钙的原因是
________________________。
③实验中所得固体渣经过处理,可回收的主要金属有________和________。
(3)得到的粗产品经C装置提纯,应控制温度为________℃。
(4)SnCl 产品中含有少量AsCl 杂质。取10.00 g产品溶于水中,用0.020 00 mol·L-1的KMnO 标准溶液
4 3 4
滴定,终点时消耗KMnO 标准溶液6.00 mL。测定过程中发生的相关反应有 AsCl +3HO===H AsO +
4 3 2 3 3
3HCl 和 5HAsO +2KMnO +6HCl===5H AsO +2MnCl +2KCl+3HO。该滴定实验的指示剂是
3 3 4 3 4 2 2
________,产品中SnCl 的质量分数为________%(保留小数点后一位)。
4
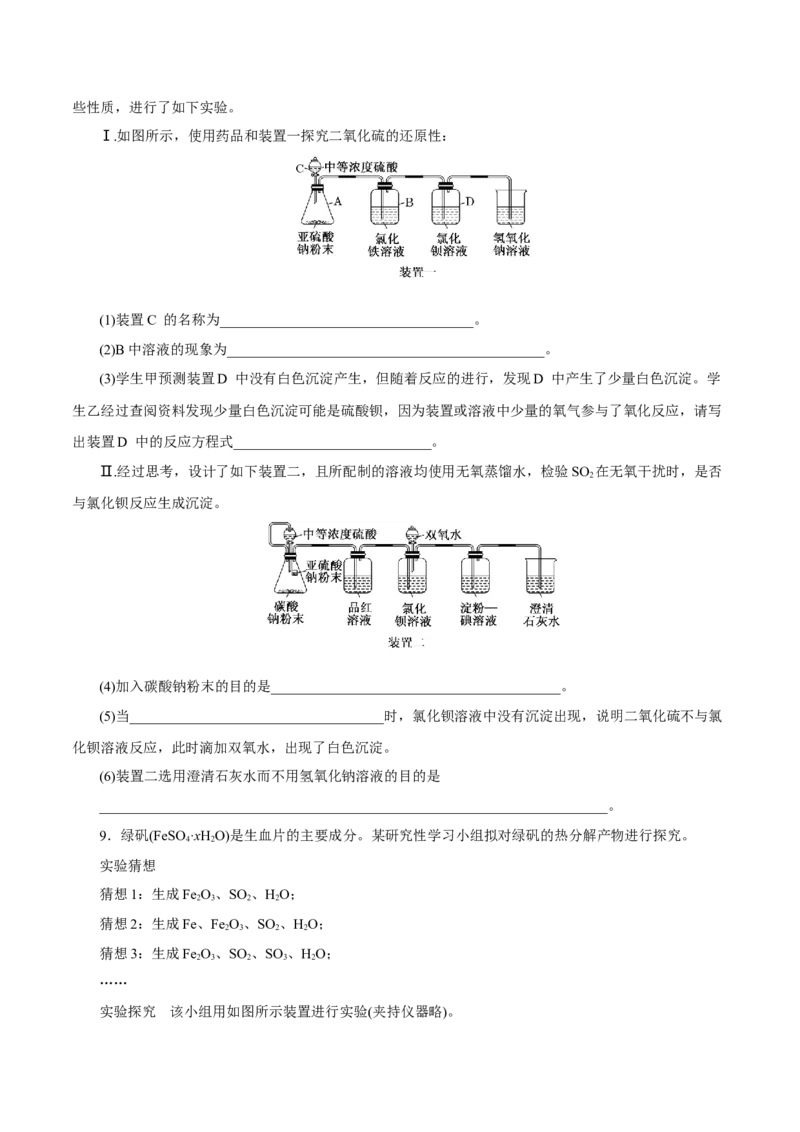
8.SO 为无色气体,有强烈刺激性气味,是大气主要污染物之一,某学习小组为了探究二氧化硫的某
2些性质,进行了如下实验。
Ⅰ.如图所示,使用药品和装置一探究二氧化硫的还原性:
(1)装置C 的名称为____________________________________。
(2)B中溶液的现象为_____________________________________________。
(3)学生甲预测装置D 中没有白色沉淀产生,但随着反应的进行,发现D 中产生了少量白色沉淀。学
生乙经过查阅资料发现少量白色沉淀可能是硫酸钡,因为装置或溶液中少量的氧气参与了氧化反应,请写
出装置D 中的反应方程式____________________________。
Ⅱ.经过思考,设计了如下装置二,且所配制的溶液均使用无氧蒸馏水,检验SO 在无氧干扰时,是否
2
与氯化钡反应生成沉淀。
(4)加入碳酸钠粉末的目的是_________________________________________。
(5)当____________________________________时,氯化钡溶液中没有沉淀出现,说明二氧化硫不与氯
化钡溶液反应,此时滴加双氧水,出现了白色沉淀。
(6)装置二选用澄清石灰水而不用氢氧化钠溶液的目的是
________________________________________________________________________。
9.绿矾(FeSO ·xHO)是生血片的主要成分。某研究性学习小组拟对绿矾的热分解产物进行探究。
4 2
实验猜想
猜想1:生成Fe O、SO 、HO;
2 3 2 2
猜想2:生成Fe、Fe O、SO 、HO;
2 3 2 2
猜想3:生成Fe O、SO 、SO 、HO;
2 3 2 3 2
……
实验探究 该小组用如图所示装置进行实验(夹持仪器略)。请回答下列问题:
(1)实验操作的先后顺序是________(填字母)。
a.熄灭酒精灯,冷却
b.先检查装置的气密性,后加入药品
c.点燃酒精灯,加热
d.在“气体入口”处通入干燥的N
2
其中操作d的作用是____________________________________________________。
(2)在实验过程中,观察到A中固体变红棕色,B中无水CuSO ______________________,C中试纸的
4
颜色变化是________________。
(3)反应结束后,取A中固体进行实验,实验操作及现象如下:
①将固体加入盛有足量稀硫酸的试管中,固体完全溶解,且无气体放出;
②取①中溶液滴入适量KMnO 溶液中,KMnO 溶液不褪色;
4 4
③取①中溶液滴入KSCN溶液中,溶液变红色。
由此得出结论:红棕色固体为________。
(4)D中有白色沉淀生成,该沉淀的化学式为____________________。有同学认为还应该增加一个实
验,取D中沉淀,加入一定量的盐酸以确定其组成,从而确定FeSO ·xHO的分解产物,你认为是否需
4 2
要?说明你的理由:____________________________________。
实验结论
(5)硫酸亚铁晶体加热分解的化学方程式为__________________________________。
1.从宏观现象探究微观本质是重要的化学学科素养。
Ⅰ.以亚硫酸钠(Na SO )为实验对象,探究其性质。实验如下:
2 3
――→――→――→
――→――→――→
(1)写出上述实验中②的离子方程式:______________________________。
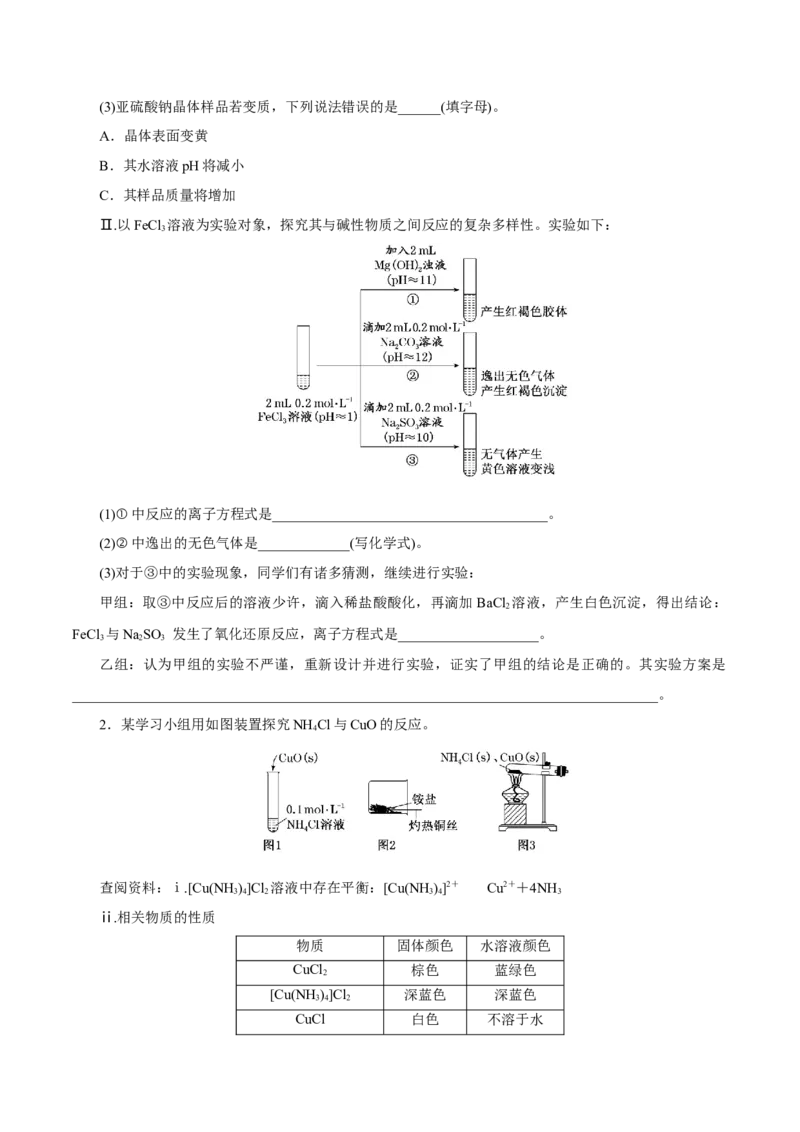
(2)通过上述实验可知,在空气中久置的亚硫酸钠固体中会混有________(填化学式)。(3)亚硫酸钠晶体样品若变质,下列说法错误的是______(填字母)。
A.晶体表面变黄
B.其水溶液pH将减小
C.其样品质量将增加
Ⅱ.以FeCl 溶液为实验对象,探究其与碱性物质之间反应的复杂多样性。实验如下:
3
(1)①中反应的离子方程式是_______________________________________。
(2)②中逸出的无色气体是_____________(写化学式)。
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
甲组:取③中反应后的溶液少许,滴入稀盐酸酸化,再滴加BaCl 溶液,产生白色沉淀,得出结论:
2
FeCl 与NaSO 发生了氧化还原反应,离子方程式是____________________。
3 2 3
乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是
___________________________________________________________________________________。
2.某学习小组用如图装置探究NH Cl与CuO的反应。
4
查阅资料:ⅰ.[Cu(NH)]Cl 溶液中存在平衡:[Cu(NH )]2+Cu2++4NH
3 4 2 3 4 3
ⅱ.相关物质的性质
物质 固体颜色 水溶液颜色
CuCl 棕色 蓝绿色
2
[Cu(NH )]Cl 深蓝色 深蓝色
3 4 2
CuCl 白色 不溶于水(1)实验Ⅰ:如图1,一段时间后,固体部分溶解,固体表面无颜色变化,溶液变为蓝色。固体溶解的
原因是__________________________________________。
(2)实验Ⅱ:如图2,将铜丝加热变黑后迅速插入疏松的氯化铵固体中,有白烟生成,2分钟后取出铜
丝,黑色消失变回红色。
①已知氯化铵与氧化铜反应生成两种单质,其中一种为无色气体,写出该反应的化学方程式
________________________________________________。
②若将氯化铵换为硫酸铵,观察不到上述现象,原因是_______________________。
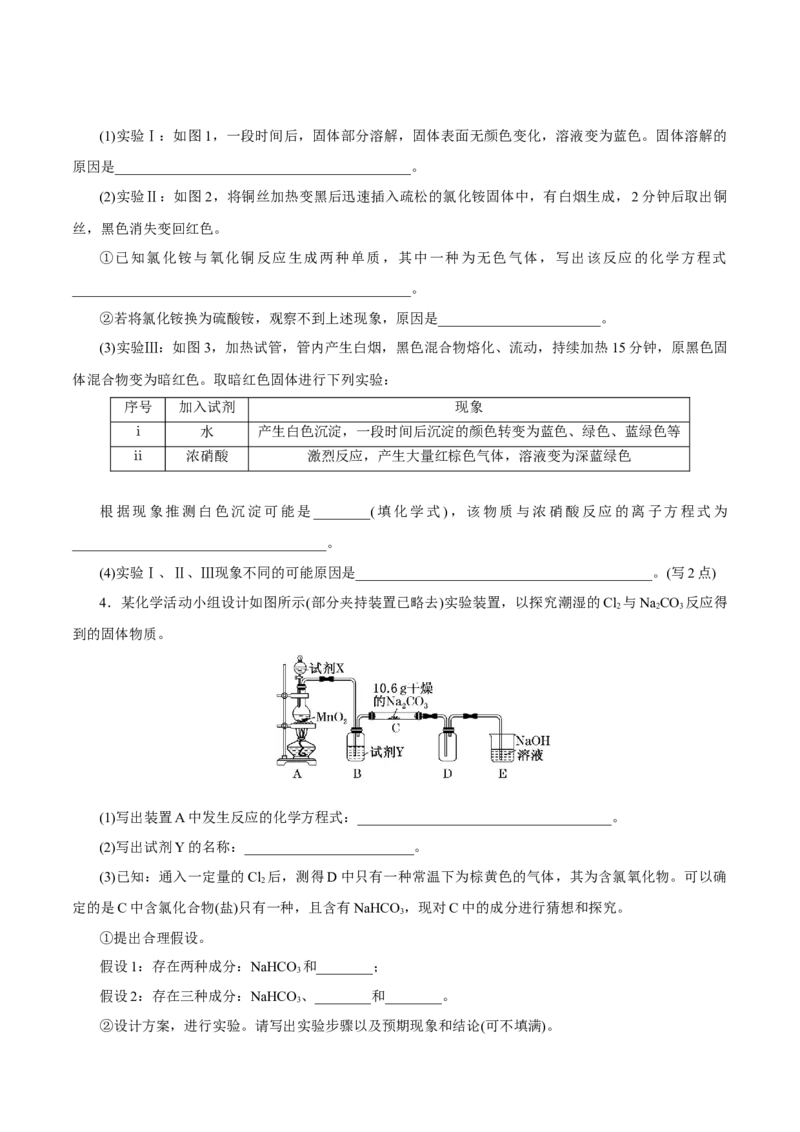
(3)实验Ⅲ:如图3,加热试管,管内产生白烟,黑色混合物熔化、流动,持续加热15分钟,原黑色固
体混合物变为暗红色。取暗红色固体进行下列实验:
序号 加入试剂 现象
ⅰ 水 产生白色沉淀,一段时间后沉淀的颜色转变为蓝色、绿色、蓝绿色等
ⅱ 浓硝酸 激烈反应,产生大量红棕色气体,溶液变为深蓝绿色
根据现象推测白色沉淀可能是________(填化学式),该物质与浓硝酸反应的离子方程式为
____________________________________。
(4)实验Ⅰ、Ⅱ、Ⅲ现象不同的可能原因是__________________________________________。(写2点)
4.某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl 与NaCO 反应得
2 2 3
到的固体物质。
(1)写出装置A中发生反应的化学方程式:____________________________________。
(2)写出试剂Y的名称:________________________。
(3)已知:通入一定量的Cl 后,测得D中只有一种常温下为棕黄色的气体,其为含氯氧化物。可以确
2
定的是C中含氯化合物(盐)只有一种,且含有NaHCO ,现对C中的成分进行猜想和探究。
3
①提出合理假设。
假设1:存在两种成分:NaHCO 和________;
3
假设2:存在三种成分:NaHCO 、________和________。
3
②设计方案,进行实验。请写出实验步骤以及预期现象和结论(可不填满)。限选实验试剂和仪器:蒸馏水、稀HNO 、BaCl 溶液、澄清石灰水、AgNO 溶液、试管、小烧杯、胶
3 2 3
头滴管。
实验步骤 预期现象和结论
步骤1:取C中的少量固体样品于试管中,滴加足量蒸馏水至固体溶
—
解,然后将所得溶液分别置于a、b试管中
步骤2:
步骤3:
(4)已知 C 中有 0.1 mol Cl 参加反应。若假设 1 成立,可推知 C 中反应的化学方程式为
2
____________________________________________________________。
5.亚硝酸钠(NaNO )是一种常见的食品添加剂。某实验小组制备NaNO 并对其性质进行探究。
2 2
资料:Ag+与NO反应,可生成AgNO 白色沉淀或无色配离子。
2
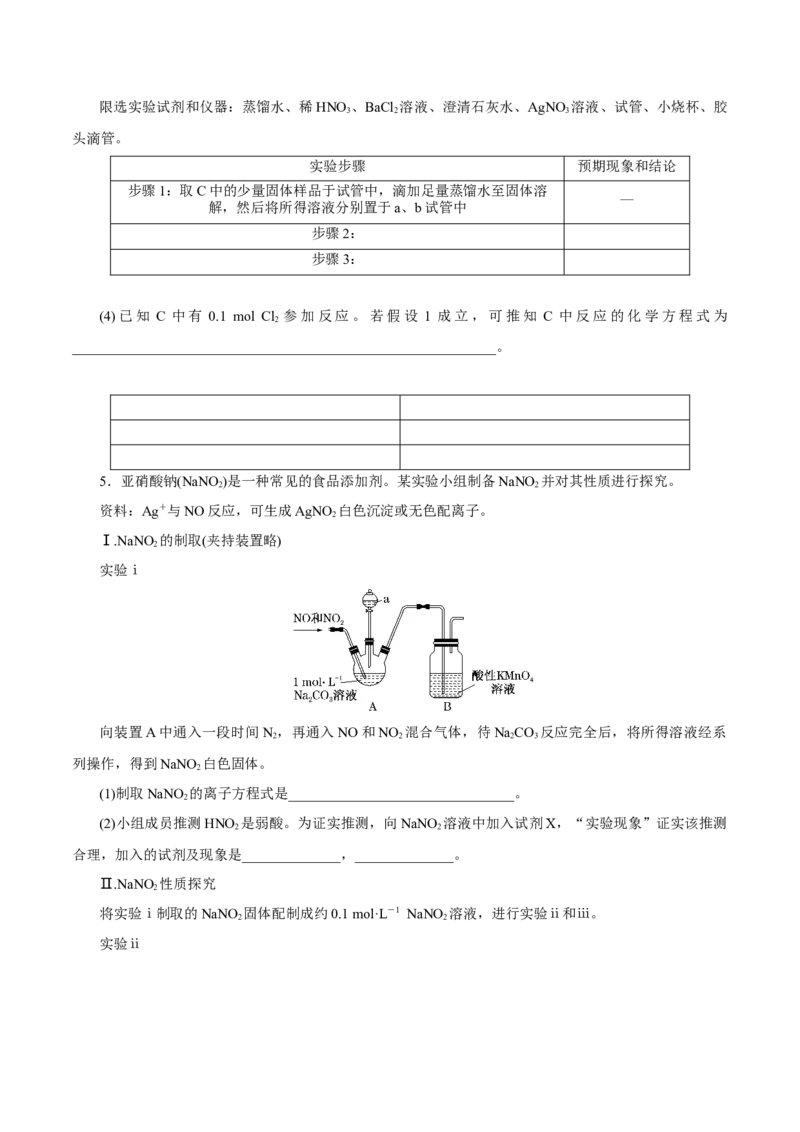
Ⅰ.NaNO 的制取(夹持装置略)
2
实验ⅰ
向装置A中通入一段时间N ,再通入NO和NO 混合气体,待NaCO 反应完全后,将所得溶液经系
2 2 2 3
列操作,得到NaNO 白色固体。
2
(1)制取NaNO 的离子方程式是________________________________。
2
(2)小组成员推测HNO 是弱酸。为证实推测,向NaNO 溶液中加入试剂X,“实验现象”证实该推测
2 2
合理,加入的试剂及现象是______________,______________。
Ⅱ.NaNO 性质探究
2
将实验ⅰ制取的NaNO 固体配制成约0.1 mol·L-1 NaNO 溶液,进行实验ⅱ和ⅲ。
2 2
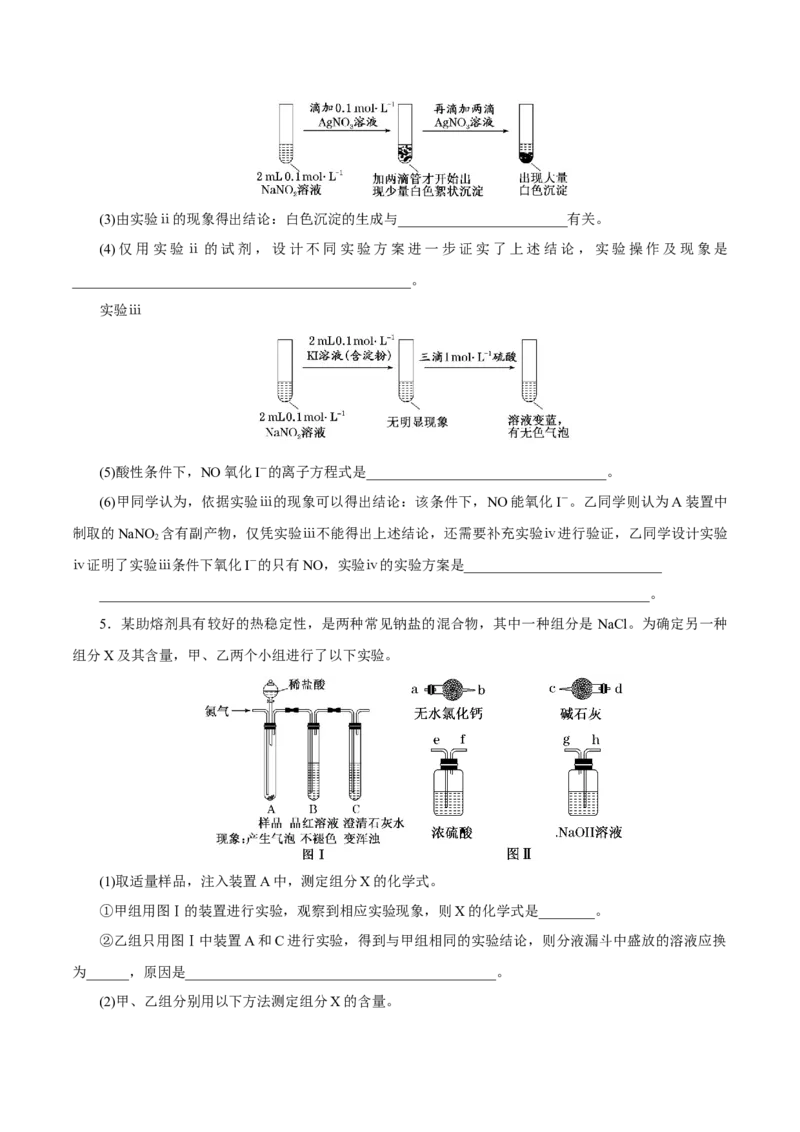
实验ⅱ(3)由实验ⅱ的现象得出结论:白色沉淀的生成与________________________有关。
(4)仅用实验ⅱ的试剂,设计不同实验方案进一步证实了上述结论,实验操作及现象是
________________________________________________。
实验ⅲ
(5)酸性条件下,NO氧化I-的离子方程式是__________________________________。
(6)甲同学认为,依据实验ⅲ的现象可以得出结论:该条件下,NO能氧化I-。乙同学则认为A装置中
制取的NaNO 含有副产物,仅凭实验ⅲ不能得出上述结论,还需要补充实验ⅳ进行验证,乙同学设计实验
2
ⅳ证明了实验ⅲ条件下氧化I-的只有NO,实验ⅳ的实验方案是____________________________
______________________________________________________________________________。
5.某助熔剂具有较好的热稳定性,是两种常见钠盐的混合物,其中一种组分是 NaCl。为确定另一种
组分X及其含量,甲、乙两个小组进行了以下实验。
(1)取适量样品,注入装置A中,测定组分X的化学式。
①甲组用图Ⅰ的装置进行实验,观察到相应实验现象,则X的化学式是________。
②乙组只用图Ⅰ中装置A和C进行实验,得到与甲组相同的实验结论,则分液漏斗中盛放的溶液应换
为______,原因是____________________________________________。
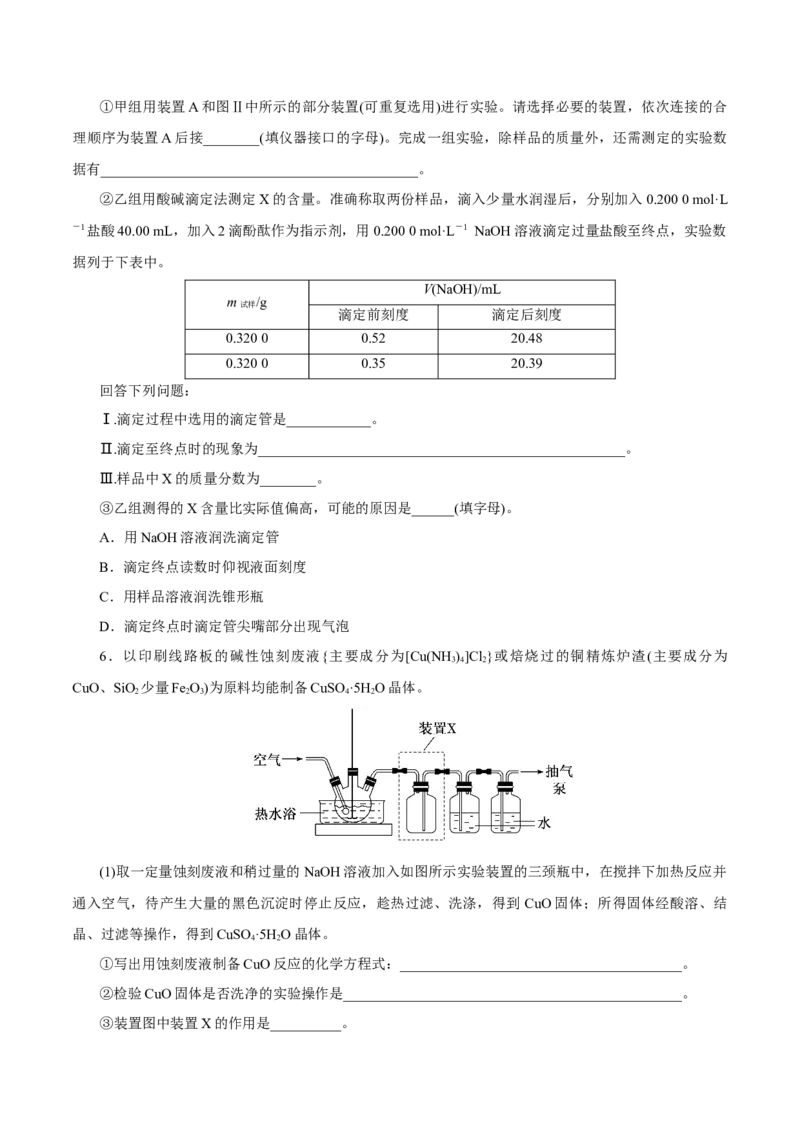
(2)甲、乙组分别用以下方法测定组分X的含量。①甲组用装置A和图Ⅱ中所示的部分装置(可重复选用)进行实验。请选择必要的装置,依次连接的合
理顺序为装置A后接________(填仪器接口的字母)。完成一组实验,除样品的质量外,还需测定的实验数
据有_____________________________________________。
②乙组用酸碱滴定法测定X的含量。准确称取两份样品,滴入少量水润湿后,分别加入0.200 0 mol·L
-1盐酸40.00 mL,加入2滴酚酞作为指示剂,用0.200 0 mol·L-1 NaOH溶液滴定过量盐酸至终点,实验数
据列于下表中。
V(NaOH)/mL
m /g
试样
滴定前刻度 滴定后刻度
0.320 0 0.52 20.48
0.320 0 0.35 20.39
回答下列问题:
Ⅰ.滴定过程中选用的滴定管是____________。
Ⅱ.滴定至终点时的现象为____________________________________________________。
Ⅲ.样品中X的质量分数为________。
③乙组测得的X含量比实际值偏高,可能的原因是______(填字母)。
A.用NaOH溶液润洗滴定管
B.滴定终点读数时仰视液面刻度
C.用样品溶液润洗锥形瓶
D.滴定终点时滴定管尖嘴部分出现气泡
6.以印刷线路板的碱性蚀刻废液{主要成分为[Cu(NH )]Cl }或焙烧过的铜精炼炉渣(主要成分为
3 4 2
CuO、SiO 少量Fe O)为原料均能制备CuSO ·5H O晶体。
2 2 3 4 2
(1)取一定量蚀刻废液和稍过量的NaOH溶液加入如图所示实验装置的三颈瓶中,在搅拌下加热反应并
通入空气,待产生大量的黑色沉淀时停止反应,趁热过滤、洗涤,得到 CuO固体;所得固体经酸溶、结
晶、过滤等操作,得到CuSO ·5H O晶体。
4 2
①写出用蚀刻废液制备CuO反应的化学方程式:________________________________________。
②检验CuO固体是否洗净的实验操作是________________________________________________。
③装置图中装置X的作用是__________。(2)以焙烧过的铜精炼炉渣为原料制备CuSO ·5H O晶体时,请补充完整相应的实验方案:取一定量焙
4 2
烧过的铜精炼炉渣,______________________________________,将滤液加热浓缩、冷却结晶、过滤、晾
干,得到CuSO ·5H O晶体。
4 2
已知:①该实验中pH=3.2时,Fe3+完全沉淀;pH=4.7时,Cu2+开始沉淀。②实验中可选用的试剂:
1.0 mol·L-1 HSO 、1.0 mol·L-1HCl、1.0 mol·L-1 NaOH。
2 4
(3)通过下列方法测定产品纯度:准确称取0.500 0 g CuSO ·5H O样品,加适量水溶解,转移至碘量瓶
4 2
中,加过量KI溶液并用稀HSO 酸化,以淀粉溶液为指示剂,用0.100 0 mol·L-1 Na SO 标准溶液滴定至
2 4 2 2 3
终点,消耗 NaSO 的溶液 19.80 mL。测定过程中发生下列反应:2Cu2++4I-===2CuI↓+I 、2SO+
2 2 3 2 2
I===S O+2I-。计算CuSO ·5H O样品的纯度(写出计算过程):____________________________。
2 4 4 2
7.实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见下图,相关物质的物理性质见附表)。
相对分 密度/
物质 沸点/℃
子质量 (g·cm-3)
溴 160 3.119 58.8
苯甲醛 106 1.04 179
1,2二氯乙烷 99 1.235 1 83.5
间溴苯甲醛 185 1.587 229
其实验步骤如下:
步骤1:将三颈烧瓶中的一定配比的无水AlCl 、1,2二氯乙烷和苯甲醛(5.3 g)充分混合后,升温至60
3
℃,缓慢滴加经浓硫酸干燥过的液溴,保温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用 10% NaHCO 溶液
3
洗涤。
步骤3:经洗涤的有机相加入适量无水硫酸钙固体,放置一段时间后过滤。
步骤4:为了防止间溴苯甲醛因温度过高被氧化,向步骤3处理得到的间溴苯甲醛中加入少量锌粉,
同时采用某种技术,收集相应馏分,其中收集到间溴苯甲醛为3.7 g。
(1)实验装置中采用的加热方式为________,冷凝管的作用为______________,锥形瓶中的试剂应为
________。
(2)步骤1所加入的无水AlCl 的作用为_____________。
3(3)步骤2中用10% NaHCO 溶液洗涤有机相,是为了除去溶于有机相中的______________________(填
3
化学式)。
(4)步骤3中加入的无水硫酸钙固体的目的是________________________。
(5)步骤4中,“某种技术”为____________。
(6)本实验所得到的间溴苯甲醛产率是________。
8.乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料,可用作止痛剂、退热
剂、防腐剂和染料中间体。乙酰苯胺的制备原理为:
实验参数:
名称 苯胺 乙酸 乙酰苯胺
式量 93 60 135
性状 无色油状液体,具有还原性 无色液体 白色晶体
密度/(g·cm-3) 1.02 1.05 1.22
沸点/℃ 184.4 118.1 304
微溶于水 易溶于水 微溶于冷水,溶于热水
溶解度
易溶于乙醇、乙醚等 易溶于乙醇、乙醚 易溶于乙醇、乙醚
实验装置如图:
注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离。
实验步骤:
步骤1:在圆底烧瓶中加入无水苯胺9.30 mL,冰醋酸15.4 mL,锌粉0.100 g, 安装仪器,加入沸石,
调节加热温度,使分馏柱顶温度控制在105 ℃左右,反应约60~80 min,反应生成的水及少量醋酸被蒸
出。
步骤2:在搅拌下,趁热将烧瓶中物料以细流状倒入盛有100 mL冰水的烧杯中,剧烈搅拌,并冷却结
晶,抽滤、洗涤、干燥,得到乙酰苯胺粗品。
步骤3:将此粗乙酰苯胺进行重结晶,晾干,称重,计算产率。
(1)步骤1中所选圆底烧瓶的最佳规格是_____(填字母)。
a.25 mL b.50 mL c.150 mL d.200 mL(2)实验中加入少量锌粉的目的是_________________________________。
(3)步骤1加热可用________(填“水浴”“油浴”或“直接加热”)。从化学平衡的角度分析,控制分
馏柱上端的温度在105 ℃左右的原因是_______________________________。
(4)步骤2中结晶时,若冷却后仍无晶体析出,可采用的方法是__________________。洗涤乙酰苯胺粗
品最合适的试剂是________(填字母)。
a.用少量冷水洗 b.用少量热水洗
c.先用冷水洗,再用热水洗 d.用酒精洗
(5)乙酰苯胺粗品因含杂质而显色,欲用重结晶进行提纯,步骤如下:热水溶解、________、过滤、洗
涤、干燥(选取正确的操作并排序)。
a.蒸发结晶 b.冷却结晶
c.趁热过滤 d.加入活性炭
(6)该实验最终得到纯品9.18 g,则乙酰苯胺的产率是________%(结果保留一位小数)。
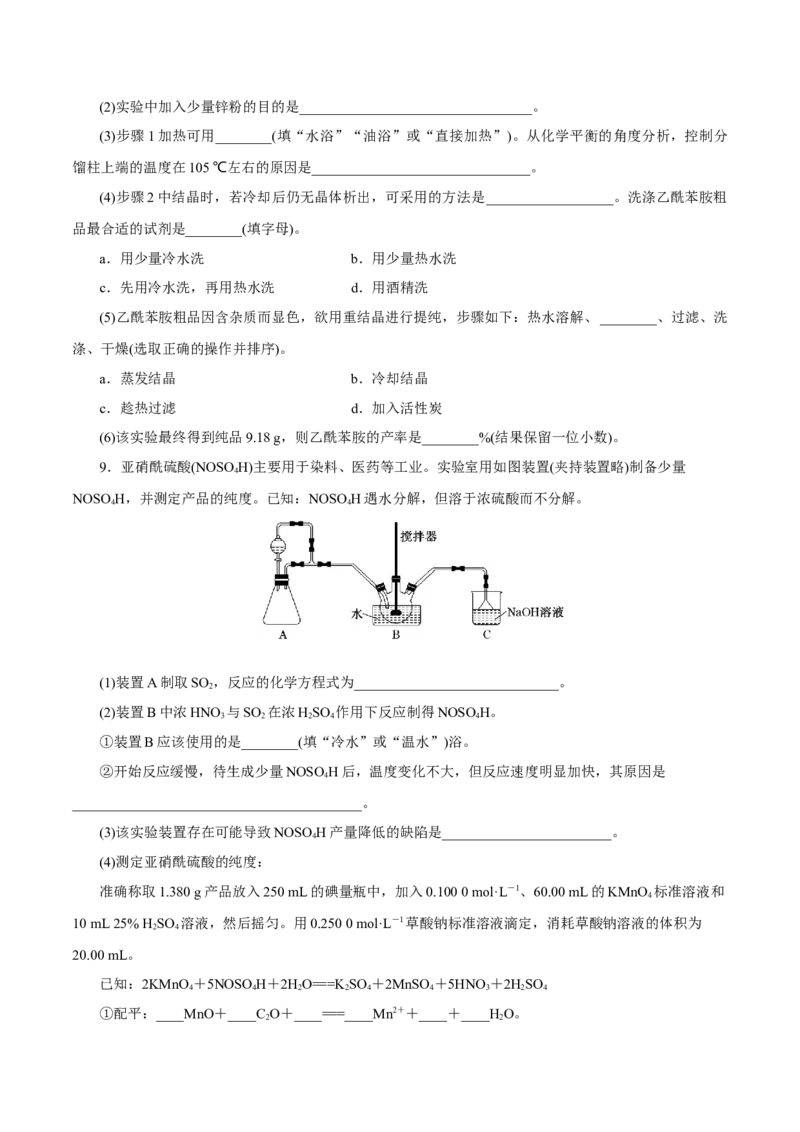
9.亚硝酰硫酸(NOSOH)主要用于染料、医药等工业。实验室用如图装置(夹持装置略)制备少量
4
NOSOH,并测定产品的纯度。已知:NOSOH遇水分解,但溶于浓硫酸而不分解。
4 4
(1)装置A制取SO ,反应的化学方程式为_____________________________。
2
(2)装置B中浓HNO 与SO 在浓HSO 作用下反应制得NOSOH。
3 2 2 4 4
①装置B应该使用的是________(填“冷水”或“温水”)浴。
②开始反应缓慢,待生成少量NOSOH后,温度变化不大,但反应速度明显加快,其原因是
4
_________________________________________。
(3)该实验装置存在可能导致NOSOH产量降低的缺陷是________________________。
4
(4)测定亚硝酰硫酸的纯度:
准确称取1.380 g产品放入250 mL的碘量瓶中,加入0.100 0 mol·L-1、60.00 mL的KMnO 标准溶液和
4
10 mL 25% HSO 溶液,然后摇匀。用0.250 0 mol·L-1草酸钠标准溶液滴定,消耗草酸钠溶液的体积为
2 4
20.00 mL。
已知:2KMnO +5NOSOH+2HO===K SO +2MnSO +5HNO+2HSO
4 4 2 2 4 4 3 2 4
①配平:____MnO+____C O+____===____Mn2++____+____HO。
2 2②滴定终点时的现象为____________________________。
③亚硝酰硫酸的纯度=______________。[M(NOSOH)=127 g·mol-1]
4
10.氧化亚铜在强酸性溶液中发生歧化反应,某小组同学设计如下实验制备氧化亚铜并测定其纯度。
(1)该小组同学利用葡萄糖还原CuSO 溶液制备氧化亚铜。
4
①配制490 mL 0.1 mol·L-1 CuSO 溶液,需要称取胆矾晶体的质量为___________,完成该实验操作需
4
要的玻璃仪器除胶头滴管外还要_________________________。
②该反应最适宜温度为80~90 ℃,为探究反应发生的最低温度,应选用的加热方式为__________。
(2)某同学为检验Cu O样品中是否含有CuO,设计如下实验方案:将Cu O样品与足量稀硫酸反应,观
2 2
察到溶液呈蓝色,即得出结论:样品中含有CuO杂质。若探究该同学的方案和结论是否合理,需用化学方
程式__________________________来进行解释。
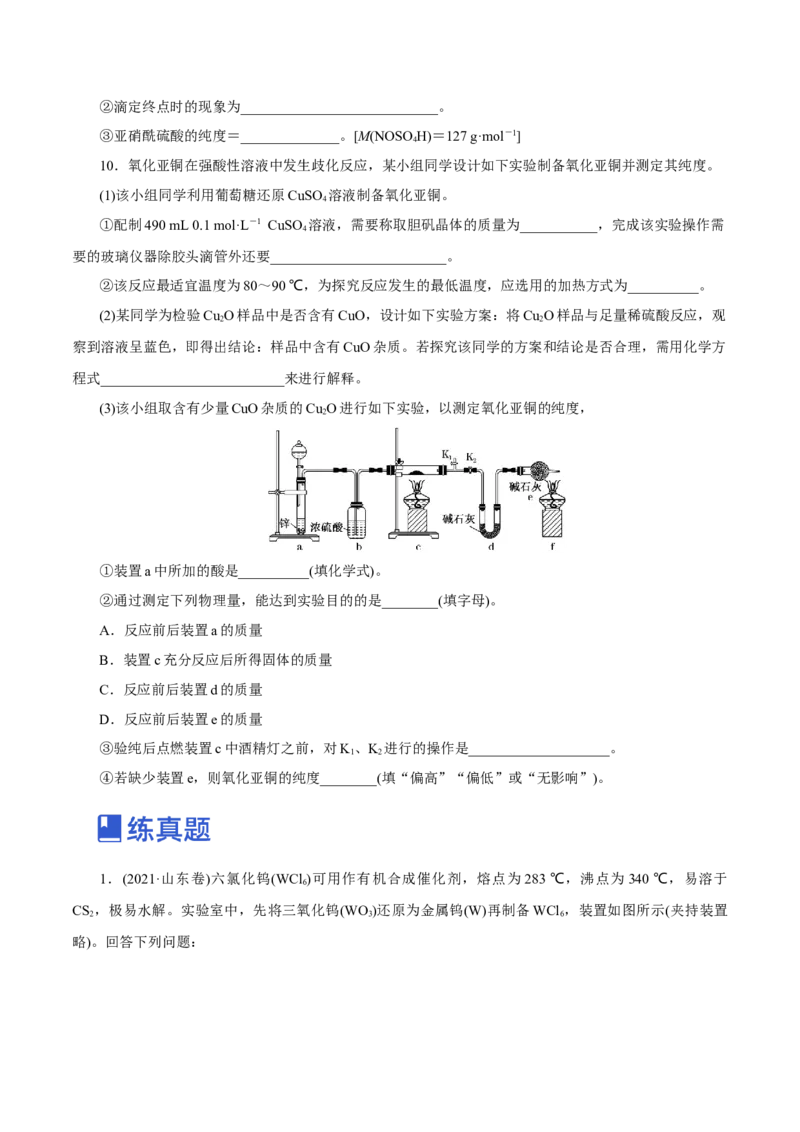
(3)该小组取含有少量CuO杂质的Cu O进行如下实验,以测定氧化亚铜的纯度,
2
①装置a中所加的酸是__________(填化学式)。
②通过测定下列物理量,能达到实验目的的是________(填字母)。
A.反应前后装置a的质量
B.装置c充分反应后所得固体的质量
C.反应前后装置d的质量
D.反应前后装置e的质量
③验纯后点燃装置c中酒精灯之前,对K、K 进行的操作是____________________。
1 2
④若缺少装置e,则氧化亚铜的纯度________(填“偏高”“偏低”或“无影响”)。
1.(2021·山东卷)六氯化钨(WCl )可用作有机合成催化剂,熔点为283 ℃,沸点为340 ℃,易溶于
6
CS ,极易水解。实验室中,先将三氧化钨(WO)还原为金属钨(W)再制备WCl ,装置如图所示(夹持装置
2 3 6
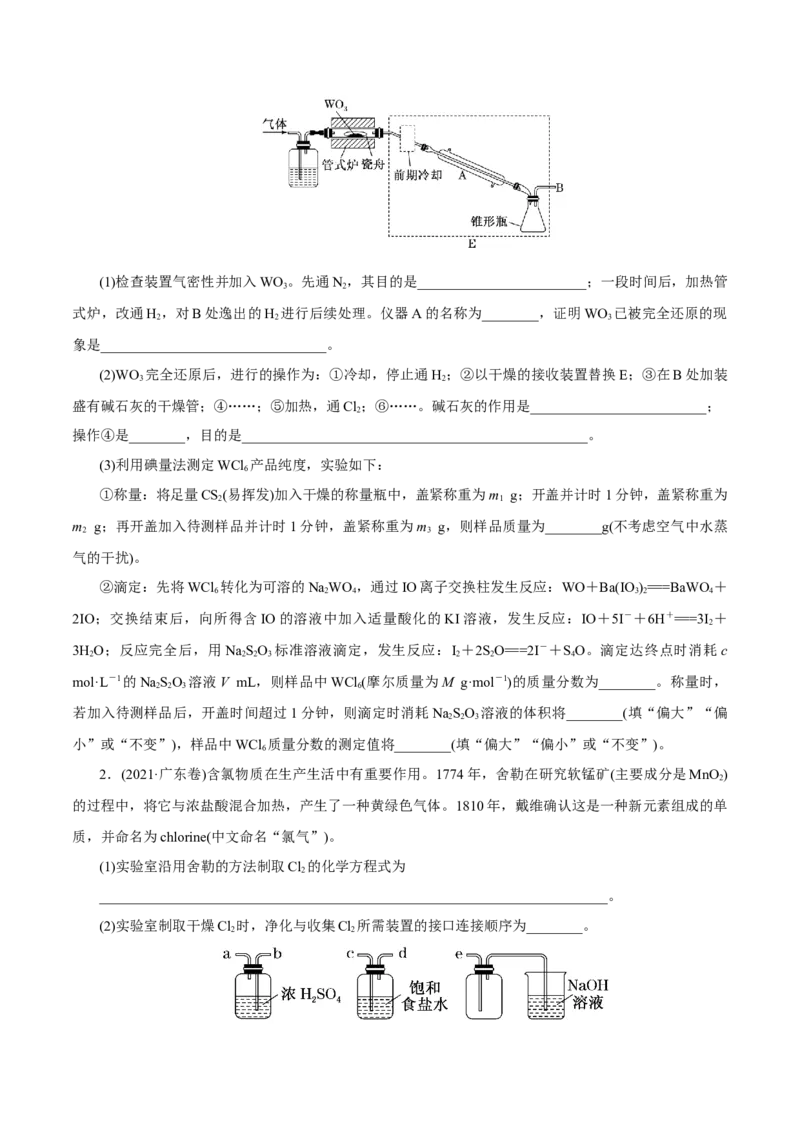
略)。回答下列问题:(1)检查装置气密性并加入WO。先通N,其目的是________________________;一段时间后,加热管
3 2
式炉,改通H ,对B处逸出的H 进行后续处理。仪器A的名称为________,证明WO 已被完全还原的现
2 2 3
象是________________________________。
(2)WO 完全还原后,进行的操作为:①冷却,停止通H ;②以干燥的接收装置替换E;③在B处加装
3 2
盛有碱石灰的干燥管;④……;⑤加热,通Cl;⑥……。碱石灰的作用是_________________________;
2
操作④是________,目的是_________________________________________________。
(3)利用碘量法测定WCl 产品纯度,实验如下:
6
①称量:将足量CS(易挥发)加入干燥的称量瓶中,盖紧称重为m g;开盖并计时1分钟,盖紧称重为
2 1
m g;再开盖加入待测样品并计时1分钟,盖紧称重为m g,则样品质量为________g(不考虑空气中水蒸
2 3
气的干扰)。
②滴定:先将WCl 转化为可溶的NaWO ,通过IO离子交换柱发生反应:WO+Ba(IO)===BaWO +
6 2 4 3 2 4
2IO;交换结束后,向所得含IO的溶液中加入适量酸化的KI溶液,发生反应:IO+5I-+6H+===3I +
2
3HO;反应完全后,用NaSO 标准溶液滴定,发生反应:I +2SO===2I-+SO。滴定达终点时消耗c
2 2 2 3 2 2 4
mol·L-1的NaSO 溶液V mL,则样品中WCl(摩尔质量为M g·mol-1)的质量分数为________。称量时,
2 2 3 6
若加入待测样品后,开盖时间超过1分钟,则滴定时消耗NaSO 溶液的体积将________(填“偏大”“偏
2 2 3
小”或“不变”),样品中WCl 质量分数的测定值将________(填“偏大”“偏小”或“不变”)。
6
2.(2021·广东卷)含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是MnO )
2
的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单
质,并命名为chlorine(中文命名“氯气”)。
(1)实验室沿用舍勒的方法制取Cl 的化学方程式为
2
________________________________________________________________________。
(2)实验室制取干燥Cl 时,净化与收集Cl 所需装置的接口连接顺序为________。
2 2(3)某氯水久置后不能使品红溶液褪色,可推测氯水中________已分解。检验此久置氯水中Cl-存在的
操作及现象是__________________________________________________________________________。
(4)某合作学习小组进行以下实验探究。
①实验任务 通过测定溶液电导率,探究温度对AgCl溶解度的影响。
②查阅资料 电导率是表征电解质溶液导电能力的物理量。温度一定时,强电解质稀溶液的电导率随
溶液中离子浓度的增大而增大;离子浓度一定时,稀溶液电导率随温度的升高而增大。25 ℃时,K (AgCl)
sp
=1.8×10-10。
③提出猜想
猜想a:较高温度的AgCl饱和溶液的电导率较大。
猜想b:AgCl在水中的溶解度S(45 ℃)>S(35 ℃)>S(25 ℃)。
④设计实验、验证猜想 取试样Ⅰ、Ⅱ、Ⅲ(不同温度下配制的AgCl饱和溶液),在设定的测试温度
下,进行表1中实验1~3,记录数据。
表1
实验序号 试样 测试温度/℃ 电导率/(μS·cm-1)
1 Ⅰ:25 ℃的AgCl饱和溶液 25 A
1
2 Ⅱ:35 ℃的AgCl饱和溶液 35 A
2
3 Ⅲ:45 ℃的AgCl饱和溶液 45 A
3
⑤数据分析、交流讨论 25 ℃的AgCl饱和溶液中,c(Cl-)=________________mol·L-1。实验结果为
A>A>A 。小组同学认为,此结果可以证明③中的猜想 a成立,但不足以证明猜想b成立。结合②中信
3 2 1
息,猜想b不足以成立的理由有______________________________________________________________。
⑥优化实验 小组同学为进一步验证猜想b,在实验1~3的基础上完善方案,进行实验4和5。请完
成表2中内容。
表2
实验序号 试样 测试温度/℃ 电导率/(μS·cm-1)
4 Ⅰ ________ B
1
5 ____ ________ B
2
⑦实验总结 根据实验1~5的结果,并结合②中信息,小组同学认为猜想b也成立。猜想b成立的判
断依据是__________________。
3.(2021·广东卷)含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是
)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素
组成的单质,并命名为chlorine(中文命名“氯气”)。(1)实验室沿用舍勒的方法制取 的化学方程式为_______。
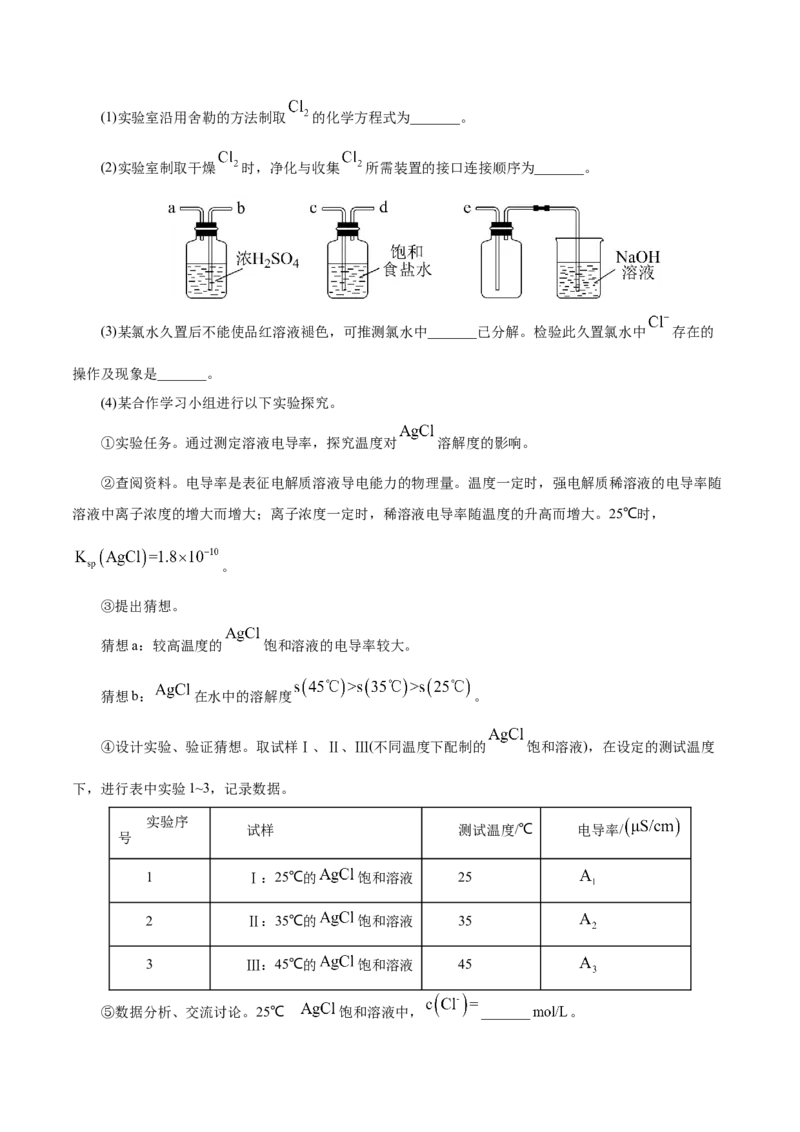
(2)实验室制取干燥 时,净化与收集 所需装置的接口连接顺序为_______。
(3)某氯水久置后不能使品红溶液褪色,可推测氯水中_______已分解。检验此久置氯水中 存在的
操作及现象是_______。
(4)某合作学习小组进行以下实验探究。
①实验任务。通过测定溶液电导率,探究温度对 溶解度的影响。
②查阅资料。电导率是表征电解质溶液导电能力的物理量。温度一定时,强电解质稀溶液的电导率随
溶液中离子浓度的增大而增大;离子浓度一定时,稀溶液电导率随温度的升高而增大。25℃时,
。
③提出猜想。
猜想a:较高温度的 饱和溶液的电导率较大。
猜想b: 在水中的溶解度 。
④设计实验、验证猜想。取试样Ⅰ、Ⅱ、Ⅲ(不同温度下配制的 饱和溶液),在设定的测试温度
下,进行表中实验1~3,记录数据。
实验序
试样 测试温度/℃ 电导率/
号
1 Ⅰ:25℃的 饱和溶液 25
2 Ⅱ:35℃的 饱和溶液 35
3 Ⅲ:45℃的 饱和溶液 45
⑤数据分析、交流讨论。25℃ 的饱和溶液中, _______ 。实验结果为 。小组同学认为,此结果可以证明③中的猜想 成立,但不足以证明猜想
成立。结合②中信息,猜想 不足以成立的理由有_______。
⑥优化实验。小组同学为进一步验证猜想 ,在实验1~3的基础上完善方案,进行实验4和5。请在答
题卡上完成表中内容。
实验序
试样 测试温度/℃ 电导率/
号
4 Ⅰ _______
5 _______ _______
⑦实验总结。根据实验1~5的结果,并结合②中信息,小组同学认为猜想 也成立。猜想 成立的判
断依据是_______。
4.(2022·河北卷)某研究小组为了更准确检测香菇中添加剂亚硫酸盐的含量,设计实验如下:
①三颈烧瓶中加入 香菇样品和 水;锥形瓶中加入 水、 淀粉溶液,并预加
的碘标准溶液,搅拌。
②以 流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,至终点时
滴定消耗了 碘标准溶液。
③做空白实验,消耗了 碘标准溶液。
④用适量 替代香菇样品,重复上述步骤,测得 的平均回收率为95%。
已知: ,
回答下列问题:(1)装置图中仪器a、b的名称分别为_______、_______。
(2)三颈烧瓶适宜的规格为_______(填标号)。
A. B. C.
(3)解释加入 ,能够生成 的原因:_______。
(4)滴定管在使用前需要_______、洗涤、润洗;滴定终点时溶液的颜色为_______;滴定反应的离
子方程式为_______。
(5)若先加磷酸再通氮气,会使测定结果_______(填“偏高”“偏低”或“无影响”)。
(6)该样品中亚硫酸盐含量为_______ (以 计,结果保留三位有效数字)。
5.(2021·全国甲卷)胆矾(CuSO ·5H O)易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的CuO(杂
4 2
质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
(1)制备胆矾时,用到的实验仪器除量筒、酒精灯、玻璃棒、漏斗外,还必须使用的仪器有________(填
标号)。
A.烧杯 B.容量瓶
C.蒸发皿 D.移液管
(2)将CuO加入到适量的稀硫酸中,加热,其主要反应的化学方程式为
________________________________________________________________________,
与直接用废铜和浓硫酸反应相比,该方法的优点是________________________________________。
(3)待CuO完全反应后停止加热,边搅拌边加入适量HO,冷却后用NH ·H O调pH为3.5~4,再煮沸
2 2 3 2
10 min,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、________、乙醇洗涤、________,得
到胆矾。其中,控制溶液pH为3.5~4的目的是______________________________,煮沸10 min的作用是
____________________________________________________。
(4)结晶水测定:称量干燥坩埚的质量为m,加入胆矾后总质量为m。将坩埚加热至胆矾全部变为白
1 2
色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为m。根据实验数据,胆矾分子中结
3
晶水的个数为________(写表达式)。
(5)下列操作中,会导致结晶水数目测定值偏高的是________(填标号)。
①胆矾未充分干燥 ②坩埚未置于干燥器中冷却 ③加热时有少量胆矾迸溅出来
6. (2021·湖南卷)碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料制备碳酸
钠,并测定产品中少量碳酸氢钠的含量,过程如下:
步骤I.Na CO 的制备
2 3步骤Ⅱ.产品中NaHCO 含量测定
3
①称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中;
②移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用 盐酸标准溶液滴定,溶液
由红色变至近无色(第一滴定终点),消耗盐酸 ;
③在上述锥形瓶中再加入2滴指示剂N,继续用 盐酸标准溶液滴定至终点(第二滴定终
点),又消耗盐酸 ;
④平行测定三次, 平均值为22.45, 平均值为23.51。
已知:(i)当温度超过35℃时,NH HCO 开始分解。
4 3
(ii)相关盐在不同温度下的溶解度表
温度/ 0 10 20 30 40 50 60
NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3
NH HCO 11.9 15.8 21.0 27.0
4 3
NaHCO 6.9 8.2 9.6 11.1 12.7 14.5 16.4
3
.
NH Cl 294 33.3 37.2 41.4 45.8 50.4 55.2
4
回答下列问题:
(1)步骤I中晶体A的化学式为_______,晶体A能够析出的原因是______________________;
(2)步骤I中“300℃加热”所选用的仪器是____________(填标号);
A. B. C. D.
(3)指示剂N为_______,描述第二滴定终点前后颜色变化______________________;(4)产品中NaHCO 的质量分数为______________________(保留三位有效数字);
3
(5)第一滴定终点时,某同学俯视读数,其他操作均正确,则NaHCO 质量分数的计算结果
3
____________(填“偏大”“偏小”或“无影响”)。
7.(2021·辽宁卷) 磁性材料在很多领域具有应用前景,其制备过程如下(各步均在 氛围
中进行):
①称取 ,配成 溶液,转移至恒压滴液漏斗中。
②向三颈烧瓶中加入 溶液。
③持续磁力搅拌,将 溶液以 的速度全部滴入三颈烧瓶中,100℃下回流3h。
④冷却后过滤,依次用热水和乙醇洗涤所得黑色沉淀,在 干燥。
⑤管式炉内焙烧2h,得产品3.24g。
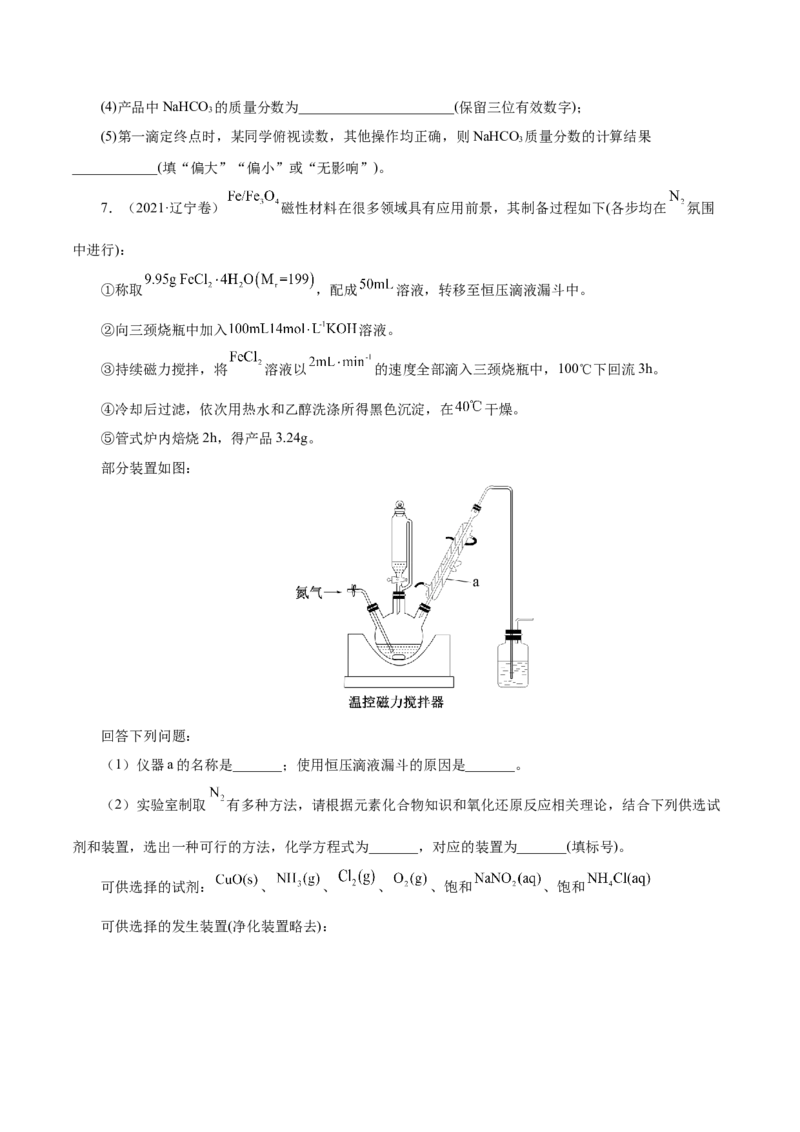
部分装置如图:
回答下列问题:
(1)仪器a的名称是_______;使用恒压滴液漏斗的原因是_______。
(2)实验室制取 有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试
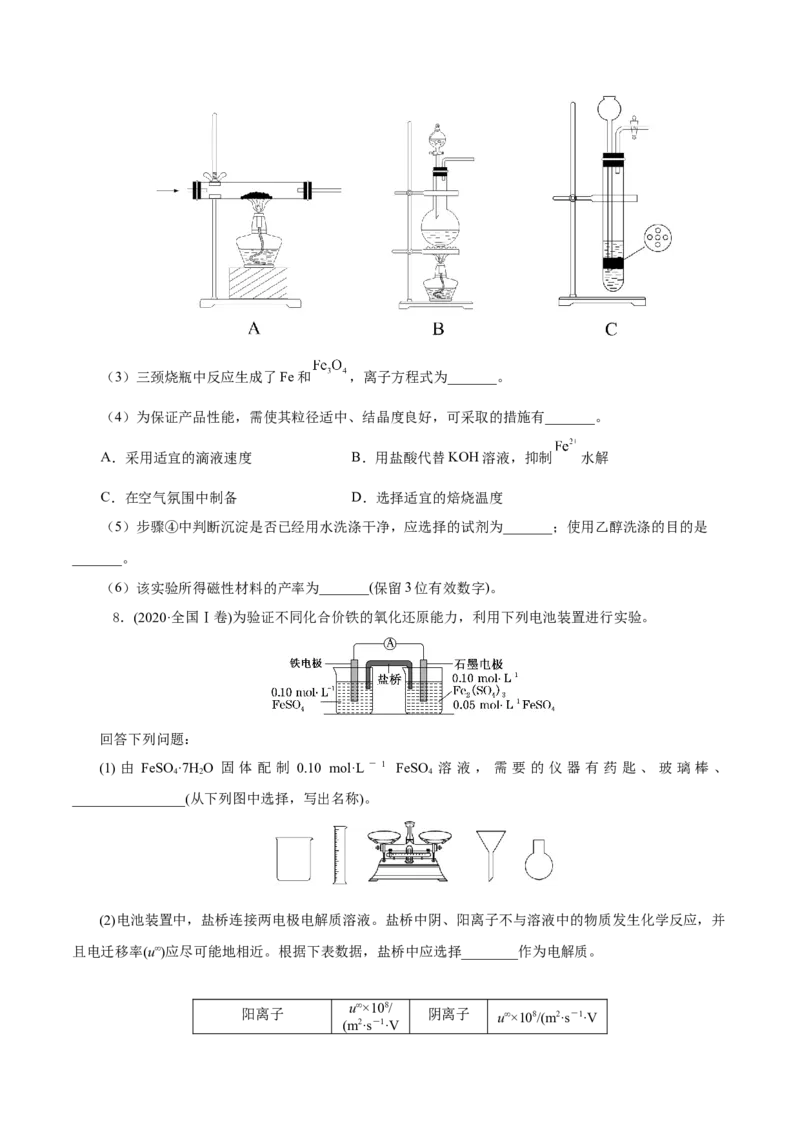
剂和装置,选出一种可行的方法,化学方程式为_______,对应的装置为_______(填标号)。
可供选择的试剂: 、 、 、 、饱和 、饱和
可供选择的发生装置(净化装置略去):(3)三颈烧瓶中反应生成了Fe和 ,离子方程式为_______。
(4)为保证产品性能,需使其粒径适中、结晶度良好,可采取的措施有_______。
A.采用适宜的滴液速度 B.用盐酸代替KOH溶液,抑制 水解
C.在空气氛围中制备 D.选择适宜的焙烧温度
(5)步骤④中判断沉淀是否已经用水洗涤干净,应选择的试剂为_______;使用乙醇洗涤的目的是
_______。
(6)该实验所得磁性材料的产率为_______(保留3位有效数字)。
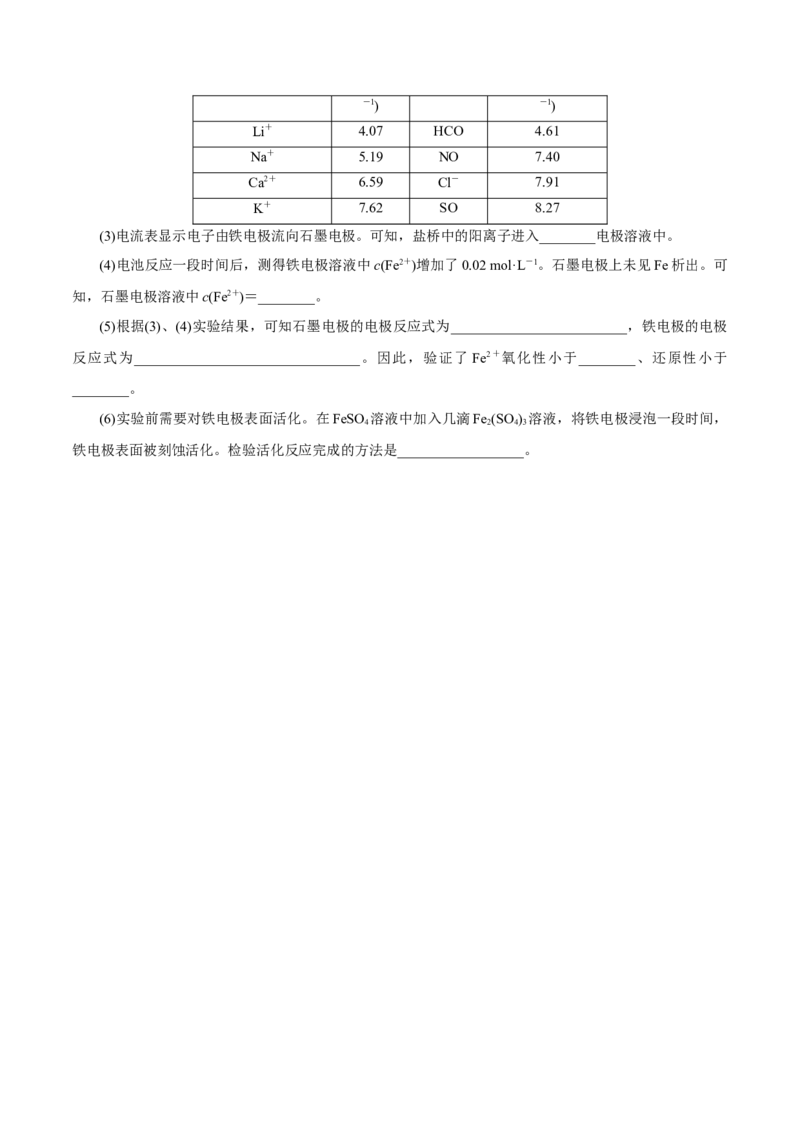
8.(2020·全国Ⅰ卷)为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
回答下列问题:
(1) 由 FeSO ·7H O 固 体 配 制 0.10 mol·L - 1 FeSO 溶 液 , 需 要 的 仪 器 有 药 匙 、 玻 璃 棒 、
4 2 4
________________(从下列图中选择,写出名称)。
(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并
且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择________作为电解质。
u∞×108/
阳离子 阴离子 u∞×108/(m2·s-1·V
(m2·s-1·V-1) -1)
Li+ 4.07 HCO 4.61
Na+ 5.19 NO 7.40
Ca2+ 6.59 Cl- 7.91
K+ 7.62 SO 8.27
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________电极溶液中。
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可
知,石墨电极溶液中c(Fe2+)=________。
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为_________________________,铁电极的电极
反应式为________________________________。因此,验证了 Fe2+氧化性小于________、还原性小于
________。
(6)实验前需要对铁电极表面活化。在FeSO 溶液中加入几滴Fe (SO ) 溶液,将铁电极浸泡一段时间,
4 2 4 3
铁电极表面被刻蚀活化。检验活化反应完成的方法是__________________。