文档内容
训练(十三) 铝及其重要化合物
1.(2021·河北承德检测)下列有关铝及其化合物的性质说法正确的是( )
A.Al O 熔点高,可用作耐高温材料
2 3
B.用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,发现熔化后的液态
铝滴落下来,所以金属铝的熔点较低
C.把用砂纸打磨过的铝条放入浓硝酸中,产生红棕色气体
D.把氯化铝溶液滴入浓氢氧化钠溶液中,产生大量白色沉淀
A [AlO 的熔点高,可用作耐高温材料,A项正确;用坩埚钳夹住一小块用砂纸仔细打
2 3
磨过的铝箔在酒精灯上加热,发现熔化后的液态铝不会滴落下来,因为铝表面生成氧化铝,
氧化铝的熔点高,B项错误;常温下,铝单质与浓硝酸发生钝化,生成致密氧化膜阻止反应进
一步进行,不会产生红棕色气体,C项错误;把氯化铝溶液滴入浓氢氧化钠溶液中,开始氢氧
化钠过量,不会产生白色沉淀,随着反应进行,后来有白色沉淀,D项错误。]
2.(2021·陕西榆林高三调研)明矾[KAl(SO)·12H O]在造纸等方面应用广泛。实验室中
4 2 2
采用废易拉罐(含有Al和少量Fe、Mg杂质)制备明矾的流程如图所示:
下列叙述错误的是( )
A.回收处理废易拉罐有利于保护环境和资源再利用
B.“沉淀”为Al (CO)
2 3 3
C.“操作a”中包含蒸发浓缩、冷却结晶、过滤等
D.上述流程中可用过量CO 代替NH HCO
2 4 3
B [回收处理废易拉罐,有利于资源的再利用,同时减少了环境污染,A项正确;NaAlO
2
溶液中加入NH HCO 溶液,发生反应:AlO+HCO+HO===Al(OH) ↓+CO,则所得“沉
4 3 2 3
淀”为Al(OH) ,B项错误;明矾易溶于水,从溶液中获取明矾的操作是蒸发浓缩、冷却结晶、
3
过滤、洗涤等,C 项正确;NaAlO 溶液中通入过量 CO ,发生反应:CO +AlO+
2 2 2
2HO===Al(OH) ↓+HCO,故可用过量CO 代替NH HCO ,D项正确。]
2 3 2 4 3
3.(2021·天津静海检测)下列各组物质,不能按a―→b―→c(“―→”表示反应一步完
成)关系转化的是( )
选项 a b c
A Al O NaAlO Al(OH)
2 3 2 3
B AlCl Al(OH) NaAlO
3 3 2
C Al Al(OH) Al O
3 2 3
D MgCl Mg(OH) MgO
2 2C [AlO 溶于NaOH溶液生成NaAlO ,NaAlO 溶液中通入CO 生成Al(OH) ,A项正
2 3 2 2 2 3
确;AlCl 与氨水反应生成Al(OH) ,Al(OH) 溶于NaOH溶液生成NaAlO ,B项正确;铝不能
3 3 3 2
直接生成Al(OH) ,C项错误;MgCl 与NaOH溶液反应生成Mg(OH) ,Mg(OH) 加热分解生
3 2 2 2
成MgO,D项正确。]
4.(2021·原创题)下列有关铝及其化合物的说法中正确的是( )
A.室温下,将铝片放入浓硝酸中,无明显实验现象,说明铝与浓硝酸不发生反应
B.氧化铝和氢氧化铝都是两性化合物,均可用于治疗胃酸过多
C.明矾是常用的净水剂,净水时发生的反应为:Al3++3H
2
O⇌Al (OH)
3
(胶体)+3H+
D.AlCl 溶液中加入足量氨水,产生的白色沉淀立即溶解:Al3++4NH ·H O===AlO+
3 3 2
4NH+2HO
2
C [室温下,Al在浓硝酸中发生钝化,无明显现象,A项错误;Al(OH) 用于治疗胃酸过
3
多,而Al O 则不能,B项错误;明矾溶于水电离产生Al3+,发生水解生成Al(OH) 胶体,用于
2 3 3
吸附水中悬浮杂质,起到净水作用,C项正确;Al(OH) 不能溶于过量氨水,应为Al3++
3
3NH ·HO=== Al(OH) ↓+3NH,D项错误。]
3 2 3
5.(2021·湖北武汉联考)铵明矾[NH Al(SO )·12H O]是分析化学常用基准试剂,其制备
4 4 2 2
过程如下。下列分析不正确的是( )
A.过程Ⅰ反应:2NH HCO +NaSO ===2NaHCO↓+(NH )SO
4 3 2 4 3 4 2 4
B.检验溶液B中阴离子的试剂仅需BaCl 溶液
2
C.若省略过程Ⅱ则铵明矾产率明显减小
D.向铵明矾溶液中逐滴加入NaOH溶液先后观察到:刺激性气体逸出→白色沉淀生成
→白色沉淀消失
D [过程Ⅰ是利用了相同温度下,NaHCO 的溶解度远小于 NH HCO 、NaSO 和
3 4 3 2 4
(NH )SO 的溶解度的性质,NH HCO 与 NaSO 发生复分解反应:2NH HCO +
4 2 4 4 3 2 4 4 3
NaSO ===2NaHCO↓+(NH )SO ,析出溶解度较小的NaHCO 晶体,A项正确; 滤液A中
2 4 3 4 2 4 3
含有SO及未反应的HCO等阴离子,用稀HSO 调节pH=2,HCO与H+发生反应生成CO、
2 4 2
HO,此时溶液B呈酸性,直接加入BaCl 溶液检验SO即可,溶液中产生白色沉淀,B项正确;
2 2
省略过程Ⅱ,会使溶液B中混入HCO离子,而HCO与Al3+会发生相互促进的双水解反应,
生成Al(OH) 沉淀,导致铵明矾的产率的明显减小,C项正确;铵明矾溶液中含有的NH、Al3+
3
都能与OH-发生反应,由于Al3+与NH ·HO能发生反应生成Al(OH) 沉淀,故铵明矾溶液
3 2 3
中加入NaOH溶液后,Al3+先与OH-反应生成白色Al(OH) 沉淀,随后NH与OH-反应生成
3
NH ·HO,而NH ·HO不稳定,部分发生分解放出刺激性气体NH ,当NaOH溶液过量时,
3 2 3 2 3Al(OH) 与OH-反应生成NaAlO ,Al(OH) 沉淀逐渐溶解,最后完全消失,D项错误。]
3 2 3
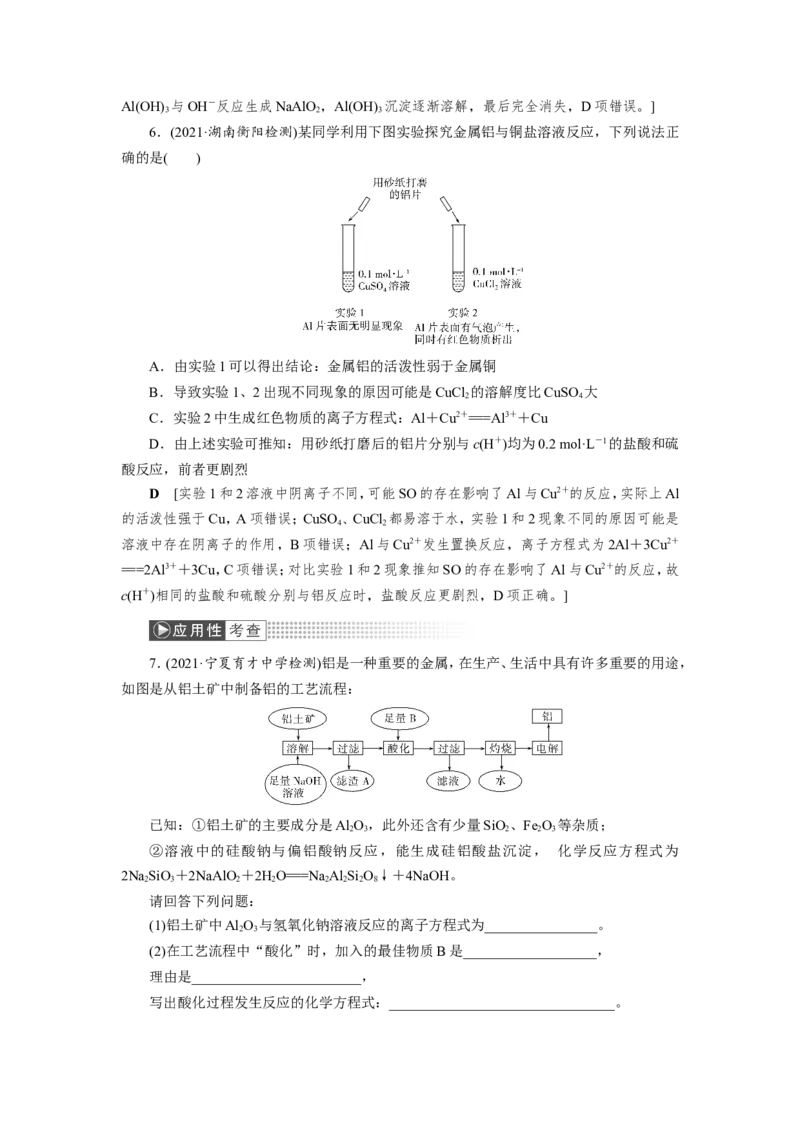
6.(2021·湖南衡阳检测)某同学利用下图实验探究金属铝与铜盐溶液反应,下列说法正
确的是( )
A.由实验1可以得出结论:金属铝的活泼性弱于金属铜
B.导致实验1、2出现不同现象的原因可能是CuCl 的溶解度比CuSO 大
2 4
C.实验2中生成红色物质的离子方程式:Al+Cu2+===Al3++Cu
D.由上述实验可推知:用砂纸打磨后的铝片分别与c(H+)均为0.2 mol·L-1的盐酸和硫
酸反应,前者更剧烈
D [实验1和2溶液中阴离子不同,可能SO的存在影响了Al与Cu2+的反应,实际上Al
的活泼性强于Cu,A项错误;CuSO 、CuCl 都易溶于水,实验1和2现象不同的原因可能是
4 2
溶液中存在阴离子的作用,B项错误;Al与Cu2+发生置换反应,离子方程式为2Al+3Cu2+
===2Al3++3Cu,C项错误;对比实验1和2现象推知SO的存在影响了Al与Cu2+的反应,故
c(H+)相同的盐酸和硫酸分别与铝反应时,盐酸反应更剧烈,D项正确。]
7.(2021·宁夏育才中学检测)铝是一种重要的金属,在生产、生活中具有许多重要的用途,
如图是从铝土矿中制备铝的工艺流程:
已知:①铝土矿的主要成分是Al O,此外还含有少量SiO、Fe O 等杂质;
2 3 2 2 3
②溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀, 化学反应方程式为
2NaSiO+2NaAlO +2HO===Na Al Si O↓+4NaOH。
2 3 2 2 2 2 2 8
请回答下列问题:
(1)铝土矿中Al O 与氢氧化钠溶液反应的离子方程式为________________。
2 3
(2)在工艺流程中“酸化”时,加入的最佳物质B是___________________,
理由是________________________,
写出酸化过程发生反应的化学方程式:________________________________。(3)工业上用Al O 与C、Cl 在高温条件下反应制取AlCl ,理论上每消耗6.0 g碳单质,转
2 3 2 3
移1 mol电子,则反应的化学方程式为__________________________________________。
(4)某同学推测铝与氧化铁发生铝热反应得到的熔融物中还含有Fe O,设计了如下方案
2 3
来验证:取一块该熔融物投入少量稀硫酸中,反应一段时间后,向反应后的混合液中滴加物
质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有Fe O。
2 3
物质甲是__________(填化学式),请判断该同学设计的实验方案的合理性________(填
“合理”或“不合理”)。原因是______________________________________
(若合理,则不用填写)。
解析 (1)铝土矿中Al O 与NaOH溶液反应生成NaAlO 和HO,离子方程式为Al O+
2 3 2 2 2 3
2OH-===2AlO+HO。
2
(2)由于Al(OH) 不溶于HCO 等弱酸,易溶于强酸,故在工艺流程中“酸化”时,常通
3 2 3
入过量CO 气体,其优点是Al(OH) 不会溶解,便于控制反应,且原料的价格低廉,反应的化
2 3
学方程式为CO+NaAlO +2HO===Al(OH) ↓+NaHCO 。
2 2 2 3 3
(3)理论上每消耗6.0 g碳单质(即0.5 mol),转移1 mol电子,则C元素由0价变为+2价,
据此推测反应产生 CO,结合得失电子守恒和原子守恒写出化学方程式:Al O +3C+
2 3
3Cl=====2AlCl +3CO。
2 3
(4)检验溶液中是否含有Fe3+,常加入KSCN溶液,若溶液变成血红色,则含有Fe3+,否
则不含Fe3+。由于铝热反应所得固体中含有Fe、Al、Al O,而Fe3+具有较强氧化性,可与Fe、
2 3
Al反应生成Fe2+,故不能检验出是否含有Fe3+。
答案 (1)AlO+2OH-===2AlO+HO
2 3 2
(2)CO CO 过量时氢氧化铝不会溶解,反应易控制,且原料廉价 CO +NaAlO +
2 2 2 2
2HO===Al(OH) ↓+NaHCO
2 3 3
(3)AlO+3C+3Cl=====2AlCl +3CO
2 3 2 3
(4)KSCN 不合理 Fe3+能与Fe、Al反应生成Fe2+,不能检出Fe3+