文档内容
第 30 讲 盐类水解
目录
考情分析 知识点3 水解常数及应用
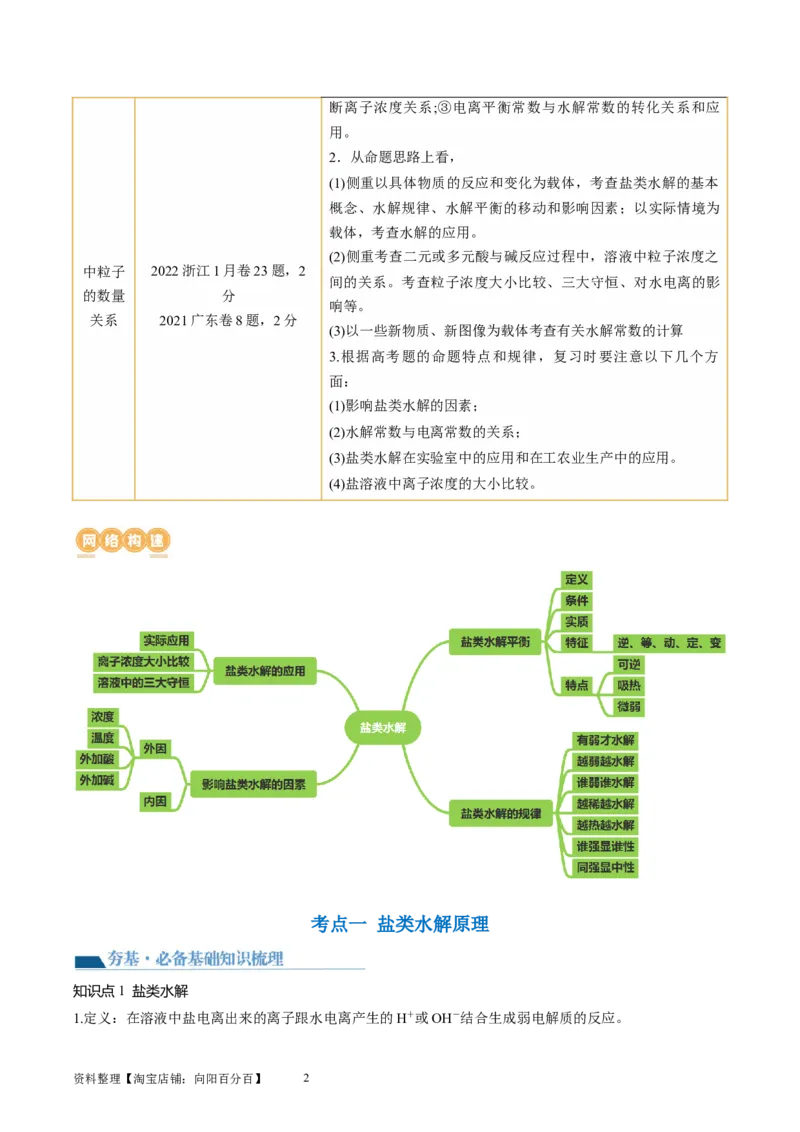
网络构建 【提升·必考题型归纳】
考向1 考查盐类水解的影响因素
考点一 盐类水解原理
考向2 考查盐类水解的应用
【夯基·必备基础知识梳理】
考向3 考查水解常数的应用与计算
知识点1 盐类水解
知识点2 盐类水解规律
考点三 水溶液中粒子的数量关系
知识点3 盐类水解方程式的书写
【夯基·必备基础知识梳理】
【提升·必考题型归纳】
知识点1 电解质溶液中的三大守恒
考向1 考查盐类的水解及溶液的酸碱性
知识点2 电解质溶液中粒子浓度大小比较
考向2 考查盐类水解规律及应用
知识点3 水溶液中函数图像分析
考点二 盐类水解的影响因素及应用
【提升·必考题型归纳】
考向1 考查单一溶液中粒子浓度大小比较
【夯基·必备基础知识梳理】
考向2 考查混合溶液中粒子浓度大小比较
知识点1 影响盐类水解的因素
知识点2 盐类水解的应用
真题感悟
考点要 考题统计 考情分析
求
2023浙江1月卷2题,2分 分析近三年的高考试题,高考命题在本讲有以下规律:
盐类水 2022北京卷1题,3分 1.从考查题型和内容上看,高考命题以选择题为主来呈现,考
解原理 2021北京卷12题,3分 查内容主要有以下两个方面:
2023北京卷3题,3分
(1)考查盐类水解的基本概念,依托实验背景,考查水解平衡的
盐类水
影响因素。
2022浙江6月卷19题,2
解的应
(2)与工农业生产相结合,考查盐类水解的应用。
分
用
2021河北卷6题,3分
(3)以单一溶液和混合溶液为背景,考查溶液中粒子浓度关系。
(4)借助图像的形式考查①水解方程式的书写;②结合滴定图像判
水溶液
2023天津卷10题,3分
资料整理【淘宝店铺:向阳百分百】 1断离子浓度关系;③电离平衡常数与水解常数的转化关系和应
用。
2.从命题思路上看,
(1)侧重以具体物质的反应和变化为载体,考查盐类水解的基本
概念、水解规律、水解平衡的移动和影响因素;以实际情境为
载体,考查水解的应用。
(2)侧重考查二元或多元酸与碱反应过程中,溶液中粒子浓度之
中粒子 2022浙江1月卷23题,2
间的关系。考查粒子浓度大小比较、三大守恒、对水电离的影
的数量 分
响等。
关系 2021广东卷8题,2分
(3)以一些新物质、新图像为载体考查有关水解常数的计算
3.根据高考题的命题特点和规律,复习时要注意以下几个方
面:
(1)影响盐类水解的因素;
(2)水解常数与电离常数的关系;
(3)盐类水解在实验室中的应用和在工农业生产中的应用。
(4)盐溶液中离子浓度的大小比较。
考点一 盐类水解原理
知识点1 盐类水解
1.定义:在溶液中盐电离出来的离子跟水电离产生的H+或OH-结合生成弱电解质的反应。
资料整理【淘宝店铺:向阳百分百】 22.条件:可溶性盐必须有弱酸根离子或弱碱阳离子
3.实质:
盐电离→→破坏了水的电离平衡→水的电离程度增大→溶液呈碱性、酸性或中性。
4.特点
(1)可逆:水解反应是可逆反应;
(2)吸热:水解反应是酸碱中和反应的逆反应;
(3)微弱:水解反应程度很微弱。
知识点2 盐类水解规律
1. 盐的分类与盐溶液的酸碱性
盐的类型 强酸强碱盐 强酸弱碱盐 弱酸强碱盐 弱酸弱碱盐
是否水解 不水解 水解 水解 水解
比较Ka和Kb的大小确定
溶液的酸碱性 中性 酸性 碱性
溶液的酸性碱性
NaCl 、 NH Cl 、 NaS 、 CHCOONH ( 中 性 溶
4 2 3 4
代表物
KNO CuSO NaCO 液)
3 4 2 3
酸式盐不能通过简单分类来判断其溶液的酸碱性:
NaHSO 不水解,但是其溶液显酸性;
4
注意
NaHSO 电离大于水解,其溶液显酸性;
3
NaHCO 水解大于电离,其溶液显酸性。
3
2.盐类水解规律:
“有弱才水解、无弱不水解、越弱越水解、都弱都水解、越热越水解、越稀越水解、谁强显谁性、同强是
中性”。
知识点3 盐类水解方程式的书写
1.一般要求
水解记三点:①水写分子式,②中间用可逆( ),③后无沉气出。即盐类水解一般不会产生沉淀和气体,
所以不用符号“↓”和“↑”表示水解产物。如 NH Cl水解的离子方程式为NH+HO NH ·H O+H
4 2 3 2
+。
2.三种类型的盐水解离子方程式的书写
①多元弱酸盐水解:分步进行,水解离子方程式要分步表示,以第一步为主,一般只写第一步水解方程式。
如NaCO 水解的离子方程式为CO+HO HCO+OH-。
2 3 2
资料整理【淘宝店铺:向阳百分百】 3②多元弱碱盐水解:水解离子方程式一步写完。
如FeCl 水解的离子方程式为Fe3++3HO Fe(OH) +3H+。
3 2 3
③阴、阳离子相互促进的水解:水解程度较大(即产生沉淀),书写时要用“===”、“↑”、“↓”等。
如NaS溶液与AlCl 溶液混合水解的离子方程式为2Al3++3S2-+6HO===2Al(OH) ↓+3HS↑。
2 3 2 3 2
注意:多元弱酸阴离子分步水解,分步书写;多元弱碱阳离子分步水解,一步书写。
考向1 考查盐类的水解及溶液的酸碱性
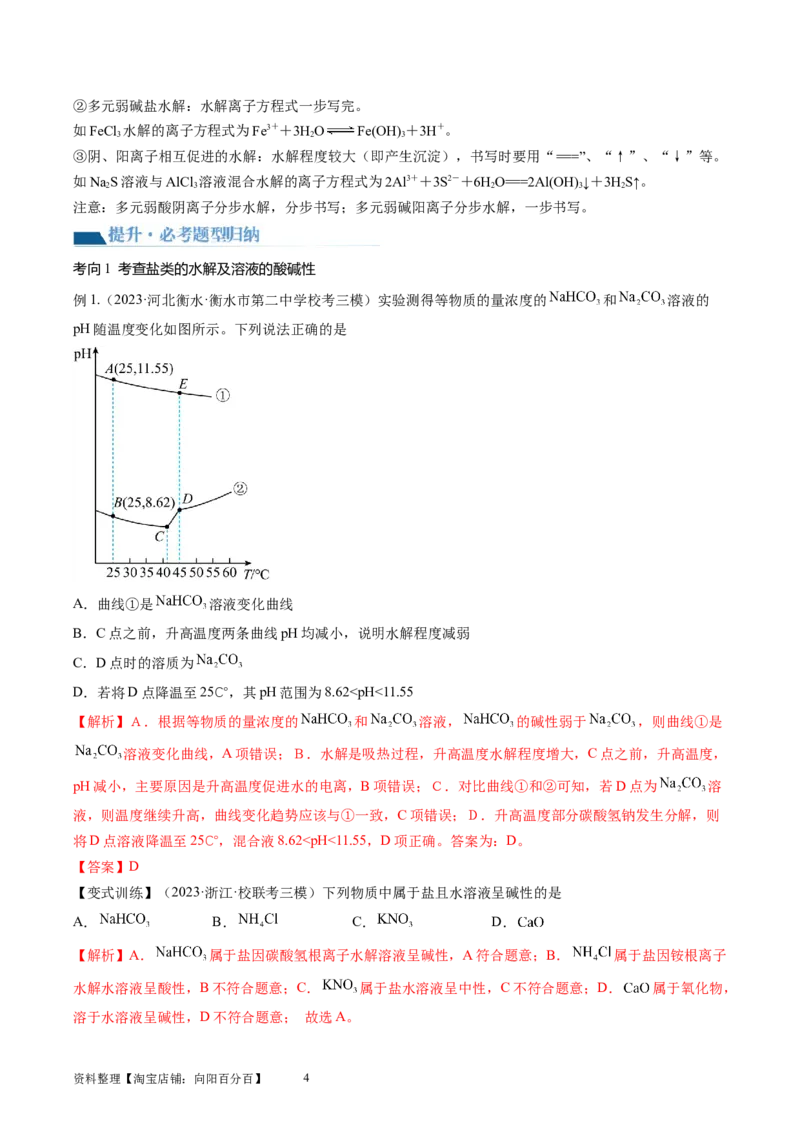
例1.(2023·河北衡水·衡水市第二中学校考三模)实验测得等物质的量浓度的 和 溶液的
pH随温度变化如图所示。下列说法正确的是
A.曲线①是 溶液变化曲线
B.C点之前,升高温度两条曲线pH均减小,说明水解程度减弱
C.D点时的溶质为
D.若将D点降温至25℃,其pH范围为8.62c(H+),溶液显碱性。同理NaHS溶液、NaHPO 溶液显碱性。
2 3 2 4
②电离程度大于水解程度,溶液显酸性,如NaHSO 溶液中:HSO H++SO(主要);HSO+HO
3 2
HSO +OH-(次要)。使c(H+)>c(OH-),溶液显酸性。同理NaH PO 溶液显酸性。
2 3 2 4
考向2 考查盐类水解规律及应用
例2.(2023·全国·模拟预测)实验测得浓度均为 的 溶
液和 溶液的pH随温度的变化情况如图所示。下列说法错误的是
A. 时, 的电离平衡常数约为
B. 后, 溶液的pH随温度的升高而增大的原因可能是
的挥发
C.升高温度, 溶液中 减小, 增大,pH减小
D. 溶液中存在:
【解析】A. 时, 的pH=a, 的电离平衡常数约为 ,故A正
确;B.升高温度,促进 电离,溶液中 增大, 后, 减小,说明醋酸的浓度降低,
的挥发会导致 降低,故B正确;C.升高温度,使 水解平衡正向移动,
溶液中 增大,故C错误;D.根据质子守恒, 溶液中
,故D正确;选C。
【答案】C
【变式训练】(2023·安徽滁州·安徽省定远县第三中学校考二模)如下图所示,只有未电离的HA分子可
自由通过交换膜。常温下,往甲室和乙室中分别加入 的 溶液( )和 的HA
溶液( ),达到平衡后,下列说法正确的是
A.常温下,HA的电离度约为0.1%
B.平衡后,甲、乙两室的pH相等
资料整理【淘宝店铺:向阳百分百】 5C.平衡后,甲室中 的物质的量浓度小于乙室中 的物质的量浓度
D.若用等物质的量浓度的NaA溶液代替 溶液,则通过交换膜的HA分子的量减少
【分析】0.1mol/L NHA溶液pH约为7,说明铵根离子和A—离子在溶液中的水解程度几乎相等,溶液中
4
HA和一水合氨的浓度约为10—7mol/L,由只有未电离的HA分子可自由通过交换膜可知,甲室溶液中HA
的浓度小于乙室,乙室中HA通过交换膜进入甲室,当两室溶液中HA浓度相等时,乙室的电离和甲室的
水解都达到平衡。
【解析】A.由0.1mol/LHA溶液pH约为3可知,HA的电离度约为 ×100%=1%,故A错误;B.
由分析可知,当两室溶液中HA浓度相等时,乙室的电离和甲室的水解都达到平衡,由于甲室中的A—离子
会抑制HA的电离,所以平衡后,甲、乙两室的溶液pH不相等,故B错误;C.由分析可知,当两室溶液
中HA浓度相等时,乙室的电离和甲室的水解都达到平衡,甲室中加入的HA抑制铵根离子的水解,溶液
中一水合氨浓度小于10—7mol/L,乙室中HA的浓度减小,电离度增大,则乙室中A—离子浓度大于
0.05mol/L×1%=0.0005mol/L,所以甲室中一水合氨的物质的量浓度小于乙室中A—离子的物质的量浓度,故
C正确;D.NaA溶液中A—离子的水解程度小于NH A溶液,溶液中HA浓度小于NH A溶液,所以若用
4 4
等物质的量浓度的NaA溶液代替NH A溶液,通过交换膜的HA分子的量增加,故D错误;故选C。
4
【答案】C
【规律总结】盐类水解的规律及拓展应用
(1)“谁弱谁水解,越弱越水解”。如酸性:HCNCHCOONa。
3 3
(2)相同条件下的水解程度
①正盐>相应酸式盐,如CO>HCO。
② 相 互 促 进 水 解 的 盐 > 单 独 水 解 的 盐 > 水 解 相 互 抑 制 的 盐 。 如 NH 的 水 解 :
(NH )CO>(NH)SO >(NH)Fe(SO )。
4 2 3 4 2 4 4 2 4 2
考点二 盐类水解的影响因素及应用
知识点1 影响盐类水解的因素
1.内因:形成盐的酸或碱越弱,其盐就越易水解。如水解程度:NaCO>NaSO ,NaCO>NaHCO 。
2 3 2 3 2 3 3
2.外因
3.以FeCl 水解为例[Fe3++3HO Fe(OH) +3H+],填写外界条件对水解平衡的影响。
3 2 3
条件 移动方向 H+数 pH 现象
升温 向右 增多 减小 颜色变深
通HCl 向左 增多 减小 颜色变浅
加HO 向右 增多 增大 颜色变浅
2
加NaHCO 向右 减小 增大 生成红褐色沉淀,放出气体
3
知识点2 盐类水解的应用
1.盐类水解的重要应用
资料整理【淘宝店铺:向阳百分百】 6应用 举例
判断溶液的
FeCl 溶液显酸性,原因是Fe3++3HO Fe(OH) +3H+
3 2 3
酸碱性
等物质的量浓度的NaX、NaY、NaZ三种盐溶液的pH分别为8、9、10,则酸
判断酸性强弱
性:HX>HY>HZ
配制或贮存易 配制CuSO 溶液时,加入少量HSO ,防止Cu2+水解;配制FeCl 溶液,加入少
4 2 4 3
水解的盐溶液 量盐酸;贮存NaCO 溶液、NaSiO 溶液不能用带磨口玻璃塞的试剂瓶
2 3 2 3
胶体的制取 制取Fe(OH) 胶体的离子方程式:Fe3++3HO=====Fe(OH) (胶体)+3H+
3 2 3
泡沫灭火器
成分为NaHCO 与Al (SO ),发生反应为Al3++3HCO===Al(OH) ↓+3CO↑
3 2 4 3 3 2
原理
作净水剂 明矾可作净水剂,原理为Al3++3HOAl(OH) (胶体)+3H+
2 3
化肥的使用 铵态氮肥与草木灰不得混用
除锈剂 NH Cl与ZnCl 溶液可作焊接时的除锈剂
4 2
比较溶液中离子 如:NaCO 溶液中离子浓度由大到小的顺序为c(Na+)>c(CO)>c(OH-)>c(HCO)
2 3
浓度的大小 >c(H+)
盐水解生成挥发性酸,蒸干灼烧后一般得氧化物。如AlCl →Al O
3 2 3
盐水解生成难挥发性酸,蒸干后得原物质。如CuSO →CuSO
4 4
判断盐溶液
考虑盐受热时是否分解。如KMnO →KMnO 和MnO
4 2 4 2
蒸干时的产物
还原性盐溶液蒸干时会被O 氧化。如NaSO →NaSO
2 2 3 2 4
弱酸的铵盐溶液蒸干后无固体剩余。如NH HCO 、(NH )CO
4 3 4 2 3
2.熟记下列因相互促进水解不能大量共存的离子组合
(1)Al3+与HCO、CO、AlO、SiO、HS-、S2-、ClO-。
(2)Fe3+与HCO、CO、AlO、SiO、ClO-。
(3)NH与SiO、AlO。
3.盐溶液蒸干灼烧时所得产物的判断
❶盐溶液水解生成难挥发性酸时,蒸干后一般得原物质,如CuSO (aq)――→CuSO (s);
4 4
盐 溶 液 水 解 生 成 易 挥 发 性 酸 时 , 蒸 干 灼 烧 后 一 般 得 对 应 的 氧 化 物 , 如
AlCl (aq)――→Al(OH) ――→Al O。
3 3 2 3
❷酸根离子易水解的强碱盐,如NaCO 溶液等蒸干后可得到原物质。
2 3
资料整理【淘宝店铺:向阳百分百】 7❸考虑盐受热时是否分解。Ca(HCO ) 、NaHCO 、KMnO 、NH Cl固体受热易分解,因此蒸干灼烧后分别
3 2 3 4 4
为 Ca(HCO )―→CaCO (CaO);NaHCO ―→NaCO ;KMnO ―→KMnO 和 MnO ;NH Cl―→NH ↑+
3 2 3 3 2 3 4 2 4 2 4 3
HCl↑。
❹还原性盐在蒸干时会被O 氧化。如NaSO (aq)蒸干得NaSO (s)。
2 2 3 2 4
❺弱酸的铵盐蒸干后无固体。如NH HCO 、(NH )CO。
4 3 4 2 3
4.缓冲溶液
(1)概念:能够抵御少量外来的酸、碱或稀释,而保持溶液的pH基本不变的溶液叫缓冲溶液。
(2)缓冲溶液的范围:pH=pKa±1 (浓度之比10倍或1/10)。
(3)缓冲溶液的类型
类型 举例 等浓度的混合溶液的酸碱性
弱酸-弱酸盐 CHCOOH-CHCOONa 酸性;pH=4.76
3 3
弱碱-弱碱盐 NH ∙H O-NH Cl 碱性;pH=9.25
3 2 4
正盐-酸式盐 NaCO-NaHCO 碱性;pH=10.30
2 3 3
酸式盐-酸 NaHC O-HC O 酸性;pH=1.68
2 4 2 2 4
知识点3 水解常数及应用
1.数学表达式
用HA表示酸,用MOH表示碱,MA表示由它们生成的盐,在MA溶液中,若M+、A-均能水解,A-+
HO HA+OH-,则A-的水解常数为K =;M++HO MOH+H+,则M+的水解常数为K =。
2 h 2 h
2.水解常数与电离常数的关系
1)推导:若NaA为强碱弱酸盐,A-+HO HA+OH-,K ===;若MCl为强酸弱碱盐,同理可得
2 h
K =。
h
2)K 与K(或K )、K 的关系
h a b W
(1)一元弱酸盐:K·K =K
a h W
(2)一元弱碱盐:K ·K =K
b h W
(3)多元弱酸盐,如Na A溶液:K = Na HA溶液K = 依次类推……
m h m-1 h
3.意义
水解常数可以表示盐的水解程度的大小,K 越大,盐类水解程度越大。
h
4.外界影响因素
水解常数是只是温度的函数,K 随温度的升高而增大。
h
5.水解常数的应用
(1)计算盐溶液中的c(H+)或c(OH-)
资料整理【淘宝店铺:向阳百分百】 8K =≈,c(OH-)=;同理,对于M++HO MOH+H+,c(H+)=。
h 2
(2)判断水解程度大小、盐溶液的酸碱性
如,对于CHCOONH 溶液,由K(CHCOOH)≈K (NH ·H O)可知,K (CHCOO-)≈K (NH),CHCOO-和
3 4 a 3 b 3 2 h 3 h 3
NH水解程度相同,CHCOONH 溶液呈中性,c(H+)=c(OH-)。
3 4
(3)判断水解程度和电离程度大小,盐溶液的酸碱性。
①单一溶液。
如,对于NaHCO 溶液,K (HCO)===2.3×10-8,K(HCO)=4.7×10-11<K (HCO),HCO电离程度小于其
3 h a h
水解程度,溶液呈碱性,c(H+)<c(OH-)。
②混合溶液。
如,对于等物质的量浓度的CHCOOH、CHCOONa混合溶液,K(CHCOOH)=1.75×10-5,K (CHCOO-)
3 3 a 3 h 3
===5.7×10-10<K(CHCOOH),CHCOO-的水解程度小于CHCOOH的电离程度,溶液显酸性,c(H+)
a 3 3 3
>c(OH-)。
考向1 考查盐类水解的影响因素
例1.(2023·广东梅州·统考三模)25 °C时,K(HClO)=4.0×10-8。下 列说法正确的是
a
A.25°C时,往pH=3的HClO溶液中加少量NaClO固体,HClO的电离程度和水电离出的c(H+ )均减小
B.将浓度均为0.1mol·L-1的NaClO和NaOH溶液加热,两种溶液的pH均变大
C.相同温度下,等pH的HCOONa和NaClO溶液中存在:c(HCOO- )>c(ClO- )
D.25 °C时,pH=7的NaClO和HClO混合溶液中存在:c(HClO)c(ClO- ),故C正确;
D.25 °C时, ,则水解平衡常数 ,则水解强于电离;由电荷守恒
,pH=7, ,则 ,由水解强于电离可
知, ,故D错误;答案选C。
【答案】C
【变式训练】(2023·北京海淀·101中学校考三模)实验测得10mL0.50mol•L-1NH Cl溶液、
4
10mL0.50mol•L-1CHCOONa溶液的pH分别随温度与稀释加水量的变化如图所示。已知25℃时CHCOOH
3 3
和NH •H O电离常数均为1.8×10-5。下列说法不正确的是
3 2
A.图中实线表示pH随加水量的变化,虚线表示pH随温度的变化
B.将NH Cl溶液加水稀释至浓度 mol•L-1,溶液pH变化值小于lgx
4
C.随温度升高,K 增大,CHCOONa溶液中c(H+)增大,pH减小,c(OH-)减小
w 3
D.25℃时稀释相同倍数的NH Cl溶液与CHCOONa溶液中:c(Na+)-c(CHCOO-)=c(Cl-)-c(NH )
4 3 3
【分析】由题中信息可知,图中两条曲线为10 mL 0. 50 mol·L-1 NH Cl溶液、10 mL 0.50mol·L-1CHCOONa
4 3
溶液的pH分别随温度与稀释加水量的变化曲线,由于两种盐均能水解,水解反应为吸热过程,且温度越
高、浓度越小其水解程度越大。氯化铵水解能使溶液呈酸性,浓度越小,虽然水程度越大,但其溶液的酸
性越弱,故其pH越大;醋酸钠水解能使溶液呈碱性,浓度越小,其水溶液的碱性越弱,故其pH越小;温
度越高,水的电离度越大。因此,图中的实线为pH随加水量的变化,虚线表示pH随温度的变化。
【解析】A.由分析可知,图中实线表示pH随加水量的变化,虚线表示pH随温度的变化,A说法正确;
B.将NH Cl溶液加水稀释至浓度 mol·L-1时,若氯化铵的水解平衡不发生移动,则其中的c(H+)变为
4
原来的 ,则溶液的pH将增大lgx,但是,加水稀释时,氯化铵的水解平衡向正反应方向移动,c(H+)大于
原来的 ,因此,溶液pH的变化值小于lgx,B说法正确;C.随温度升高,水的电离程度变大,因此水
的离子积变大,即K 增大;随温度升高,CHCOONa的水解程度变大,溶液中c(OH-)增大,因此,C说法
w 3
不正确;D. 25℃时稀释相同倍数的NH C1溶液与CHCOONa溶液中均分别存在电荷守恒,c(Na+ )
4 3
+c(H+) =c(OH-)+c(CH COO- ) ,c(NH +)+c(H+ ) =c(Cl-)+c(OH- )。因此,氯化铵溶液中,c(Cl-)-c(NH +)
3 4 4
=c(H+ )-c(OH- ),醋酸钠溶液中,c(Na+ )-c(CHCOO- )= c(OH-) -c(H+) 。由于25 ℃时CHCOOH和
3 3
NH ·H O的电离常数均为1.8 ×10-5,因此,由于原溶液的物质的量浓度相同,稀释相同倍数后的NH C1溶
3 2 4
液与CHCOONa溶液,溶质的物质的量浓度仍相等,由于电离常数相同,其中盐的水解程度是相同的,因
3
此,两溶液中c(OH-) -c(H+)(两者差的绝对值)相等,故c(Na+ )-c(CHCOO- )=c(Cl-)-c(NH +),D说法正确。
3 4
故选C。
【答案】C
资料整理【淘宝店铺:向阳百分百】 10【名师归纳】盐类水解易受温度、浓度、溶液的酸碱性等因素的影响,以氯化铁水解为例,当改变条件如
升温、通入HCl气体、加水、加铁粉、加碳酸氢钠等时,应从移动方向、pH的变化、水解程度、现象等
方面去归纳总结,加以分析掌握。
考向2 考查盐类水解的应用
例2.(2023·广东惠州·统考一模)勤劳致富,越努力越幸福。下列劳动项目与所述的化学知识没有关联的
是
选项 劳动项目 化学知识
A 明矾净水 明矾具有氧化性
B 小苏打用作发泡剂烘焙面包 小苏打受热分解产生气体
C 用热的纯碱溶液洗去油污 热的纯碱溶液水解显碱性
D 用厨余垃圾制肥料 厨余垃圾含N、P等元素
【解析】A.明矾净水的基本原理是明矾在水中能电离出铝离子,铝离子与水电离产生的氢氧根结合,产
生氢氧化铝胶体,与明矾具有氧化性无关,A项中的劳动项目与所述的化学知识没有关联;B.小苏打为
NaHCO ,受热分解出CO 气体,可以用作发泡剂烘焙面包,B项中的劳动项目与所述的化学知识有关联;
3 2
C.碳酸钠为强碱弱酸盐,水解显碱性,加热促进盐类的水解,油脂可以在碱性环境下水解生成具有可溶
性盐和甘油,所以可以用热的纯碱溶液洗去油污,C项中的劳动项目与所述的化学知识有关联;D.厨余
垃圾含N、P等元素,是植物生成需要的元素,所以可以用厨余垃圾制肥料,,C项中的劳动项目与所述
的化学知识有关联。答案选A。
【答案】A
【变式训练】(2023·河南·校联考模拟预测)氯化铁是实验室中经常使用的物质,根据下列实验目的设计
的实验方案正确的是
选
实验目的 实验方案
项
称量一定质量的氯化铁固体先溶于较浓的盐酸中,再加入蒸
A 实验室配制FeCl 溶液
3
馏水稀释至所需浓度
向酸性高锰酸钾溶液中滴入少量氯化铁溶液,观察溶液颜色
B 检验配制的FeCl 溶液中是否含有Fe2+
3
的变化
制备氢氧化铁胶体并鉴别氯化铁溶液与 煮沸少许饱和氯化铁溶液一段时间后,采用丁达尔现象鉴别
C
氢氧化铁胶体 所得物质和氯化铁溶液
向FeCl 溶液中先滴加一定量的NaF溶液,再滴加几滴KSCN
3
D 验证铁离子的氧化性
溶液,未出现红色
【解析】A.配制FeCl 溶液时加入HCl抑制水解,A正确;B.酸性高锰酸钾溶液也可以氧化Cl-,B错误;
3
C.制备氢氧化铁胶体,向沸腾的蒸馏水中逐滴加入1~2mL饱和氯化铁溶液,继续煮沸至液体呈红褐色,停
资料整理【淘宝店铺:向阳百分百】 11止加热,C错误;D.F-与Fe3+反生成更为稳的无色 ,滴入SCN-后,Fe3+无法与SCN-结合,与氧化
性无关,D错误;故答案为:A。
【答案】A
【名师归纳】配制盐溶液时,为抑制盐的水解而加入酸或碱,但应注意不能引入杂质离子,加入的酸应是
与盐中的酸根对应的强酸,如配制FeCl 溶液加盐酸;加入的碱应是与盐中的阳离子对应的强碱,如配制
3
NaS溶液要加NaOH溶液。
2
考向3 考查水解常数的应用与计算
例3.(2023·陕西西安·统考一模)25℃时,将HCl气体缓慢通入0.1mol•L-1的氨水中,溶液的pH、体系中
粒子浓度的对数值(lgc)与反应物的物质的量之比[t= ]的关系如图所示。若忽略溶液体积变化,
下列有关说法错误的是
A.t=0.5时,c(NH )>c(Cl-)
B.25℃时,NH 的水解平衡常数K 的数量级为10-10
h
C.P 所示溶液:2c(Cl-)=c(NH )+c(NH•H O)
1 3 2
D.P 所示溶液:c(Cl-)>100c(NH •H O)
2 3 2
【分析】本题给出的图是溶液的pH、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比[t=
]的关系图,最左边纵坐标是离子浓度的对数,右边的纵坐标是pH值,横坐标是反应物的物
质的量之比,图示中NH 离子与NH •H O交叉点对应的pH值是9.25,可以计算铵根离子的水解常数,根
3 2
据电荷守恒可以判断A选项,根据物料守恒可以判断C选项,根据水解常数可以判断D选项。
【解析】A.t=0.5时,对应的pH值大于7,c(H+)< c(OH-),由电荷守恒c(N )+c(H+)=c(Cl-)+c(OH-)得出
c(NH )>c(Cl-),故A正确;B.NH 离子与NH •H O交叉点对应的pH值是9.25,c(N )= c(NH •H O),
3 2 3 2
c(H+)= ,带入铵根离子的水解常数公式K= = ,数量级为 ,故B正确;C.
h
资料整理【淘宝店铺:向阳百分百】 12P 点 =1.0,根据物料守恒c(Cl-)=c(NH )+c(NH•H O),故C错误;D.P 点对应的pH=7,
1 3 2 2
c(H+)= c(OH-)= 推出c(NH )=c(Cl-),K= = ,得出 = ,得出
h
c(Cl-)= c(NH •H O),故D正确;答案选C。
3 2
【答案】C
【变式训练】(2023·陕西咸阳·统考三模)某化学兴趣小组利用传感技术探究0.01mol•L-1的碳酸钠溶液滴
定100mL0.01mol•L-1盐酸溶液的实验,得到反应过程中的c( )、c( )、c(HCO)的变化曲线(假定
2 3
滴定过程中HCO 不分解和忽略CO 的逸出)如图所示。下列说法正确的是
2 3 2
已知:25℃时,HCO 的K =4×10-7,K =5×10-11;lg4=0.6。
2 3 a1 a2
A.曲线I为c(HCO )的变化曲线,V=10
1
B.25℃时,碳酸钠的水解常数K =2.5×10-8
h1
C.水的电离程度:a>c>b
D.c点溶液pH=6.4
【分析】用0.01mol•L-1的碳酸钠溶液滴定100mL0.01mol•L-1盐酸溶液过程中,最开始酸过量,产生
HCO,继续滴加碳酸钠,HCO 减少, 增加,最后 逐渐增多。因此曲线I、Ⅱ、Ⅲ分别代表
2 3 2 3
HCO、 、 。
2 3
【解析】A.由分析可知,曲线I代表HCO,根据 可知100mL
2 3
0.01mol•L-1HCl应恰好消耗50mL 0.01mol•L-1的碳酸钠溶液,故V=50,A错误;B.25℃时,碳酸钠的水
1
解常数 ,B错误;C. 、 均促进水电离, 含量越高,水电离
程度越大,根据图像可知,水的电离程度:ac(H PO -)>c(HPO 2-)>c(PO 3-)。
3 4 2 4 4 4
(2)多元弱酸的正盐溶液:多元弱酸的酸根离子分步水解,水解程度逐级减弱。
如在NaCO 溶液中:c(Na+)>c(CO 2-)>c(OH-)>c(HCO-)。
2 3 3 3
(3)多元弱酸酸式盐:分析酸式酸根电离与水解大小。
如NaHCO 溶液中HCO -水解大于电离,则;c(Na+)>c(HCO-)>c(OH-)>c(H CO)>c(H+)>c(CO 2-)。
3 3 3 2 3 3
NaHSO 溶液中HSO -电离大于水解,则c(Na+)>c(HSO -)c(H+)>c(SO2-)>c(OH-)>c(H SO )。
3 3 3 3 2 3
2.混合溶液中各离子浓度的比较
混合溶液要综合分析电离、水解等因素。如在0.1 mol·L-1 NH Cl溶液和0.1 mol·L-1的氨水混合溶液中,
4
各离子浓度大小的顺序为c(NH +)>c(Cl-)>c(OH-)>c(H+)。
4
3.不同溶液中同一离子浓度的比较
不同溶液要看溶液中其他离子对该离子的影响。如在相同物质的量浓度的下列溶液中:
①NH Cl②CHCOONH ③NH HSO ,c(NH +)由大到小的顺序为③>①>②。
4 3 4 4 4 4
4.电解质溶液中粒子浓度大小比较的思维模型
知识点3 水溶液中函数图像分析
1.稀释曲线
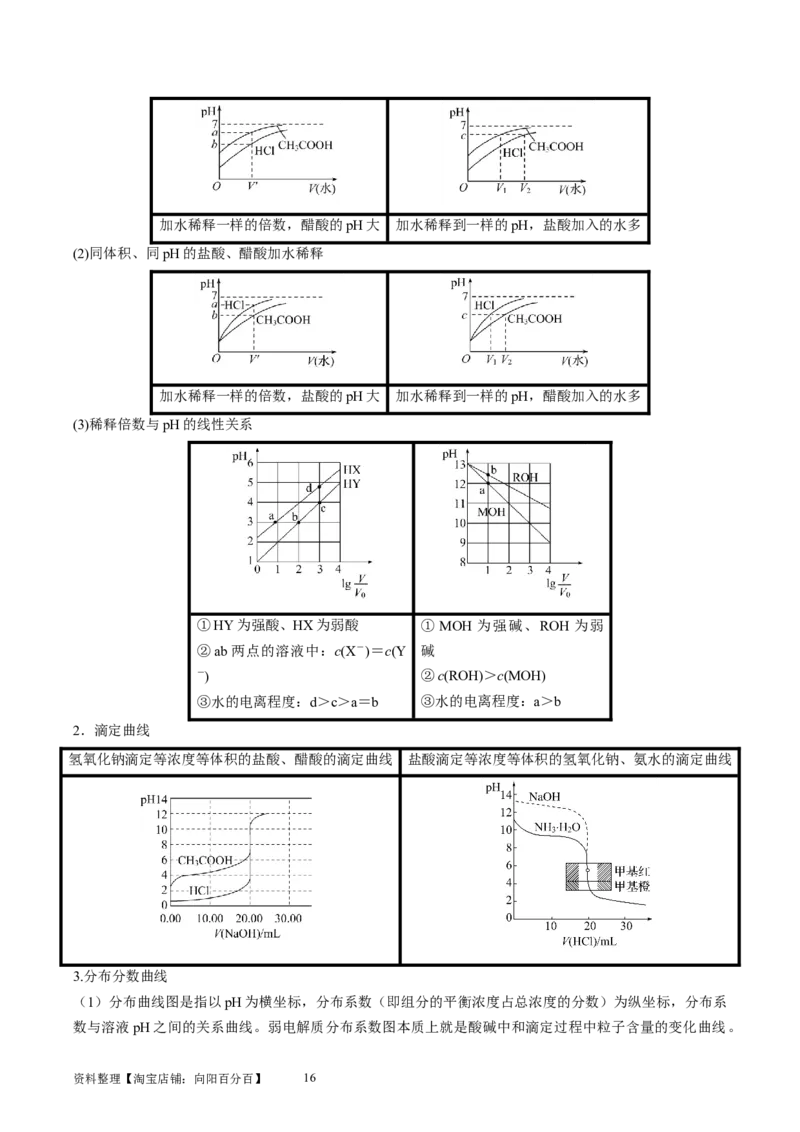
(1)同体积、同浓度的盐酸、醋酸加水稀释
资料整理【淘宝店铺:向阳百分百】 15加水稀释一样的倍数,醋酸的pH大 加水稀释到一样的pH,盐酸加入的水多
(2)同体积、同pH的盐酸、醋酸加水稀释
加水稀释一样的倍数,盐酸的pH大 加水稀释到一样的pH,醋酸加入的水多
(3)稀释倍数与pH的线性关系
①HY为强酸、HX为弱酸 ① MOH 为强碱、ROH 为弱
②ab两点的溶液中:c(X-)=c(Y 碱
-) ②c(ROH)>c(MOH)
③水的电离程度:d>c>a=b ③水的电离程度:a>b
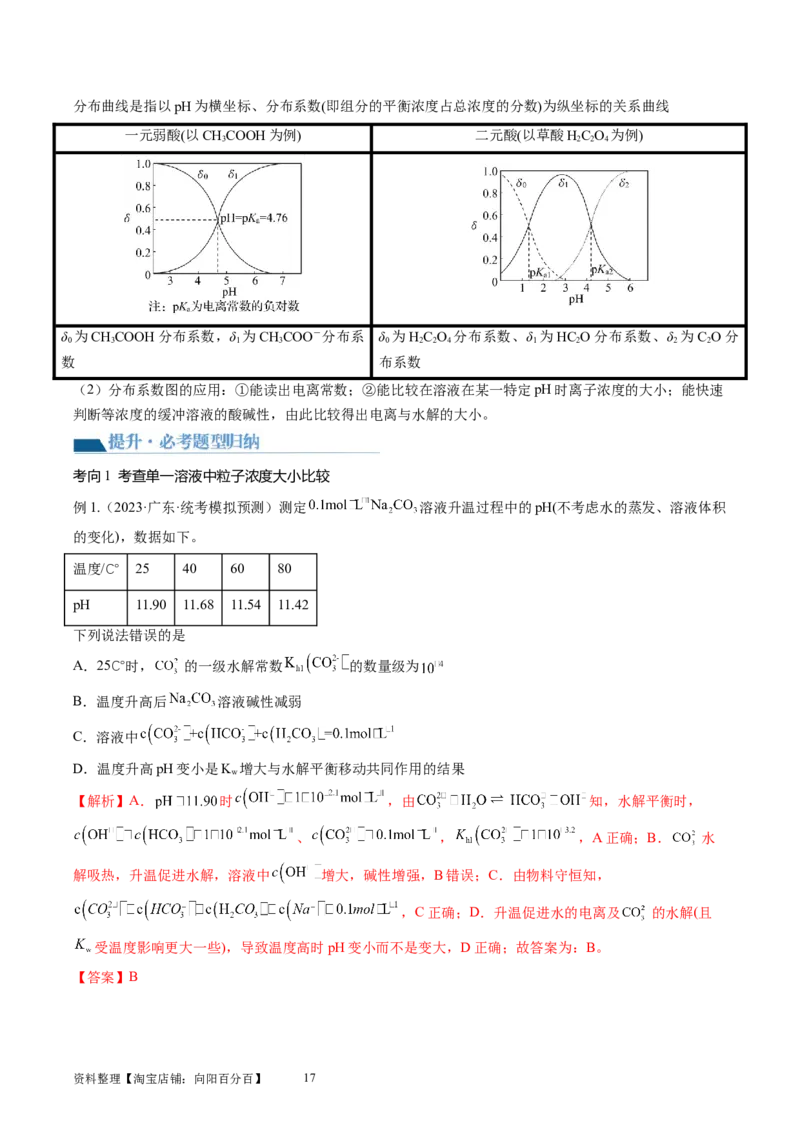
2.滴定曲线
氢氧化钠滴定等浓度等体积的盐酸、醋酸的滴定曲线 盐酸滴定等浓度等体积的氢氧化钠、氨水的滴定曲线
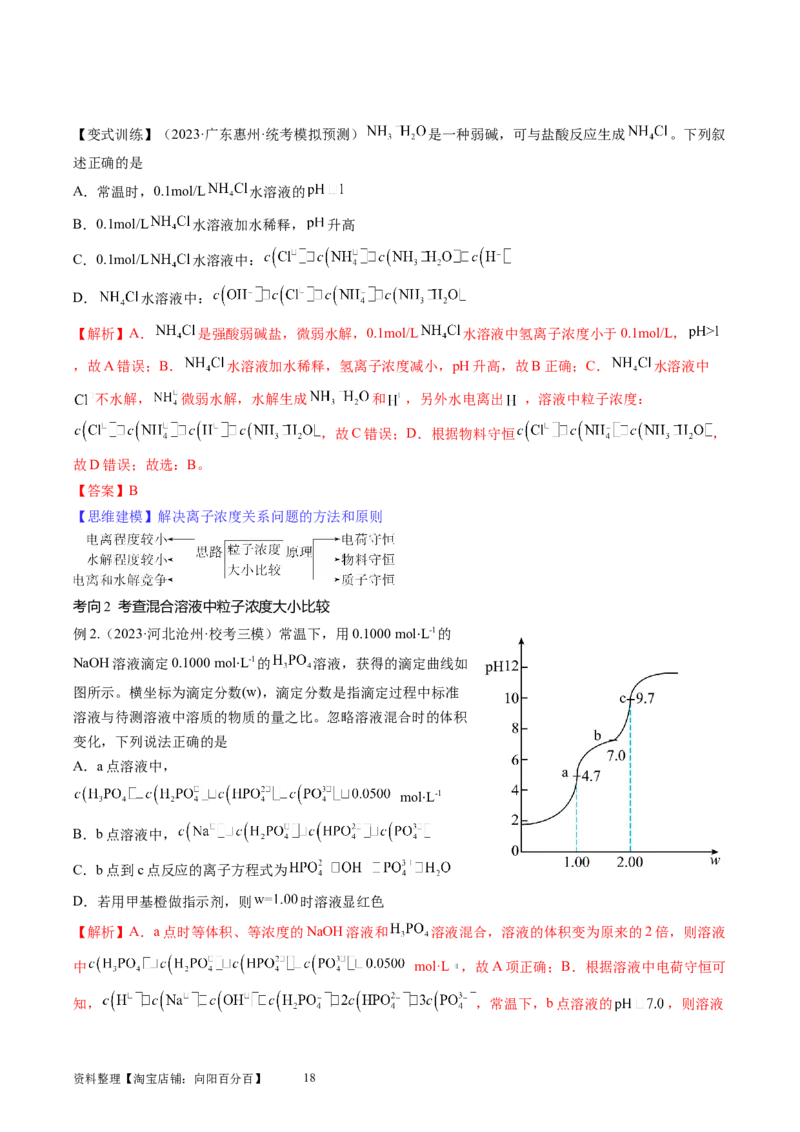
3.分布分数曲线
(1)分布曲线图是指以pH为横坐标,分布系数(即组分的平衡浓度占总浓度的分数)为纵坐标,分布系
数与溶液pH之间的关系曲线。弱电解质分布系数图本质上就是酸碱中和滴定过程中粒子含量的变化曲线。
资料整理【淘宝店铺:向阳百分百】 16分布曲线是指以pH为横坐标、分布系数(即组分的平衡浓度占总浓度的分数)为纵坐标的关系曲线
一元弱酸(以CHCOOH为例) 二元酸(以草酸HC O 为例)
3 2 2 4
δ 为CHCOOH分布系数,δ 为CHCOO-分布系 δ 为HC O 分布系数、δ 为HC O分布系数、δ 为C O分
0 3 1 3 0 2 2 4 1 2 2 2
数 布系数
(2)分布系数图的应用:①能读出电离常数;②能比较在溶液在某一特定pH时离子浓度的大小;能快速
判断等浓度的缓冲溶液的酸碱性,由此比较得出电离与水解的大小。
考向1 考查单一溶液中粒子浓度大小比较
例1.(2023·广东·统考模拟预测)测定 溶液升温过程中的pH(不考虑水的蒸发、溶液体积
的变化),数据如下。
温度/℃ 25 40 60 80
pH 11.90 11.68 11.54 11.42
下列说法错误的是
A.25℃时, 的一级水解常数 的数量级为
B.温度升高后 溶液碱性减弱
C.溶液中
D.温度升高pH变小是K 增大与水解平衡移动共同作用的结果
w
【解析】A. 时 ,由 知,水解平衡时,
、 , ,A正确;B. 水
解吸热,升温促进水解,溶液中 增大,碱性增强,B错误;C.由物料守恒知,
,C正确;D.升温促进水的电离及 的水解(且
受温度影响更大一些),导致温度高时pH变小而不是变大,D正确;故答案为:B。
【答案】B
资料整理【淘宝店铺:向阳百分百】 17【变式训练】(2023·广东惠州·统考模拟预测) 是一种弱碱,可与盐酸反应生成 。下列叙
述正确的是
A.常温时,0.1mol/L 水溶液的
B.0.1mol/L 水溶液加水稀释, 升高
C.0.1mol/L 水溶液中:
D. 水溶液中:
【解析】A. 是强酸弱碱盐,微弱水解,0.1mol/L 水溶液中氢离子浓度小于0.1mol/L,
,故A错误;B. 水溶液加水稀释,氢离子浓度减小,pH升高,故B正确;C. 水溶液中
不水解, 微弱水解,水解生成 和 ,另外水电离出 ,溶液中粒子浓度:
,故C错误;D.根据物料守恒 ,
故D错误;故选:B。
【答案】B
【思维建模】解决离子浓度关系问题的方法和原则
考向2 考查混合溶液中粒子浓度大小比较
例2.(2023·河北沧州·校考三模)常温下,用0.1000 molL-1的
NaOH溶液滴定0.1000 molL-1的 溶液,获得的滴定⋅ 曲线如
图所示。横坐标为滴定分数⋅(w),滴定分数是指滴定过程中标准
溶液与待测溶液中溶质的物质的量之比。忽略溶液混合时的体积
变化,下列说法正确的是
A.a点溶液中,
molL-1
⋅
B.b点溶液中,
C.b点到c点反应的离子方程式为
D.若用甲基橙做指示剂,则 时溶液显红色
【解析】A.a点时等体积、等浓度的NaOH溶液和 溶液混合,溶液的体积变为原来的2倍,则溶液
中 mol·L ,故A项正确;B.根据溶液中电荷守恒可
知, ,常温下,b点溶液的 ,则溶液
资料整理【淘宝店铺:向阳百分百】 18中 ,则 ,故B项错误;C.a点时等物质的量
的NaOH和 反应,溶液中的溶质是 ,c点时,参加反应的NaOH与 的物质的量之比
为2∶1,溶液中的溶质是 ,因此,a点到c点整个阶段中的反应为 ,
故C项错误;D.甲基橙的变色范围为3.1~4.4, 时, ,若用甲基橙做指示剂,溶液显黄
色,故D项错误;答案选A。
【答案】A
【变式训练】(2021·广东广州·广州市培正中学校考三模)25℃时,有
的一组醋酸、醋酸钠混合溶液,溶液中 、
与pH的关系如图所示。下列有关溶液中离子浓度关
系的叙述错误的是
A. 的溶液中:
B.W点的溶液中:
C. 的溶液中:
D.向W点所表示的1.0L溶液中通入0.05molHCl气体(溶液体积变化可忽略):
【分析】混合溶液为醋酸和醋酸钠的混合溶液,且c(CHCOOH)+c(CH COO-)=0.1mol/L,根据图分析,当
3 3
pH增加时,浓度增大的应为CHCOO-,浓度减小的应为CHCOOH;
3 3
【解析】A.根据图分析,当pH=5.5时,c(CHCOO-)>c(CHCOOH)>c(H+)>c(OH-),故A正确;B.W
3 3
点溶液c(CHCOOH)=c(CH COO-),溶液中存在电荷守恒:c(Na+)+c(H+)═c(OH-)+c(CH COO-),故B正确;
3 3 3
C.pH=3.5的溶液中,溶液呈酸性,由电荷守恒知c(Na+)+c(H+)-c(OH-)+c(CH COOH)=c(CH COO-)
3 3
+c(CH COOH)=0.1mol/L,故C正确;D.加入HCl气体可使溶液酸性增强,CHCOOH浓度增加而
3 3
CHCOO-降低,由于W点平衡时溶液中醋酸和醋酸根离子浓度相同,所以二者分别为0.05mol/L,通入1.0
3
L 溶液中通入0.05 mol HCl 气体,则反应恰好生成0.1mol/L的醋酸溶液,由质子守恒:c(H+)=c(CH COO-)
3
+c(OH-),故D错误,故选:D。
【答案】D
【易错提醒】1.电荷守恒式中不只是各离子浓度的简单相加。如2c(CO)的化学计量数2代表一个CO带2
个负电荷,不可漏掉。
2.物料守恒式中,离子浓度系数不能漏写或颠倒。如NaS溶液中的物料守恒式中,“2”表示c(Na+)是溶
2
液中各种硫元素存在形式的硫原子总浓度的2倍。
3.等式考虑守恒原理,不等式考虑平衡原理
(1)等式一般与电荷守恒、物料守恒、质子守恒相联系。如果给定的等式不是三个守恒式,可以把三个守恒
资料整理【淘宝店铺:向阳百分百】 19式变化形式后相互作差,加以推导即可。
(2)如果给定的是不等式,要先考虑等式,对等式的一边加入或减少某离子,即可变成不等式。
1.(2023·浙江·高考真题)硫酸铜应用广泛,下列说法不正确的是
A. 元素位于周期表p区 B.硫酸铜属于强电解质
C.硫酸铜溶液呈酸性 D.硫酸铜能使蛋白质变性
【答案】A
【解析】A.Cu为29号元素,位于IB族,属于ds区元素,故A错误;B.硫酸铜属于盐类,在水溶液中
能完全电离,属于强电解质,故B正确;C.硫酸铜为强酸弱碱盐,铜离子水解使溶液呈酸性,故C正确;
D.铜离子为重金属离子,能使蛋白质变性,故D正确;故选:A。
2.(2022·浙江·统考高考真题)关于反应 ,达到平衡
后,下列说法不正确的是
A.升高温度,氯水中的 减小
B.氯水中加入少量醋酸钠固体,上述平衡正向移动, 增大
C.取氯水稀释, 增大
D.取两份氯水,分别滴加 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明
上述反应存在限度
【答案】D
【解析】A.HClO受热易分解,升高温度,HClO分解,平衡正向移动,c(HClO)减小,A正确;B.氯水
中加入少量醋酸钠固体,醋酸根离子和氢离子结合生成醋酸分子,氢离子浓度减小,平衡正向移动,
c(HClO)增大,B正确;C.氯水稀释,平衡正向移动,而c(HClO)和c(Cl-)均减小,但HClO本身也存在电
离平衡HClO H++ClO-,稀释促进了HClO的电离,使c(HClO)减少更多,因此 增大,C正确;
⇌
D.氯水中加硝酸银产生白色沉淀,证明溶液中有氯离子,氯水中加淀粉碘化钾溶液,溶液变蓝,证明生
成了碘单质,溶液中有强氧化性的物质,而氯气和次氯酸都有强氧化性,不能证明反应物和生成物共存,
即不能证明上述反应存在限度,D错误;答案选D。
3.(2022·北京·高考真题)2022年3月神舟十三号航天员在中国空间站进行了“天宫课堂”授课活动。其
中太空“冰雪实验”演示了过饱和醋酸钠溶液的结晶现象。下列说法不正确的是
A.醋酸钠是强电解质
B.醋酸钠晶体与冰都是离子晶体
C.常温下,醋酸钠溶液的
D.该溶液中加入少量醋酸钠固体可以促进醋酸钠晶体析出
【答案】B
【解析】A.醋酸钠在水溶液中能完全电离,醋酸钠是强电解质,故A正确;B.醋酸钠晶体是离子晶体,
资料整理【淘宝店铺:向阳百分百】 20冰是分子晶体,故B错误;C.醋酸钠是强碱弱酸盐,常温下,醋酸钠溶液的 ,故C正确;D.过
饱和醋酸钠溶液处于亚稳态,加入少量醋酸钠固体可以促进醋酸钠晶体析出,形成饱和溶液,故D正确;
选B。
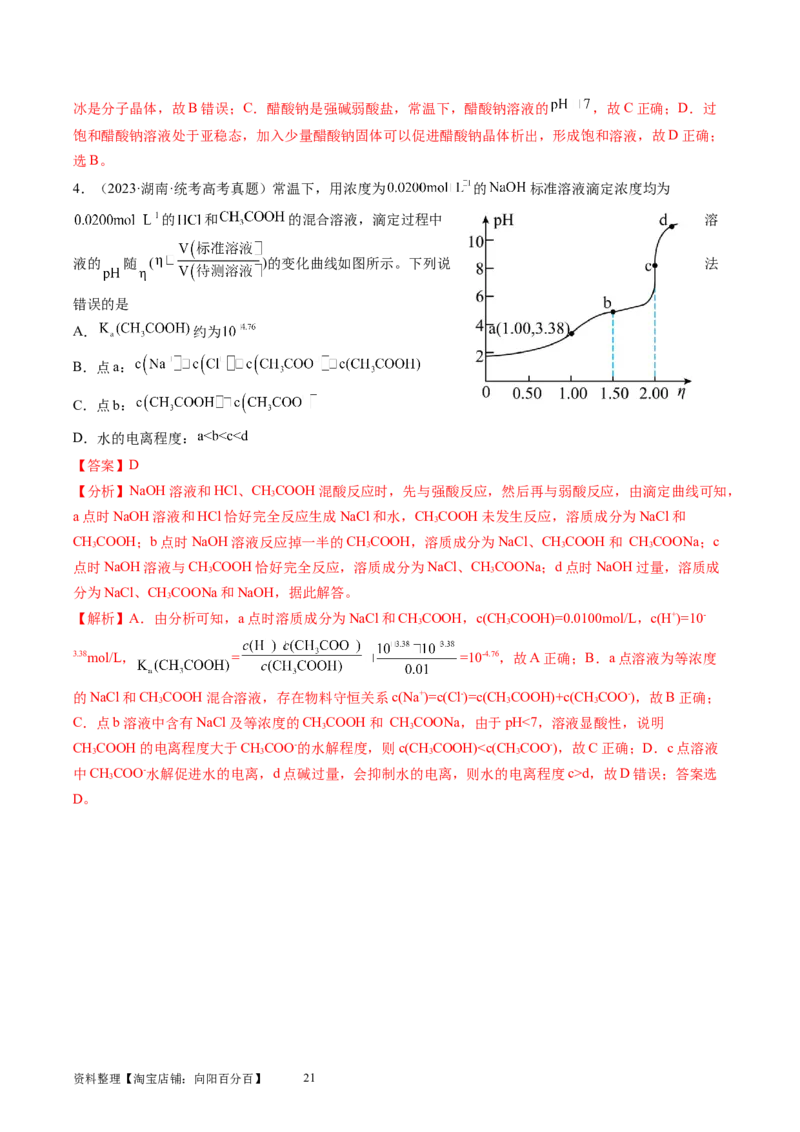
4.(2023·湖南·统考高考真题)常温下,用浓度为 的 标准溶液滴定浓度均为
的 和 的混合溶液,滴定过程中 溶
液的 随 ( )的变化曲线如图所示。下列说 法
错误的是
A. 约为
B.点a:
C.点b:
D.水的电离程度:
【答案】D
【分析】NaOH溶液和HCl、CHCOOH混酸反应时,先与强酸反应,然后再与弱酸反应,由滴定曲线可知,
3
a点时NaOH溶液和HCl恰好完全反应生成NaCl和水,CHCOOH未发生反应,溶质成分为NaCl和
3
CHCOOH;b点时NaOH溶液反应掉一半的CHCOOH,溶质成分为NaCl、CHCOOH和 CHCOONa;c
3 3 3 3
点时NaOH溶液与CHCOOH恰好完全反应,溶质成分为NaCl、CHCOONa;d点时NaOH过量,溶质成
3 3
分为NaCl、CHCOONa和NaOH,据此解答。
3
【解析】A.由分析可知,a点时溶质成分为NaCl和CHCOOH,c(CHCOOH)=0.0100mol/L,c(H+)=10-
3 3
3.38mol/L, = =10-4.76,故A正确;B.a点溶液为等浓度
的NaCl和CHCOOH混合溶液,存在物料守恒关系c(Na+)=c(Cl-)=c(CH COOH)+c(CH COO-),故B正确;
3 3 3
C.点b溶液中含有NaCl及等浓度的CHCOOH和 CHCOONa,由于pH<7,溶液显酸性,说明
3 3
CHCOOH的电离程度大于CHCOO-的水解程度,则c(CHCOOH)d,故D错误;答案选
3
D。
资料整理【淘宝店铺:向阳百分百】 21