文档内容
第三十一、三十二讲 化学实验基础
【基础巩固】
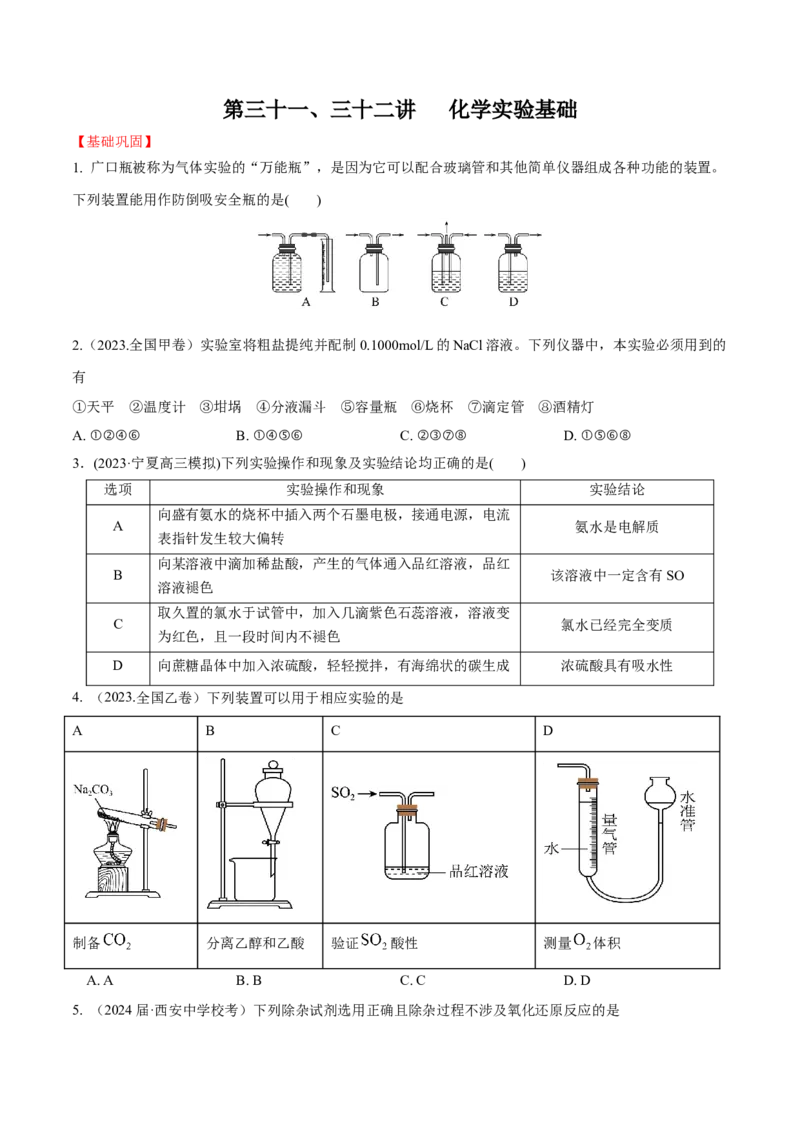
1. 广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其他简单仪器组成各种功能的装置。
下列装置能用作防倒吸安全瓶的是( )
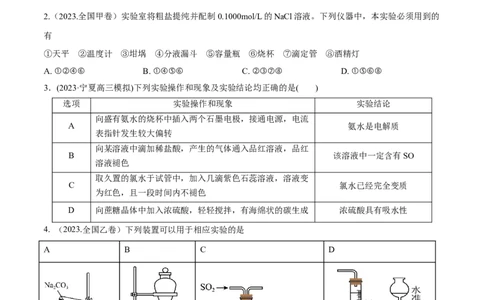
2.(2023.全国甲卷)实验室将粗盐提纯并配制0.1000mol/L的NaCl溶液。下列仪器中,本实验必须用到的
有
①天平 ②温度计 ③坩埚 ④分液漏斗 ⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A. ①②④⑥ B. ①④⑤⑥ C. ②③⑦⑧ D. ①⑤⑥⑧
3.(2023·宁夏高三模拟)下列实验操作和现象及实验结论均正确的是( )
选项 实验操作和现象 实验结论
向盛有氨水的烧杯中插入两个石墨电极,接通电源,电流
A 氨水是电解质
表指针发生较大偏转
向某溶液中滴加稀盐酸,产生的气体通入品红溶液,品红
B 该溶液中一定含有SO
溶液褪色
取久置的氯水于试管中,加入几滴紫色石蕊溶液,溶液变
C 氯水已经完全变质
为红色,且一段时间内不褪色
D 向蔗糖晶体中加入浓硫酸,轻轻搅拌,有海绵状的碳生成 浓硫酸具有吸水性
4. (2023.全国乙卷)下列装置可以用于相应实验的是
A B C D
制备 分离乙醇和乙酸 验证 酸性 测量 体积
A. A B. B C. C D. D
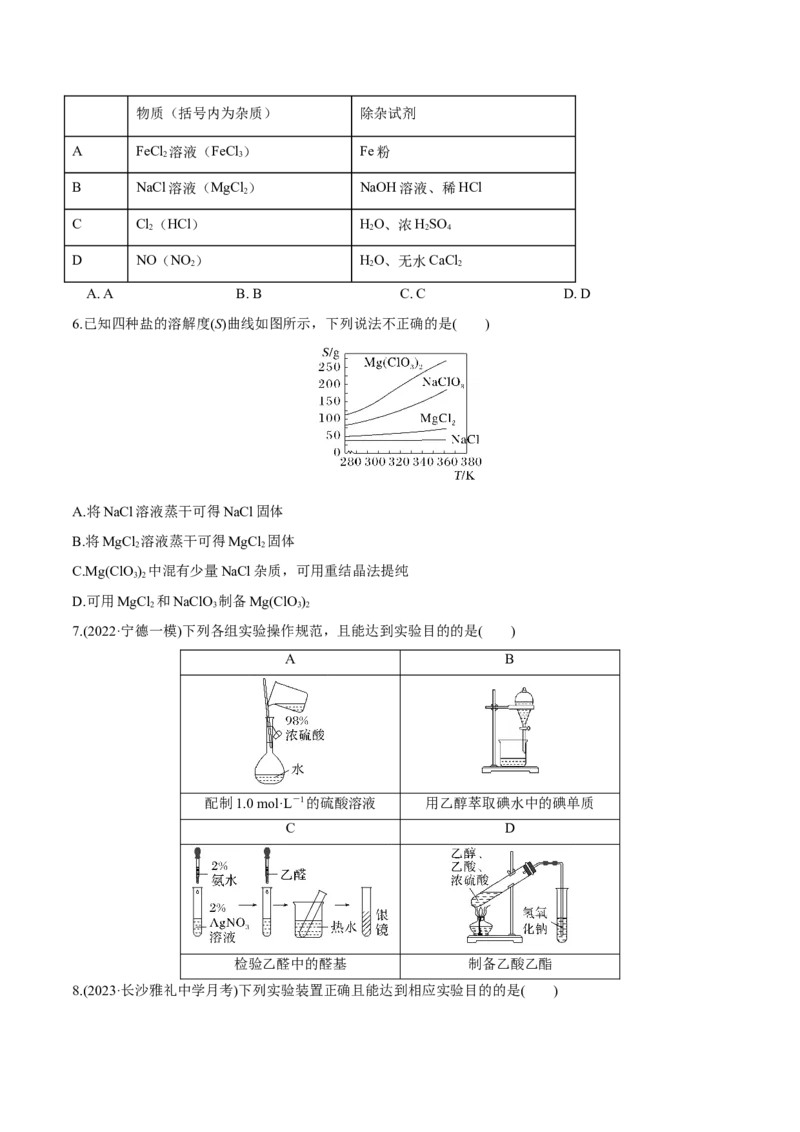
5. (2024届·西安中学校考)下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是物质(括号内为杂质) 除杂试剂
A FeCl 溶液(FeCl ) Fe粉
2 3
B NaCl溶液(MgCl ) NaOH溶液、稀HCl
2
C Cl(HCl) HO、浓HSO
2 2 2 4
D NO(NO ) HO、无水CaCl
2 2 2
A. A B. B C. C D. D
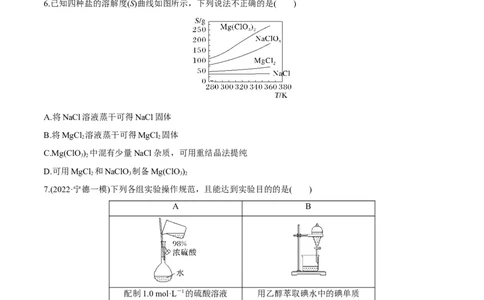
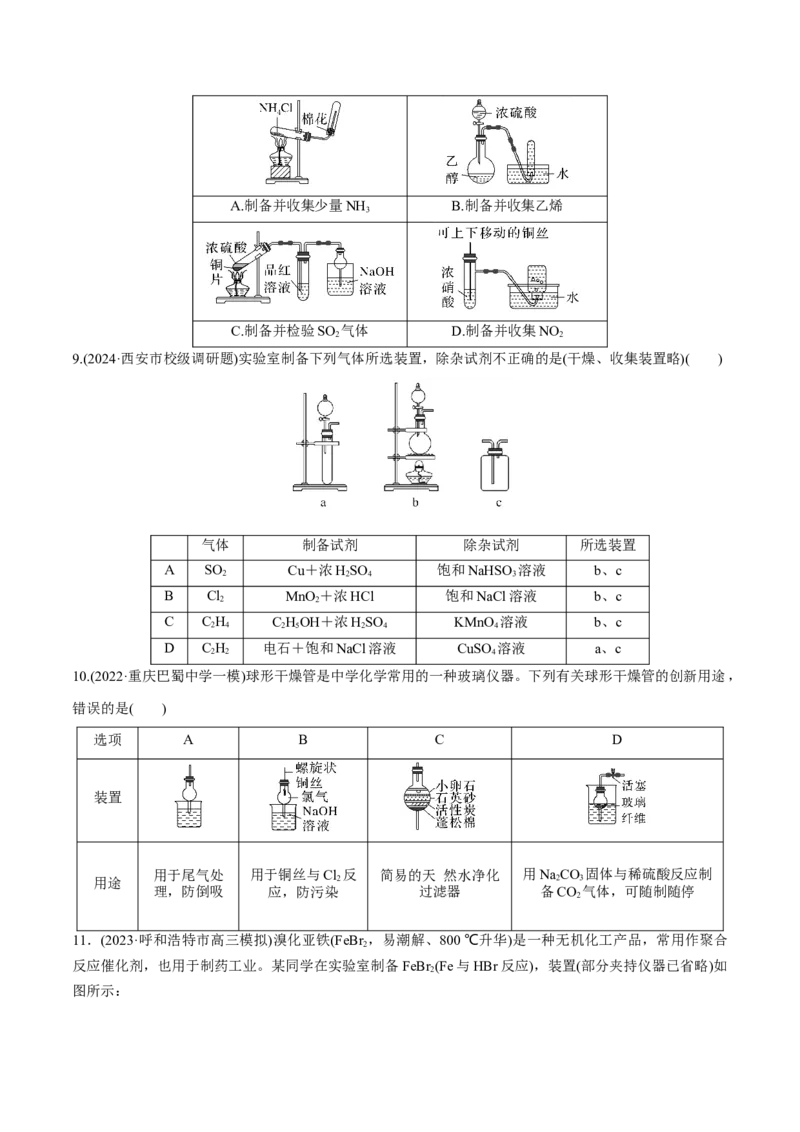
6.已知四种盐的溶解度(S)曲线如图所示,下列说法不正确的是( )
A.将NaCl溶液蒸干可得NaCl固体
B.将MgCl 溶液蒸干可得MgCl 固体
2 2
C.Mg(ClO ) 中混有少量NaCl杂质,可用重结晶法提纯
3 2
D.可用MgCl 和NaClO 制备Mg(ClO)
2 3 3 2
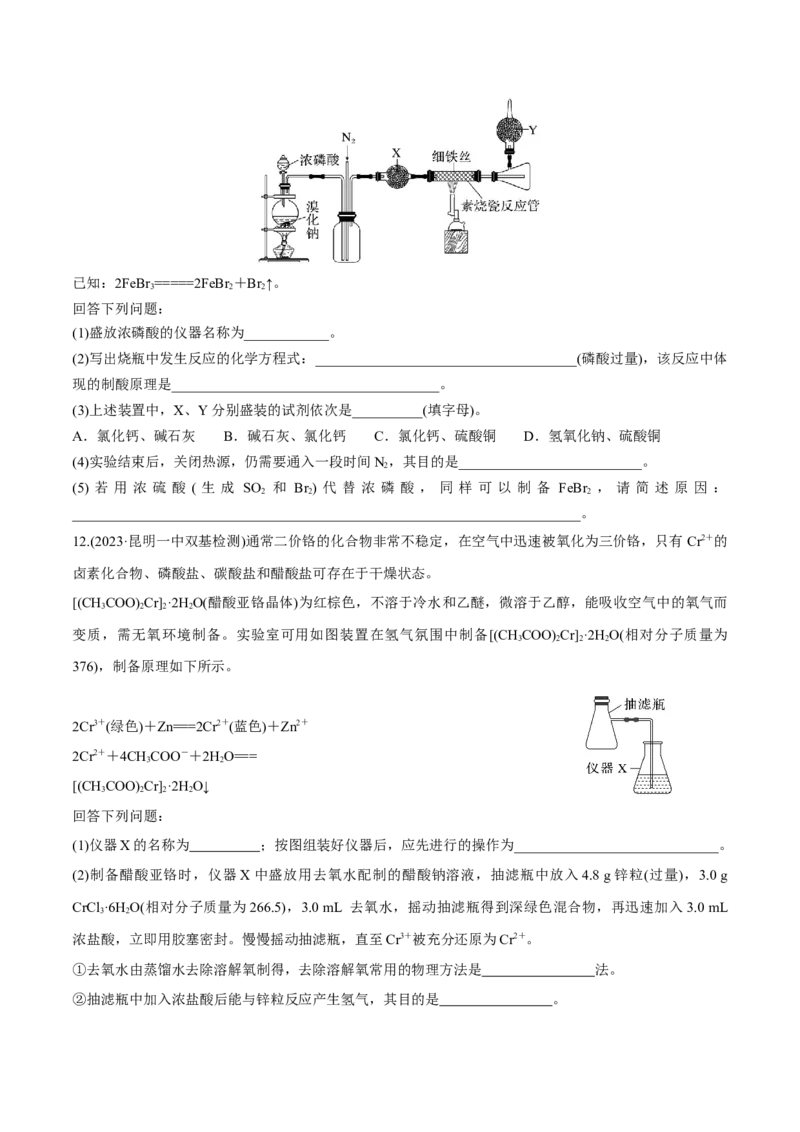
7.(2022·宁德一模)下列各组实验操作规范,且能达到实验目的的是( )
A B
配制1.0 mol·L-1的硫酸溶液 用乙醇萃取碘水中的碘单质
C D
检验乙醛中的醛基 制备乙酸乙酯
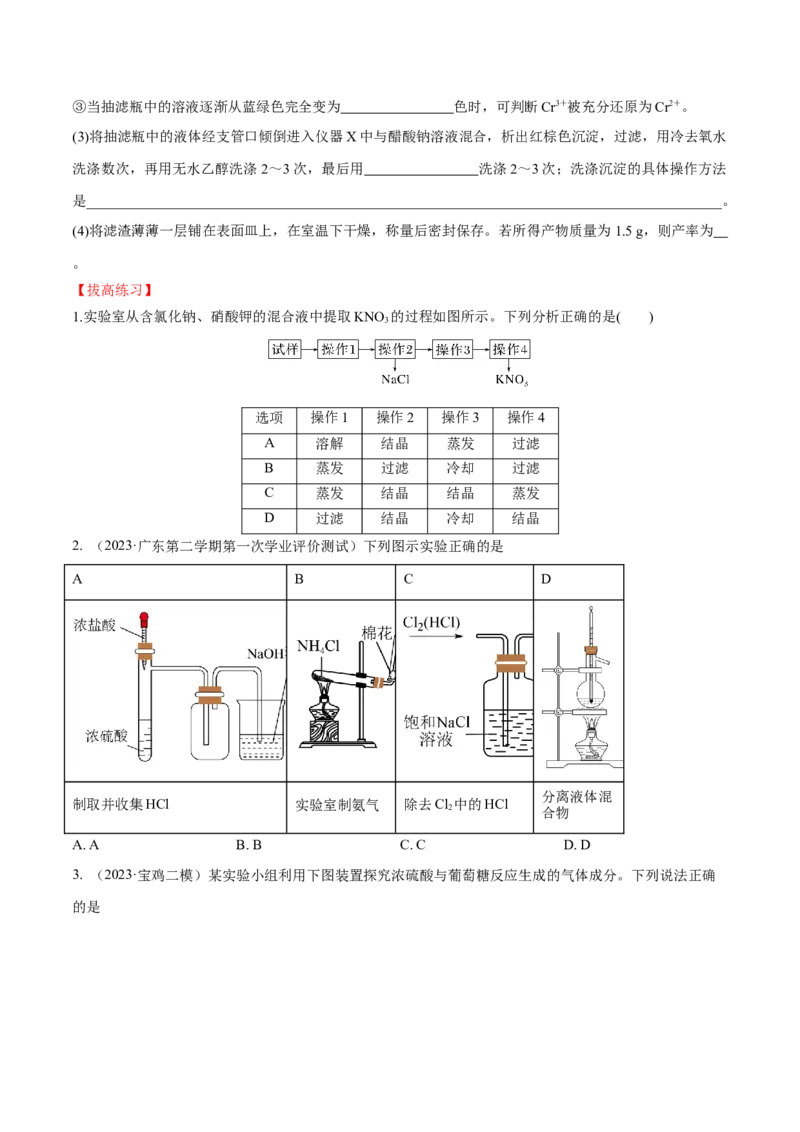
8.(2023·长沙雅礼中学月考)下列实验装置正确且能达到相应实验目的的是( )A.制备并收集少量NH B.制备并收集乙烯
3
C.制备并检验SO 气体 D.制备并收集NO
2 2
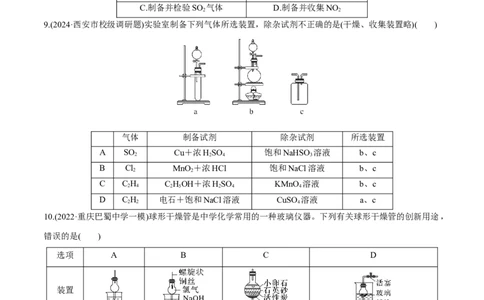
9.(2024·西安市校级调研题)实验室制备下列气体所选装置,除杂试剂不正确的是(干燥、收集装置略)( )
气体 制备试剂 除杂试剂 所选装置
A SO Cu+浓HSO 饱和NaHSO 溶液 b、c
2 2 4 3
B Cl MnO +浓HCl 饱和NaCl溶液 b、c
2 2
C C H C HOH+浓HSO KMnO 溶液 b、c
2 4 2 5 2 4 4
D C H 电石+饱和NaCl溶液 CuSO 溶液 a、c
2 2 4
10.(2022·重庆巴蜀中学一模)球形干燥管是中学化学常用的一种玻璃仪器。下列有关球形干燥管的创新用途,
错误的是( )
选项 A B C D
装置
用于尾气处 用于铜丝与Cl 反 简易的天 然水净化 用NaCO 固体与稀硫酸反应制
用途 2 2 3
理,防倒吸 应,防污染 过滤器 备CO 气体,可随制随停
2
11.(2023·呼和浩特市高三模拟)溴化亚铁(FeBr ,易潮解、800 ℃升华)是一种无机化工产品,常用作聚合
2
反应催化剂,也用于制药工业。某同学在实验室制备FeBr (Fe与HBr反应),装置(部分夹持仪器已省略)如
2
图所示:已知:2FeBr =====2FeBr +Br ↑。
3 2 2
回答下列问题:
(1)盛放浓磷酸的仪器名称为____________。
(2)写出烧瓶中发生反应的化学方程式:_____________________________________(磷酸过量),该反应中体
现的制酸原理是______________________________________。
(3)上述装置中,X、Y分别盛装的试剂依次是__________(填字母)。
A.氯化钙、碱石灰 B.碱石灰、氯化钙 C.氯化钙、硫酸铜 D.氢氧化钠、硫酸铜
(4)实验结束后,关闭热源,仍需要通入一段时间N,其目的是__________________________。
2
(5) 若 用 浓 硫 酸 ( 生 成 SO 和 Br ) 代 替 浓 磷 酸 , 同 样 可 以 制 备 FeBr , 请 简 述 原 因 :
2 2 2
________________________________________________________________________。
12.(2023·昆明一中双基检测)通常二价铬的化合物非常不稳定,在空气中迅速被氧化为三价铬,只有 Cr2+的
卤素化合物、磷酸盐、碳酸盐和醋酸盐可存在于干燥状态。
[(CH COO) Cr]·2H O(醋酸亚铬晶体)为红棕色,不溶于冷水和乙醚,微溶于乙醇,能吸收空气中的氧气而
3 2 2 2
变质,需无氧环境制备。实验室可用如图装置在氢气氛围中制备[(CH COO) Cr]·2H O(相对分子质量为
3 2 2 2
376),制备原理如下所示。
2Cr3+(绿色)+Zn===2Cr2+(蓝色)+Zn2+
2Cr2++4CHCOO-+2HO===
3 2
[(CH COO) Cr]·2H O↓
3 2 2 2
回答下列问题:
(1)仪器X的名称为 ;按图组装好仪器后,应先进行的操作为_____________________________。
(2)制备醋酸亚铬时,仪器X中盛放用去氧水配制的醋酸钠溶液,抽滤瓶中放入4.8 g锌粒(过量),3.0 g
CrCl ·6H O(相对分子质量为266.5),3.0 mL 去氧水,摇动抽滤瓶得到深绿色混合物,再迅速加入3.0 mL
3 2
浓盐酸,立即用胶塞密封。慢慢摇动抽滤瓶,直至Cr3+被充分还原为Cr2+。
①去氧水由蒸馏水去除溶解氧制得,去除溶解氧常用的物理方法是 法。
②抽滤瓶中加入浓盐酸后能与锌粒反应产生氢气,其目的是 。③当抽滤瓶中的溶液逐渐从蓝绿色完全变为 色时,可判断Cr3+被充分还原为Cr2+。
(3)将抽滤瓶中的液体经支管口倾倒进入仪器X中与醋酸钠溶液混合,析出红棕色沉淀,过滤,用冷去氧水
洗涤数次,再用无水乙醇洗涤2~3次,最后用 洗涤2~3次;洗涤沉淀的具体操作方法
是__________________________________________________________________________________________。
(4)将滤渣薄薄一层铺在表面皿上,在室温下干燥,称量后密封保存。若所得产物质量为1.5 g,则产率为
。
【拔高练习】
1.实验室从含氯化钠、硝酸钾的混合液中提取KNO 的过程如图所示。下列分析正确的是( )
3
选项 操作1 操作2 操作3 操作4
A 溶解 结晶 蒸发 过滤
B 蒸发 过滤 冷却 过滤
C 蒸发 结晶 结晶 蒸发
D 过滤 结晶 冷却 结晶
2. (2023·广东第二学期第一次学业评价测试)下列图示实验正确的是
A B C D
分离液体混
制取并收集HCl 实验室制氨气 除去Cl 中的HCl
2 合物
A. A B. B C. C D. D
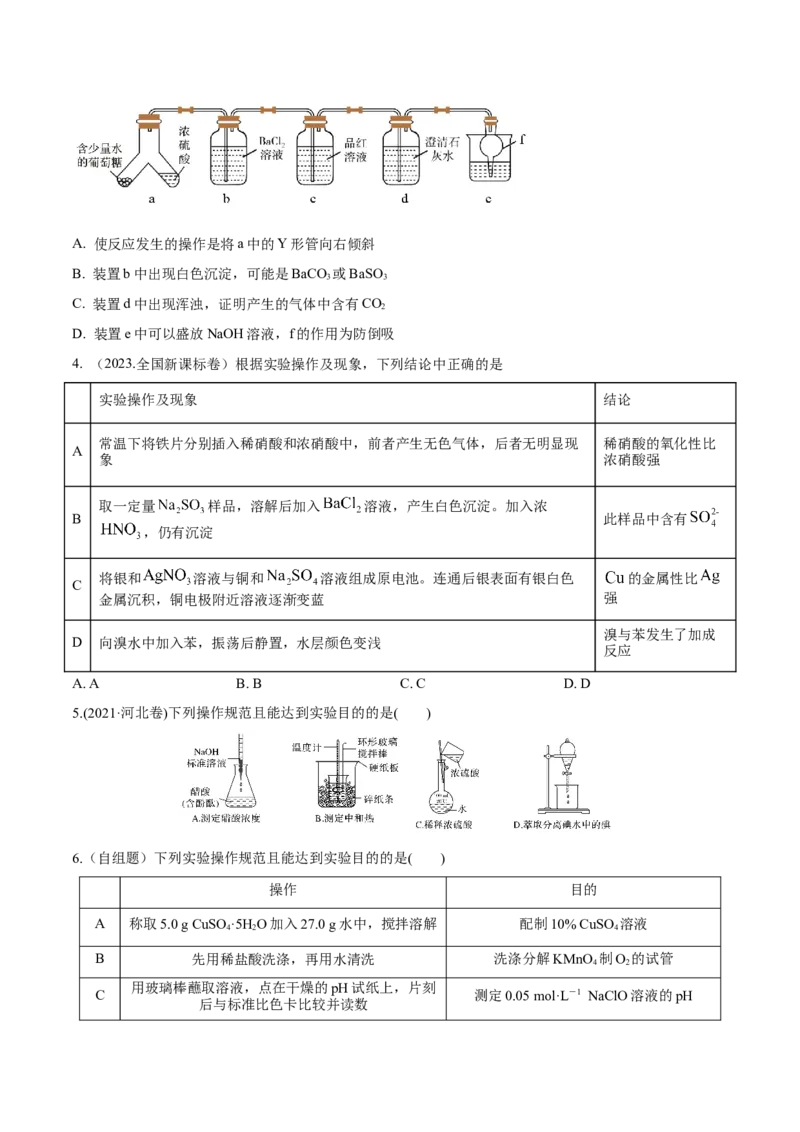
3. (2023·宝鸡二模)某实验小组利用下图装置探究浓硫酸与葡萄糖反应生成的气体成分。下列说法正确
的是A. 使反应发生的操作是将a中的Y形管向右倾斜
B. 装置b中出现白色沉淀,可能是BaCO 或BaSO
3 3
C. 装置d中出现浑浊,证明产生的气体中含有CO
2
D. 装置e中可以盛放NaOH溶液,f的作用为防倒吸
4. (2023.全国新课标卷)根据实验操作及现象,下列结论中正确的是
实验操作及现象 结论
常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显现 稀硝酸的氧化性比
A
象 浓硝酸强
取一定量 样品,溶解后加入 溶液,产生白色沉淀。加入浓
B 此样品中含有
,仍有沉淀
将银和 溶液与铜和 溶液组成原电池。连通后银表面有银白色 的金属性比
C
金属沉积,铜电极附近溶液逐渐变蓝 强
溴与苯发生了加成
D 向溴水中加入苯,振荡后静置,水层颜色变浅
反应
A. A B. B C. C D. D
5.(2021·河北卷)下列操作规范且能达到实验目的的是( )
6.(自组题)下列实验操作规范且能达到实验目的的是( )
操作 目的
A 称取5.0 g CuSO ·5H O加入27.0 g水中,搅拌溶解 配制10% CuSO 溶液
4 2 4
B 先用稀盐酸洗涤,再用水清洗 洗涤分解KMnO 制O 的试管
4 2
用玻璃棒蘸取溶液,点在干燥的pH试纸上,片刻
C 测定0.05 mol·L-1 NaClO溶液的pH
后与标准比色卡比较并读数将粗碘放入烧杯中,烧杯口放一盛满冷水的烧瓶,
D 提纯混有NH Cl的粗碘
隔石棉网对烧杯加热,然后收集烧瓶外壁的固体 4
7.(自组题)下列有关实验的方案设计、现象和结论都正确的是( )
选项 目的 方案设计 现象和结论
检验某溶液中是否 向该溶液中滴加几滴新制氯水,振荡,再加入 溶液变为红色,则该溶
A
含有Fe2+ 少量KSCN溶液 液中含有Fe2+
在试管中加入0.5 g淀粉和4 mL 2 mol·
判断淀粉是否完全 溶液显蓝色,则说明淀
B L-1 HSO 溶液,加热,冷却后,取少量水解
2 4
水解 粉未水解
后的溶液于试管中,加入碘酒
向两支试管中各加入2 mL 10% H O 溶液,再 滴加 CuCl 溶液的试管
2 2 2
探究Cu2+、Mn2+的
C 分别加入 2 滴 1 mol·L-1 CuCl 溶液、2 滴 1 出现气泡快,说明Cu2+
2
催化效果
mol·L-1 MnSO 溶液 的催化效果好
4
装有 FeS固体的试管产
向两支试管中加入等物质的量的CuS和FeS固
比较 CuS 和 FeS 的 生气泡,装有CuS固体
D 体,然后分别加入等体积 2 mol·L-1的HCl溶
K 大小 的试管无明显现象,则
sp
液
证明K (FeS)>K (CuS)
sp sp
8.(2022·全国乙卷)由实验操作和现象,可得出相应正确结论的是( )
实验操作 现象 结论
向NaBr溶液中滴加过量氯水,再加入
A 先变橙色,后变蓝色 氧化性:Cl>Br >I
淀粉-KI溶液 2 2 2
向蔗糖溶液中滴加稀硫酸,水浴加
B 无砖红色沉淀 蔗糖未发生水解
热,加入新制的Cu(OH) 悬浊液
2
石蜡油加强热,将产生的气体通入Br
C 2 溶液由红棕色变无色 气体中含有不饱和烃
的CCl 溶液
4
试管口湿润的蓝色石
D 加热试管中的聚氯乙烯薄膜碎片 氯乙烯加聚是可逆反应
蕊试纸变红
9.(2023·河南名校联盟质检)关于下列实验,实验现象或结论错误的是( )
实验 实验现象或结论可以准确测量碱式碳酸镁分解生成的水和二氧化碳的
A
量
B 若a、b中均有颜色变化,则X只能为单质气体
C 比较碳酸钠和碳酸氢钠的稳定性
D 该装置利用正压制备氢氧化亚铁
10..(2022·海淀区期末)下列实验方案能达到实验目的的是( )
选项 A B
目的 制备并收集乙酸乙酯 制备氢氧化铁胶体
实验
方案
选项 C D
目的 证明AgI的溶解度小于AgCl 探究化学反应速率的影响因素
实验
方案
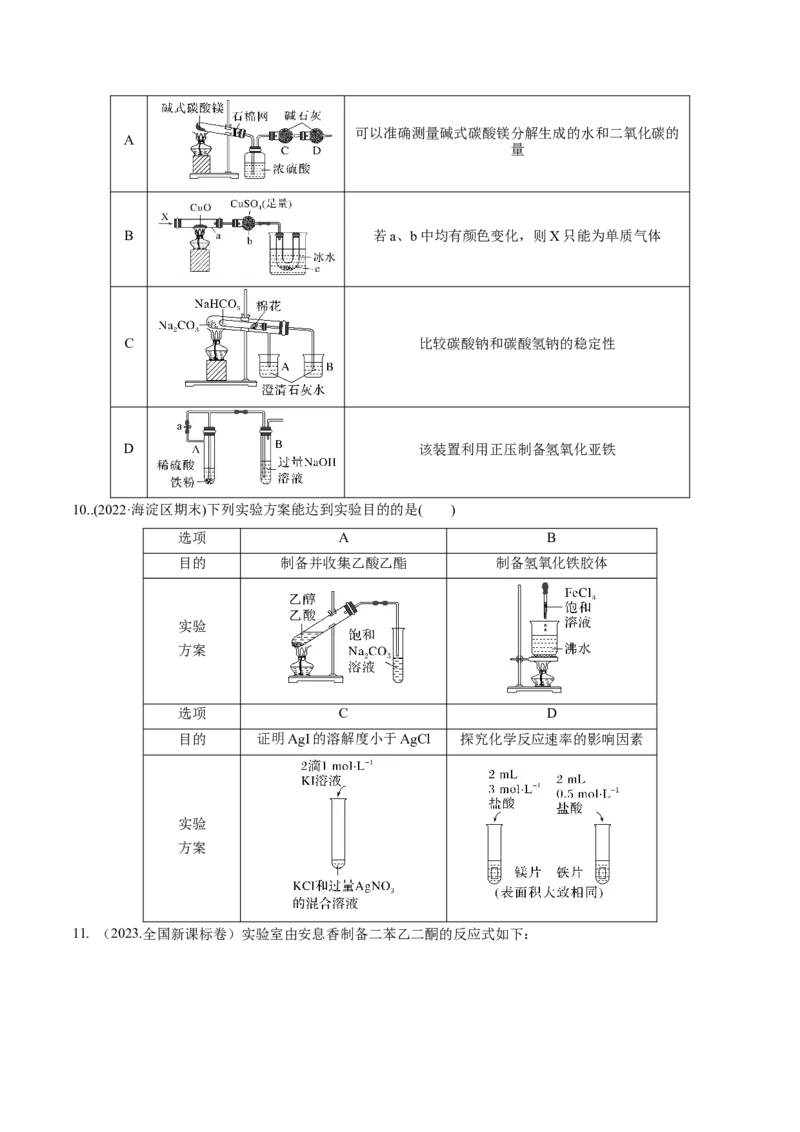
11. (2023.全国新课标卷)实验室由安息香制备二苯乙二酮的反应式如下:相关信息列表如下:
物质 性状 熔点/℃ 沸点/℃ 溶解性
安息香 白色固体 133 344 难溶于冷水,溶于热水、乙醇、乙酸
淡黄色固 不溶于水
二苯乙二酮 95 347
体 溶于乙醇、苯、乙酸
冰乙酸 无色液体 17 118 与水、乙醇互溶
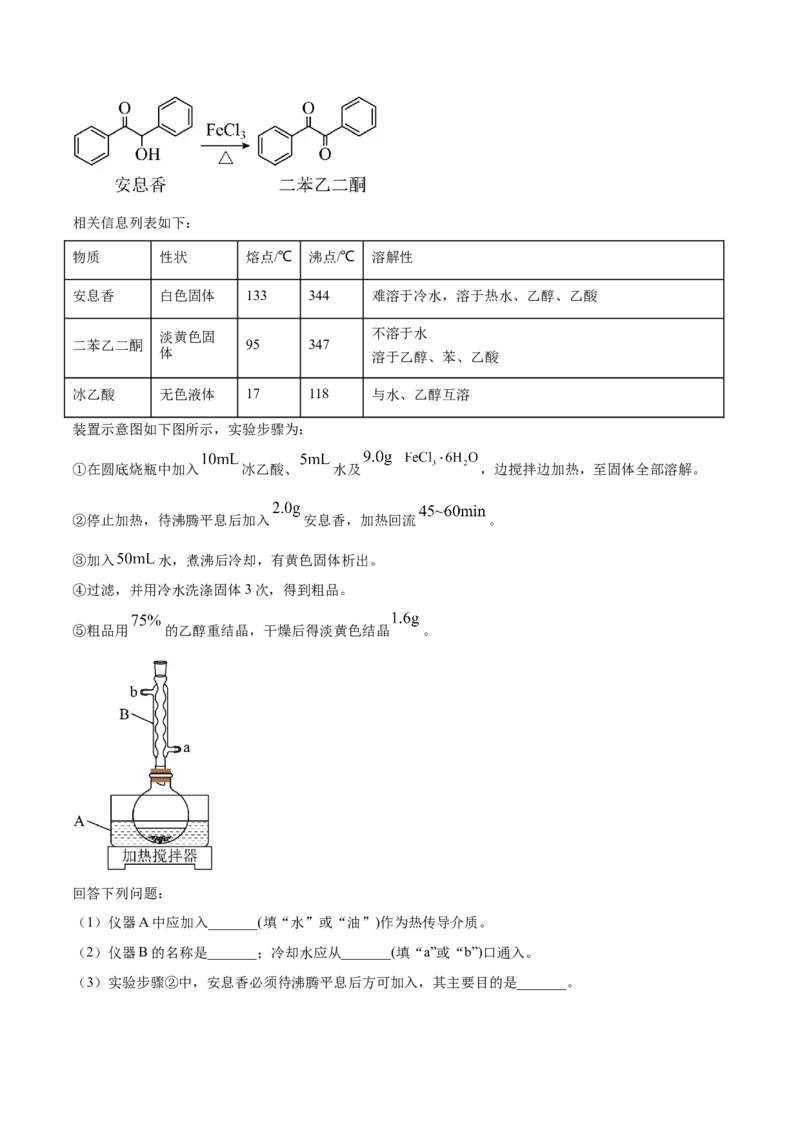
装置示意图如下图所示,实验步骤为:
①在圆底烧瓶中加入 冰乙酸、 水及 ,边搅拌边加热,至固体全部溶解。
②停止加热,待沸腾平息后加入 安息香,加热回流 。
③加入 水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用 的乙醇重结晶,干燥后得淡黄色结晶 。
回答下列问题:
(1)仪器A中应加入_______(填“水”或“油”)作为热传导介质。
(2)仪器B的名称是_______;冷却水应从_______(填“a”或“b”)口通入。
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是_______。(4)在本实验中, 为氧化剂且过量,其还原产物为_______;某同学尝试改进本实验:采用催化量
的 并通入空气制备二苯乙二酮。该方案是否可行_______?简述判断理由_______。
(5)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是_______。
(6)若粗品中混有少量未氧化的安息香,可用少量_______洗涤的方法除去(填标号)。若要得到更高纯度
的产品,可用重结晶的方法进一步提纯。
a.热水 b.乙酸 c.冷水 d.乙醇
(7)本实验的产率最接近于_______(填标号)。
a. b. c. d.
12.(2023·湖南卷)金属 对 有强吸附作用,被广泛用于硝基或羰基等不饱和基团的催化氢化反应,
将块状 转化成多孔型雷尼 后,其催化活性显著提高。
已知:①雷尼 暴露在空气中可以自燃,在制备和使用时,需用水或有机溶剂保持其表面“湿润”;
②邻硝基苯胺在极性有机溶剂中更有利于反应的进行。
某实验小组制备雷尼 并探究其催化氢化性能的实验如下:
步骤1:雷尼 的制备
步骤2:邻硝基苯胺的催化氢化反应
反应的原理和实验装置图如下(夹持装置和搅拌装置略)。装置Ⅰ用于储存 和监测反应过程。
回答下列问题:
(1)操作(a)中,反应的离子方程式是_______;(2)操作(d)中,判断雷尼 被水洗净的方法是_______;
(3)操作(e)中,下列溶剂中最有利于步骤2中氢化反应的是_______;
A. 丙酮 B. 四氯化碳 C. 乙醇 D. 正己烷
(4)向集气管中充入 时,三通阀的孔路位置如下图所示:发生氢化反应时,集气管向装置Ⅱ供气,此
时孔路位置需调节为_______;
(5)仪器M的名称是_______;
(6)反应前应向装置Ⅱ中通入 一段时间,目的是_______;
(7)如果将三颈瓶N中的导气管口插入液面以下,可能导致的后果是_______;
(8)判断氢化反应完全的现象是_______。