文档内容
第三十一、三十二讲 化学实验基础
【基础巩固】
1. 广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其他简单仪器组成各种功能的装置。
下列装置能用作防倒吸安全瓶的是( )
【答案】 B
【解析】 A项装置是排液量气装置,通过量筒中液体的体积可知广口瓶中气体的体积,A项不符合题意;
B项装置可作为安全瓶,用于防倒吸,原因是进气管较短,若发生倒吸,倒吸液会盛装在该安全瓶中,不
会再倒流到前一装置中,B项符合题意;C项装置是混气装置,进入广口瓶中的两气体可充分混合,C项
不符合题意;D项装置是洗气装置,D项不符合题意。
2.(2023.全国甲卷)实验室将粗盐提纯并配制0.1000mol/L的NaCl溶液。下列仪器中,本实验必须用到的
有
①天平 ②温度计 ③坩埚 ④分液漏斗 ⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A. ①②④⑥ B. ①④⑤⑥ C. ②③⑦⑧ D. ①⑤⑥⑧
【答案】 D
【解析】 实验室将粗盐提纯时,需要将其溶于一定量的水中,然后将其中的硫酸根离子、钙离子、镁离
子依次用稍过量的氯化钡溶液、碳酸钠溶液和氢氧化钠溶液除去,该过程中有过滤操作,需要用到烧杯、
漏斗和玻璃棒;将所得滤液加适量盐酸酸化后蒸发结晶得到较纯的食盐,该过程要用到蒸发皿和酒精灯;
用提纯后得到的精盐配制溶液的基本步骤有称量、溶解、转移、洗涤、定容、摇匀等操作,需要用到天平、
容量瓶、烧杯、玻璃棒、胶头滴管等。综上所述,本实验必须用到的有①天平、⑤容量瓶、⑥烧杯、⑧酒
精灯,因此本题选D。
3.(2023·宁夏高三模拟)下列实验操作和现象及实验结论均正确的是( )
选项 实验操作和现象 实验结论
向盛有氨水的烧杯中插入两个石墨电极,接通电源,电流
A 氨水是电解质
表指针发生较大偏转
向某溶液中滴加稀盐酸,产生的气体通入品红溶液,品红
B 该溶液中一定含有SO
溶液褪色
取久置的氯水于试管中,加入几滴紫色石蕊溶液,溶液变
C 氯水已经完全变质
为红色,且一段时间内不褪色
资料整理【淘宝店铺:向阳百分百】D 向蔗糖晶体中加入浓硫酸,轻轻搅拌,有海绵状的碳生成 浓硫酸具有吸水性
【答案】 C
【解析】 氨水是混合物,不属于电解质,A项错误;该溶液中也可能含有SO、HSO等,B项错误;石
2
蕊不褪色说明氯水中已不含有Cl 或HClO,已经完全变质,C项正确;结论应为浓硫酸具有脱水性,D项
2
错误。
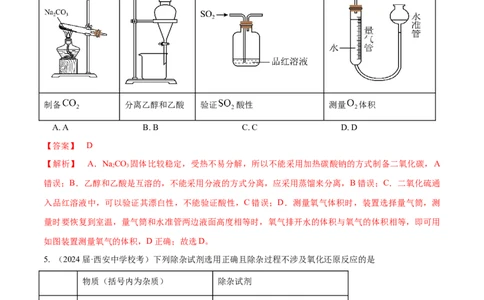
4. (2023.全国乙卷)下列装置可以用于相应实验的是
A B C D
制备 分离乙醇和乙酸 验证 酸性 测量 体积
A. A B. B C. C D. D
【答案】 D
【解析】 A.NaCO 固体比较稳定,受热不易分解,所以不能采用加热碳酸钠的方式制备二氧化碳,A
2 3
错误;B.乙醇和乙酸是互溶的,不能采用分液的方式分离,应采用蒸馏来分离,B错误;C.二氧化硫通
入品红溶液中,可以验证其漂白性,不能验证酸性,C错误;D.测量氧气体积时,装置选择量气筒,测
量时要恢复到室温,量气筒和水准管两边液面高度相等时,氧气排开水的体积与氧气的体积相等,即可用
如图装置测量氧气的体积,D正确;故选D。
5. (2024届·西安中学校考)下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是
物质(括号内为杂质) 除杂试剂
A FeCl 溶液(FeCl ) Fe粉
2 3
B NaCl溶液(MgCl ) NaOH溶液、稀HCl
2
C Cl(HCl) HO、浓HSO
2 2 2 4
D NO(NO ) HO、无水CaCl
2 2 2
A. A B. B C. C D. D
【答案】 B
【解析】 发生的反应中,存在元素的化合价变化,与氧化还原反应有关;反之,不存在元素的化合价变
资料整理【淘宝店铺:向阳百分百】化,则与氧化还原反应无关,以此解答该题。A.FeCl 与Fe反应生成FeCl ,2FeCl +Fe=3FeCl ,此过程中
3 2 3 2
Fe的化合价发生变化,涉及到了氧化还原反应,故A不符合题意;B.MgCl 与NaOH溶液发生复分解反应
2
MgCl +2NaOH=Mg(OH) +2NaCl,过量的NaOH溶液可用HCl除去HCl+NaOH=NaCl+H O ,此过程中
2 2 2
没有元素化合价发生变化,未涉及氧化还原反应,故B符合题意;C.部分氯气与HO 发生反应生成氯化氢
2
和次氯酸,应该用饱和食盐水除去HCl,除杂方法不正确,故C不符合题意;D.NO 与水反应生成硝酸和
2
NO。反应过程中氮元素化合价发生变化,涉及到了氧化还原反应,故D不符合题意;综上所述,应选B。
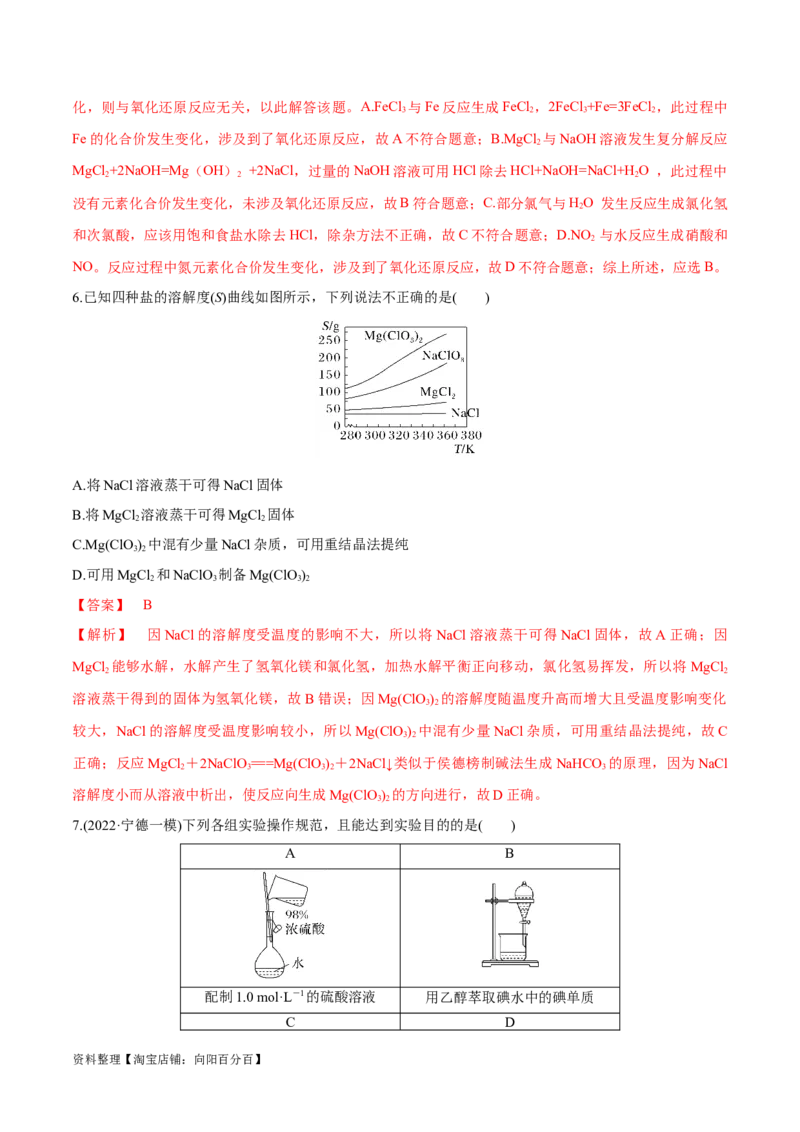
6.已知四种盐的溶解度(S)曲线如图所示,下列说法不正确的是( )
A.将NaCl溶液蒸干可得NaCl固体
B.将MgCl 溶液蒸干可得MgCl 固体
2 2
C.Mg(ClO ) 中混有少量NaCl杂质,可用重结晶法提纯
3 2
D.可用MgCl 和NaClO 制备Mg(ClO)
2 3 3 2
【答案】 B
【解析】 因NaCl的溶解度受温度的影响不大,所以将NaCl溶液蒸干可得NaCl固体,故A正确;因
MgCl 能够水解,水解产生了氢氧化镁和氯化氢,加热水解平衡正向移动,氯化氢易挥发,所以将 MgCl
2 2
溶液蒸干得到的固体为氢氧化镁,故B错误;因Mg(ClO) 的溶解度随温度升高而增大且受温度影响变化
3 2
较大,NaCl的溶解度受温度影响较小,所以Mg(ClO) 中混有少量NaCl杂质,可用重结晶法提纯,故C
3 2
正确;反应MgCl +2NaClO===Mg(ClO ) +2NaCl↓类似于侯德榜制碱法生成NaHCO 的原理,因为NaCl
2 3 3 2 3
溶解度小而从溶液中析出,使反应向生成Mg(ClO) 的方向进行,故D正确。
3 2
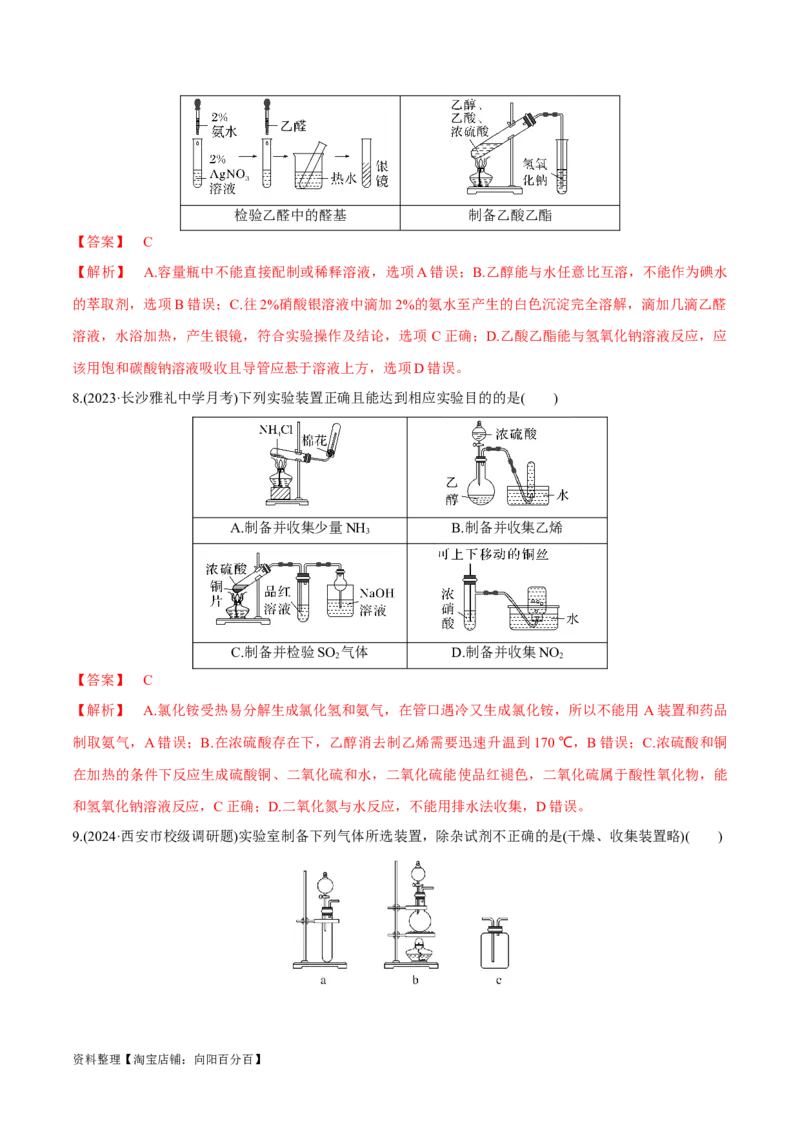
7.(2022·宁德一模)下列各组实验操作规范,且能达到实验目的的是( )
A B
配制1.0 mol·L-1的硫酸溶液 用乙醇萃取碘水中的碘单质
C D
资料整理【淘宝店铺:向阳百分百】检验乙醛中的醛基 制备乙酸乙酯
【答案】 C
【解析】 A.容量瓶中不能直接配制或稀释溶液,选项A错误;B.乙醇能与水任意比互溶,不能作为碘水
的萃取剂,选项B错误;C.往2%硝酸银溶液中滴加2%的氨水至产生的白色沉淀完全溶解,滴加几滴乙醛
溶液,水浴加热,产生银镜,符合实验操作及结论,选项 C正确;D.乙酸乙酯能与氢氧化钠溶液反应,应
该用饱和碳酸钠溶液吸收且导管应悬于溶液上方,选项D错误。
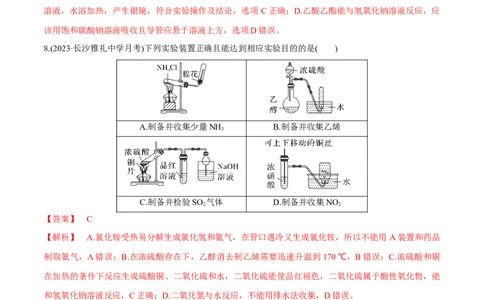
8.(2023·长沙雅礼中学月考)下列实验装置正确且能达到相应实验目的的是( )
A.制备并收集少量NH B.制备并收集乙烯
3
C.制备并检验SO 气体 D.制备并收集NO
2 2
【答案】 C
【解析】 A.氯化铵受热易分解生成氯化氢和氨气,在管口遇冷又生成氯化铵,所以不能用 A装置和药品
制取氨气,A错误;B.在浓硫酸存在下,乙醇消去制乙烯需要迅速升温到170 ℃,B错误;C.浓硫酸和铜
在加热的条件下反应生成硫酸铜、二氧化硫和水,二氧化硫能使品红褪色,二氧化硫属于酸性氧化物,能
和氢氧化钠溶液反应,C正确;D.二氧化氮与水反应,不能用排水法收集,D错误。
9.(2024·西安市校级调研题)实验室制备下列气体所选装置,除杂试剂不正确的是(干燥、收集装置略)( )
资料整理【淘宝店铺:向阳百分百】气体 制备试剂 除杂试剂 所选装置
A SO Cu+浓HSO 饱和NaHSO 溶液 b、c
2 2 4 3
B Cl MnO +浓HCl 饱和NaCl溶液 b、c
2 2
C C H C HOH+浓HSO KMnO 溶液 b、c
2 4 2 5 2 4 4
D C H 电石+饱和NaCl溶液 CuSO 溶液 a、c
2 2 4
【答案】 C
【解析】 A.铜与浓硫酸在加热条件下反应得到二氧化硫,生成的二氧化硫中可能会带出SO ,可用饱和
3
亚硫酸氢钠溶液除去SO 得到二氧化硫气体,装置可选b、c,故A正确;B.二氧化锰与浓盐酸加热生成氯
3
气,氯气中混有挥发出的HCl气体,可用饱和食盐水除去,装置可选b、c,故B正确;C.乙烯能被高锰酸
钾氧化,不能用高锰酸钾溶液除去乙烯中的杂质气体,故 C错误;D.电石和饱和食盐水常温下反应生成乙
炔,因电石中含有硫化物,同时会生成硫化氢,可用硫酸铜溶液将硫化氢沉淀除去,装置应选a、c,故D
正确。
10.(2022·重庆巴蜀中学一模)球形干燥管是中学化学常用的一种玻璃仪器。下列有关球形干燥管的创新用途,
错误的是( )
选项 A B C D
装置
用于尾气处 用于铜丝与Cl 反 简易的天 然水净化 用NaCO 固体与稀硫酸反应制
用途 2 2 3
理,防倒吸 应,防污染 过滤器 备CO 气体,可随制随停
2
【答案】 D
【解析】 A.球形结构可用于尾气处理,防倒吸,A正确;B.氯气与NaOH反应,球形结构可防止倒吸,
图中装置可用于铜丝与Cl 反应,防污染,B正确;C.活性炭具有吸附性,装置可作简易的天然水净化过滤
2
器,C正确;D.Na CO 固体易溶于水和稀硫酸,与稀硫酸接触后,关闭活塞不能使固液分离,则制备 CO
2 3 2
气体时不能随制随停,D错误。
11.(2023·呼和浩特市高三模拟)溴化亚铁(FeBr ,易潮解、800 ℃升华)是一种无机化工产品,常用作聚合
2
反应催化剂,也用于制药工业。某同学在实验室制备FeBr (Fe与HBr反应),装置(部分夹持仪器已省略)如
2
图所示:
资料整理【淘宝店铺:向阳百分百】已知:2FeBr =====2FeBr +Br ↑。
3 2 2
回答下列问题:
(1)盛放浓磷酸的仪器名称为____________。
(2)写出烧瓶中发生反应的化学方程式:_____________________________________(磷酸过量),该反应中体
现的制酸原理是______________________________________。
(3)上述装置中,X、Y分别盛装的试剂依次是__________(填字母)。
A.氯化钙、碱石灰 B.碱石灰、氯化钙 C.氯化钙、硫酸铜 D.氢氧化钠、硫酸铜
(4)实验结束后,关闭热源,仍需要通入一段时间N,其目的是__________________________。
2
(5) 若 用 浓 硫 酸 ( 生 成 SO 和 Br ) 代 替 浓 磷 酸 , 同 样 可 以 制 备 FeBr , 请 简 述 原 因 :
2 2 2
________________________________________________________________________。
【答案】 (1)分液漏斗 (2)NaBr+HPO (浓)=====NaH PO +HBr↑ 难挥发性酸制取挥发性酸(或高沸点
3 4 2 4
酸制取低沸点酸) (3)A (4)将装置中的HBr全部排到干燥管中,被试剂Y完全吸收,避免污染环境 (5)
浓硫酸代替浓磷酸,生成SO 和Br ,SO 不与铁反应,Br 和铁反应生成FeBr ,FeBr 在高温下又分解为
2 2 2 2 3 3
FeBr 和Br
2 2
12.(2023·昆明一中双基检测)通常二价铬的化合物非常不稳定,在空气中迅速被氧化为三价铬,只有 Cr2+的
卤素化合物、磷酸盐、碳酸盐和醋酸盐可存在于干燥状态。
[(CH COO) Cr]·2H O(醋酸亚铬晶体)为红棕色,不溶于冷水和乙醚,微溶于乙醇,能吸收空气中的氧气而
3 2 2 2
变质,需无氧环境制备。实验室可用如图装置在氢气氛围中制备[(CH COO) Cr]·2H O(相对分子质量为
3 2 2 2
376),制备原理如下所示。
2Cr3+(绿色)+Zn===2Cr2+(蓝色)+Zn2+
2Cr2++4CHCOO-+2HO===
3 2
[(CH COO) Cr]·2H O↓
3 2 2 2
回答下列问题:
(1)仪器X的名称为 ;按图组装好仪器后,应先进行的操作为_____________________________。
(2)制备醋酸亚铬时,仪器X中盛放用去氧水配制的醋酸钠溶液,抽滤瓶中放入4.8 g锌粒(过量),3.0 g
CrCl ·6H O(相对分子质量为266.5),3.0 mL 去氧水,摇动抽滤瓶得到深绿色混合物,再迅速加入3.0 mL
3 2
资料整理【淘宝店铺:向阳百分百】浓盐酸,立即用胶塞密封。慢慢摇动抽滤瓶,直至Cr3+被充分还原为Cr2+。
①去氧水由蒸馏水去除溶解氧制得,去除溶解氧常用的物理方法是 法。
②抽滤瓶中加入浓盐酸后能与锌粒反应产生氢气,其目的是 。
③当抽滤瓶中的溶液逐渐从蓝绿色完全变为 色时,可判断Cr3+被充分还原为Cr2+。
(3)将抽滤瓶中的液体经支管口倾倒进入仪器X中与醋酸钠溶液混合,析出红棕色沉淀,过滤,用冷去氧水
洗涤数次,再用无水乙醇洗涤2~3次,最后用 洗涤2~3次;洗涤沉淀的具体操作方法
是__________________________________________________________________________________________。
(4)将滤渣薄薄一层铺在表面皿上,在室温下干燥,称量后密封保存。若所得产物质量为1.5 g,则产率为
。
【答案】 (1)锥形瓶 检查装置的气密性
(2)①煮沸 ②排出装置中的空气,防止生成的Cr2+被氧化 ③蓝
(3)乙醚 向漏斗中加入试剂,直至浸没过沉淀,等待试剂自然流下 (4)71.4%
【解析】 (1)仪器X是锥形瓶;组装好装置后,紧接着要检查装置的气密性;(2)①气体的溶解度随温度
的升高而降低,一般用煮沸的方法除去水中的溶解氧;②为了防止 Cr2+被氧化,需在无氧环境下进行制备
实验,氢气的作用是排出装置中的空气;③根据题目信息,Cr2+为蓝色,当抽滤瓶中的溶液完全变为蓝色
时,可判断Cr3+被充分还原为Cr2+;(3)醋酸亚铬晶体不溶于乙醚,所以最后用乙醚洗涤2~3次,洗涤沉
淀的操作方法是向漏斗中加入试剂,直至浸没过沉淀,等待试剂自然流下;(4)根据Cr原子守恒,列出关
系式:
得出[(CH COO) Cr]·2H O的理论产量为2.1 g,产率=×100%=×100%≈71.4%。
3 2 2 2
【拔高练习】
1.实验室从含氯化钠、硝酸钾的混合液中提取KNO 的过程如图所示。下列分析正确的是( )
3
选项 操作1 操作2 操作3 操作4
A 溶解 结晶 蒸发 过滤
B 蒸发 过滤 冷却 过滤
C 蒸发 结晶 结晶 蒸发
D 过滤 结晶 冷却 结晶
资料整理【淘宝店铺:向阳百分百】【答案】 B
【解析】 氯化钠的溶解度受温度的影响小,蒸发浓缩可析出晶体,硝酸钾的溶解度受温度的影响大,降
低温度可析出大量晶体,所以蒸发结晶可得到氯化钠,冷却结晶可得到硝酸钾,故B正确。
2. (2023·广东第二学期第一次学业评价测试)下列图示实验正确的是
A B C D
分离液体混
制取并收集HCl 实验室制氨气 除去Cl 中的HCl
2 合物
A. A B. B C. C D. D
【答案】 C
【解析】 A.A装置由于HCl极易溶于水,故需防倒吸装置,即烧杯中的导管需接一倒扣的漏斗,A错
误;B.加热NH Cl得不到氨气,需加热NH Cl和Ca(OH) 的混合物,B错误;C.除去氯气中的氯化氢用
4 4 2
饱和食盐水,洗气装置长进短出,C正确;D.采用蒸馏法分离互溶的沸点相差较大的液体时,蒸馏烧瓶
中温度计水银球的位置在蒸馏烧瓶支管口,D错误;故答案为:C。
3. (2023·宝鸡二模)某实验小组利用下图装置探究浓硫酸与葡萄糖反应生成的气体成分。下列说法正确
的是
A. 使反应发生的操作是将a中的Y形管向右倾斜
B. 装置b中出现白色沉淀,可能是BaCO 或BaSO
3 3
C. 装置d中出现浑浊,证明产生的气体中含有CO
2
D. 装置e中可以盛放NaOH溶液,f的作用为防倒吸
【答案】 D
资料整理【淘宝店铺:向阳百分百】【解析】 浓硫酸具有脱水性,使葡萄糖脱水生成碳,碳和浓硫酸反应生成 CO 和SO 。A.葡萄糖为固
2 2
体,浓硫酸和葡萄糖混合,将Y形管向左倾斜,浓硫酸倒入含少量水的葡萄糖中,A项错误;B.CO 和
2
SO 和氯化钡溶液均不反应,若装置b中出现白色沉淀,是SO 和O 和氯化钡反应生成的BaSO ,B项错
2 2 2 4
误;C.c中的品红溶液不能完全吸收SO ,SO 、CO 均能使澄清石灰水变浑浊,C项错误;D.污染性尾
2 2 2
气为SO ,可以用NaOH溶液吸收,球形干燥管的作用为防倒吸,D项正确;故选D。
2
4. (2023.全国新课标卷)根据实验操作及现象,下列结论中正确的是
实验操作及现象 结论
常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显现 稀硝酸的氧化性比
A
象 浓硝酸强
取一定量 样品,溶解后加入 溶液,产生白色沉淀。加入浓
B 此样品中含有
,仍有沉淀
将银和 溶液与铜和 溶液组成原电池。连通后银表面有银白色 的金属性比
C
金属沉积,铜电极附近溶液逐渐变蓝 强
溴与苯发生了加成
D 向溴水中加入苯,振荡后静置,水层颜色变浅
反应
A. A B. B C. C D. D
【答案】 C
【解析】 A.常温下,铁片与浓硝酸会发生钝化,导致现象不明显,但稀硝酸与铁不发生钝化,会产生
气泡,所以不能通过该实验现象比较浓硝酸和稀硝酸的氧化性强弱,A错误;B.浓硝酸会氧化亚硫酸根
生成硫酸根,仍然产生白色沉淀,所以不能通过该实验现象判断样品中含有硫酸根,B错误;C.铜比银
活泼,在形成原电池过程中,做负极,发生氧化反应,生成了铜离子,导致溶液变为蓝色,所以该实验可
以比较铜和银的金属性强弱,C正确;D.向溴水中加入苯,苯可将溴萃取到上层,使下层水层颜色变浅,
不是溴与苯发生了加成反应,D错误;故选C。
5.(2021·河北卷)下列操作规范且能达到实验目的的是( )
【答案】 A
【解析】 用NaOH标准溶液测定醋酸浓度时,NaOH标准溶液放于碱式滴定管中,醋酸放于锥形瓶中,
资料整理【淘宝店铺:向阳百分百】由于二者反应生成的CHCOONa溶液显碱性,故用酚酞做指示剂,A符合题意;中和热测定时大、小烧杯
3
口应相平,填充满碎纸片并加盖以减小热量损失,B不符合题意;不能在容量瓶中稀释浓硫酸,C不符合
题意;分液时,分液漏斗下管口应紧靠烧杯内壁,D不符合题意。
6.(自组题)下列实验操作规范且能达到实验目的的是( )
操作 目的
A 称取5.0 g CuSO ·5H O加入27.0 g水中,搅拌溶解 配制10% CuSO 溶液
4 2 4
B 先用稀盐酸洗涤,再用水清洗 洗涤分解KMnO 制O 的试管
4 2
用玻璃棒蘸取溶液,点在干燥的pH试纸上,片刻
C 测定0.05 mol·L-1 NaClO溶液的pH
后与标准比色卡比较并读数
将粗碘放入烧杯中,烧杯口放一盛满冷水的烧瓶,
D 提纯混有NH Cl的粗碘
隔石棉网对烧杯加热,然后收集烧瓶外壁的固体 4
【答案】 A
【解析】 A.5.0 g CuSO ·5H O中含CuSO 3.2 g,加入27.0 g水中,搅拌溶解得到32 g CuSO 溶液,溶
4 2 4 4
质的质量分数为:×100%=10%,故A正确;B.洗涤分解KMnO 制O 的试管,试管内壁附着MnO 需要用
4 2 2
浓盐酸并加热洗涤,再用水洗涤,故B错误;C.测定0.05 mol·L-1 NaClO溶液的pH,由于NaClO具有强
氧化性,能使试纸褪色,故不能用pH试纸测其pH,C错;D.提纯混有NH Cl的粗碘,因NH Cl受热分解
4 4
生成氨气和氯化氢,冷却后又结合成NH Cl,故不能用加热的方法分离,D错误。
4
7.(自组题)下列有关实验的方案设计、现象和结论都正确的是( )
选项 目的 方案设计 现象和结论
检验某溶液中是否 向该溶液中滴加几滴新制氯水,振荡,再加入 溶液变为红色,则该溶
A
含有Fe2+ 少量KSCN溶液 液中含有Fe2+
在试管中加入0.5 g淀粉和4 mL 2 mol·
判断淀粉是否完全 溶液显蓝色,则说明淀
B L-1 HSO 溶液,加热,冷却后,取少量水解
2 4
水解 粉未水解
后的溶液于试管中,加入碘酒
向两支试管中各加入2 mL 10% H O 溶液,再 滴加 CuCl 溶液的试管
2 2 2
探究Cu2+、Mn2+的
C 分别加入 2 滴 1 mol·L-1 CuCl 溶液、2 滴 1 出现气泡快,说明Cu2+
2
催化效果
mol·L-1 MnSO 溶液 的催化效果好
4
装有 FeS固体的试管产
向两支试管中加入等物质的量的CuS和FeS固
比较 CuS 和 FeS 的 生气泡,装有CuS固体
D 体,然后分别加入等体积 2 mol·L-1的HCl溶
K 大小 的试管无明显现象,则
sp
液
证明K (FeS)>K (CuS)
sp sp
【答案】 D
资料整理【淘宝店铺:向阳百分百】【解析】 Fe2+能被新制氯水氧化成Fe3+,应先加KSCN溶液无现象,后加新制氯水溶液变红色,证明溶
液中含有Fe2+,故A错误;溶液显蓝色,说明淀粉未完全水解或未水解,故B错误;CuCl 溶液和MnSO
2 4
溶液的阴离子不同,不能排除阴离子的干扰,故C错误。
8.(2022·全国乙卷)由实验操作和现象,可得出相应正确结论的是( )
实验操作 现象 结论
向NaBr溶液中滴加过量氯水,再加入
A 先变橙色,后变蓝色 氧化性:Cl>Br >I
淀粉-KI溶液 2 2 2
向蔗糖溶液中滴加稀硫酸,水浴加
B 无砖红色沉淀 蔗糖未发生水解
热,加入新制的Cu(OH) 悬浊液
2
石蜡油加强热,将产生的气体通入Br
C 2 溶液由红棕色变无色 气体中含有不饱和烃
的CCl 溶液
4
试管口湿润的蓝色石
D 加热试管中的聚氯乙烯薄膜碎片 氯乙烯加聚是可逆反应
蕊试纸变红
【答案】 C
【解析】 向NaBr溶液中滴加过量氯水,过量的氯水可以将碘离子氧化为碘单质,无法证明溴单质的氧
化性强于碘单质,A错误;向蔗糖溶液中滴加稀硫酸,水浴加热后,应先加入氢氧化钠溶液使体系呈碱性,
再加新制氢氧化铜悬浊液检验,若不加氢氧化钠,未反应的稀硫酸会和新制的氢氧化铜反应,则不会产生
砖红色沉淀,不能说明蔗糖是否发生水解,B错误;石蜡油加强热,产生的气体能使溴的四氯化碳溶液褪
色,说明气体中含有不饱和烃,C正确;聚氯乙烯加强热会发生焦化、分解反应,产生能使湿润的蓝色石
蕊试纸变红的气体,说明产生了氯化氢,与氯乙烯加聚反应条件不同,不能说明氯乙烯加聚是可逆反应,
D错误。
9.(2023·河南名校联盟质检)关于下列实验,实验现象或结论错误的是( )
实验 实验现象或结论
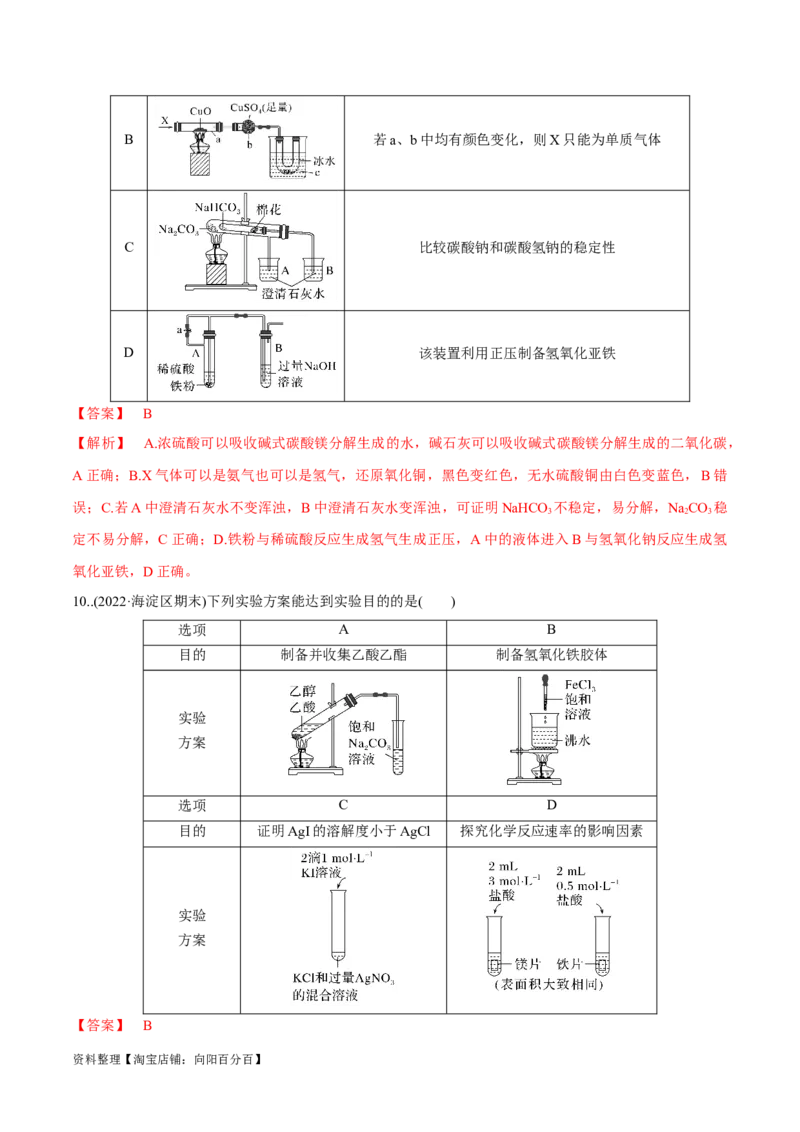
可以准确测量碱式碳酸镁分解生成的水和二氧化碳的
A
量
资料整理【淘宝店铺:向阳百分百】B 若a、b中均有颜色变化,则X只能为单质气体
C 比较碳酸钠和碳酸氢钠的稳定性
D 该装置利用正压制备氢氧化亚铁
【答案】 B
【解析】 A.浓硫酸可以吸收碱式碳酸镁分解生成的水,碱石灰可以吸收碱式碳酸镁分解生成的二氧化碳,
A正确;B.X气体可以是氨气也可以是氢气,还原氧化铜,黑色变红色,无水硫酸铜由白色变蓝色,B错
误;C.若A中澄清石灰水不变浑浊,B中澄清石灰水变浑浊,可证明NaHCO 不稳定,易分解,NaCO 稳
3 2 3
定不易分解,C正确;D.铁粉与稀硫酸反应生成氢气生成正压,A中的液体进入B与氢氧化钠反应生成氢
氧化亚铁,D正确。
10..(2022·海淀区期末)下列实验方案能达到实验目的的是( )
选项 A B
目的 制备并收集乙酸乙酯 制备氢氧化铁胶体
实验
方案
选项 C D
目的 证明AgI的溶解度小于AgCl 探究化学反应速率的影响因素
实验
方案
【答案】 B
资料整理【淘宝店铺:向阳百分百】【解析】 乙酸和乙醇在浓硫酸催化下才能发生酯化反应,A项错误;向沸水中滴入饱和氯化铁溶液,继
续煮沸至溶液呈红褐色,停止加热,得到氢氧化铁胶体,B项正确;KCl和过量AgNO 溶液混合,Ag+过
3
量,滴入KI溶液,Ag+与I-反应产生黄色沉淀,不能说明AgCl转化为AgI,因此不能证明AgI的溶解度
小于AgCl,C项错误;金属不同、盐酸浓度不同,同时存在两个变量,不能判断影响反应速率的因素,D
项错误。
11. (2023.全国新课标卷)实验室由安息香制备二苯乙二酮的反应式如下:
相关信息列表如下:
物质 性状 熔点/℃ 沸点/℃ 溶解性
安息香 白色固体 133 344 难溶于冷水,溶于热水、乙醇、乙酸
淡黄色固 不溶于水
二苯乙二酮 95 347
体 溶于乙醇、苯、乙酸
冰乙酸 无色液体 17 118 与水、乙醇互溶
装置示意图如下图所示,实验步骤为:
①在圆底烧瓶中加入 冰乙酸、 水及 ,边搅拌边加热,至固体全部溶解。
②停止加热,待沸腾平息后加入 安息香,加热回流 。
③加入 水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用 的乙醇重结晶,干燥后得淡黄色结晶 。
资料整理【淘宝店铺:向阳百分百】回答下列问题:
(1)仪器A中应加入_______(填“水”或“油”)作为热传导介质。
(2)仪器B的名称是_______;冷却水应从_______(填“a”或“b”)口通入。
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是_______。
(4)在本实验中, 为氧化剂且过量,其还原产物为_______;某同学尝试改进本实验:采用催化量
的 并通入空气制备二苯乙二酮。该方案是否可行_______?简述判断理由_______。
(5)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是_______。
(6)若粗品中混有少量未氧化的安息香,可用少量_______洗涤的方法除去(填标号)。若要得到更高纯度
的产品,可用重结晶的方法进一步提纯。
a.热水 b.乙酸 c.冷水 d.乙醇
(7)本实验的产率最接近于_______(填标号)。
a. b. c. d.
【答案】(1)油 (2)①. 球形冷凝管 ②. a (3)防暴沸
(4)①. FeCl ②. 可行 ③. 空气可以将还原产物FeCl 又氧化为FeCl ,FeCl 可循环参与反应
2 2 3 3
(5)抑制氯化铁水解 (6)a (7)b
【解析】【分析】在圆底烧瓶中加入10 mL冰乙酸,5mL水,及9.0gFeCl · 6H O,加热至固体全部溶解,
3 2
停止加热,待沸腾平息后加入2.0g安息香,加热回流45-60min,反应结束后加入50mL水,煮沸后冷却,
析出黄色固体,即为二苯乙二酮,过滤,用冷水洗涤固体三次,得到粗品,再用 75%乙醇重结晶,干燥后
得到产品1.6g,据此解答。
【小问1详解】该实验需要加热使冰乙酸沸腾,冰乙酸的沸点超过了100℃,应选择油浴加热,所以仪器
A中应加入油作为热传导介质,故答案为:油;
资料整理【淘宝店铺:向阳百分百】【小问2详解】根据仪器的结构特征可知,B为球形冷凝管,为了充分冷却,冷却水应从a口进,b口出,
故答案为:球形冷凝管;a;
【小问3详解】步骤②中,若沸腾时加入安息香,会暴沸,所以需要沸腾平息后加入,故答案为:防暴沸;
【小问4详解】FeCl 为氧化剂,则铁的化合价降低,还原产物为FeCl ,若采用催化量的FeCl 并通入空气
3 2 3
制备二苯乙二酮,空气可以将还原产物FeCl 又氧化为FeCl ,FeCl 可循环参与反应,故答案为:FeCl ;
2 3 3 2
可行;空气可以将还原产物FeCl 又氧化为FeCl ,FeCl 可循环参与反应;
2 3 3
【小问5详解】氯化铁易水解,所以步骤①~③中,乙酸除做溶剂外,另一主要作用是抑制氯化铁水解;
【小问6详解】根据安息香和二苯乙二酮的溶解特征,安息香溶于热水,二苯乙二酮不溶于水,所以可以
采用热水洗涤粗品除去安息香,故答案为:a;
【小问7详解】由于安息香(C H O)与二苯乙二酮(C H O)的相对分子质量相差不大,因此二苯乙
14 12 2 14 10 2
二酮的理论产量与安息香近似相等约为2.0g。则产率约为 =80%,故答案为:b。
12.(2023·湖南卷)金属 对 有强吸附作用,被广泛用于硝基或羰基等不饱和基团的催化氢化反应,
将块状 转化成多孔型雷尼 后,其催化活性显著提高。
已知:①雷尼 暴露在空气中可以自燃,在制备和使用时,需用水或有机溶剂保持其表面“湿润”;
②邻硝基苯胺在极性有机溶剂中更有利于反应的进行。
某实验小组制备雷尼 并探究其催化氢化性能的实验如下:
步骤1:雷尼 的制备
步骤2:邻硝基苯胺的催化氢化反应
反应的原理和实验装置图如下(夹持装置和搅拌装置略)。装置Ⅰ用于储存 和监测反应过程。
资料整理【淘宝店铺:向阳百分百】回答下列问题:
(1)操作(a)中,反应的离子方程式是_______;
(2)操作(d)中,判断雷尼 被水洗净的方法是_______;
(3)操作(e)中,下列溶剂中最有利于步骤2中氢化反应的是_______;
A. 丙酮 B. 四氯化碳 C. 乙醇 D. 正己烷
(4)向集气管中充入 时,三通阀的孔路位置如下图所示:发生氢化反应时,集气管向装置Ⅱ供气,此
时孔路位置需调节为_______;
(5)仪器M的名称是_______;
(6)反应前应向装置Ⅱ中通入 一段时间,目的是_______;
(7)如果将三颈瓶N中的导气管口插入液面以下,可能导致的后果是_______;
(8)判断氢化反应完全的现象是_______。
【答案】(1)2Al+2OH-+2H O=2AlO +3H ↑
2 2
(2)取最后一次洗涤液于试管中,滴加几滴酚酞,如果溶液不变粉红色,则证明洗涤干净,否则没有洗
涤干净 (3)C (4)B (5)恒压滴液漏斗
(6)排除装置中的空气,防止雷尼 自燃 (7)管道中气流不稳,不利于监测反应过程
(8)集气管中液面不再改变
【解析】本题一道工业流程兼实验的综合题,首先用氢氧化钠溶液溶解镍铝合金中的铝,过滤后先后用碱
和水来洗涤固体镍,随后加入有机溶剂制得雷尼镍悬浮液,用于步骤2中邻硝基苯胺的催化氢化,以此解
题。
【小问1详解】铝可以和氢氧化钠反应生成偏铝酸钠和氢气,离子方程式为:2Al+2OH-+2H O=2AlO
2
+3H ↑;
2
【小问2详解】由于水洗之前是用碱洗,此时溶液显碱性,故可以用酸碱指示剂来判断是否洗净,具体方
法为,取最后一次洗涤液于试管中,滴加几滴酚酞,如果溶液不变粉红色,则证明洗涤干净,否则没有洗
资料整理【淘宝店铺:向阳百分百】涤干净;
【小问3详解】根据题给信息可知,邻硝基苯胺在极性有机溶剂中更有利于反应的进行,在丙酮,四氯化
碳,乙醇,正己烷中极性较强的为乙醇,故选C;
【小问4详解】向集气管中充入 时,氢气从左侧进入,向下进入集气管,则当由集气管向装置Ⅱ供气,
此时孔路位置需调节为气体由下方的集气管,向右进入装置Ⅱ,应该选B,而装置C方式中左侧会漏气,
不符合题意,故选B;
【小问5详解】由图可知,仪器M的名称是恒压滴液漏斗;
【小问6详解】根据题给信息可知,雷尼 暴露在空气中可以自燃,故反应前向装置Ⅱ中通入 一段时
间,目的是排除装置中的空气,防止雷尼 自燃;
【小问7详解】如果将三颈瓶N中的导气管口插入液面以下,则会在三颈瓶中产生气泡,从而导致管道中
气流不稳,不利于监测反应过程;
【小问8详解】反应完成后,氢气不再被消耗,则集气管中液面不再改变。
资料整理【淘宝店铺:向阳百分百】