文档内容
专题 15 晶体结构与性质
第 43 练 分子晶体与共价晶体
1.下列晶体中由原子直接构成的分子晶体是( )
A.氯化钠 B.氦气 C.金刚石 D.金属
2.下列化合物固态时属于分子晶体的是( )
A.HCl B.SiO C.Hg D.NH Cl
2 4
3.当SO 晶体熔化时,下述各项中发生变化的是( )
3
A.化学键 B.硫与氧的原子个数之比 C.分子构型 D.分子间作用力
4.下列物质中,属于共价晶体的化合物是( )
A.水晶 B.晶体硅 C.金刚石 D.干冰
5.共价晶体一定具有的性质是( )
A.熔点高 B.易导热 C.能导电 D.良好的延展性
6.在常温常压下呈气态的化合物,降温使其固化得到的晶体属于( )
A.分子晶体 B.共价晶体
C.离子晶体 D.何种晶体无法判断
7.干冰熔点很低是由于( )
A.CO 是非极性分子 B.C==O键的键能很小
2
C.CO 化学性质不活泼 D.CO 分子间的作用力较弱
2 2
8.下列关于分子晶体的说法不正确的是( )
A.分子晶体中含有分子 B.固态或熔融态时均能导电
C.分子间以分子间作用力相结合 D.熔、沸点一般比较低
9.下列有关分子晶体的叙述正确的是( )
A.分子内均存在共价键
B.非金属氧化物呈固态时,一定属于分子晶体
C.分子晶体中一定存在氢键
D.分子晶体熔化时一定破坏了范德华力
10.分子晶体具有某些特征的本质原因是( )
A.组成晶体的基本微粒是分子
B.熔融时不导电
C.基本构成微粒间以分子间作用力相结合D.熔点一般比较低
11.下列说法正确的是( )
A.冰融化时,分子中H—O键发生断裂
B.分子晶体中,分子间作用力越大,通常熔点越高
C.分子晶体中,共价键键能越大,分子的熔、沸点越高
D.分子晶体中,分子间作用力越大,分子越稳定
12.下列各组物质,均属于化合物且均形成分子晶体的是( )
A.PH 、H、C H B.PCl 、CO、HNO
3 2 10 8 3 2 3
C.SO 、SiO、PO D.CCl 、NaCl、HO
2 2 2 5 4 2
13.下列有关分子晶体熔点的高低叙述中,正确的是( )
A.Cl>I B.SiCl >CCl
2 2 4 4
C.PH >NH D.C(CH)>CHCHCHCHCH
3 3 3 4 3 2 2 2 3
14.下列有关共价晶体的叙述,错误的是( )
A.共价晶体中,原子不遵循紧密堆积原则 B.共价晶体中不存在独立的分子
C.共价晶体的熔点和硬度较高 D.共价晶体熔化时不破坏化学键
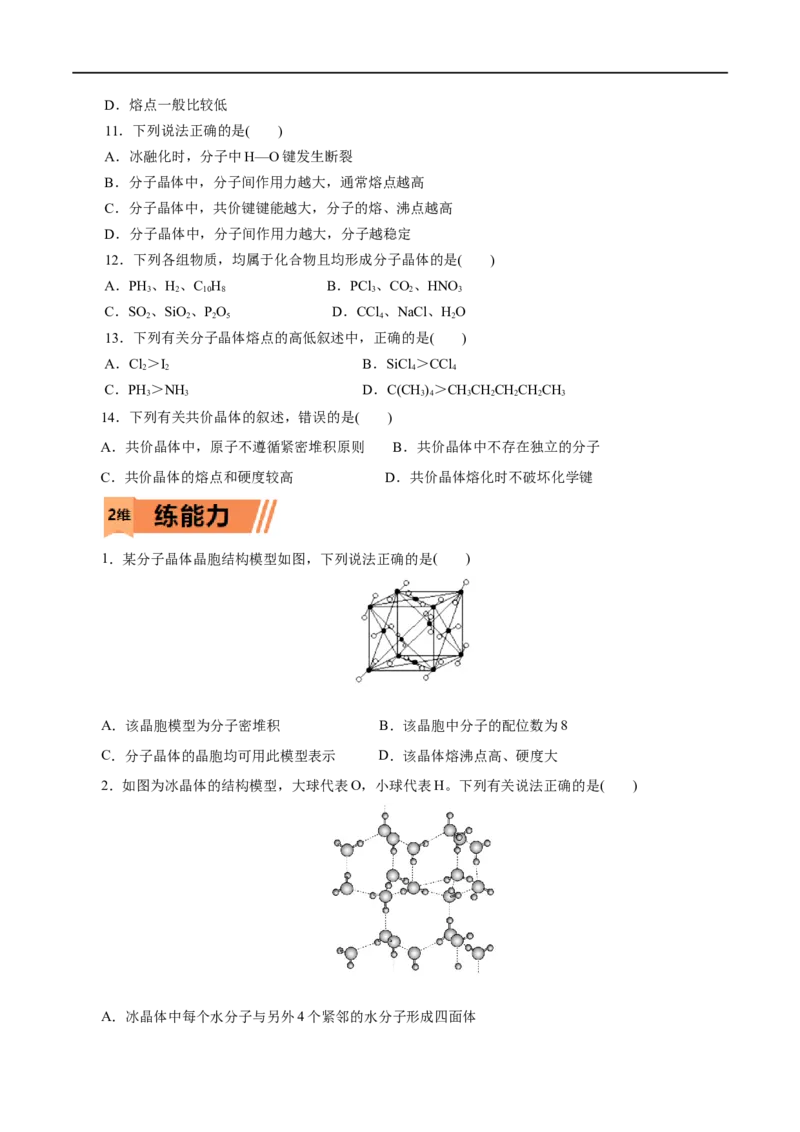
1.某分子晶体晶胞结构模型如图,下列说法正确的是( )
A.该晶胞模型为分子密堆积 B.该晶胞中分子的配位数为8
C.分子晶体的晶胞均可用此模型表示 D.该晶体熔沸点高、硬度大
2.如图为冰晶体的结构模型,大球代表O,小球代表H。下列有关说法正确的是( )
A.冰晶体中每个水分子与另外4个紧邻的水分子形成四面体B.冰晶体具有三维骨架结构,是共价晶体
C.水分子间通过H—O形成冰晶体
D.冰融化后,水分子之间空隙增大
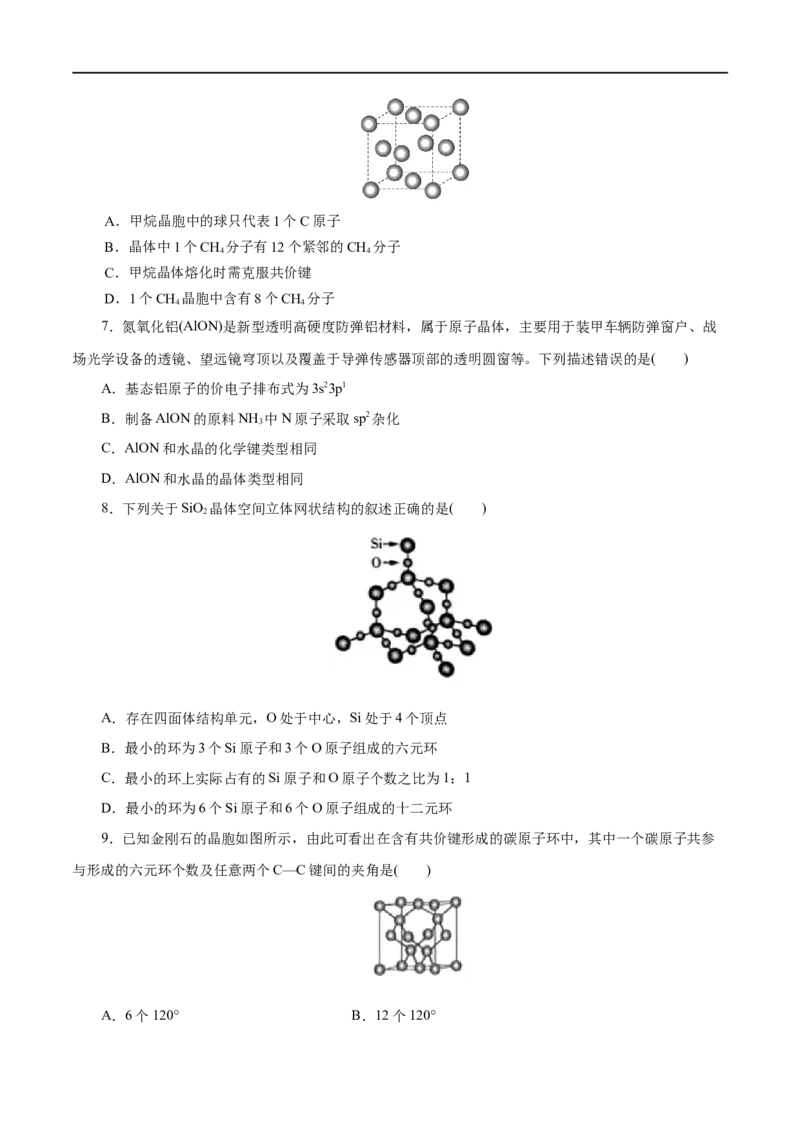
3.甲烷晶体的晶胞结构如图所示,下列说法正确的是( )
A.甲烷晶胞中的球只代表1个C原子
B.晶体中1个CH 分子周围有12个紧邻的CH 分子
4 4
C.甲烷晶体熔化时需克服共价键
D.1个CH 晶胞中含有8个CH 分子
4 4
4.我国的激光技术在世界上处于领先地位,科学家用激光将置于铁室中石墨靶上的碳原子炸松,与
此同时再用射频电火花喷射氮气,碳、氮原子结合成碳氮化合物薄膜。所得化合物可能比金刚石更坚硬,
其原因可能是( )
A.碳、氮原子构成平面结构的晶体
B.碳氮键长比金刚石中的碳碳键长更短
C.氮原子电子数比碳原子电子数多
D.碳、氮的单质的化学性质均不活泼
5.下列有关共价晶体的叙述不正确的是( )
A.金刚石和二氧化硅晶体的最小结构单元都是正四面体
B.含1molC的金刚石中C-C键数目是2N ,1 mol SiO 晶体中Si-O键数目是4 N
A 2 A
C.水晶和干冰在熔化时,晶体中的共价键都会断裂
D.SiO 晶体是共价晶体,所以晶体中不存在分子,SiO 不是它的分子式
2 2
6.下列关于SiO 和金刚石的叙述正确的是( )
2
A.SiO 的晶体结构中,每个 原子与2个O原子直接相连
2
B.通常状况下,60g SiO 晶体中含有的分子数为N (N 表示阿伏加德罗常数的值)
2 A A
C.金刚石的网状结构中,由共价键形成的最小环上有6个碳原子
D.1mol金刚石中含有4N 个C-C键(N 表示阿伏加德罗常数的值)
A A
7.现在已能在高压下将CO 转化为具有类似SiO 结构的原子晶体,下列关于CO 原子晶体的说法中
2 2 2
正确的是( )A.CO 的原子晶体中存在范德华力,每1 mol CO 原子晶体中含有2N π键
2 2 A
B.在一定条件下,CO 原子晶体转化为CO 分子晶体是物理变化
2 2
C.熔点:金刚石>原子晶体CO
2
D.在CO 的原子晶体中,每个C原子周围结合4个O原子,每个O原子与两个C原子相结合
2
8.下列说法中正确的是( )
A.冰融化时,分子中H—O键发生断裂
B.共价晶体中,共价键越强,共价晶体的熔点越高
C.分子晶体中,共价键键能越大,该分子晶体的熔、沸点一定越高
D.稀有气体形成的晶体属于共价晶体
9.下列分子晶体,关于熔点、沸点高低的叙述中,正确的是( )
A.Cl>I B.SiCl PH D.C(CH)>CH CHCHCHCH
2 2 4 4 3 3 3 4 3 2 2 2 3
10.根据下表中的有关数据分析,下列说法错误的是( )
AlCl SiCl 晶体硼 金刚石 晶体硅
3 4
熔点/℃ 194 -70 2180 >3500 1410
沸点/℃ 181 57 3650 4827 2355
A.SiCl 、AlCl 是分子晶体
4 3
B.晶体硼是共价晶体
C.晶体硅是共价晶体
D.金刚石中的C-C键比晶体硅中的Si-Si键弱
1.德、俄两国化学家共同宣布,在高压下氮气会发生聚合得到一种低熔点物质——高聚氮,这种高
聚氮的氮氮键比N 分子中的氮氮三键要弱得多。下列有关高聚氮的说法不正确的是( )
2
A.高聚氮晶体属于分子晶体 B.高聚氮是一种单质
C.高聚氮的沸点高于氮气 D.高聚氮转变成氮气是氧化还原反应
2.下列有关冰和干冰的叙述不正确的是( )
A.干冰和冰都是由分子密堆积形成的晶体
B.冰晶体中每个水分子周围只有4个紧邻的水分子
C.干冰比冰的熔点低得多,常压下易升华
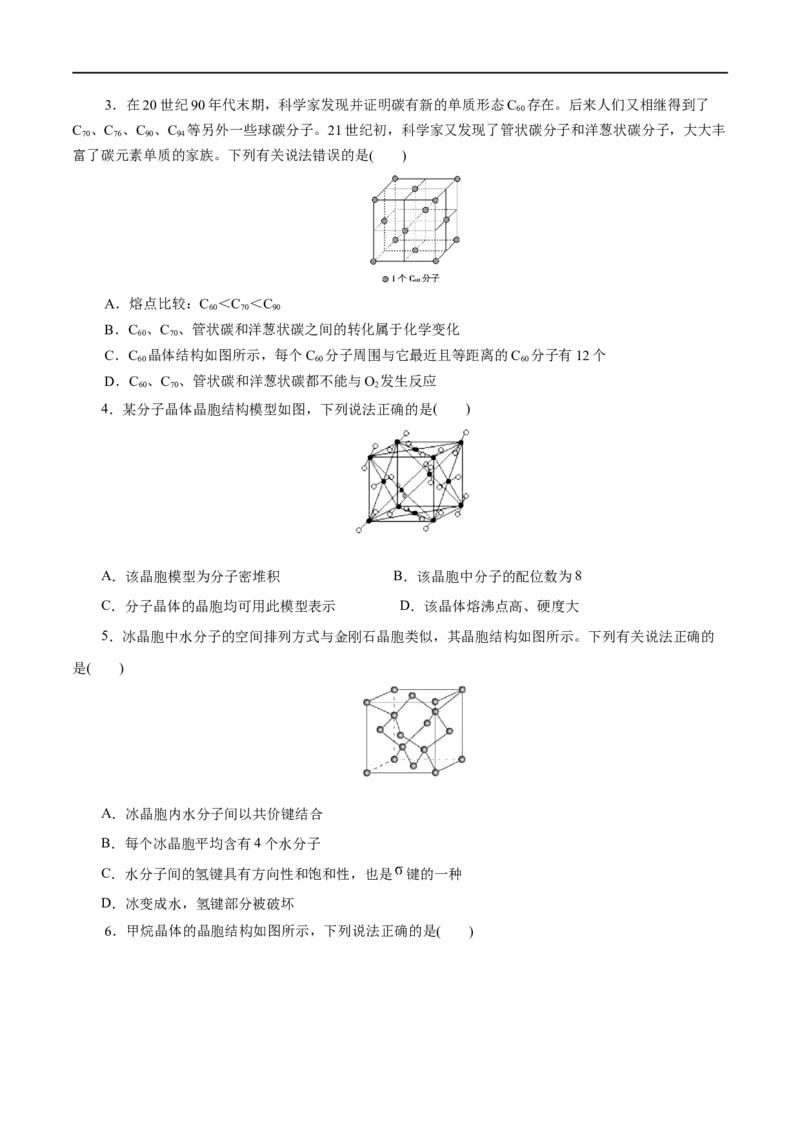
D.干冰中只存在范德华力不存在氢键,一个分子周围有12个紧邻的分子3.在20世纪90年代末期,科学家发现并证明碳有新的单质形态C 存在。后来人们又相继得到了
60
C 、C 、C 、C 等另外一些球碳分子。21世纪初,科学家又发现了管状碳分子和洋葱状碳分子,大大丰
70 76 90 94
富了碳元素单质的家族。下列有关说法错误的是( )
A.熔点比较:C <C <C
60 70 90
B.C 、C 、管状碳和洋葱状碳之间的转化属于化学变化
60 70
C.C 晶体结构如图所示,每个C 分子周围与它最近且等距离的C 分子有12个
60 60 60
D.C 、C 、管状碳和洋葱状碳都不能与O 发生反应
60 70 2
4.某分子晶体晶胞结构模型如图,下列说法正确的是( )
A.该晶胞模型为分子密堆积 B.该晶胞中分子的配位数为8
C.分子晶体的晶胞均可用此模型表示 D.该晶体熔沸点高、硬度大
5.冰晶胞中水分子的空间排列方式与金刚石晶胞类似,其晶胞结构如图所示。下列有关说法正确的
是( )
A.冰晶胞内水分子间以共价键结合
B.每个冰晶胞平均含有4个水分子
C.水分子间的氢键具有方向性和饱和性,也是 键的一种
D.冰变成水,氢键部分被破坏
6.甲烷晶体的晶胞结构如图所示,下列说法正确的是( )A.甲烷晶胞中的球只代表1个C原子
B.晶体中1个CH 分子有12个紧邻的CH 分子
4 4
C.甲烷晶体熔化时需克服共价键
D.1个CH 晶胞中含有8个CH 分子
4 4
7.氮氧化铝(AlON)是新型透明高硬度防弹铝材料,属于原子晶体,主要用于装甲车辆防弹窗户、战
场光学设备的透镜、望远镜穹顶以及覆盖于导弹传感器顶部的透明圆窗等。下列描述错误的是( )
A.基态铝原子的价电子排布式为3s23p1
B.制备AlON的原料NH 中N原子采取sp2杂化
3
C.AlON和水晶的化学键类型相同
D.AlON和水晶的晶体类型相同
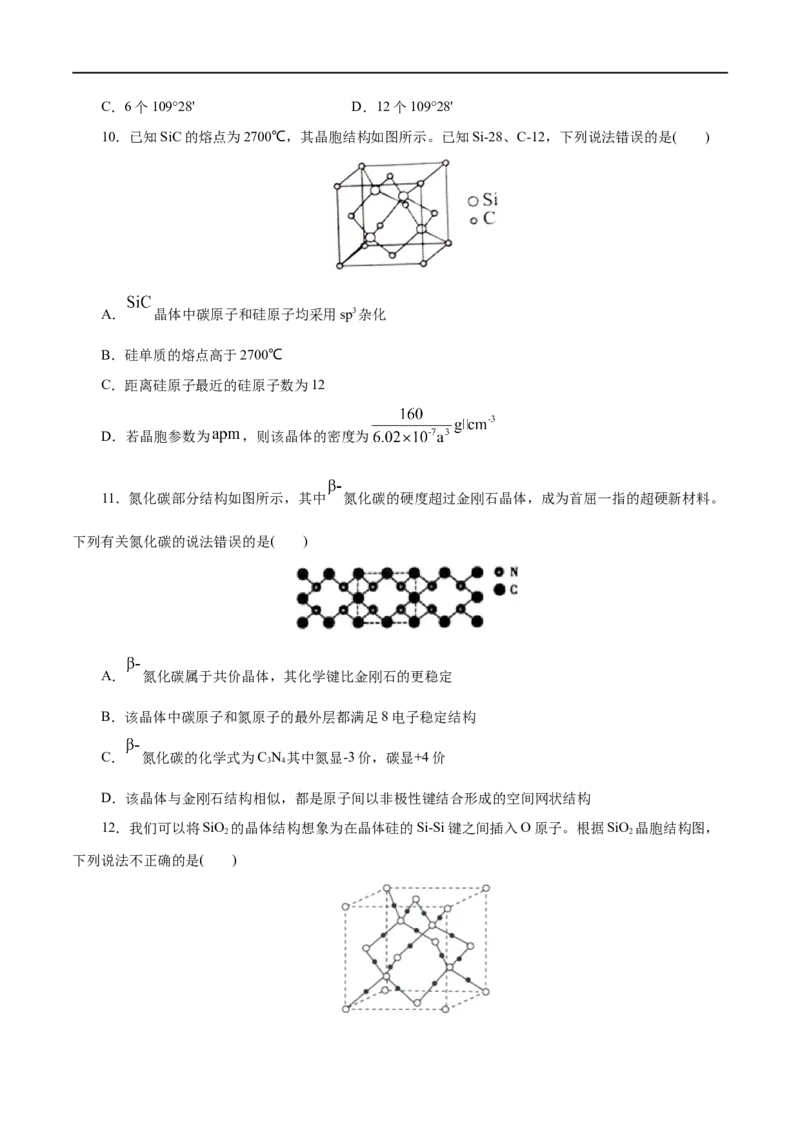
8.下列关于SiO 晶体空间立体网状结构的叙述正确的是( )
2
A.存在四面体结构单元,O处于中心,Si处于4个顶点
B.最小的环为3个Si原子和3个O原子组成的六元环
C.最小的环上实际占有的Si原子和O原子个数之比为1:1
D.最小的环为6个Si原子和6个O原子组成的十二元环
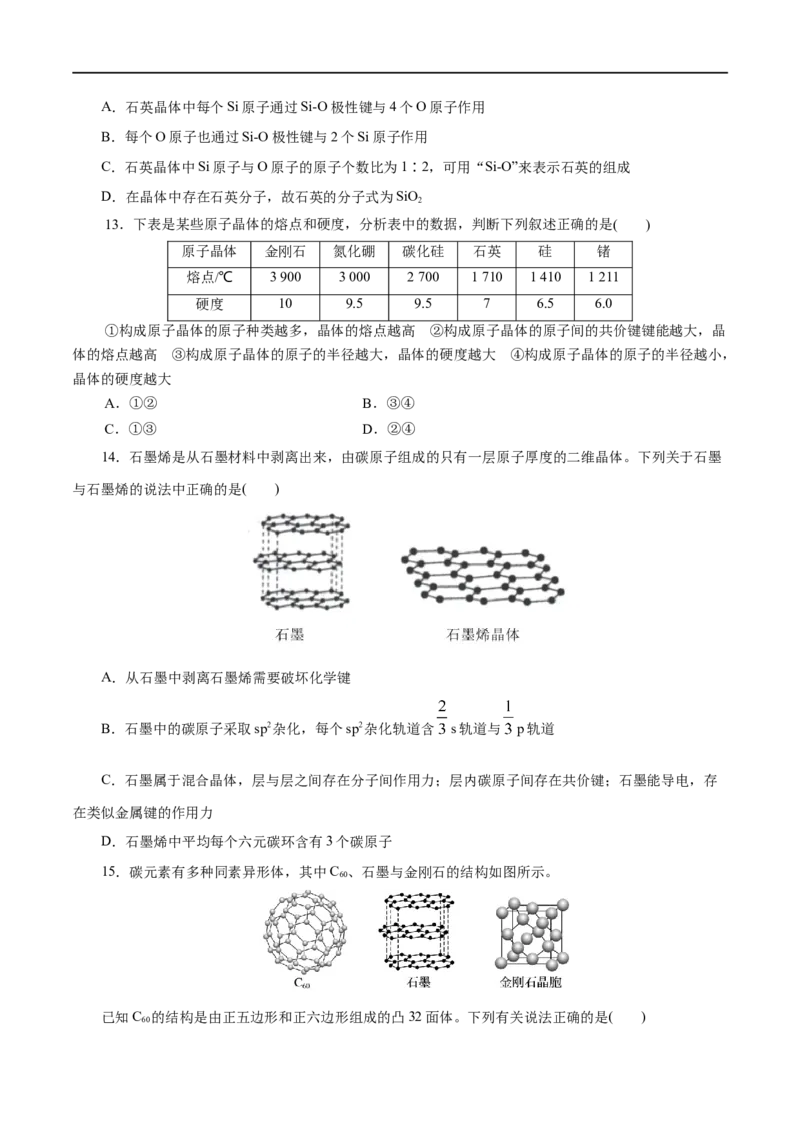
9.已知金刚石的晶胞如图所示,由此可看出在含有共价键形成的碳原子环中,其中一个碳原子共参
与形成的六元环个数及任意两个C—C键间的夹角是( )
A.6个120° B.12个120°C.6个109°28' D.12个109°28'
10.已知SiC的熔点为2700℃,其晶胞结构如图所示。已知Si-28、C-12,下列说法错误的是( )
A. 晶体中碳原子和硅原子均采用sp3杂化
B.硅单质的熔点高于2700℃
C.距离硅原子最近的硅原子数为12
D.若晶胞参数为 ,则该晶体的密度为
11.氮化碳部分结构如图所示,其中 氮化碳的硬度超过金刚石晶体,成为首屈一指的超硬新材料。
下列有关氮化碳的说法错误的是( )
A. 氮化碳属于共价晶体,其化学键比金刚石的更稳定
B.该晶体中碳原子和氮原子的最外层都满足8电子稳定结构
C. 氮化碳的化学式为C N 其中氮显-3价,碳显+4价
3 4
D.该晶体与金刚石结构相似,都是原子间以非极性键结合形成的空间网状结构
12.我们可以将SiO 的晶体结构想象为在晶体硅的Si-Si键之间插入O原子。根据SiO 晶胞结构图,
2 2
下列说法不正确的是( )A.石英晶体中每个Si原子通过Si-O极性键与4个O原子作用
B.每个O原子也通过Si-O极性键与2个Si原子作用
C.石英晶体中Si原子与O原子的原子个数比为1∶2,可用“Si-O”来表示石英的组成
D.在晶体中存在石英分子,故石英的分子式为SiO
2
13.下表是某些原子晶体的熔点和硬度,分析表中的数据,判断下列叙述正确的是( )
原子晶体 金刚石 氮化硼 碳化硅 石英 硅 锗
熔点/℃ 3 900 3 000 2 700 1 710 1 410 1 211
硬度 10 9.5 9.5 7 6.5 6.0
①构成原子晶体的原子种类越多,晶体的熔点越高 ②构成原子晶体的原子间的共价键键能越大,晶
体的熔点越高 ③构成原子晶体的原子的半径越大,晶体的硬度越大 ④构成原子晶体的原子的半径越小,
晶体的硬度越大
A.①② B.③④
C.①③ D.②④
14.石墨烯是从石墨材料中剥离出来,由碳原子组成的只有一层原子厚度的二维晶体。下列关于石墨
与石墨烯的说法中正确的是( )
A.从石墨中剥离石墨烯需要破坏化学键
B.石墨中的碳原子采取sp2杂化,每个sp2杂化轨道含 s轨道与 p轨道
C.石墨属于混合晶体,层与层之间存在分子间作用力;层内碳原子间存在共价键;石墨能导电,存
在类似金属键的作用力
D.石墨烯中平均每个六元碳环含有3个碳原子
15.碳元素有多种同素异形体,其中C 、石墨与金刚石的结构如图所示。
60
已知C 的结构是由正五边形和正六边形组成的凸32面体。下列有关说法正确的是( )
60A.C 中含有20个正五边形和12个正六边形
60
B.石墨的层内碳原子之间只存在 σ 键
C.石墨中层间碳原子之间存在化学键
D.如图所示的金刚石晶胞中有8个碳原子