文档内容
第 5 讲 氧化还原反应
【练基础】
1.我国古代就有湿法炼铜的记载“曾青得铁则化为铜”,反应为Fe+CuSO=Cu+FeSO 。有关该反应的说
4 4
法正确的是
A.Fe被还原 B.Fe失去2个电子
C.CuSO 发生氧化反应 D.CuSO 失去电子
4 4
2.菜谱中记载:河虾不宜与西红柿同食。主要原因是河虾中含有+5价砷,西红柿中含有比较多的维生素
C,两者同食时会生成有毒的+3价砷。下列说法正确的是
A.在该反应中维生素C作氧化剂 B.由上述信息可推知砒霜(As O)有毒
2 3
C.因为河虾中含有砷元素,所以不能食用 D.上述反应中河虾中的+5价砷被氧化
3.2Al+2NaOH+6H O=2Na[Al(OH) ]+3H ,下列说法正确的是
2 4 2
A.还原剂与氧化剂物质的量之比1∶1
B.氧化剂只有水
C.用氨水也能溶解铝单质
D.还原产物与氧化产物的物质的量之比为2∶3
4.《天工开物》中关于胡粉 的制法如下:每铅百斤,熔化,削成薄片,卷作简,安木
甑内。甑下甑中各安醋一瓶,外以盐泥固济,纸糊甑缝。安火四两,养之七日。期足启开,铅片皆生霜粉,
扫入水缸内。下列叙述错误的是
A.制备胡粉的过程中未洗及氧化还原反应
B. 属于弱电解质
C.胡粉属于碱式盐
D.“外以盐泥固济,纸糊甑缝”主要目的之一是防止醋酸挥发逸出
5.下列所加物质的作用与其还原性无关的是
A.果蔬饮料中加入维C B.向葡萄酒中添加少量SO
2
C.月饼脱氧剂包中有铁粉 D.面粉发酵时加入少量小苏打
6.下列变化过程没有涉及氧化还原反应的是
A.打磨过的铝箔加热熔化但不滴落
B.Fe(OH) 白色沉淀在空气中放置变成红褐色
2
C.NaO 加入水中后,带火星的木条复燃
2 2
D.用干燥洁净的铂丝蘸取氯化钾溶液放到酒精喷灯火焰上灼烧,透过蓝色钴玻璃观察火焰呈紫色7.下列应用涉及氧化还原反应的是
A.用TiCl 制备纳米级TiO
4 2
B.高铁酸钾(K FeO)用作新型水处理剂
2 4
C.用明矾溶液除去铜制品表面的铜绿
D.工业上将NH 和CO 通入饱和食盐水制备小苏打
3 2
8.反应3NO +HO=2HNO +NO中,当有6 mol e-发生转移时,被氧化的物质与被还原的物质的物质的量
2 2 3
之比为
A.1∶1 B.1∶2 C.2∶1 D.3∶1
9.关于反应4OF+H S=SF+2HF+4O,下列说法正确的是
2 2 2 6 2
A.OF 在该反应中同时发生氧化反应和还原反应
2 2
B.O 是氧化产物
2
C.氧化剂与还原剂的物质的量之比为4:1
D.若2.24LH S被反应,则转移电子为0.8mol
2
10.关于反应 ,下列说法正确的是
A. 中的氮元素被氧化
B. 既是氧化剂又是还原剂
C.氧化剂与氧化产物的物质的量之比为1∶1
D.还原产物与氧化产物的物质的量之比为1∶4
【练提升】
11.有下列四个反应:
①
②
③
④
下列说法正确的是
A.反应①②③④中的氧化产物依次是 、 、 、B.氧化性:
C.根据反应①一定可以推理得到
D.在反应③中,当有 参加反应时,有 被氧化
12.一定量的某硫铁矿(主要成分Fe S,S为-2价)与100 mL盐酸怡好完全反应矿石中其他成分不与盐酸反
x
应),生成2.4 g硫单质、0.30 mol FeCl 和一定量HS气体,且溶液中无Fe3+,则下列说法不正确的是
2 2
A.该硫黄铁矿中Fe S的x=0.75
x
B.该硫黄铁矿中,Fe2+与Fe3+的物质的量之比为1:1
C.HS气体在标准状况下体积为6.72 L
2
D.该盐酸的物质的量浓度为6.0 mol/L
13.从含砷(As)的有毒工业废水中提取粗As O,流程如下:
2 3
已知:As与P同为VA族元素;Ca (AsO) 微溶于水,Ca (AsO) 难溶于水。
3 3 2 3 4 2
下列说法不正确的是
A.试剂①的作用是将 氧化为
B.滤液①主要成分为NaOH溶液
C.滤液②主要成分可以循环利用
D.“还原”的离子方程式:2H++2 +2SO=2 +AsO↓+H O
2 2 3 2
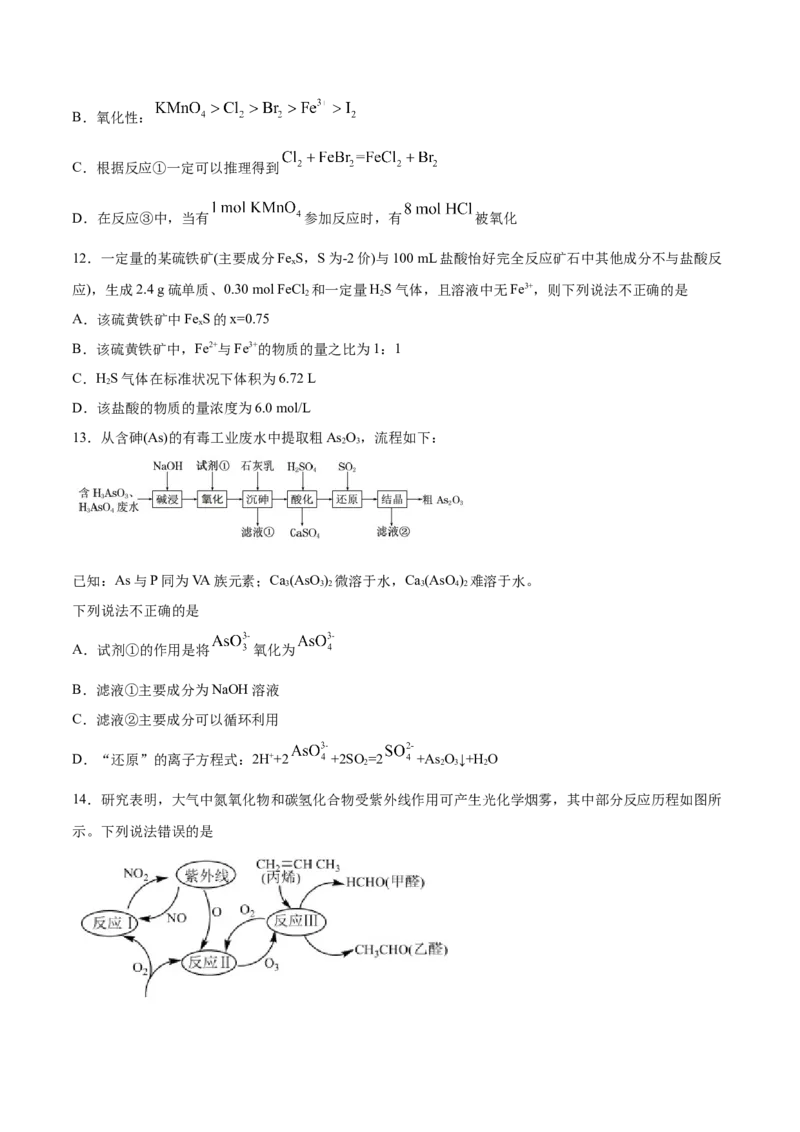
14.研究表明,大气中氮氧化物和碳氢化合物受紫外线作用可产生光化学烟雾,其中部分反应历程如图所
示。下列说法错误的是A.整个过程中O 作催化剂和氧化剂
3
B.反应Ⅲ的方程式为 CH=CHCH +2O →HCHO+CH CHO+2O
2 3 3 3 2
C.光化学烟雾中含甲醛、乙醛等有机物
D.反应Ⅰ、反应Ⅲ均属于氧化还原反应
15.ClO 是国际上公认的安全绿色消毒剂。工业上利用甲醇还原NaClO 的方法制备ClO 的反应原理为:
2 3 2
NaClO+H SO +CH OH→C1O ↑+HCOOH+Na H(SO )↓+H O(未配平),下列说法错误的是
3 2 4 3 2 3 4 2 2
A.HCOOH为该反应的氧化产物
B.生成2.24L C1O 时,电子转移数是0.1N
2 A
C.反应中氧化剂和还原剂物质的量之比为4:1
D.ClO 和SO 均能漂白纸张,但漂白原理不同
2 2
16.硫元素的几种化合物存在下列转化关系:
浓HSO SO Na SO 溶液 NaSO S
2 4 2 2 3 2 2 3
下列判断不正确的是
A.反应①中浓硫酸作氧化剂 B.反应②表明SO 有酸性氧化物的性质
2
C.反应③的原子利用率是100% D.反应④稀HSO 作还原剂
2 4
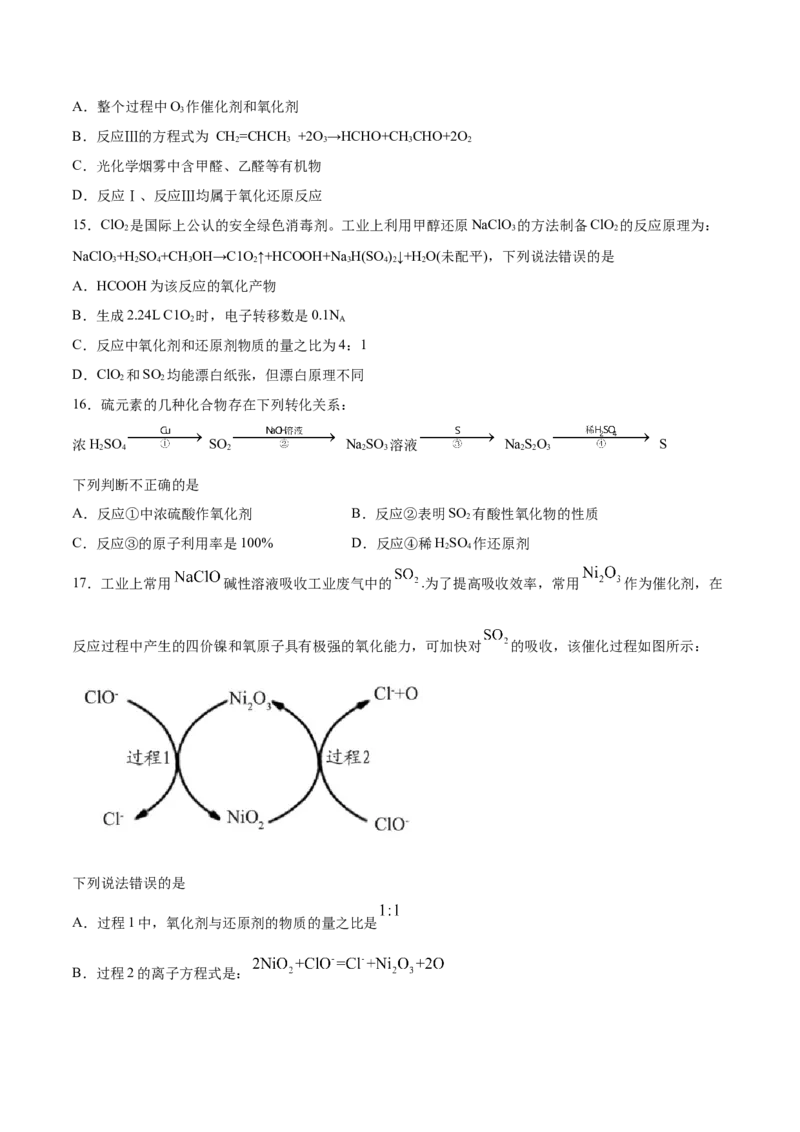
17.工业上常用 碱性溶液吸收工业废气中的 .为了提高吸收效率,常用 作为催化剂,在
反应过程中产生的四价镍和氧原子具有极强的氧化能力,可加快对 的吸收,该催化过程如图所示:
下列说法错误的是
A.过程1中,氧化剂与还原剂的物质的量之比是
B.过程2的离子方程式是:C.吸收反应的总方程式是:
D.用 代替 脱硫效果更好
18.以黄铁矿(主要成分 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境
的污染,其中一种流程如图所示。下列说法错误的是
A.黄铁矿中的 在煅烧过程中作还原剂
B.欲得到更纯的 ,反应①应通入过量的 气体
C.还原铁粉用盐酸溶解后,可用 溶液滴定法来测定其纯度
D.加热 制备 的化学方程式为
19.根据溶液中发生的两个反应:① ;②
。下列说法不正确的是
A.反应①中氧化剂和还原剂的物质的量之比为
B.酸性条件下,氧化性:
C.实验室将高锰酸钾酸化时,常用硫酸酸化而不用盐酸酸化
D.反应②中每生成 的气体,则反应中转移的电子的物质的量为
20.用Cu S、FeS处理酸性废水中的Cr O ,发生的反应如下:
2 2
反应①:Cu S+Cr O +H+→Cu2++SO +Cr3++H O(未配平)
2 2 2反应②:FeS+Cr O +H+→Fe3++SO +Cr3++H O(未配平)
2 2
下列判断错误的是
A.反应①中还原剂与氧化剂的物质的量之比为3:5
B.用相同物质的量的Cu S和FeS处理Cr O 时,Cu S消耗更多Cr O
2 2 2 2
C.处理等物质的量的Cr O 时,反应①和②中消耗H+的物质的量相等
2
D.用FeS处理废水不仅可以除去Cr O ,还可吸附悬浮杂质
2