文档内容
第 36 讲 晶胞结构分析与计算
[复习目标] 1.掌握均摊法计算的一般方法,能根据晶胞中微粒的位置计算晶胞的化学式。
2.掌握晶体密度与晶胞参数计算的一般步骤。
考点一 晶胞模型与均摊法计算
1.晶胞中微粒数的计算方法——均摊法
(1)长方体(包括立方体)晶胞中不同位置的粒子数的计算
如某个粒子为N个晶胞所共有,则该粒子有属于这个晶胞。中学中常见的晶胞为立方晶胞,
立方晶胞中微粒数的计算方法如图1。
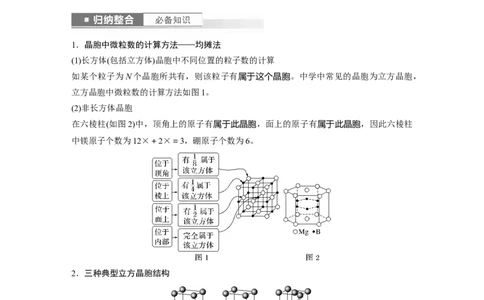
(2)非长方体晶胞
在六棱柱(如图2)中,顶角上的原子有属于此晶胞,面上的原子有属于此晶胞,因此六棱柱
中镁原子个数为12×+2×=3,硼原子个数为6。
2.三种典型立方晶胞结构
3.晶胞中微粒配位数的计算
一个粒子周围最邻近的粒子数称为配位数,它反映了晶体中粒子排列的紧密程度。
(1)晶体中原子(或分子)的配位数
若晶体中的微粒为同种原子或同种分子,则某原子(或分子)的配位数指的是该原子(或分子)
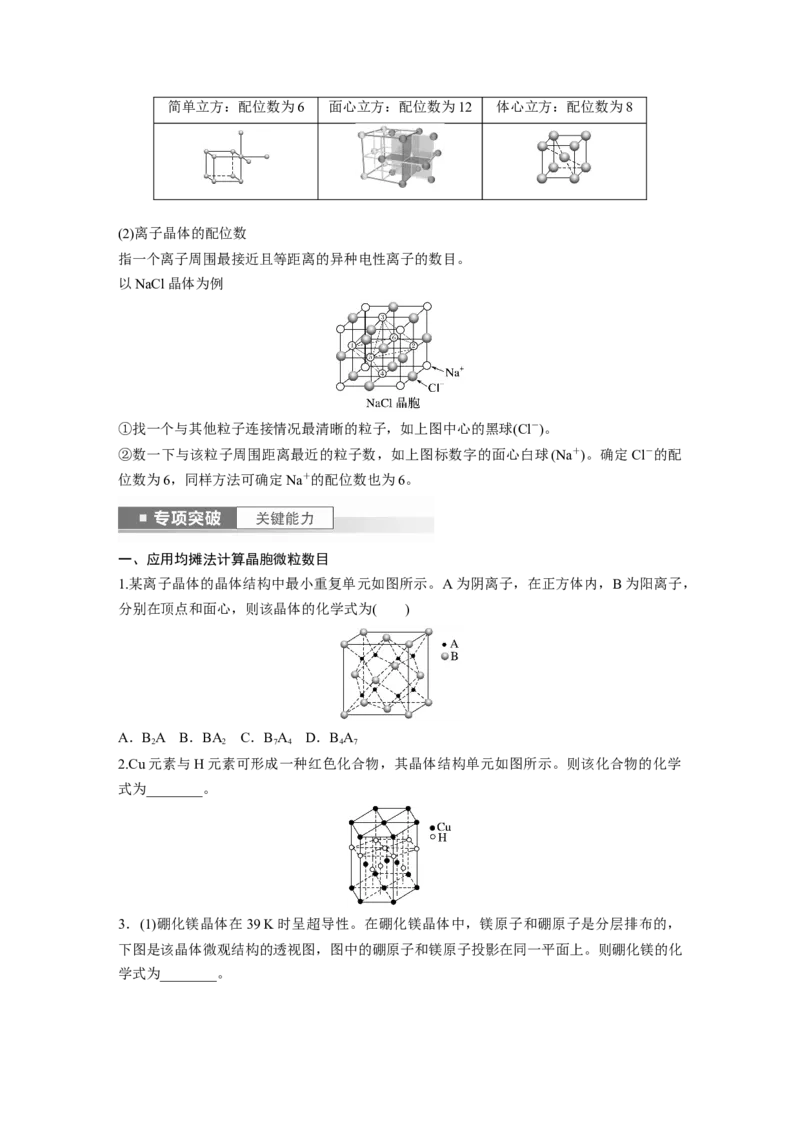
最接近且等距离的原子(或分子)的数目,常见晶胞的配位数如下:简单立方:配位数为6 面心立方:配位数为12 体心立方:配位数为8
(2)离子晶体的配位数
指一个离子周围最接近且等距离的异种电性离子的数目。
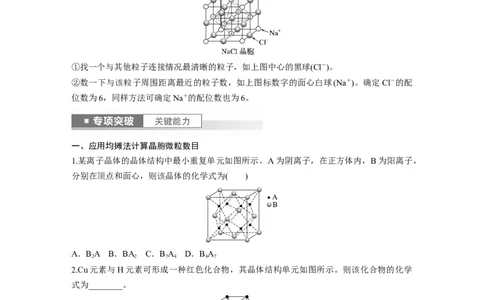
以NaCl晶体为例
①找一个与其他粒子连接情况最清晰的粒子,如上图中心的黑球(Cl-)。
②数一下与该粒子周围距离最近的粒子数,如上图标数字的面心白球(Na+)。确定Cl-的配
位数为6,同样方法可确定Na+的配位数也为6。
一、应用均摊法计算晶胞微粒数目
1.某离子晶体的晶体结构中最小重复单元如图所示。A为阴离子,在正方体内,B为阳离子,
分别在顶点和面心,则该晶体的化学式为( )
A.B A B.BA C.B A D.B A
2 2 7 4 4 7
2.Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图所示。则该化合物的化学
式为________。
3.(1)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,
下图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化
学式为________。(2)在硼酸盐中,阴离子有链状、环状等多种结构形式。如图是一种链状结构的多硼酸根,
则多硼酸根离子符号为________。
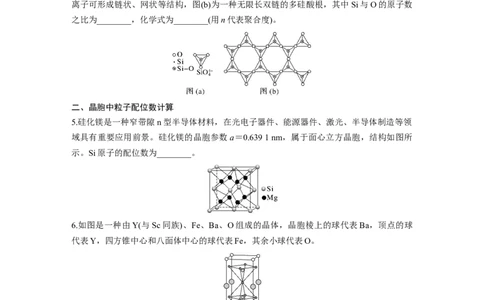
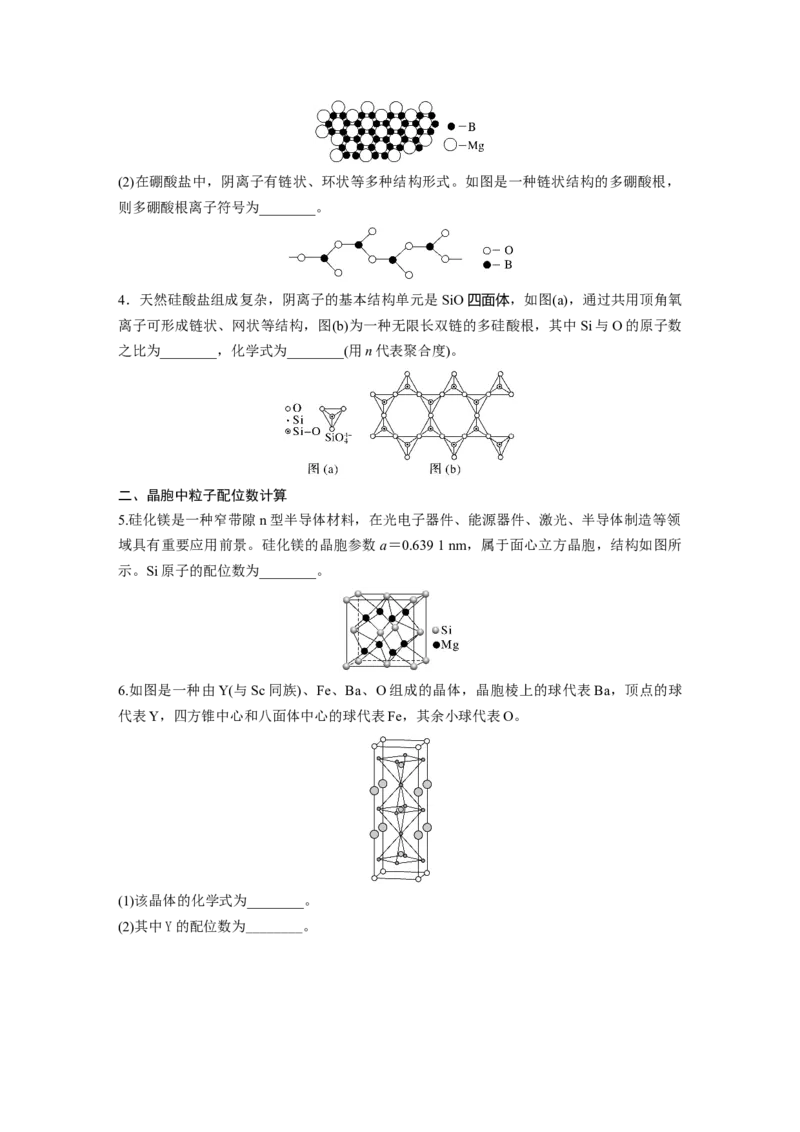
4.天然硅酸盐组成复杂,阴离子的基本结构单元是SiO四面体,如图(a),通过共用顶角氧
离子可形成链状、网状等结构,图(b)为一种无限长双链的多硅酸根,其中Si与O的原子数
之比为________,化学式为________(用n代表聚合度)。
二、晶胞中粒子配位数计算
5.硅化镁是一种窄带隙n型半导体材料,在光电子器件、能源器件、激光、半导体制造等领
域具有重要应用前景。硅化镁的晶胞参数a=0.639 1 nm,属于面心立方晶胞,结构如图所
示。Si原子的配位数为________。
6.如图是一种由Y(与Sc同族)、Fe、Ba、O组成的晶体,晶胞棱上的球代表Ba,顶点的球
代表Y,四方锥中心和八面体中心的球代表Fe,其余小球代表O。
(1)该晶体的化学式为________。
(2)其中Y的配位数为________。考点二 晶胞参数计算
1.晶胞参数
晶胞的形状和大小可以用6个参数来表示,包括晶胞的3组棱长a、b、c和3组棱相互间的
夹角α、β、γ,即晶格特征参数,简称晶胞参数。
2.晶体结构的相关计算
(1)空间利用率=×100%。
(2)金属晶体中体心立方堆积、面心立方堆积中的几组计算公式(设棱长为a)
①面对角线长=________。
②体对角线长=________。
③体心立方堆积____r=______a(r为原子半径)。
④面心立方堆积____r=______a(r为原子半径)。
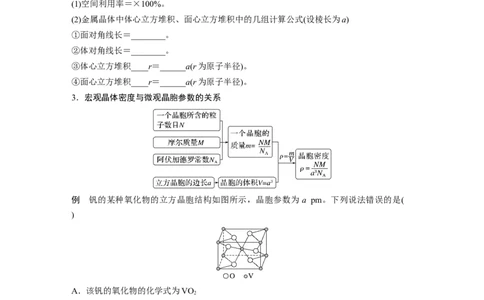
3.宏观晶体密度与微观晶胞参数的关系
例 钒的某种氧化物的立方晶胞结构如图所示,晶胞参数为 a pm。下列说法错误的是(
)
A.该钒的氧化物的化学式为VO
2
B.V原子在该晶体中的堆积方式为体心立方
C.V原子的配位数与O原子的配位数之比为1∶2
D.该晶胞的密度为 g·cm-3
1.Zn与S所形成化合物晶体的晶胞如图所示。Zn2+的配位数是________,S2-填充在Zn2+形
成的正四面体空隙中。若该晶体的密度为d g·cm-3,阿伏加德罗常数的值为N ,则该晶胞
A
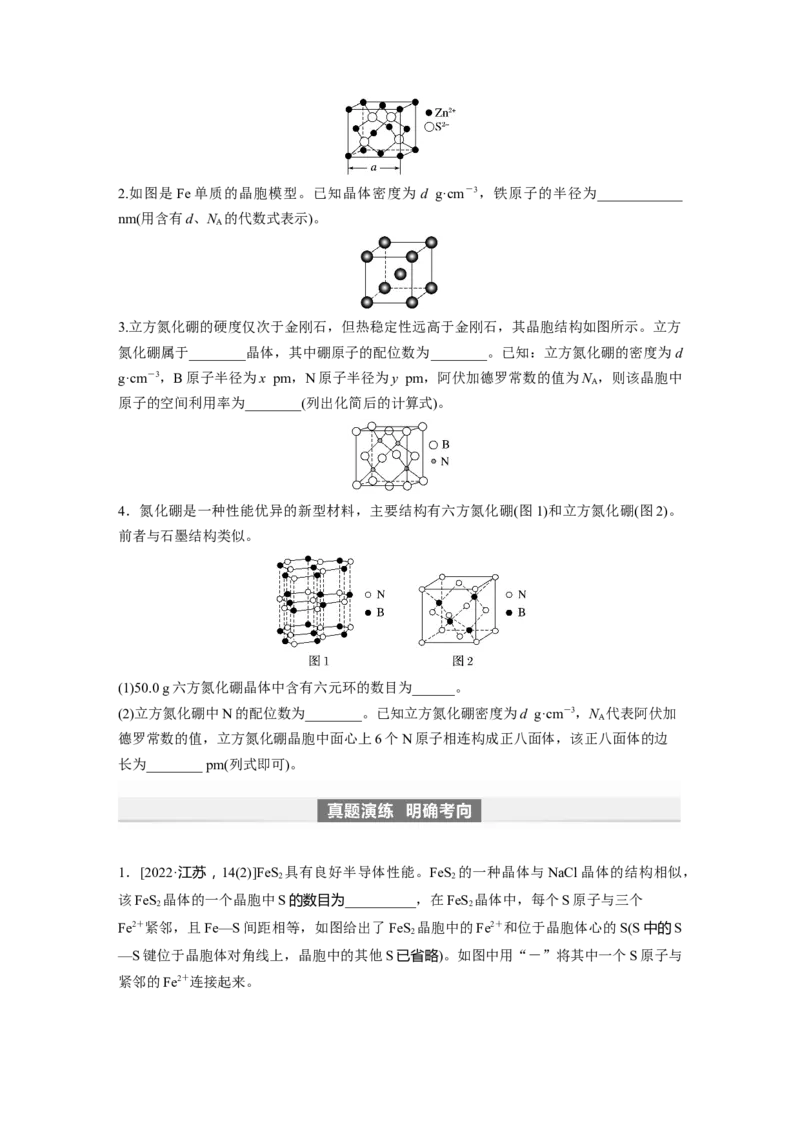
参数a= ____________ nm。2.如图是Fe单质的晶胞模型。已知晶体密度为 d g·cm-3,铁原子的半径为____________
nm(用含有d、N 的代数式表示)。
A
3.立方氮化硼的硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方
氮化硼属于________晶体,其中硼原子的配位数为________。已知:立方氮化硼的密度为d
g·cm-3,B原子半径为x pm,N原子半径为y pm,阿伏加德罗常数的值为N ,则该晶胞中
A
原子的空间利用率为________(列出化简后的计算式)。
4.氮化硼是一种性能优异的新型材料,主要结构有六方氮化硼(图1)和立方氮化硼(图2)。
前者与石墨结构类似。
(1)50.0 g六方氮化硼晶体中含有六元环的数目为______。
(2)立方氮化硼中N的配位数为________。已知立方氮化硼密度为d g·cm-3,N 代表阿伏加
A
德罗常数的值,立方氮化硼晶胞中面心上6个N原子相连构成正八面体,该正八面体的边
长为________ pm(列式即可)。
1.[2022·江苏,14(2)]FeS 具有良好半导体性能。FeS 的一种晶体与NaCl晶体的结构相似,
2 2
该FeS 晶体的一个晶胞中S的数目为__________,在FeS 晶体中,每个S原子与三个
2 2
Fe2+紧邻,且Fe—S间距相等,如图给出了FeS 晶胞中的Fe2+和位于晶胞体心的S(S中的S
2
—S键位于晶胞体对角线上,晶胞中的其他S已省略)。如图中用“-”将其中一个S原子与
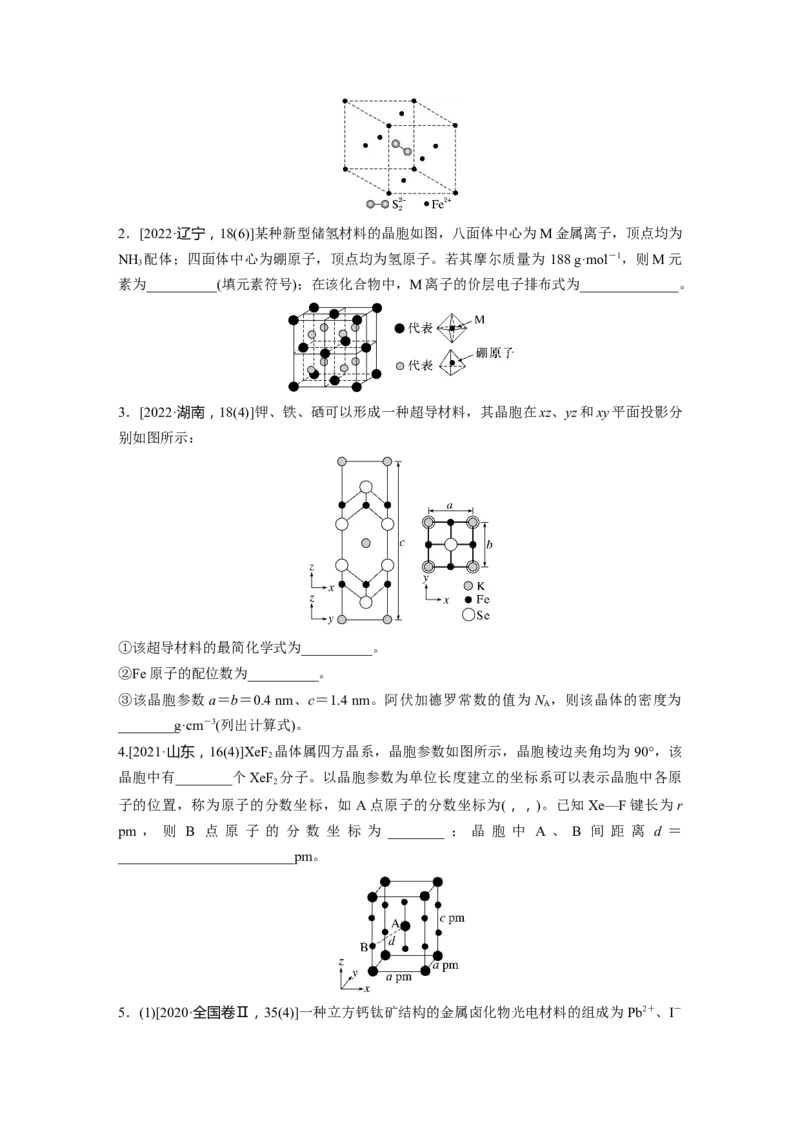
紧邻的Fe2+连接起来。2.[2022·辽宁,18(6)]某种新型储氢材料的晶胞如图,八面体中心为M金属离子,顶点均为
NH 配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为 188 g·mol-1,则M元
3
素为__________(填元素符号);在该化合物中,M离子的价层电子排布式为______________。
3.[2022·湖南,18(4)]钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分
别如图所示:
①该超导材料的最简化学式为__________。
②Fe原子的配位数为__________。
③该晶胞参数a=b=0.4 nm、c=1.4 nm。阿伏加德罗常数的值为N ,则该晶体的密度为
A
________g·cm-3(列出计算式)。
4.[2021·山东,16(4)]XeF 晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该
2
晶胞中有________个XeF 分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原
2
子的位置,称为原子的分数坐标,如 A点原子的分数坐标为(,,)。已知Xe—F键长为r
pm , 则 B 点 原 子 的 分 数 坐 标 为 ________ ; 晶 胞 中 A 、 B 间 距 离 d =
_________________________pm。
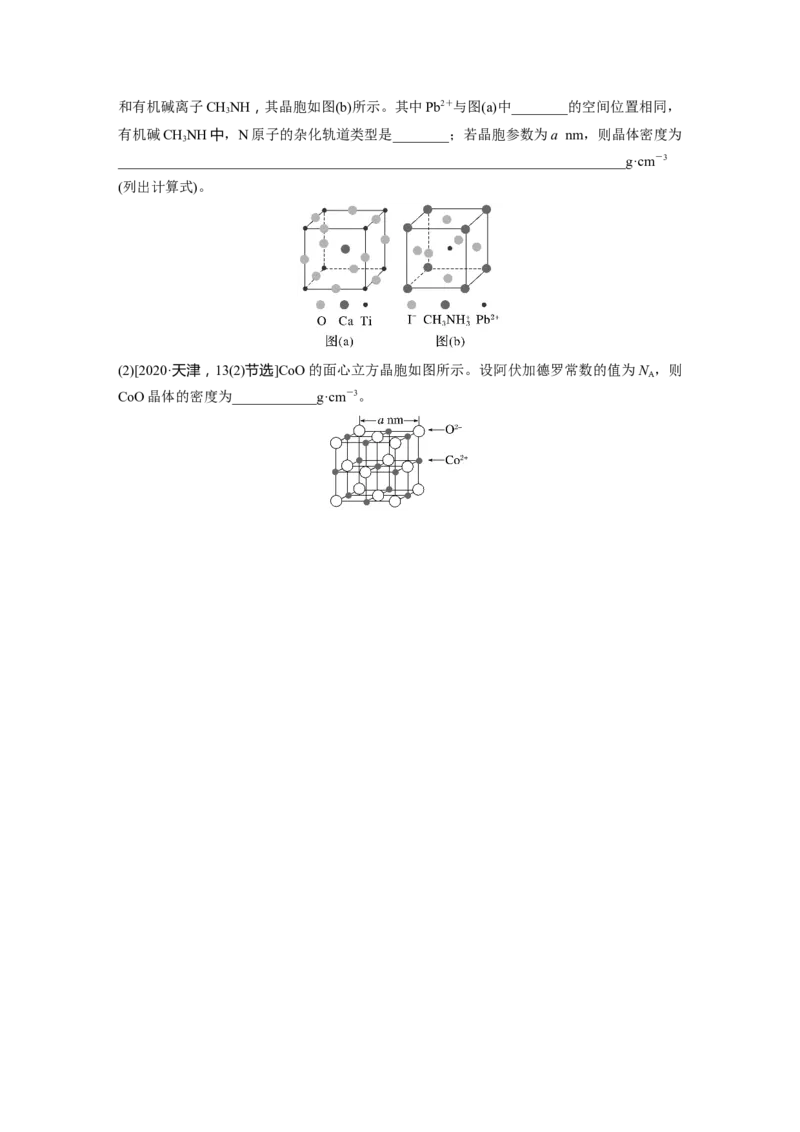
5.(1)[2020·全国卷Ⅱ,35(4)]一种立方钙钛矿结构的金属卤化物光电材料的组成为 Pb2+、I-和有机碱离子CHNH,其晶胞如图(b)所示。其中Pb2+与图(a)中________的空间位置相同,
3
有机碱CHNH中,N原子的杂化轨道类型是________;若晶胞参数为a nm,则晶体密度为
3
________________________________________________________________________g·cm-3
(列出计算式)。
(2)[2020·天津,13(2)节选]CoO的面心立方晶胞如图所示。设阿伏加德罗常数的值为N ,则
A
CoO晶体的密度为____________g·cm-3。