文档内容
1.(2022·山东潍坊模拟)砷化镓(GaAs)、碲化镉(CdTe)等太阳能电池适合光电转换,可以直
接把光能转化成电能。回答下列问题:
(1)元素As与N同族,预测As的氢化物分子的空间结构为________,其基态原子最外层p
轨道电子的自旋________(填“相同”或“相反”)。
(2)元素Cd与Zn是同一副族的相邻元素,Cd的价层电子排布式为4d105s2,Cd2+的价层电子
排布式为________。
(3)经X射线衍射实验证明在碲酸(H TeO )分子内的6个羟基排列在碲原子的周围呈八面体结
6 6
构,碲酸中碲原子的价层电子对数为______________________________________________。
(4)Te、Se 都是第Ⅵ A 族的元素,SeF 与 SF 具有相似的结构,则熔、沸点
6 6
SeF________SF (填“>”“<”或“=”,下同);二硒键和二硫键是重要的光响应动态共
6 6
价键,其光响应原理可用如图表示,已知光的波长与其能量成反比,则图中实现光响应的波
长 : λ________λ , 其 原 因 是
1 2
________________________________________________________________________
________________________________________________________________________。
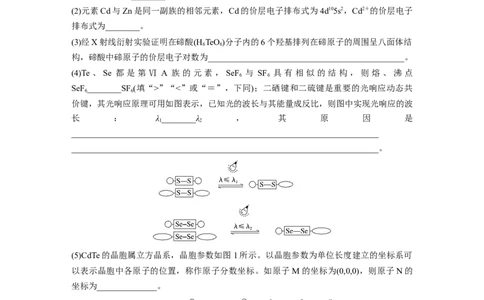
(5)CdTe的晶胞属立方晶系,晶胞参数如图1所示。以晶胞参数为单位长度建立的坐标系可
以表示晶胞中各原子的位置,称作原子分数坐标。如原子 M的坐标为(0,0,0),则原子N的
坐标为______________。
该晶胞沿其面对角线方向上的投影如图2所示,则代表Te原子的位置是________(填序号),
晶胞中原子6和11之间的距离为________pm(用含a的代数式表示)。2.(2022·安徽马鞍山模拟)人类对第二周期的元素及化合物认识最早。
(1)第二周期的元素中,I(第一电离能)从大到小排前三位的是______________。
1
(2)XeF+PtF溶于水可生成Xe和HPtF ,写出反应的化学方程式:__________________
6
___________________________________________________________________________。
(3)SCN—中C原子的杂化轨道类型为________, 其中含有两个相同的大π键,其形式为
________(用Π表示,n为原子数,m为电子数),检验Fe3+时,SCN—以 S原子配位不以N
原子配位的原因是_______________________________________________________________
______________________________________________________________________________。
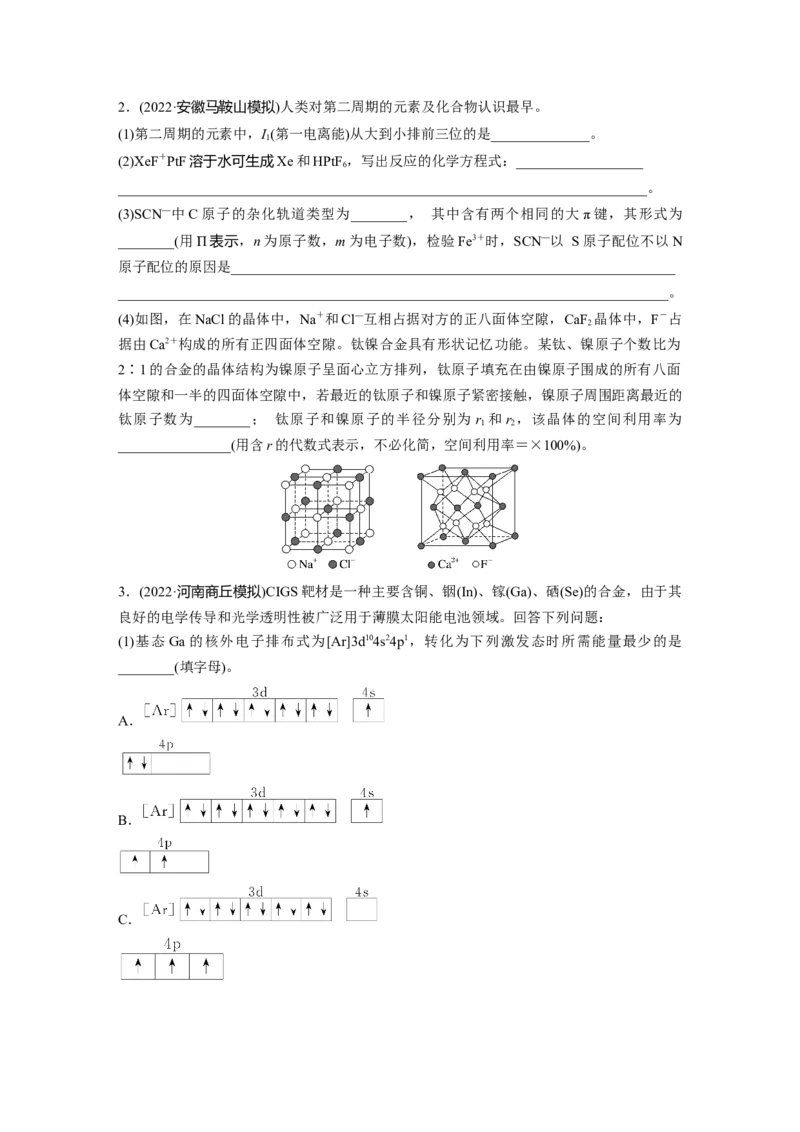
(4)如图,在NaCl的晶体中,Na+和Cl—互相占据对方的正八面体空隙,CaF 晶体中,F-占
2
据由Ca2+构成的所有正四面体空隙。钛镍合金具有形状记忆功能。某钛、镍原子个数比为
2∶1的合金的晶体结构为镍原子呈面心立方排列,钛原子填充在由镍原子围成的所有八面
体空隙和一半的四面体空隙中,若最近的钛原子和镍原子紧密接触,镍原子周围距离最近的
钛原子数为________; 钛原子和镍原子的半径分别为 r 和r ,该晶体的空间利用率为
1 2
________________(用含r的代数式表示,不必化简,空间利用率=×100%)。
3.(2022·河南商丘模拟)CIGS靶材是一种主要含铜、铟(In)、镓(Ga)、硒(Se)的合金,由于其
良好的电学传导和光学透明性被广泛用于薄膜太阳能电池领域。回答下列问题:
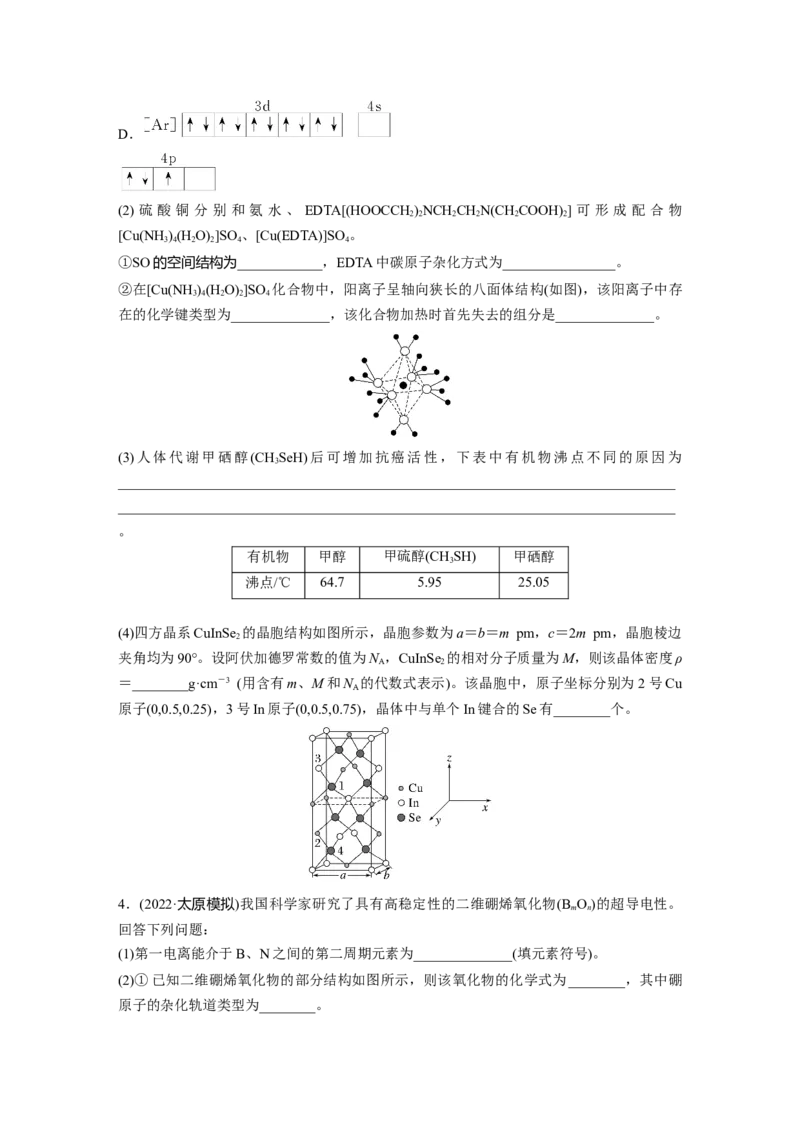
(1)基态Ga的核外电子排布式为[Ar]3d104s24p1,转化为下列激发态时所需能量最少的是
________(填字母)。
A.
B.
C.D.
(2) 硫 酸 铜 分 别 和 氨 水 、 EDTA[(HOOCCH )NCH CHN(CH COOH)] 可 形 成 配 合 物
2 2 2 2 2 2
[Cu(NH )(H O) ]SO 、[Cu(EDTA)]SO 。
3 4 2 2 4 4
①SO的空间结构为____________,EDTA中碳原子杂化方式为________________。
②在[Cu(NH )(H O) ]SO 化合物中,阳离子呈轴向狭长的八面体结构(如图),该阳离子中存
3 4 2 2 4
在的化学键类型为______________,该化合物加热时首先失去的组分是______________。
(3)人体代谢甲硒醇(CHSeH)后可增加抗癌活性,下表中有机物沸点不同的原因为
3
_______________________________________________________________________________
_______________________________________________________________________________
。
有机物 甲醇 甲硫醇(CHSH) 甲硒醇
3
沸点/℃ 64.7 5.95 25.05
(4)四方晶系CuInSe 的晶胞结构如图所示,晶胞参数为a=b=m pm,c=2m pm,晶胞棱边
2
夹角均为90°。设阿伏加德罗常数的值为N ,CuInSe 的相对分子质量为M,则该晶体密度ρ
A 2
=________g·cm-3 (用含有m、M和N 的代数式表示)。该晶胞中,原子坐标分别为2号Cu
A
原子(0,0.5,0.25),3号In原子(0,0.5,0.75),晶体中与单个In键合的Se有________个。
4.(2022·太原模拟)我国科学家研究了具有高稳定性的二维硼烯氧化物(B O)的超导电性。
m n
回答下列问题:
(1)第一电离能介于B、N之间的第二周期元素为______________(填元素符号)。
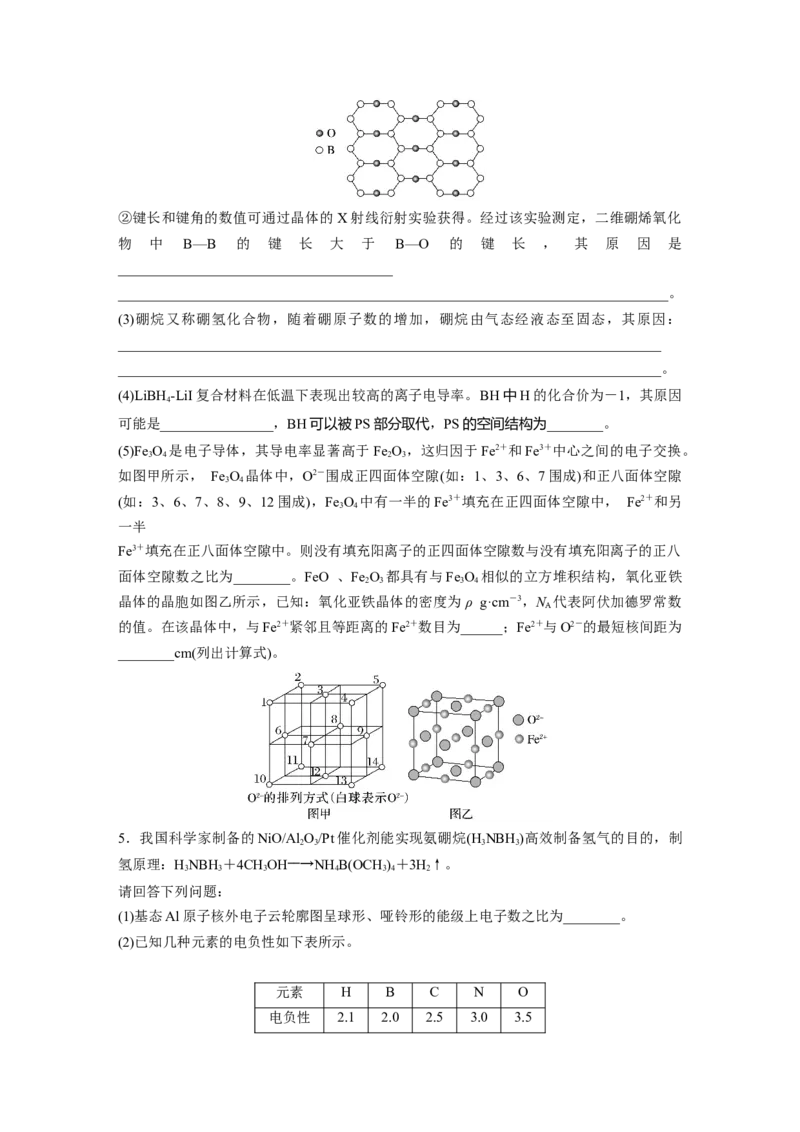
(2)①已知二维硼烯氧化物的部分结构如图所示,则该氧化物的化学式为________,其中硼
原子的杂化轨道类型为________。②键长和键角的数值可通过晶体的X射线衍射实验获得。经过该实验测定,二维硼烯氧化
物 中 B—B 的 键 长 大 于 B—O 的 键 长 , 其 原 因 是
_______________________________________
______________________________________________________________________________。
(3)硼烷又称硼氢化合物,随着硼原子数的增加,硼烷由气态经液态至固态,其原因:
_____________________________________________________________________________
_____________________________________________________________________________。
(4)LiBH -LiI复合材料在低温下表现出较高的离子电导率。BH中H的化合价为-1,其原因
4
可能是________________,BH可以被PS部分取代,PS的空间结构为________。
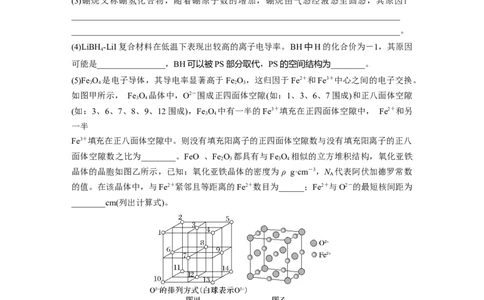
(5)Fe O 是电子导体,其导电率显著高于Fe O ,这归因于Fe2+和Fe3+中心之间的电子交换。
3 4 2 3
如图甲所示, Fe O 晶体中,O2-围成正四面体空隙(如:1、3、6、7围成)和正八面体空隙
3 4
(如:3、6、7、8、9、12围成),Fe O 中有一半的Fe3+填充在正四面体空隙中, Fe2+和另
3 4
一半
Fe3+填充在正八面体空隙中。则没有填充阳离子的正四面体空隙数与没有填充阳离子的正八
面体空隙数之比为________。FeO 、Fe O 都具有与Fe O 相似的立方堆积结构,氧化亚铁
2 3 3 4
晶体的晶胞如图乙所示,已知:氧化亚铁晶体的密度为 ρ g·cm-3,N 代表阿伏加德罗常数
A
的值。在该晶体中,与Fe2+紧邻且等距离的Fe2+数目为______;Fe2+与O2-的最短核间距为
________cm(列出计算式)。
5.我国科学家制备的NiO/Al O/Pt催化剂能实现氨硼烷(H NBH )高效制备氢气的目的,制
2 3 3 3
氢原理:HNBH +4CHOH――→NH B(OCH )+3H↑。
3 3 3 4 3 4 2
请回答下列问题:
(1)基态Al原子核外电子云轮廓图呈球形、哑铃形的能级上电子数之比为________。
(2)已知几种元素的电负性如下表所示。
元素 H B C N O
电负性 2.1 2.0 2.5 3.0 3.5①上述制氢反应中,有________种元素的原子采取sp3杂化。
②NH 中键角∠HNH________(填“大于”“小于”或“等于”)H NBH 中键角∠HNH。
3 3 3
③B、C、N、O的电负性依次增大,其主要原因是
_____________________________________________________________________________
_____________________________________________________________________________。
④在氨硼烷中,H—B中H带部分__________(填“正”或“负”)电荷。
(3)某有机硼化合物的结构简式如图1所示,1 mol该有机物中含________mol σ键。组成该
有机物的第二周期元素第一电离能由大到小的顺序为______________(填元素符号)。
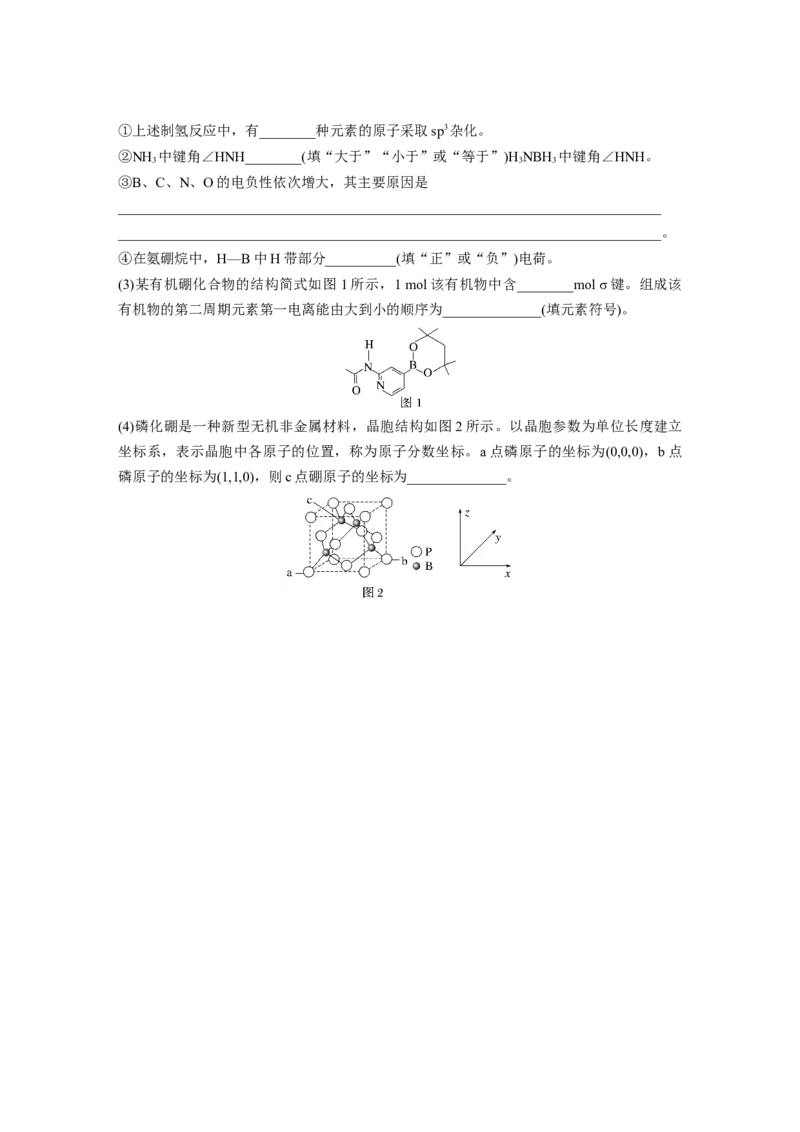
(4)磷化硼是一种新型无机非金属材料,晶胞结构如图2所示。以晶胞参数为单位长度建立
坐标系,表示晶胞中各原子的位置,称为原子分数坐标。a点磷原子的坐标为(0,0,0),b点
磷原子的坐标为(1,1,0),则c点硼原子的坐标为______________。