文档内容
第 37 讲 物质结构与性质填空题突破
[复习目标] 1.明确物质结构与性质填空题的题型特点和常考热点。2.掌握解答物质结构与
性质填空题的思维模式,提升综合运用物质结构与性质知识分析问题的能力。
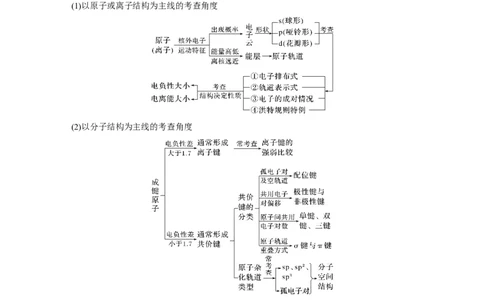
物质结构与性质填空题中的各小题之间相对独立,主要考查原子结构与性质、分子结构与性
质、晶体结构与性质,具体考查角度如下:
(1)以原子或离子结构为主线的考查角度
(2)以分子结构为主线的考查角度
(3)以晶体结构为主线的考查角度1.(2022·西安模拟)硒(Se)是一种有重要作用的元素,可以形成多种化合物。
(1)基态硒原子的核外电子排布式为_________________________________________。
(2)H SeO 的中心原子杂化类型是________,SeO的空间结构是________。
2 3
(3)H Se属于________(填“极性”或“非极性”)分子。
2
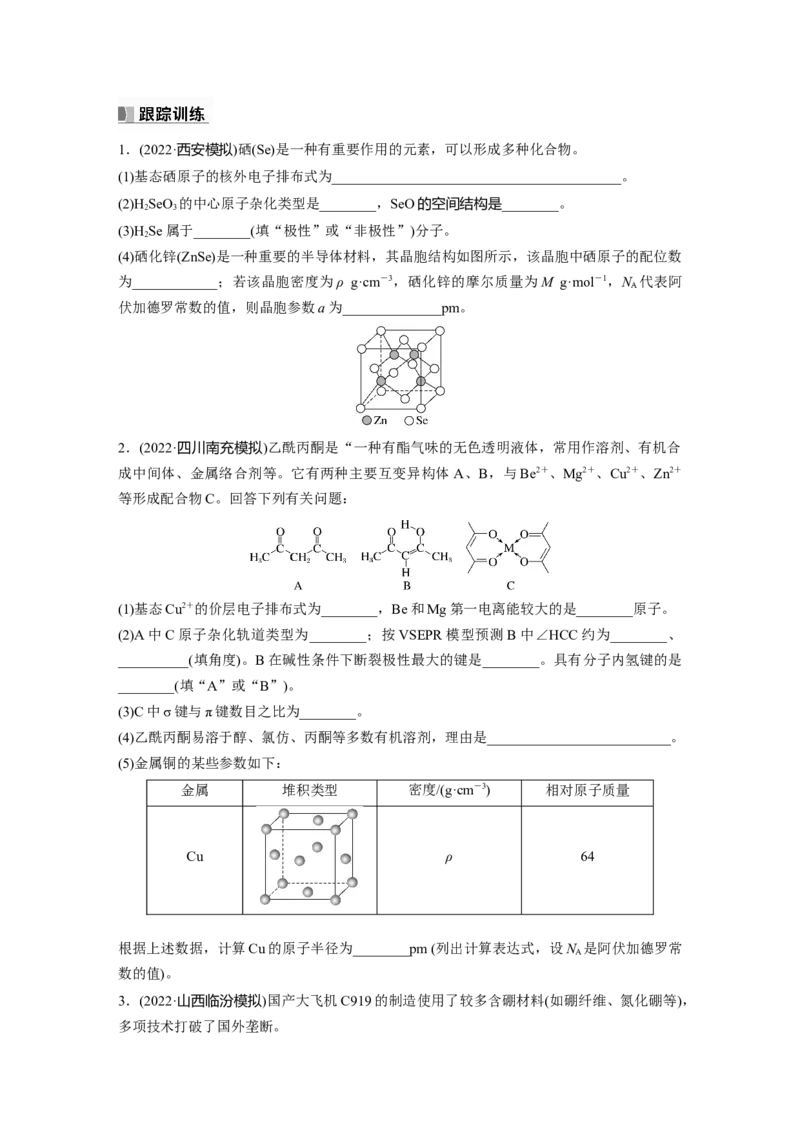
(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数
为____________;若该晶胞密度为ρ g·cm-3,硒化锌的摩尔质量为M g·mol-1,N 代表阿
A
伏加德罗常数的值,则晶胞参数a为______________pm。
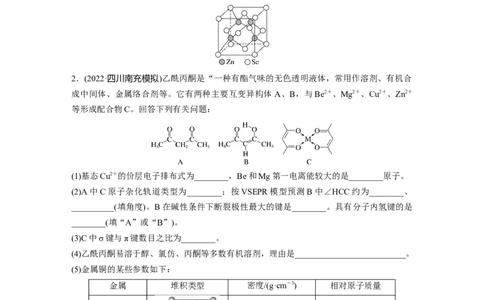
2.(2022·四川南充模拟)乙酰丙酮是“一种有酯气味的无色透明液体,常用作溶剂、有机合
成中间体、金属络合剂等。它有两种主要互变异构体 A、B,与Be2+、Mg2+、Cu2+、Zn2+
等形成配合物C。回答下列有关问题:
(1)基态Cu2+的价层电子排布式为________,Be和Mg第一电离能较大的是________原子。
(2)A中C原子杂化轨道类型为________;按VSEPR模型预测B中∠HCC约为________、
__________(填角度)。B在碱性条件下断裂极性最大的键是________。具有分子内氢键的是
________(填“A”或“B”)。
(3)C中σ键与π键数目之比为________。
(4)乙酰丙酮易溶于醇、氯仿、丙酮等多数有机溶剂,理由是__________________________。
(5)金属铜的某些参数如下:
金属 堆积类型 密度/(g·cm-3) 相对原子质量
Cu ρ 64
根据上述数据,计算Cu的原子半径为________pm (列出计算表达式,设N 是阿伏加德罗常
A
数的值)。
3.(2022·山西临汾模拟)国产大飞机C919的制造使用了较多含硼材料(如硼纤维、氮化硼等),
多项技术打破了国外垄断。(1)原子的能量由核电荷数、电子数、____________三个因素共同决定;基态B原子的核外
电子填充在________个轨道中。
(2)耐高温材料立方BN制备流程中用到NH 、BCl 和触媒剂Ca B N。
3 3 3 2 4
①Ca、B、N三种元素电负性从大到小的顺序为______________。
②BCl 中B原子的________轨道与Cl原子的________轨道形成σ键;形成BCl 过程中基态
3 3
B 原子价电子层上的电子先激发,再杂化,激发后 B 原子的价层电子轨道表示式为
________________________________________________________________________。
③BCl 在四氯化碳中的溶解度远大于NH ,原因是
3 3
________________________________________________________________________。
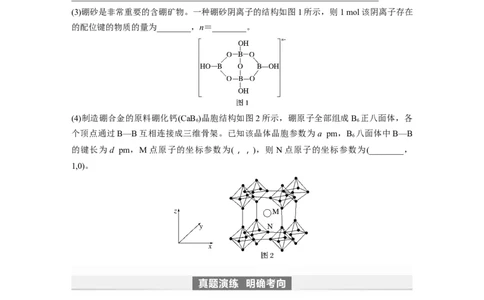
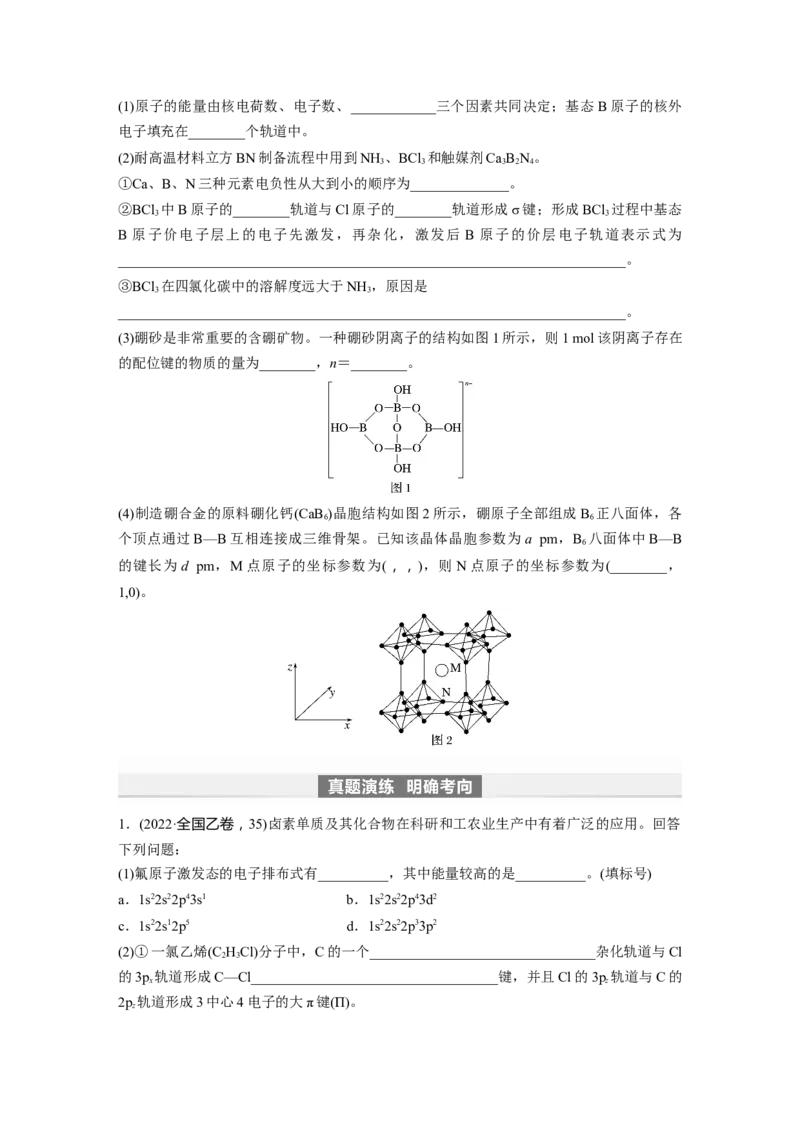
(3)硼砂是非常重要的含硼矿物。一种硼砂阴离子的结构如图1所示,则1 mol该阴离子存在
的配位键的物质的量为________,n=________。
(4)制造硼合金的原料硼化钙(CaB )晶胞结构如图2所示,硼原子全部组成B 正八面体,各
6 6
个顶点通过B—B互相连接成三维骨架。已知该晶体晶胞参数为a pm,B 八面体中B—B
6
的键长为d pm,M点原子的坐标参数为(,,),则N点原子的坐标参数为(________,
1,0)。
1.(2022·全国乙卷,35)卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答
下列问题:
(1)氟原子激发态的电子排布式有__________,其中能量较高的是__________。(填标号)
a.1s22s22p43s1 b.1s22s22p43d2
c.1s22s12p5 d.1s22s22p33p2
(2)①一氯乙烯(C HCl)分子中,C的一个________________________________杂化轨道与Cl
2 3
的3p 轨道形成C—Cl___________________________________键,并且Cl的3p 轨道与C的
x z
2p 轨道形成3中心4电子的大π键(Π)。
z②一氯乙烷(C HCl)、一氯乙烯(C HCl)、一氯乙炔(C HCl)分子中,C—Cl键长的顺序是
2 5 2 3 2
____________________________________________________,理由:(ⅰ)C的杂化轨道中 s
成分越多,形成的C—Cl越强;(ⅱ)_________________________________ ____________。
(3)卤化物 CsICl 受热发生非氧化还原反应,生成无色晶体 X 和红棕色液体 Y。X 为
2
__________。解释X的熔点比Y高的原因_________________________________________。
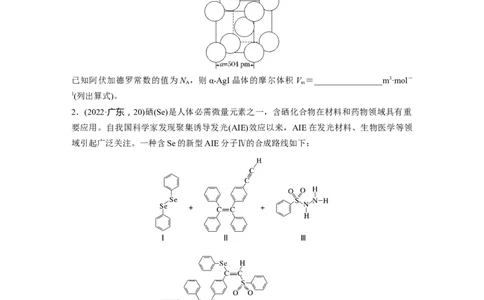
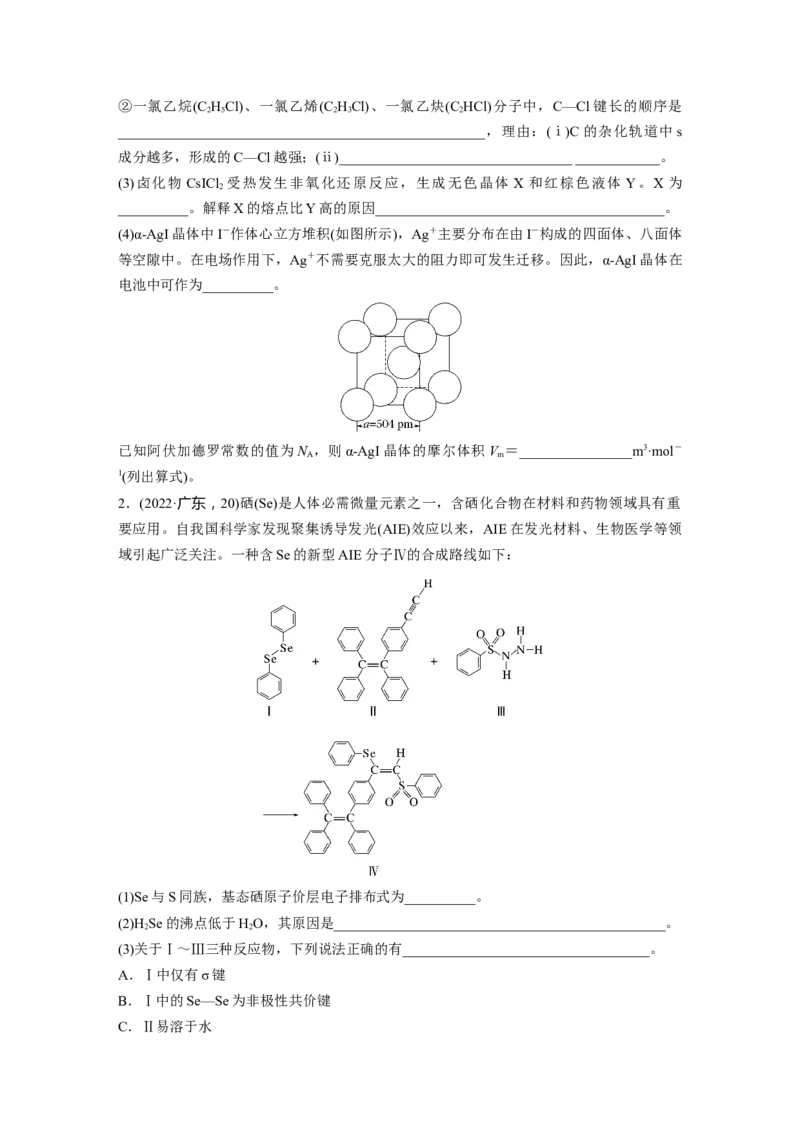
(4)α-AgI晶体中I-作体心立方堆积(如图所示),Ag+主要分布在由I-构成的四面体、八面体
等空隙中。在电场作用下,Ag+不需要克服太大的阻力即可发生迁移。因此,α-AgI晶体在
电池中可作为__________。
已知阿伏加德罗常数的值为N ,则α-AgI晶体的摩尔体积V =________________m3·mol-
A m
1(列出算式)。
2.(2022·广东,20)硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重
要应用。自我国科学家发现聚集诱导发光(AIE)效应以来,AIE在发光材料、生物医学等领
域引起广泛关注。一种含Se的新型AIE分子Ⅳ的合成路线如下:
(1)Se与S同族,基态硒原子价层电子排布式为__________。
(2)H Se的沸点低于HO,其原因是_______________________________________________。
2 2
(3)关于Ⅰ~Ⅲ三种反应物,下列说法正确的有___________________________________。
A.Ⅰ中仅有σ键
B.Ⅰ中的Se—Se为非极性共价键
C.Ⅱ易溶于水D.Ⅱ 中原子的杂化轨道类型只有sp与sp2
E.Ⅰ~Ⅲ 含有的元素中,O电负性最大
(4)Ⅳ 中具有孤电子对的原子有__________。
(5)硒的两种含氧酸的酸性强弱为HSeO_____________(填“>”或“<”)H SeO 。研究发现,
2 4 2 3
给小鼠喂食适量硒酸钠(Na SeO)可减轻重金属铊引起的中毒。SeO的空间结构为_______。
2 4
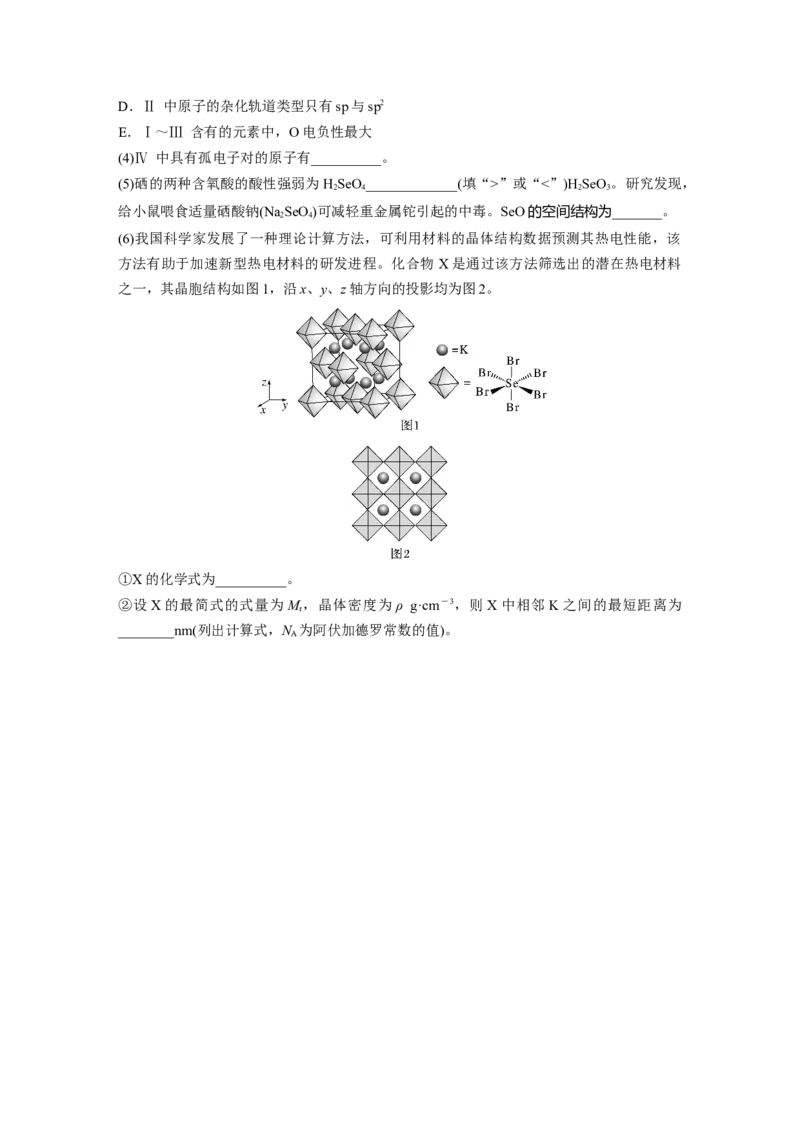
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该
方法有助于加速新型热电材料的研发进程。化合物 X是通过该方法筛选出的潜在热电材料
之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
①X的化学式为__________。
②设X的最简式的式量为 M,晶体密度为ρ g·cm-3,则X中相邻K之间的最短距离为
r
________nm(列出计算式,N 为阿伏加德罗常数的值)。
A