文档内容
第 40 讲 原电池 化学电源
[复习目标] 1.理解原电池的工作原理。2.了解常见化学电源的种类及其工作原理。3.能够书
写常见化学电源的电极反应式和总反应方程式。
考点一 原电池工作原理及应用
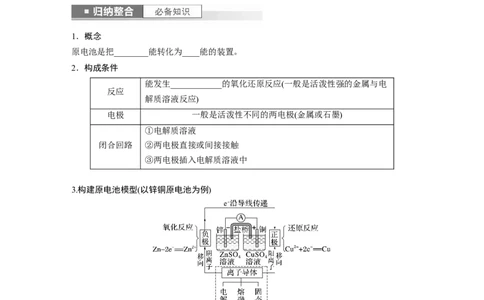
1.概念
原电池是把________能转化为____能的装置。
2.构成条件
能发生____________的氧化还原反应(一般是活泼性强的金属与电
反应
解质溶液反应)
电极 一般是活泼性不同的两电极(金属或石墨)
①电解质溶液
闭合回路 ②两电极直接或间接接触
③两电极插入电解质溶液中
3.构建原电池模型(以锌铜原电池为例)
盐桥的组成和作用
①盐桥中装有含KCl饱和溶液的琼胶,离子可在其中自由移动。
②盐桥的作用:a.连接内电路,____________;b.____________,使原电池不断产生电流。
③盐桥中离子移向:阴离子移向________,阳离子移向________。4.原电池原理的应用
(1)设计原电池
首先将氧化还原反应分成两个半反应,其次根据原电池的反应特点, 结合两个半反应找出
正、负极材料和电解质溶液。
应用举例
根据反应2FeCl +Cu===2FeCl +CuCl 设计原电池,在方框中画出装置图,指出电极材料和
3 2 2
电解质溶液,写出电极反应式:
①不含盐桥 ②含盐桥
负极:________________
正极:________________
(2)比较金属的活动性强弱:原电池中,负极一般是活动性________的金属,正极一般是活
动性________的金属(或能导电的非金属)。
(3)加快化学反应速率:氧化还原反应形成原电池时,反应速率加快。
(4)用于金属的防护:将需要保护的金属制品作原电池的________而受到保护。
1.盐桥是所有原电池构成的必要条件( )
2.原电池内部电解质中的阴离子一定移向负极,阳离子一定移向正极( )
3.构成原电池两极的电极材料一定是活泼性不同的金属( )
4.原电池中负极失去电子的总数一定等于正极得到电子的总数( )
5.使用盐桥可以提高电池的效率( )
一、原电池的设计及工作原理
1.(2022·杭州模拟)实验a:将铜片、锌片和稀硫酸组成单液原电池,铜片、锌片表面均产
生气泡。实验b:将锌片在稀HgCl 溶液中浸泡几分钟,锌片表面形成锌汞合金,再与铜片、
2
稀硫酸组成单液原电池,只有铜片表面产生气泡。下列有关说法不正确的是( )
A.实验a中锌片表面产生气泡对应的能量转化形式是化学能转化为电能
B.实验b中铜片表面产生气泡对应的能量转化形式是化学能转化为电能
C.实验a、b中原电池总反应的离子方程式均为Zn+2H+===Zn2++H↑
2
D.锌片经HgCl 溶液处理后,有利于更多的化学能转化为电能
2
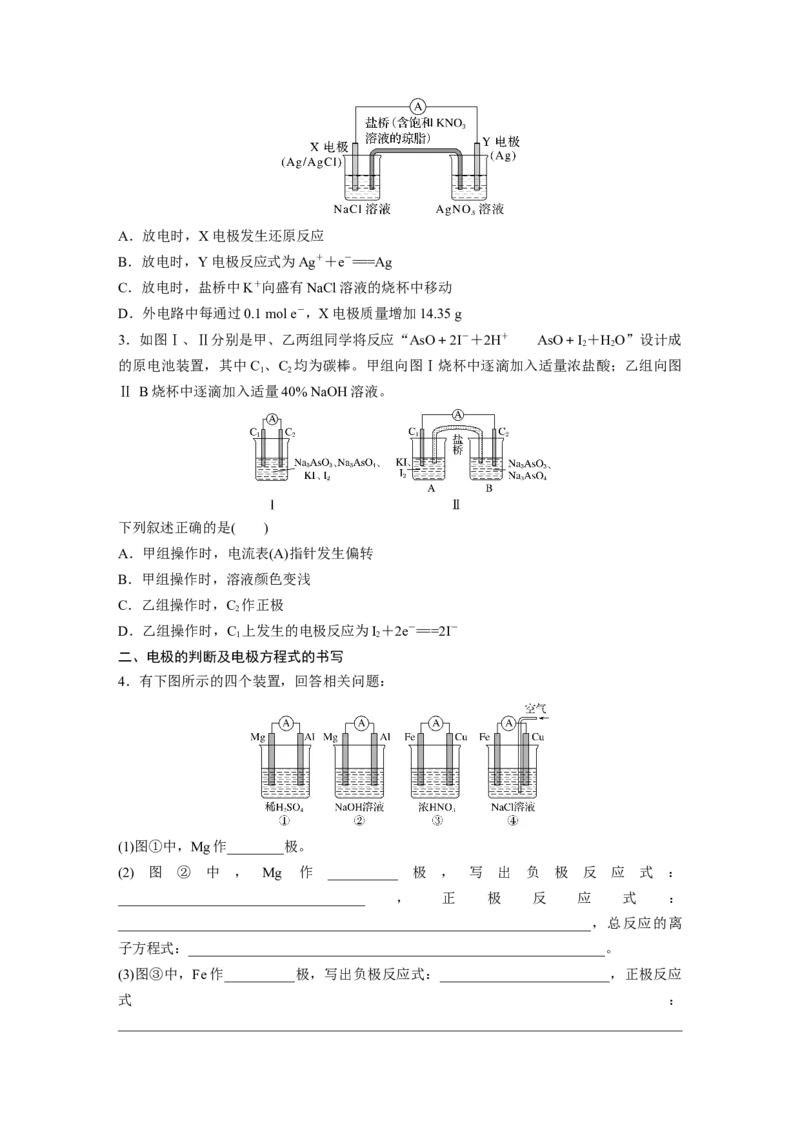
2.(2022·苏州模拟)某学习小组设计如图所示原电池装置。该电池总反应为 Cl-+Ag+
===AgCl↓。下列说法正确的是( )A.放电时,X电极发生还原反应
B.放电时,Y电极反应式为Ag++e-===Ag
C.放电时,盐桥中K+向盛有NaCl溶液的烧杯中移动
D.外电路中每通过0.1 mol e-,X电极质量增加14.35 g
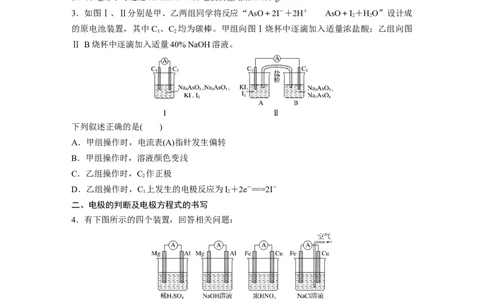
3.如图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO+2I-+2H+AsO+I +HO”设计成
2 2
的原电池装置,其中C 、C 均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图
1 2
Ⅱ B烧杯中逐滴加入适量40% NaOH溶液。
下列叙述正确的是( )
A.甲组操作时,电流表(A)指针发生偏转
B.甲组操作时,溶液颜色变浅
C.乙组操作时,C 作正极
2
D.乙组操作时,C 上发生的电极反应为I+2e-===2I-
1 2
二、电极的判断及电极方程式的书写
4.有下图所示的四个装置,回答相关问题:
(1)图①中,Mg作________极。
(2) 图 ② 中 , Mg 作 __________ 极 , 写 出 负 极 反 应 式 :
___________________________________ , 正 极 反 应 式 :
___________________________________________________________________,总反应的离
子方程式:___________________________________________________________。
(3)图③中,Fe作__________极,写出负极反应式:________________________,正极反应
式 :
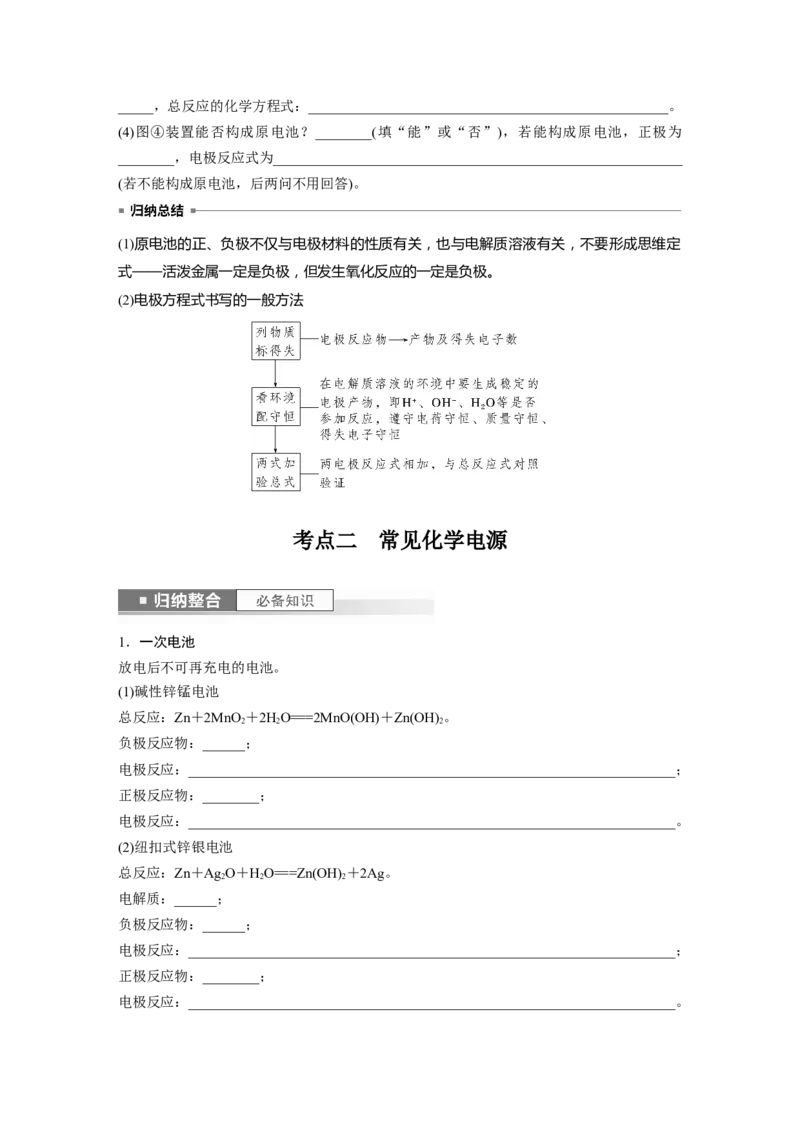
_____________________________________________________________________________________,总反应的化学方程式:___________________________________________________。
(4)图④装置能否构成原电池?________(填“能”或“否”),若能构成原电池,正极为
________,电极反应式为__________________________________________________________
(若不能构成原电池,后两问不用回答)。
(1)原电池的正、负极不仅与电极材料的性质有关,也与电解质溶液有关,不要形成思维定
式——活泼金属一定是负极,但发生氧化反应的一定是负极。
(2)电极方程式书写的一般方法
考点二 常见化学电源
1.一次电池
放电后不可再充电的电池。
(1)碱性锌锰电池
总反应:Zn+2MnO +2HO===2MnO(OH)+Zn(OH) 。
2 2 2
负极反应物:______;
电极反应:_____________________________________________________________________;
正极反应物:________;
电极反应:_____________________________________________________________________。
(2)纽扣式锌银电池
总反应:Zn+Ag O+HO===Zn(OH) +2Ag。
2 2 2
电解质:______;
负极反应物:______;
电极反应:_____________________________________________________________________;
正极反应物:________;
电极反应:_____________________________________________________________________。2.二次电池
放电后可以再充电而反复使用的电池,又称为可充电电池或蓄电池。
应用举例
铅酸蓄电池是常见的二次电池,负极反应物是______,正极反应物是______。总反应为Pb
+PbO +2HSO 2PbSO +2HO。
2 2 4 4 2
(1)放电时:
负极:________________________________________________________________________;
正极:________________________________________________________________________。
(2)充电时:
阴极:________________________________________________________________________;
阳极:________________________________________________________________________。
提醒 充电时电极的连接,负接负作阴极,正接正作阳极。
3.燃料电池
(1)氢氧燃料电池是目前最成熟的燃料电池,常见的燃料除 H 外,还有CO、水煤气(CO和
2
H)、烃类(如CH)、醇类(如CHOH)、醚类(如CHOCH )、氨(NH )、肼(H N—NH)等。如
2 4 3 3 3 3 2 2
无特别提示,燃料电池反应原理类似于燃料的燃烧。
(2)燃料电池的电解质常有四种类型,酸性溶液、碱性溶液、固体电解质(可传导O2-)、熔融
碳酸盐,不同电解质会对总反应式、电极反应式有影响。
(3)以甲醇为燃料,写出下列介质中的电极反应式。
①酸性溶液(或含质子交换膜)
②碱性溶液
③固体氧化物(其中O2-可以在固体介质中自由移动)
④熔融碳酸盐(CO)
1.铅酸蓄电池放电时,正极与负极质量均增加( )
2.二次电池充电时,二次电池的阴极连接电源的负极,发生还原反应( )
3.铅酸蓄电池放电时的负极和充电时的阳极均发生还原反应( )
4.燃料电池工作时燃料在电池中燃烧,然后热能转化为电能( )
5.在原电池中,正极本身一定不参与电极反应,负极本身一定要发生氧化反应( )
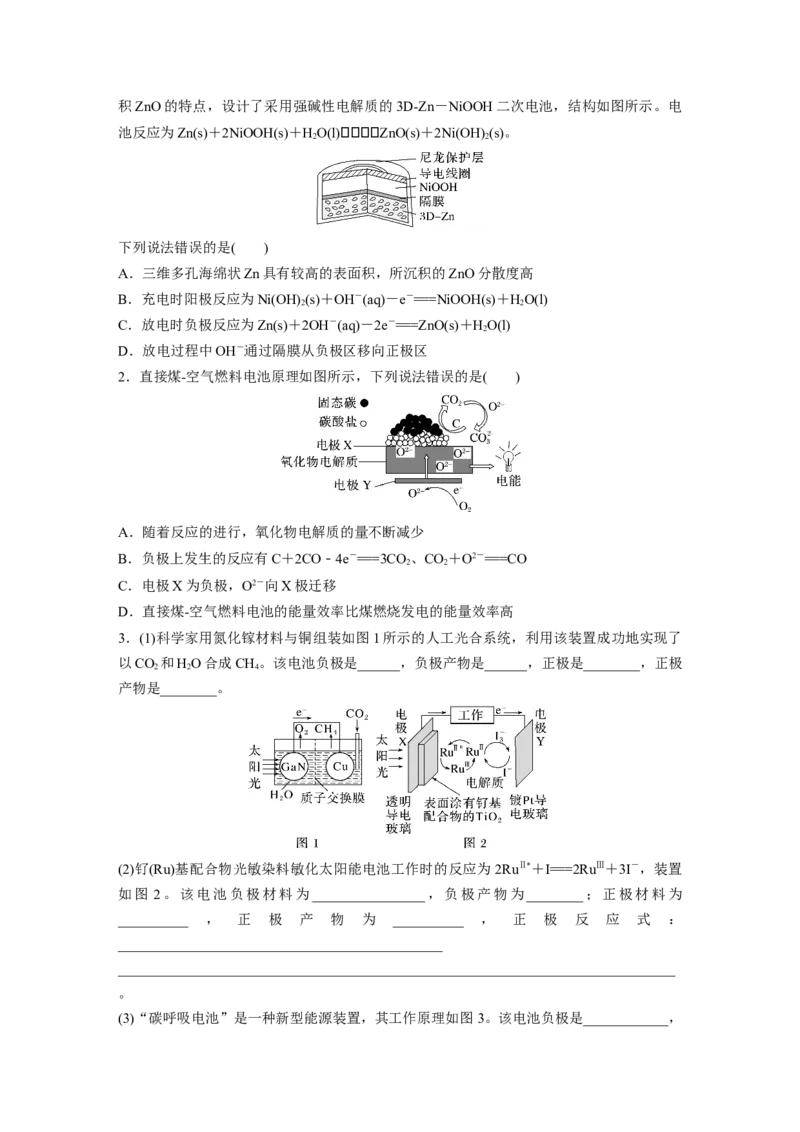
1.为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3D-Zn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3D-Zn-NiOOH二次电池,结构如图所示。电
池反应为Zn(s)+2NiOOH(s)+HO(l)ZnO(s)+2Ni(OH) (s)。
2 2
下列说法错误的是( )
A.三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B.充电时阳极反应为Ni(OH) (s)+OH-(aq)-e-===NiOOH(s)+HO(l)
2 2
C.放电时负极反应为Zn(s)+2OH-(aq)-2e-===ZnO(s)+HO(l)
2
D.放电过程中OH-通过隔膜从负极区移向正极区
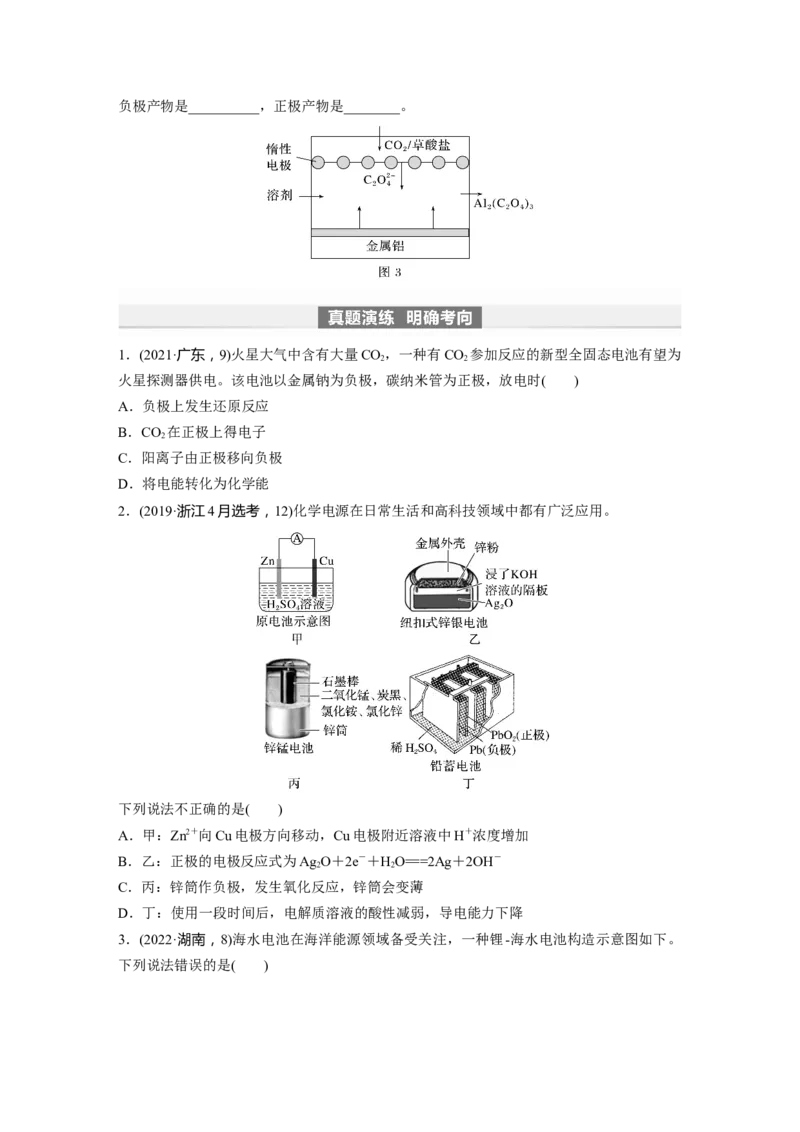
2.直接煤-空气燃料电池原理如图所示,下列说法错误的是( )
A.随着反应的进行,氧化物电解质的量不断减少
B.负极上发生的反应有C+2CO-4e-===3CO、CO+O2-===CO
2 2
C.电极X为负极,O2-向X极迁移
D.直接煤-空气燃料电池的能量效率比煤燃烧发电的能量效率高
3.(1)科学家用氮化镓材料与铜组装如图1所示的人工光合系统,利用该装置成功地实现了
以CO 和HO合成CH。该电池负极是______,负极产物是______,正极是________,正极
2 2 4
产物是________。
(2)钌(Ru)基配合物光敏染料敏化太阳能电池工作时的反应为2RuⅡ*+I===2RuⅢ+3I-,装置
如图 2。该电池负极材料为________________,负极产物为________;正极材料为
__________ , 正 极 产 物 为 __________ , 正 极 反 应 式 :
______________________________________________
_______________________________________________________________________________
。
(3)“碳呼吸电池”是一种新型能源装置,其工作原理如图3。该电池负极是____________,负极产物是__________,正极产物是________。
1.(2021·广东,9)火星大气中含有大量CO,一种有CO 参加反应的新型全固态电池有望为
2 2
火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时( )
A.负极上发生还原反应
B.CO 在正极上得电子
2
C.阳离子由正极移向负极
D.将电能转化为化学能
2.(2019·浙江4月选考,12)化学电源在日常生活和高科技领域中都有广泛应用。
下列说法不正确的是( )
A.甲:Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B.乙:正极的电极反应式为Ag O+2e-+HO===2Ag+2OH-
2 2
C.丙:锌筒作负极,发生氧化反应,锌筒会变薄
D.丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
3.(2022·湖南,8)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。
下列说法错误的是( )A.海水起电解质溶液作用
B.N极仅发生的电极反应:2HO+2e-===2OH-+H↑
2 2
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
4.(2021·山东,10)以 KOH 溶液为离子导体,分别组成 CHOH—O 、NH—O 、
3 2 2 4 2
(CH)NNH—O 清洁燃料电池,下列说法正确的是( )
3 2 2 2
A.放电过程中,K+均向负极移动
B.放电过程中,KOH物质的量均减小
C.消耗等质量燃料,(CH)NNH—O 燃料电池的理论放电量最大
3 2 2 2
D.消耗1 mol O 时,理论上NH—O 燃料电池气体产物的体积在标准状况下为11.2 L
2 2 4 2