文档内容
1.相同温度和压强下,关于物质熵的大小比较合理的是( )
A.1 mol CH (g)<1 mol H (g)
4 2
B.1 mol H O(g)<2 mol H O(g)
2 2
C.1 mol H O(s)>1 mol H O(l)
2 2
D.1 mol C(金刚石,s)>1 mol C(石墨,s)
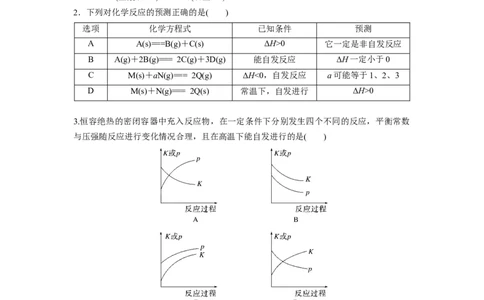
2.下列对化学反应的预测正确的是( )
选项 化学方程式 已知条件 预测
A A(s)===B(g)+C(s) ΔH>0 它一定是非自发反应
B A(g)+2B(g)=== 2C(g)+3D(g) 能自发反应 ΔH一定小于0
C M(s)+aN(g)=== 2Q(g) ΔH<0,自发反应 a可能等于1、2、3
D M(s)+N(g)=== 2Q(s) 常温下,自发进行 ΔH>0
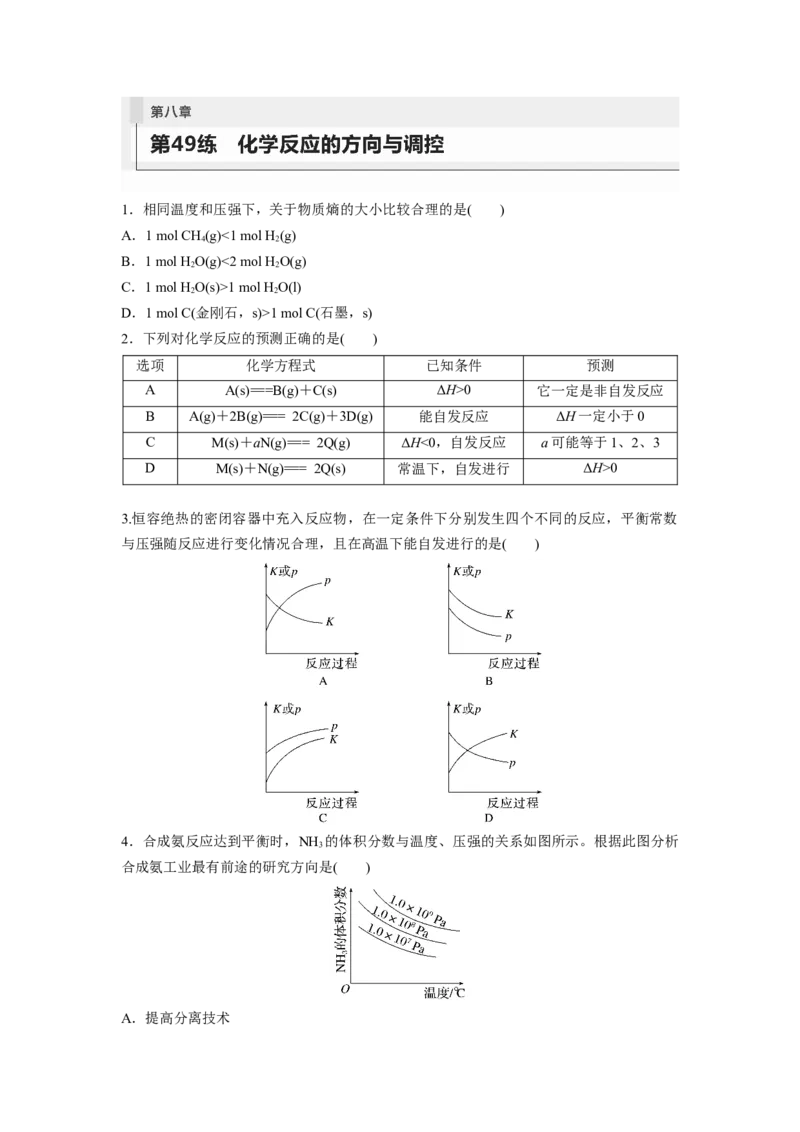
3.恒容绝热的密闭容器中充入反应物,在一定条件下分别发生四个不同的反应,平衡常数
与压强随反应进行变化情况合理,且在高温下能自发进行的是( )
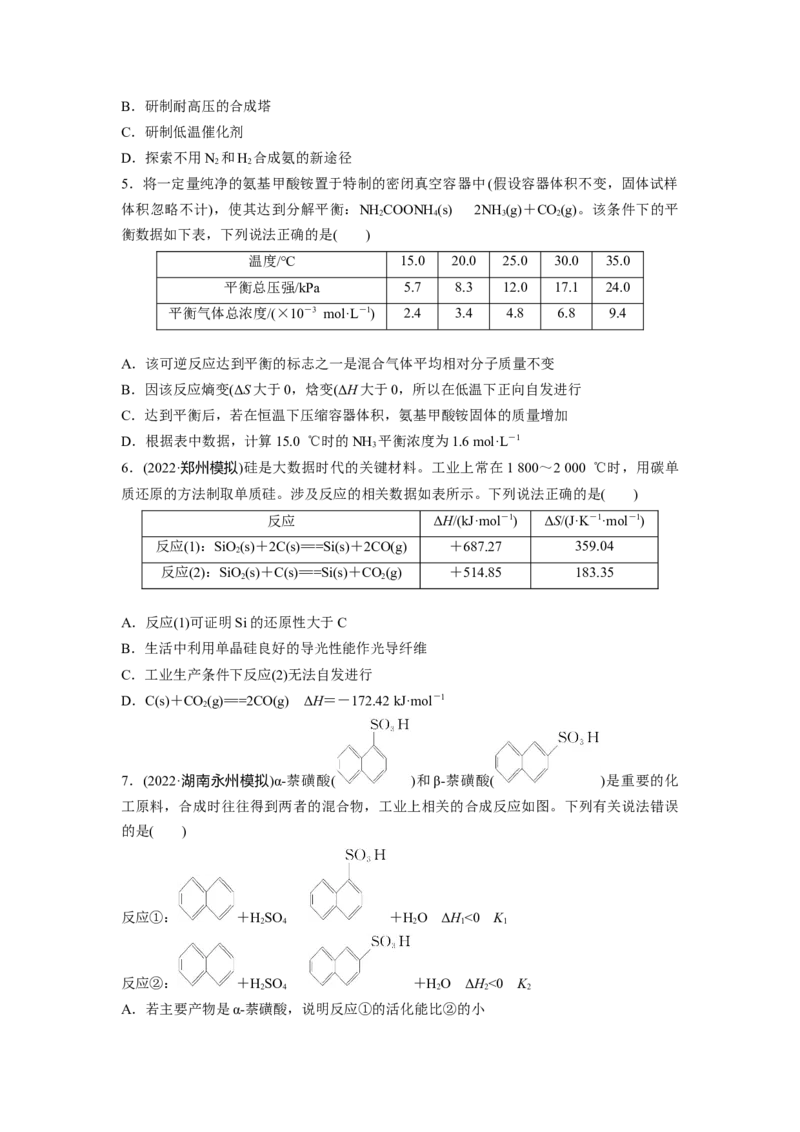
4.合成氨反应达到平衡时,NH 的体积分数与温度、压强的关系如图所示。根据此图分析
3
合成氨工业最有前途的研究方向是( )
A.提高分离技术B.研制耐高压的合成塔
C.研制低温催化剂
D.探索不用N 和H 合成氨的新途径
2 2
5.将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样
体积忽略不计),使其达到分解平衡:NH COONH(s)2NH (g)+CO(g)。该条件下的平
2 4 3 2
衡数据如下表,下列说法正确的是( )
温度/°C 15.0 20.0 25.0 30.0 35.0
平衡总压强/kPa 5.7 8.3 12.0 17.1 24.0
平衡气体总浓度/(×10-3 mol·L-1) 2.4 3.4 4.8 6.8 9.4
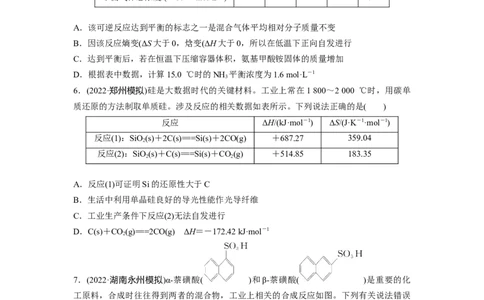
A.该可逆反应达到平衡的标志之一是混合气体平均相对分子质量不变
B.因该反应熵变(ΔS大于0,焓变(ΔH大于0,所以在低温下正向自发进行
C.达到平衡后,若在恒温下压缩容器体积,氨基甲酸铵固体的质量增加
D.根据表中数据,计算15.0 ℃时的NH 平衡浓度为1.6 mol·L-1
3
6.(2022·郑州模拟)硅是大数据时代的关键材料。工业上常在1 800~2 000 ℃时,用碳单
质还原的方法制取单质硅。涉及反应的相关数据如表所示。下列说法正确的是( )
反应 ΔH/(kJ·mol-1) ΔS/(J·K-1·mol-1)
反应(1):SiO(s)+2C(s)===Si(s)+2CO(g) +687.27 359.04
2
反应(2):SiO(s)+C(s)===Si(s)+CO(g) +514.85 183.35
2 2
A.反应(1)可证明Si的还原性大于C
B.生活中利用单晶硅良好的导光性能作光导纤维
C.工业生产条件下反应(2)无法自发进行
D.C(s)+CO(g)===2CO(g) ΔH=-172.42 kJ·mol-1
2
7.(2022·湖南永州模拟)α-萘磺酸( )和β-萘磺酸( )是重要的化
工原料,合成时往往得到两者的混合物,工业上相关的合成反应如图。下列有关说法错误
的是( )
反应①: +HSO +HO ΔH<0 K
2 4 2 1 1
反应②: +HSO +HO ΔH<0 K
2 4 2 2 2
A.若主要产物是α-萘磺酸,说明反应①的活化能比②的小B.平衡时α-萘磺酸和β-萘磺酸的物质的量浓度关系为=
C.在密闭容器中加入萘与硫酸,t min后反应达到平衡,用萘磺酸表示的反应速率为
D.α-萘磺酸与β-萘磺酸能相互转化
8.已知在100 kPa、298.15 K时,石灰石发生分解反应:
CaCO (s)===CaO(s)+CO(g) ΔH=+178.3 kJ·mol-1 ΔS=160.4 J·mol-1·K-1,则
3 2
(1)该反应________(填“能”或“不能”)正向自发进行。
(2)若温度能决定反应方向,则该反应正向自发进行的最低温度为________。
9.N 和H 生成NH 的反应为N(g)+H(g)NH (g) ΔH(298 K)=-46.2 kJ·mol-1
2 2 3 2 2 3
请回答:
(1)有利于提高合成氨平衡产率的条件有______(填字母)。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2) 、 、 为各组分的平衡分压,如 = ,p为平衡总压, 为平
衡系统中氨气的物质的量分数,N 、H 起始物质的量之比是1∶3,反应在恒定温度和总压
2 2
强p(单位是Pa)下进行,NH 的平衡产率是w,用分压代替物质的量浓度计算平衡常数K =
3 p
________________________________________________________________________。
10.(2022·重庆模拟)尿素[CO(NH)]是首个由无机物人工合成的有机物。
2 2
(1)已知:①2NH (g)+CO(g)===NH CONH (s) ΔH=-159.5 kJ·mol-1
3 2 2 2 4
②NH CONH (s)===CO(NH)(s)+HO(g) ΔH=+116.5 kJ·mol-1
2 2 4 2 2 2
则氨气与二氧化碳气体合成固态尿素和气态水的热化学方程式为________________
________________________________________________________________________。
(2)一定条件下,向容积恒定为2 L的密闭容器中加入0.10 mol CO 和0.40 mol NH ,发生反
2 3
应:2NH (g)+CO(g)CO(NH)(l)+HO(g),60 min开始达到平衡。反应中CO 的物质
3 2 2 2 2 2
的量随时间变化如下表所示:
时间/min 0 20 60 80
n(CO)/mol 0.10 0.06 0.04 0.04
2
①60 min内,上述反应的平均反应速率v(CO)=______________。
2
②NH 的平衡转化率为__________。
3
(3)一定条件下,恒容容器中,若原料气中的NH 和CO 的物质的量之比=x,发生反应:
3 2
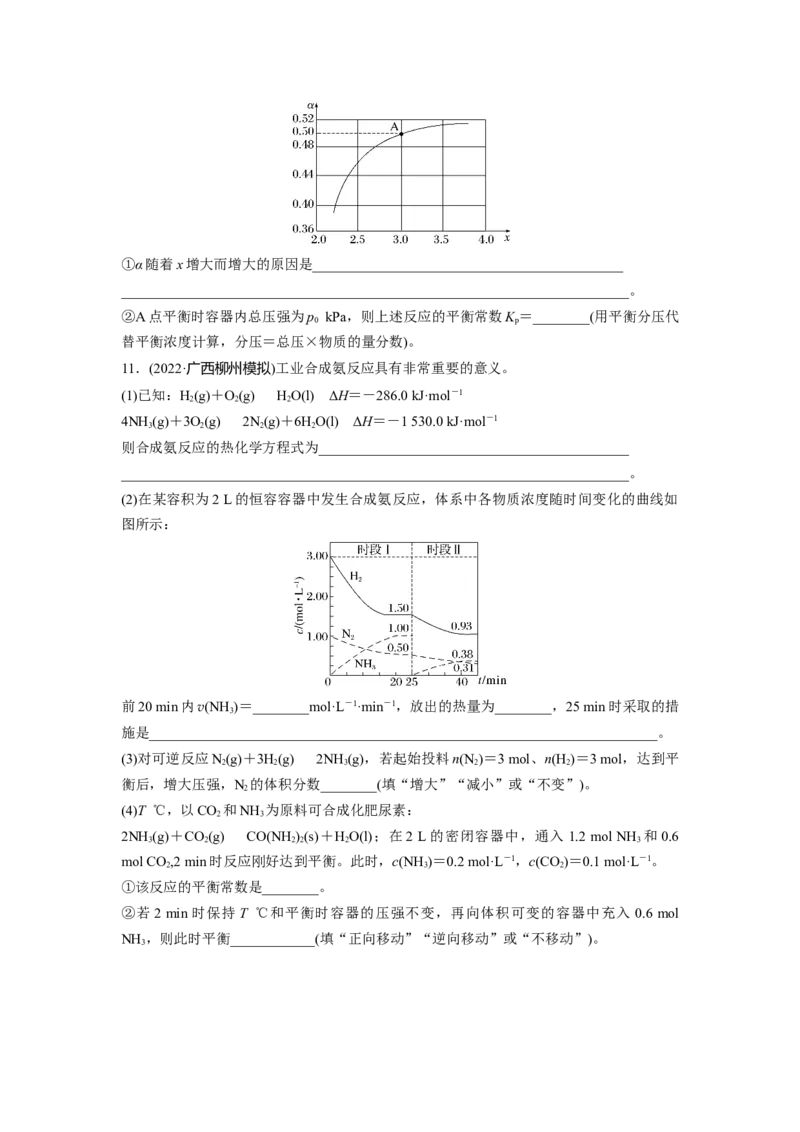
2NH (g)+CO(g)CO(NH)(l)+HO(g),x与CO 的平衡转化率(α)的关系如图所示:
3 2 2 2 2 2①α随着x增大而增大的原因是____________________________________________
________________________________________________________________________。
②A点平衡时容器内总压强为p kPa,则上述反应的平衡常数K =________(用平衡分压代
0 p
替平衡浓度计算,分压=总压×物质的量分数)。
11.(2022·广西柳州模拟)工业合成氨反应具有非常重要的意义。
(1)已知:H(g)+O(g)HO(l) ΔH=-286.0 kJ·mol-1
2 2 2
4NH (g)+3O(g)2N(g)+6HO(l) ΔH=-1 530.0 kJ·mol-1
3 2 2 2
则合成氨反应的热化学方程式为____________________________________________
________________________________________________________________________。
(2)在某容积为2 L的恒容容器中发生合成氨反应,体系中各物质浓度随时间变化的曲线如
图所示:
前20 min内v(NH )=________mol·L-1·min-1,放出的热量为________,25 min时采取的措
3
施是________________________________________________________________________。
(3)对可逆反应N(g)+3H(g)2NH (g),若起始投料n(N )=3 mol、n(H )=3 mol,达到平
2 2 3 2 2
衡后,增大压强,N 的体积分数________(填“增大”“减小”或“不变”)。
2
(4)T ℃,以CO 和NH 为原料可合成化肥尿素:
2 3
2NH (g)+CO(g)CO(NH)(s)+HO(l);在2 L的密闭容器中,通入 1.2 mol NH 和0.6
3 2 2 2 2 3
mol CO,2 min时反应刚好达到平衡。此时,c(NH )=0.2 mol·L-1,c(CO)=0.1 mol·L-1。
2 3 2
①该反应的平衡常数是________。
②若2 min时保持T ℃和平衡时容器的压强不变,再向体积可变的容器中充入 0.6 mol
NH ,则此时平衡____________(填“正向移动”“逆向移动”或“不移动”)。
3