文档内容
热点强化 20 电离常数的相关计算
1.电离常数与电离度的关系
已知25 ℃时,某浓度为c的一元弱酸HA的电离度为α,求该温度下的HA的电离常数
(K)。
a
________________________________________________________________________
________________________________________________________________________
2.计算电离常数的思维方法
(1)根据电离方程式,写出电离平衡常数表达式。
(2)根据题干信息,结合电荷守恒、元素质量守恒,找出各微粒的浓度,代入表达式即可。
(3)若有图像信息,可选择曲线上特殊点(能准确读出纵、横坐标的数值),确定各微粒的浓
度,最后代入平衡常数表达式计算。
题组一 根据溶液中微粒浓度的关系计算电离常数
1.(单一溶液)已知标准状况下,1 L水能溶解V L二氧化硫气体,且饱和溶液中的SO 有
2
与水反应生成HSO ,测得c(H+)=0.2 mol·L-1,计算该条件下的V=________(已知HSO
2 3 2 3
的第一步电离平衡常数K =0.02,忽略第二步电离和溶液体积的变化)。
a1
2.(混合溶液)(1)常温下,向a mol·L-1 CHCOONa溶液中滴加等体积的b mol·L-1盐酸使
3
溶液呈中性(不考虑盐酸和醋酸的挥发),则醋酸的电离常数K=______________(用含a和
a
b的代数式表示)。
(2)常温下,将a mol·L-1的醋酸与b mol·L-1的Ba(OH) 溶液等体积混合,充分反应后,溶
2
液中存在2c(Ba2+)=c(CHCOO-),则该混合溶液中醋酸的电离常数K=_____________(用
3 a
含a和b的代数式表示)。
题组二 利用图像节点或交点计算电离常数
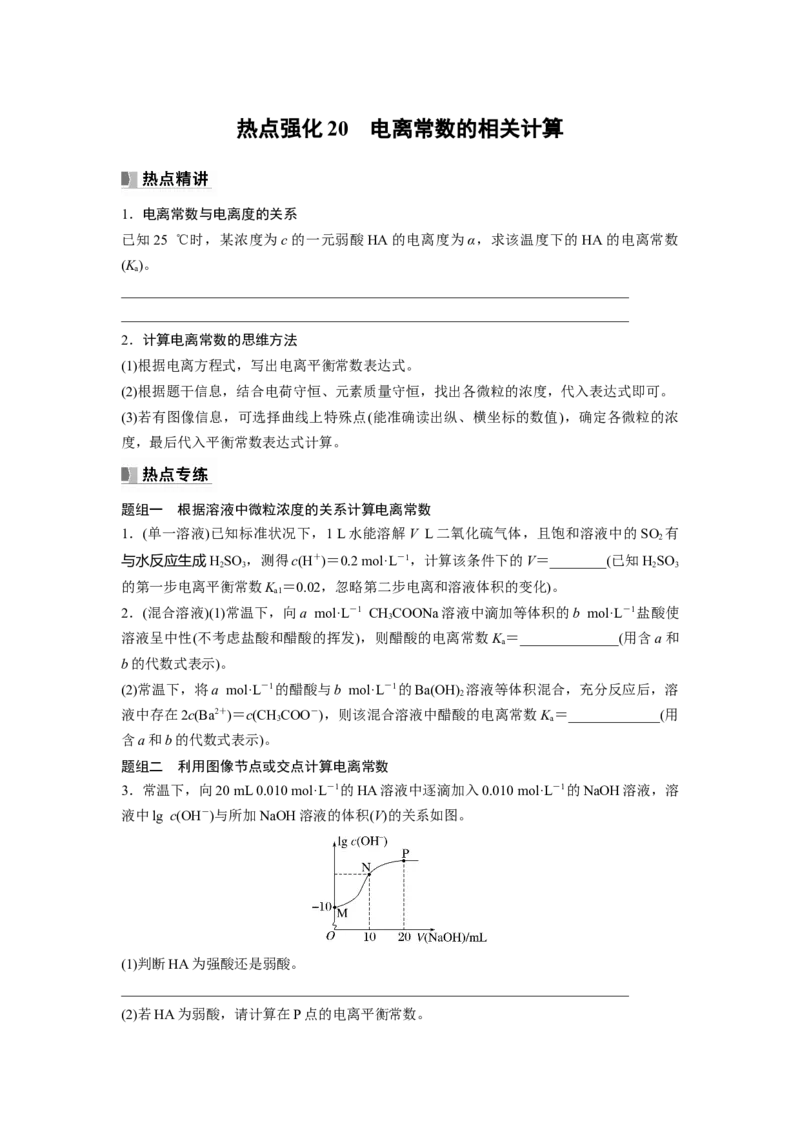
3.常温下,向20 mL 0.010 mol·L-1的HA溶液中逐滴加入0.010 mol·L-1的NaOH溶液,溶
液中lg c(OH-)与所加NaOH溶液的体积(V)的关系如图。
(1)判断HA为强酸还是弱酸。
________________________________________________________________________
(2)若HA为弱酸,请计算在P点的电离平衡常数。________________________________________________________________________
________________________________________________________________________
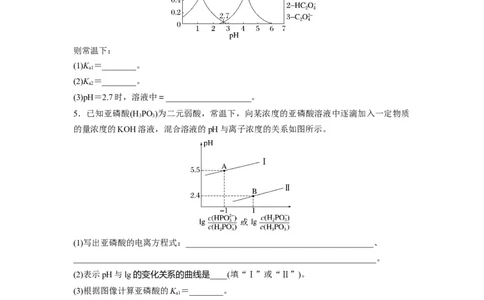
4.已知草酸为二元弱酸:HC OHC O+H+
2 2 4 2
K ,HC OC O+H+ K ,常温下,向某浓度的 HC O 溶液中逐滴加入一定浓度的
a1 2 2 a2 2 2 4
KOH溶液,所得溶液中HC O、HC O、C O三种微粒的物质的量分数(δ)与溶液pH的关系
2 2 4 2 2
如图所示。
则常温下:
(1)K =________。
a1
(2)K =________。
a2
(3)pH=2.7时,溶液中=____________________。
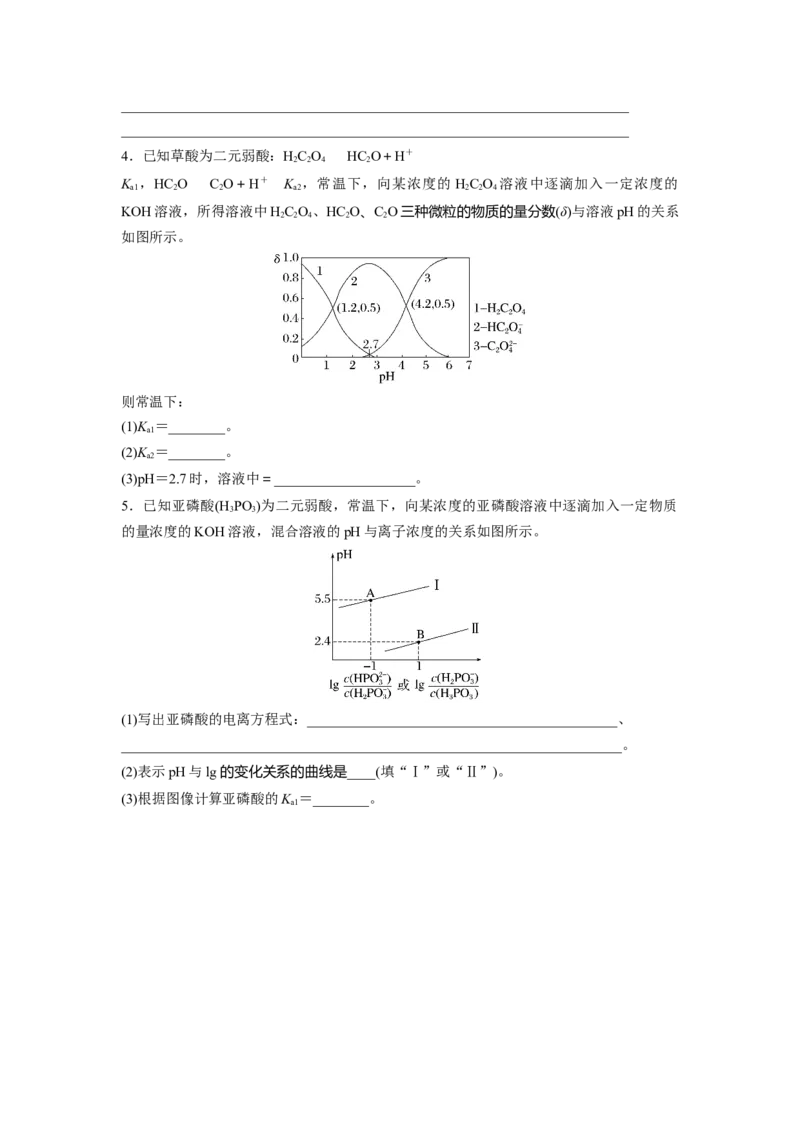
5.已知亚磷酸(H PO )为二元弱酸,常温下,向某浓度的亚磷酸溶液中逐滴加入一定物质
3 3
的量浓度的KOH溶液,混合溶液的pH与离子浓度的关系如图所示。
(1)写出亚磷酸的电离方程式:____________________________________________、
_______________________________________________________________________。
(2)表示pH与lg 的变化关系的曲线是____(填“Ⅰ”或“Ⅱ”)。
(3)根据图像计算亚磷酸的K =________。
a1