文档内容
第七章 化学反应速率与化学平衡
测试卷
时间:75分钟 分值:100分
一、选择题(每小题只有一个正确选项,共15×3分)
1.(2024·天津南开·一模)工业合成尿素以 和 作为原料,其能量转化关系如下图:
已知 。下列有关说法正确的是
A.
B.
C.
D.过程③反应速率慢,使用合适的催化剂可减小 而加快反应
【答案】C
【解析】A.二氧化碳气体转化为液态二氧化碳是一个熵减的过程,A错误;B.液态水变成气态水要吸
热, ,B错误;C.由盖斯定律可知,①+②+③得反应2NH (l)+CO (g)=HO(l)+HNCONH(l),则
3 2 2 2 2
△H=△H+△H +△H =△H +(-109.2kJ·mol-1)+(+15.5kJ·mol-1)=-103.7,则△H=-10kJ·mol-1,C正确;D.过
1 2 3 1 1
程③使用合适催化剂可降低反应的活化能,但不改变反应热△H 的大小,D错误;故选C。
3
2.(2024·江苏·二模) 法合成氨反应为 。
工业上将原料以 投入合成塔。下列说法正确的是
A.从合成塔排出的气体中,
B.当 时,反应达到平衡状态
C.使用高效催化剂可降低反应的焓变
D.升高温度,正反应速率减小,逆反应速率增大
【答案】A
【解析】A.根据反应方程式,N 和H 反应时消耗的物质的量之比为1:3,而起始投料比为1:2.8,消耗比
2 2
小于投料比,故排出的气体中,n(N ):n(H )>1:2.8,A正确;B.各物质的反应速率之比等于化学计量数
2 2
之比,故2v (H )=3v (NH )时,反应达到平衡状态,B错误;C.催化剂可以加快反应速率,但是不改变
正 2 逆 3反应热,不能降低焓变,C错误;D.升高温度,正逆反应速率都增大,D错误;本题选A。
3.(2024·辽宁沈阳·模拟预测)CO 催化加氢制CHOH的反应体系中,发生的主要反应如下:
2 3
反应1:
反应2:
恒压下,将 的混合气体以一定流速通过装有催化剂的反应管,测得出口处CO 的转化
2
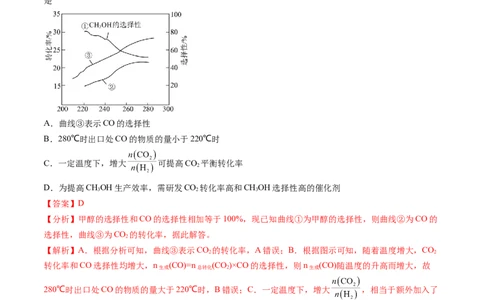
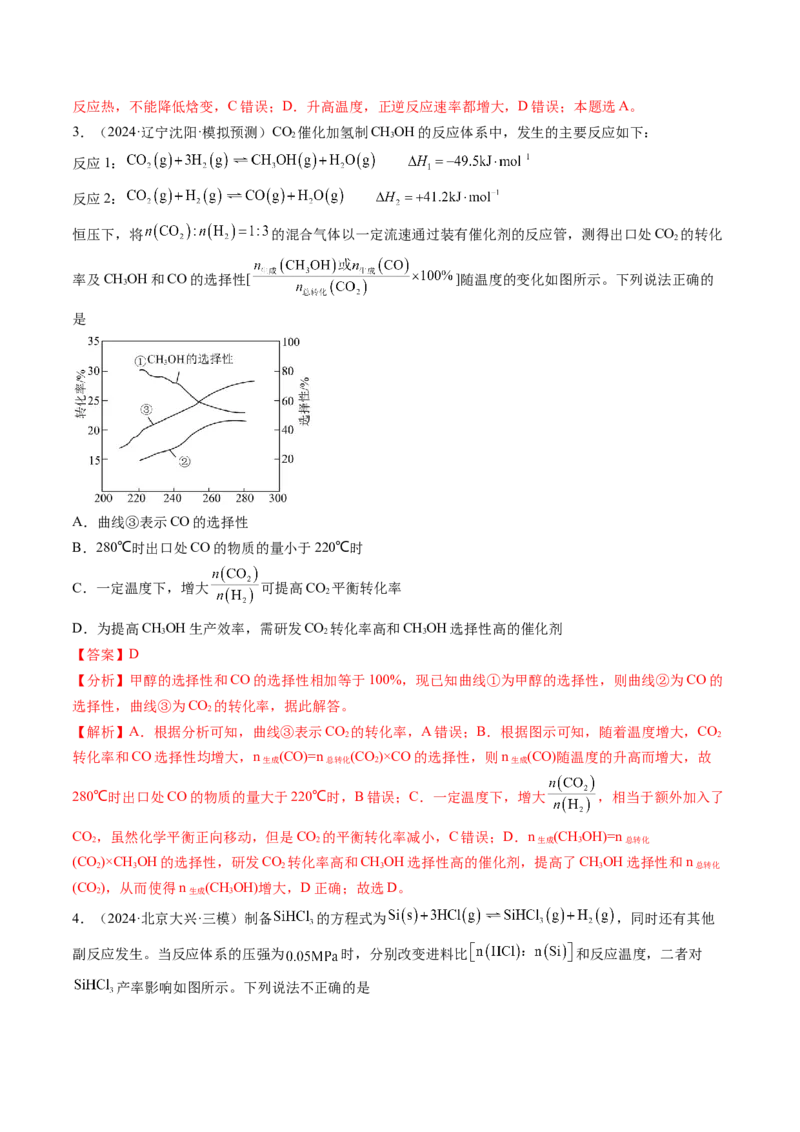
率及CHOH和CO的选择性[ ]随温度的变化如图所示。下列说法正确的
3
是
A.曲线③表示CO的选择性
B.280℃时出口处CO的物质的量小于220℃时
C.一定温度下,增大 可提高CO 平衡转化率
2
D.为提高CHOH生产效率,需研发CO 转化率高和CHOH选择性高的催化剂
3 2 3
【答案】D
【分析】甲醇的选择性和CO的选择性相加等于100%,现已知曲线①为甲醇的选择性,则曲线②为CO的
选择性,曲线③为CO 的转化率,据此解答。
2
【解析】A.根据分析可知,曲线③表示CO 的转化率,A错误;B.根据图示可知,随着温度增大,CO
2 2
转化率和CO选择性均增大,n (CO)=n (CO)×CO的选择性,则n (CO)随温度的升高而增大,故
生成 总转化 2 生成
280℃时出口处CO的物质的量大于220℃时,B错误;C.一定温度下,增大 ,相当于额外加入了
CO,虽然化学平衡正向移动,但是CO 的平衡转化率减小,C错误;D.n (CHOH)=n
2 2 生成 3 总转化
(CO)×CH OH的选择性,研发CO 转化率高和CHOH选择性高的催化剂,提高了CHOH选择性和n
2 3 2 3 3 总转化
(CO),从而使得n (CHOH)增大,D正确;故选D。
2 生成 3
4.(2024·北京大兴·三模)制备 的方程式为 ,同时还有其他
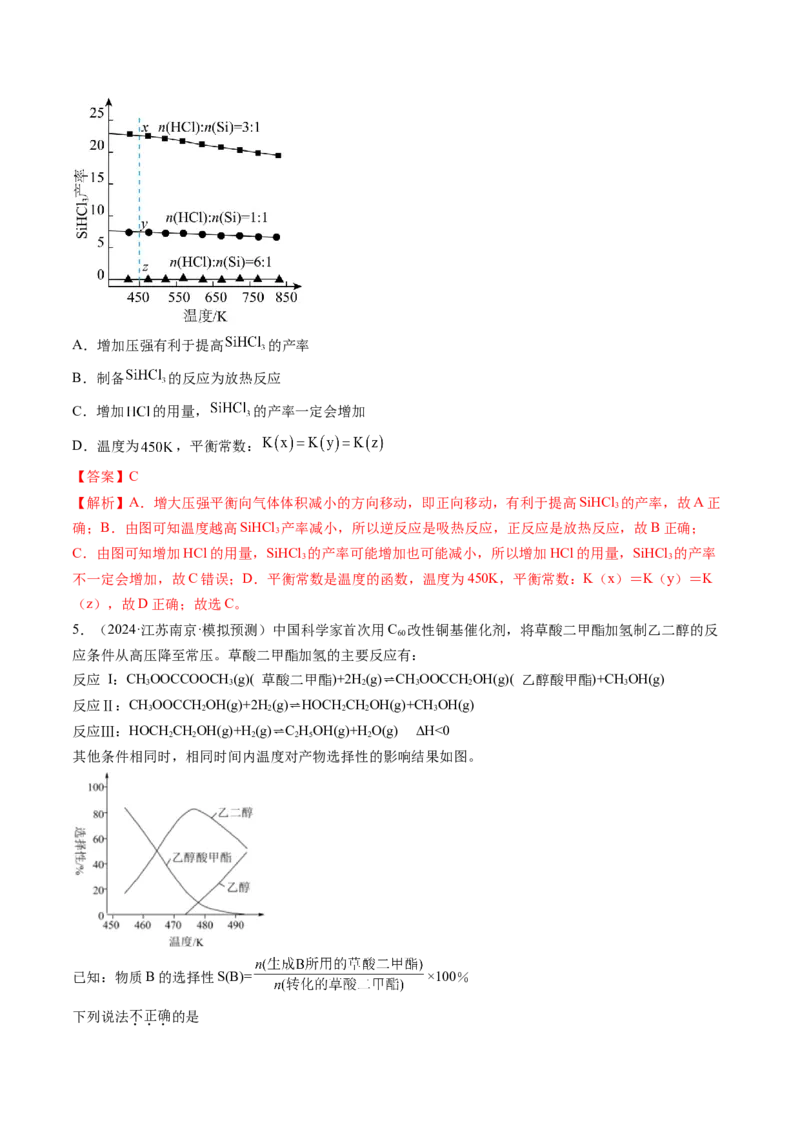
副反应发生。当反应体系的压强为 时,分别改变进料比 和反应温度,二者对
产率影响如图所示。下列说法不正确的是A.增加压强有利于提高 的产率
B.制备 的反应为放热反应
C.增加 的用量, 的产率一定会增加
D.温度为 ,平衡常数:
【答案】C
【解析】A.增大压强平衡向气体体积减小的方向移动,即正向移动,有利于提高SiHCl 的产率,故A正
3
确;B.由图可知温度越高SiHCl 产率减小,所以逆反应是吸热反应,正反应是放热反应,故B正确;
3
C.由图可知增加HCl的用量,SiHCl 的产率可能增加也可能减小,所以增加HCl的用量,SiHCl 的产率
3 3
不一定会增加,故C错误;D.平衡常数是温度的函数,温度为450K,平衡常数:K(x)=K(y)=K
(z),故D正确;故选C。
5.(2024·江苏南京·模拟预测)中国科学家首次用C 改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反
60
应条件从高压降至常压。草酸二甲酯加氢的主要反应有:
反应 I:CH
3
OOCCOOCH
3
(g)( 草酸二甲酯)+2H
2
(g)⇌CH
3
OOCCH
2
OH(g)( 乙醇酸甲酯)+CH
3
OH(g)
反应Ⅱ:CH
3
OOCCH
2
OH(g)+2H
2
(g)⇌HOCH
2
CH
2
OH(g)+CH
3
OH(g)
反应Ⅲ:HOCH
2
CH
2
OH(g)+H
2
(g)⇌C
2
H
5
OH(g)+H
2
O(g) ∆H<0
其他条件相同时,相同时间内温度对产物选择性的影响结果如图。
已知:物质B的选择性S(B)= ×100%
下列说法不正确的是A.反应I、Ⅱ均为∆H<0
B.其他条件不变,增加氢气的浓度,一定能提高乙二醇的产率
C.若不使用C 改性铜基催化剂采用高压条件能加快反应速率
60
D.用C 改性铜基催化剂催化草酸二甲醋反应制乙二醇最佳温度范围约为475~480K
60
【答案】B
【解析】A.由图可知I、Ⅱ、Ⅲ为连锁反应,即为自发进行, ,可知I、Ⅱ为 的反
应,故I、Ⅱ的 <0,故A正确;B.在乙醇酸甲酯等于乙二醇选择性时,其他条件不变,增加氢气的浓
度,乙二醇的产率不变,故B错误;C.不使用C 改性铜基催化剂,采用高压条件能加快反应速率,相当
60
于增大浓度,反应速率加快,故C正确;D.由图可知,温度为470~480K时,生成乙二醇的选择性最
高,故D正确;答案选B。
6.(2024·黑龙江双鸭山·模拟预测)逆水煤气反应对于促进能源和化工产业的发展具有重要意义,其中涉
及反应 ,已知该反应的正反应速率可表示为
,逆反应速率可表示为 为速率常数(只受温度影响),速率常数随温度的
变化如图所示,下列说法正确的是
A.
B.温度低于 时,反应向正反应方向进行
C. 时,向某平衡体系中投入等物质的量 后平衡不移动
D. 时,若 的平衡转化率大于50%,则 的平衡转化率小于50%
【答案】D
【解析】A.根据图像可知,温度升高,逆反应增大的速率更快,所以逆反应为吸热反应,A项错误;B.
反应向哪个方向进行与温度没有直接关系,B项错误;C.不知道初次平衡时各物质的关系,无法确定平
衡是否移动,C项错误;D.反应达到平衡时, , ,
,则 时反应的平衡常数为1,若 的平衡转化率大于 ,则 的平衡
转化率一定小于 ,D项正确;故选:D。
7.(2024·海南省直辖县级单位·模拟预测)工业上用 生产甲醇的反应为
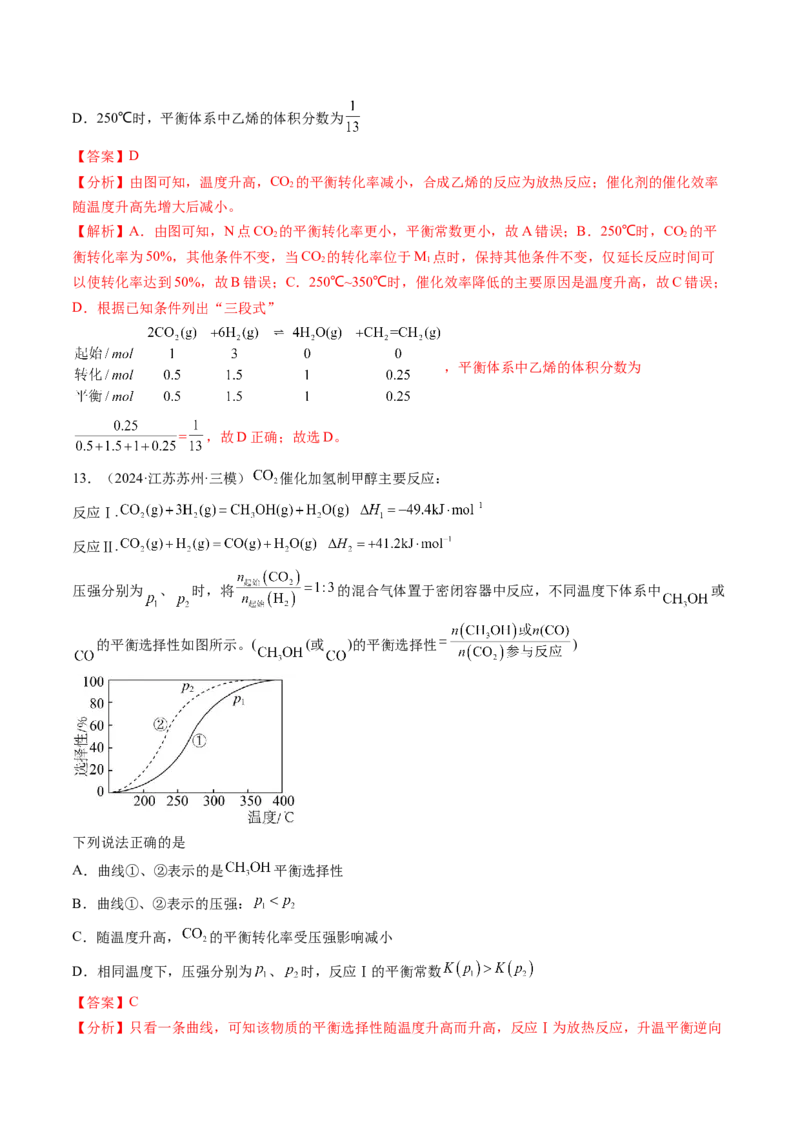
。在一定条件下的密闭容器中,分别充入 的混合气体, 的平衡转化率与温度、压强的关系如图所示:
下列说法正确的是
A.
B.压强
C.a、b点的平衡常数:
D.体系中气体的总物质的量不变时,反应达到平衡
【答案】D
【解析】A.随着温度的升高,CO的转化率减小,说明平衡逆向移动,升高温度平衡逆向移动,故反应放
热, ,A错误;B.保持温度不变,增大压强,平衡正向移动,CO的转化率增大,故压强
,B错误;C.温度不变,平衡常数不变,故 ,C错误;D.无论反应怎么反应,
物质的量都会改变,体系中气体的总物质的量不变时,反应达到平衡,D正确; 故选D。
8.(2024·重庆·模拟预测) 与 在固载金属催化剂上存在以下两个反应:
反应Ⅰ:
反应Ⅱ:
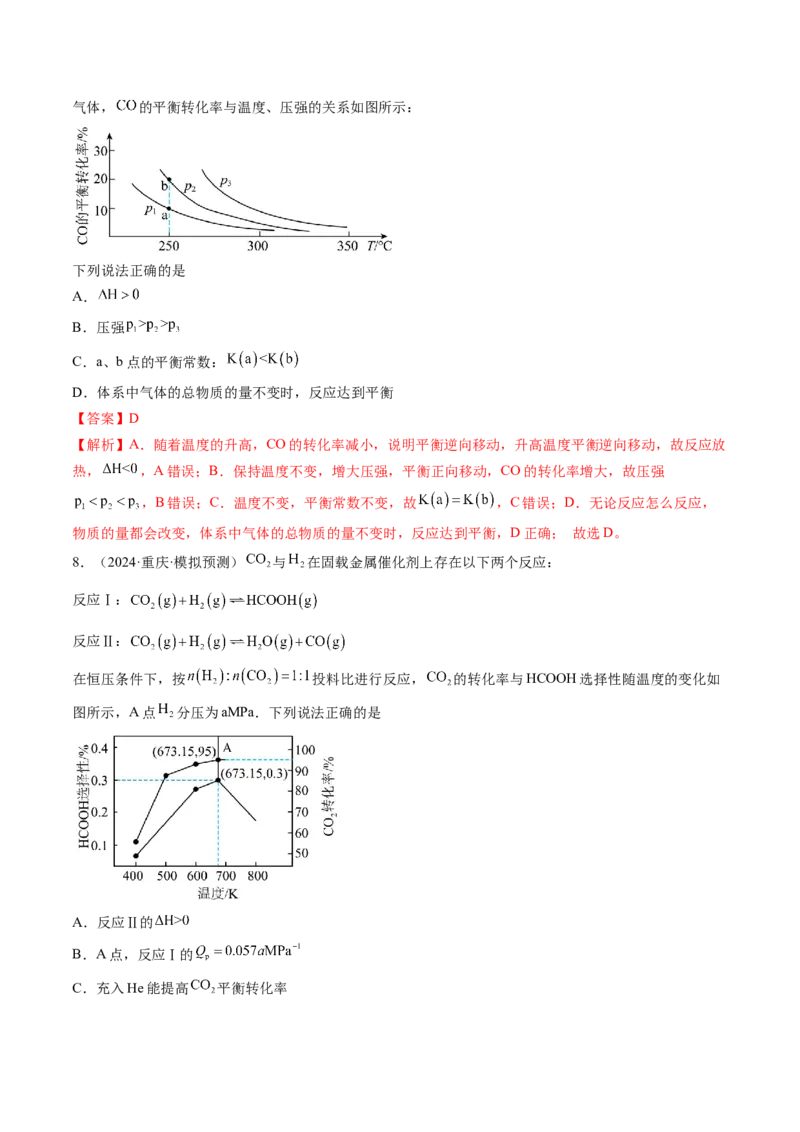
在恒压条件下,按 投料比进行反应, 的转化率与HCOOH选择性随温度的变化如
图所示,A点 分压为aMPa.下列说法正确的是
A.反应Ⅱ的
B.A点,反应Ⅰ的
C.充入He能提高 平衡转化率D. ,升高温度, 比 增加更多
【答案】A
【解析】A.由图可知,温度在400~700K 的转化率与HCOOH选择性随温度升高而增大,升高温度
的转化率增大,平衡正向移动,说明反应Ⅱ是吸热反应即 ,故A正确;B.不妨设初始投料为
n(H )=n(CO )=1mol,673.15K时,CO 的转化率为95%,HCOOH的选择性为0.3%,所以
2 2 2
n(HCOOH)=1×95%×0.3%mol,由于反应I和反应Ⅱ中H 和CO 都是1∶1反应,所以此时
2 2
n(H )=n(CO )=1×5%mol,则此时p(CO)=p(H)=aMPa,p(HCOOH)= αMPa,所以反应I的压力商计
2 2 2 2
算式Q= MPa-1,故B错误;C.恒压条件,再充入He,则容器体积变大,相当于
p
减压,反应I为气体系数之和减小的反应,平衡逆向移动,CO 的转化率减小,故C错误;D.随温度升
2
高,二氧化碳的转化率升高,但HCOOH的选择性却迅速下降,说明反应Ⅱ的反应速率增加更显著,则
,升高温度, 比 增加更多,故D错误;故选A。
9.(2024·江苏宿迁·三模)丁烷催化脱氢是工业制备丁烯的主要方法,反应如下:CHCHCHCH(g)
3 2 2 3
CH=CHCHCH(g)+H(g) ΔH>0。为探究工业生产丁烯的合适温度,在体积为1 L的容器中,充入10 mol
2 2 3 2
丁烷,使用SiO-CrO 复合催化剂催化丁烷脱氢,相同时间内丁烷的转化率和主要产物的收率分布如图所
2 x
示。
[收率=(生成某产物的量/投入的原料量)×100%]。
下列说法不正确的是
A.590℃生成丁烯的物质的量为0.55 mol
B.590℃以后,温度升高,丁烯的收率降低,原因是副产物增多
C.丁烷转化率增大的原因一定是温度升高平衡右移,丁烷的转化率增大
D.欲使工业生产丁烯的收率更高,应选用低温下选择性更好的高效催化剂
【答案】D
【解析】A.590℃时,丁烯的收率为20%,丁烷转化率为27.5%,所以生成的正丁烯的物质的量为
10×20%×27.5%=0.55mol,A正确;B.由图可知590℃时丁烯的收率最高,温度再高,丁烯的收率降低,副产物增多,B正确;C.制备乙烯的反应为吸热反应,升高温度平衡正向移动,丁烷的转化率增大,C正
确;D.由图可知,降温目标产物的收率降低,D错误;故选D。
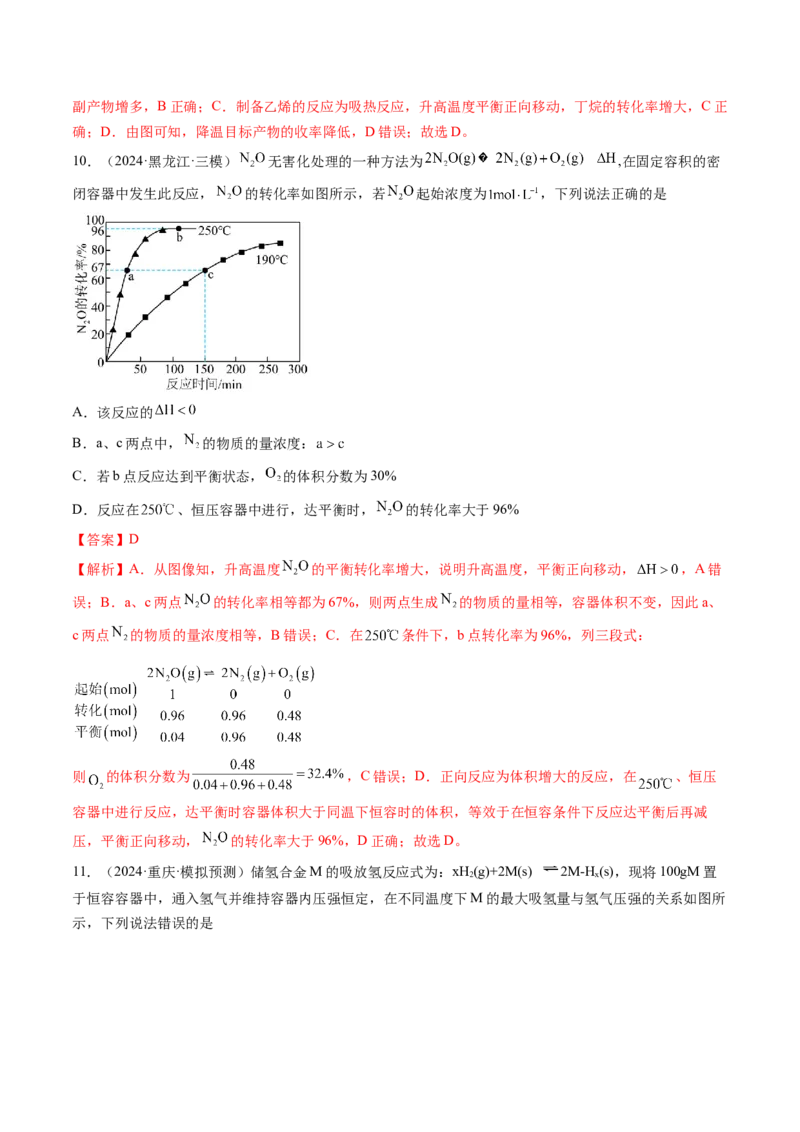
10.(2024·黑龙江·三模) 无害化处理的一种方法为 ,在固定容积的密
闭容器中发生此反应, 的转化率如图所示,若 起始浓度为 ,下列说法正确的是
A.该反应的
B.a、c两点中, 的物质的量浓度:
C.若b点反应达到平衡状态, 的体积分数为30%
D.反应在 、恒压容器中进行,达平衡时, 的转化率大于96%
【答案】D
【解析】A.从图像知,升高温度 的平衡转化率增大,说明升高温度,平衡正向移动, ,A错
误;B.a、c两点 的转化率相等都为67%,则两点生成 的物质的量相等,容器体积不变,因此a、
c两点 的物质的量浓度相等,B错误;C.在 条件下,b点转化率为96%,列三段式:
则 的体积分数为 ,C错误;D.正向反应为体积增大的反应,在 、恒压
容器中进行反应,达平衡时容器体积大于同温下恒容时的体积,等效于在恒容条件下反应达平衡后再减
压,平衡正向移动, 的转化率大于96%,D正确;故选D。
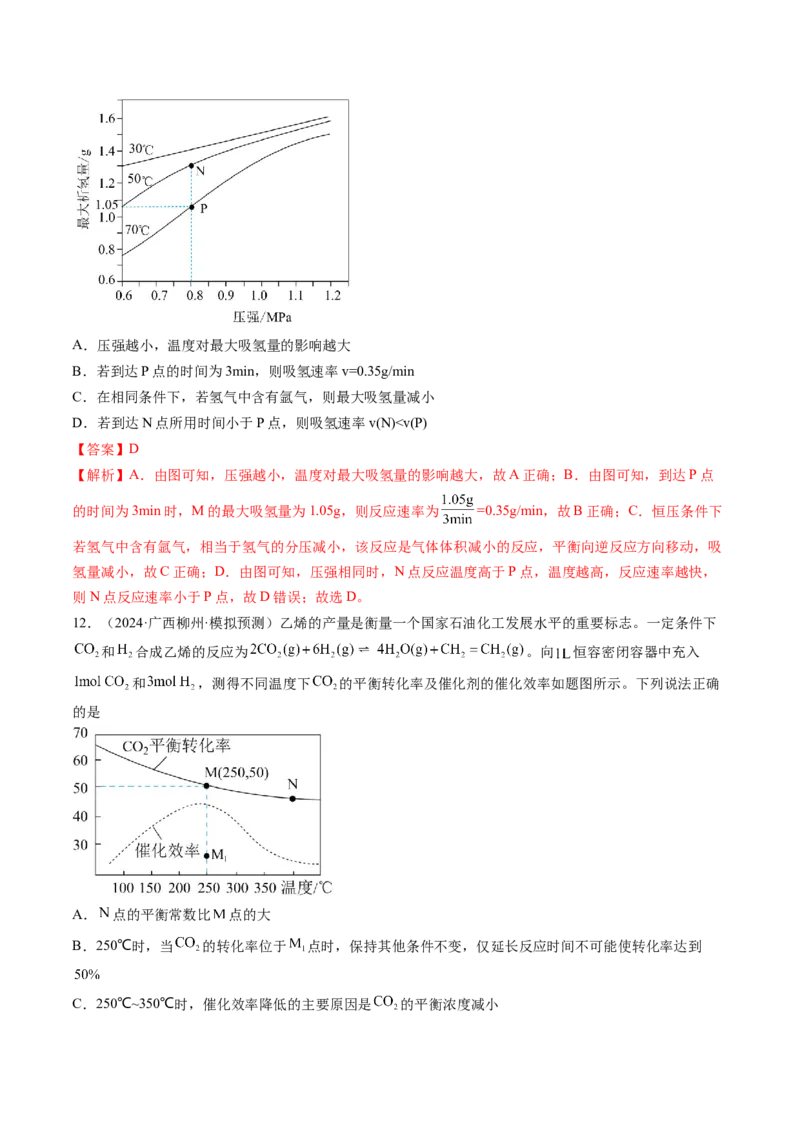
11.(2024·重庆·模拟预测)储氢合金M的吸放氢反应式为:xH(g)+2M(s) 2M-H (s),现将100gM置
2 x
于恒容容器中,通入氢气并维持容器内压强恒定,在不同温度下M的最大吸氢量与氢气压强的关系如图所
示,下列说法错误的是A.压强越小,温度对最大吸氢量的影响越大
B.若到达P点的时间为3min,则吸氢速率v=0.35g/min
C.在相同条件下,若氢气中含有氩气,则最大吸氢量减小
D.若到达N点所用时间小于P点,则吸氢速率v(N)P ,B错误;C.随温度升高,CO的平衡选择性接近100%,可知升温后主要发生反
1 2
应Ⅱ,反应Ⅱ的平衡移动与压强无关,故随温度升高, 的平衡转化率受压强影响减小,C正确;D.
平衡常数只与温度有关,温度相同平衡常数相同,D错误;故选C。
14.(2024·湖南·模拟预测)二甲醇是一种绿色能源,也是一种化工原料。在体积均为 的容器I、Ⅱ中
分别充入 和 ,发生反应: 。相对容器Ⅱ,
容器I仅改变温度或压强一个条件。两个容器同时发生化学反应, 的转化率与时间关系如图,下列叙
述正确的是
A.该反应中,产物总能量大于反应物总能量
B.其他条件相同,压强,容器I 容器Ⅱ
C.容器Ⅱ中 内 平均速率为
D.容器I条件下,平衡常数 为27
【答案】C
【分析】根据图像可知,容器I先达到平衡,说明Ⅰ容器反应速率大于Ⅱ容器,则Ⅰ容器改变的条件可能
是升高温度或增大压强。同时从图中还可知平衡时容器Ⅱ中 的转化率更高,说明Ⅰ容器改变的条件相
对于Ⅱ容器而言促使反应平衡逆向移动,若为升高温度,则反应的化学平衡逆向移动,正反应为放热反
应。若为增大压强,反应的化学平衡正向移动,则Ⅰ中 的转化率应该大于Ⅱ,故不可能是增大压强,
因此Ⅰ改变的条件是升高温度。
【解析】A.根据以上分析可知反应为放热反应,则产物总能量小于反应物总能量,故A项错误;B.若
其他条件相同,容器I比容器Ⅱ先达到平衡状态,且正反应是体积减小的,因此改变的条件是温度,故温
度:容器I>容器Ⅱ,故B项错误;C.容器Ⅱ中0∼6min内,CO 的转化率为40%,即反应消耗CO 的物
2 2
质的量为1mol×40%=0.4mol,H 消耗1.2mol,则H 平均速率为 ,故C项正确;
2 2
D.容器I条件下,4min时达到平衡状态,CO 转化率为50%,根据三段式得:
2平衡常数 ,故D项错误;故本题选
C。
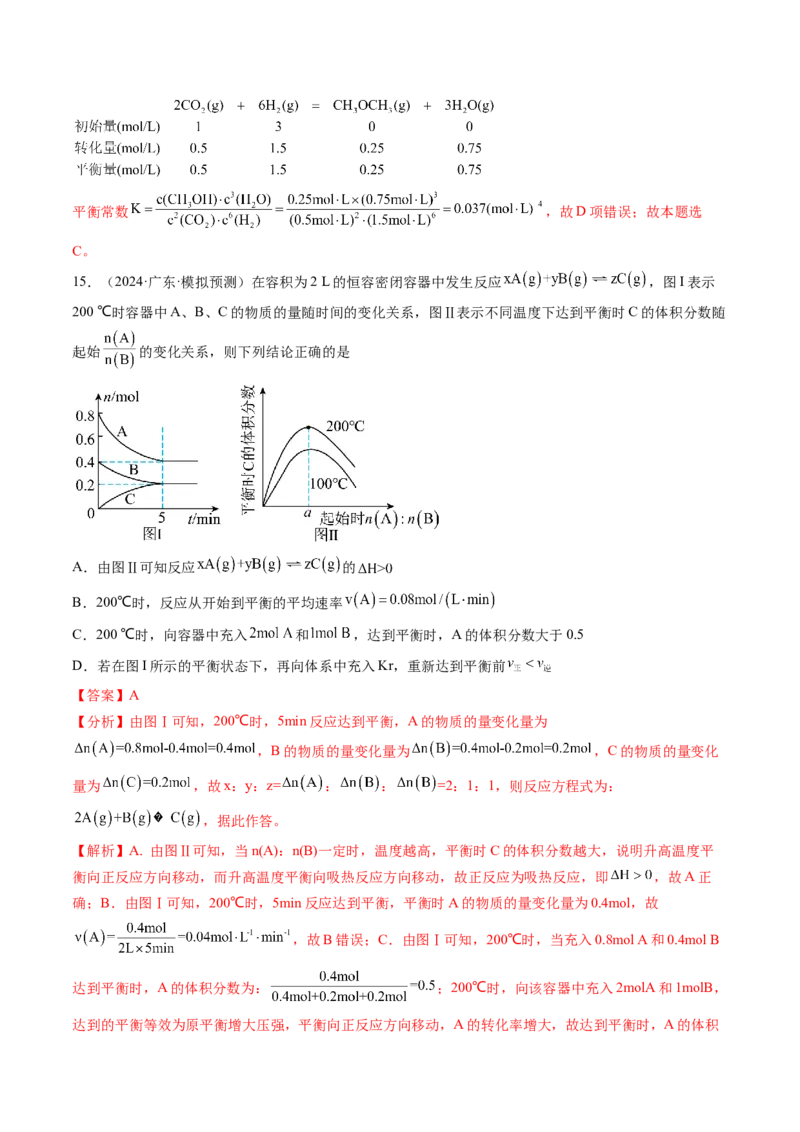
15.(2024·广东·模拟预测)在容积为2 L的恒容密闭容器中发生反应 ,图I表示
200 ℃时容器中A、B、C的物质的量随时间的变化关系,图Ⅱ表示不同温度下达到平衡时C的体积分数随
起始 的变化关系,则下列结论正确的是
A.由图Ⅱ可知反应 的
B.200℃时,反应从开始到平衡的平均速率
C.200 ℃时,向容器中充入 和 ,达到平衡时,A的体积分数大于0.5
D.若在图I所示的平衡状态下,再向体系中充入Kr,重新达到平衡前
【答案】A
【分析】由图Ⅰ可知,200℃时,5min反应达到平衡,A的物质的量变化量为
,B的物质的量变化量为 ,C的物质的量变化
量为 ,故x:y:z= : : =2:1:1,则反应方程式为:
,据此作答。
【解析】A. 由图Ⅱ可知,当n(A):n(B)一定时,温度越高,平衡时C的体积分数越大,说明升高温度平
衡向正反应方向移动,而升高温度平衡向吸热反应方向移动,故正反应为吸热反应,即 ,故A正
确;B.由图Ⅰ可知,200℃时,5min反应达到平衡,平衡时A的物质的量变化量为0.4mol,故
,故B错误;C.由图Ⅰ可知,200℃时,当充入0.8mol A和0.4mol B
达到平衡时,A的体积分数为: ;200℃时,向该容器中充入2molA和1molB,
达到的平衡等效为原平衡增大压强,平衡向正反应方向移动,A的转化率增大,故达到平衡时,A的体积分数小于0.5,故C错误;D.恒温恒容条件下,在图Ⅰ所示的平衡状态下,再向体系中充入Kr,由于容
器容积不变,则混合物中各物质的浓度不变,正逆反应速率不变,平衡不移动,故v(正)=v(逆),故D错
误;故答案选A。
二、非选择题(共4小题,共55分)
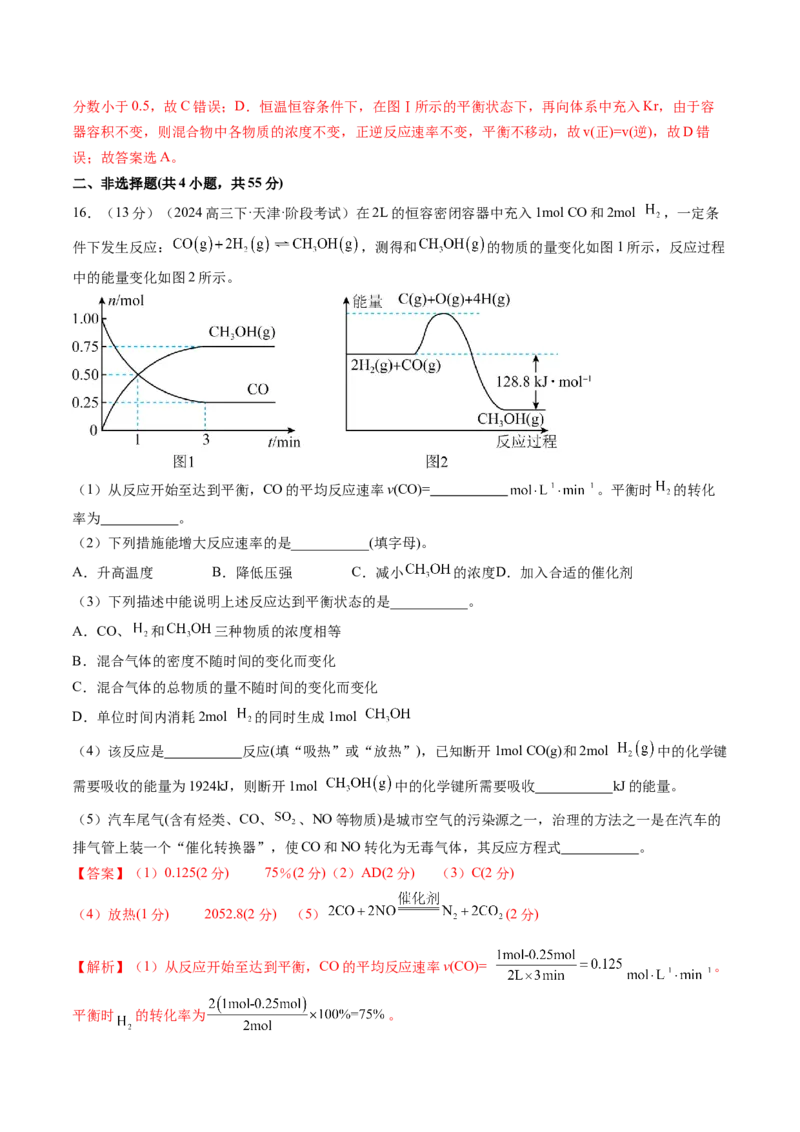
16.(13分)(2024高三下·天津·阶段考试)在2L的恒容密闭容器中充入1mol CO和2mol ,一定条
件下发生反应: ,测得和 的物质的量变化如图1所示,反应过程
中的能量变化如图2所示。
(1)从反应开始至达到平衡,CO的平均反应速率v(CO)= 。平衡时 的转化
率为 。
(2)下列措施能增大反应速率的是___________(填字母)。
A.升高温度 B.降低压强 C.减小 的浓度D.加入合适的催化剂
(3)下列描述中能说明上述反应达到平衡状态的是___________。
A.CO、 和 三种物质的浓度相等
B.混合气体的密度不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内消耗2mol 的同时生成1mol
(4)该反应是 反应(填“吸热”或“放热”),已知断开1mol CO(g)和2mol 中的化学键
需要吸收的能量为1924kJ,则断开1mol 中的化学键所需要吸收 kJ的能量。
(5)汽车尾气(含有烃类、CO、 、NO等物质)是城市空气的污染源之一,治理的方法之一是在汽车的
排气管上装一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式 。
【答案】(1)0.125(2分) 75%(2分)(2)AD(2分) (3)C(2分)
(4)放热(1分) 2052.8(2分) (5) (2分)
【解析】(1)从反应开始至达到平衡,CO的平均反应速率v(CO)= 。
平衡时 的转化率为 。(2)多种因素能影响化学反应速率,其中增大反应物的浓度、增大气体压强、使用正催化剂、升温等均
能加快反应速率。则能增大反应速率的是A(升高温度)和 D(加入合适的催化剂) ,故AD符合。
(3)A.某瞬间的含量跟起始状态有关、CO、 和 三种物质的浓度相等、不一定说明它们不再
改变、不能说明已达平衡,A不符合题意;B.气体质量始终不变、容积体积的不变,故气体密度不变不
能说明已平衡,B不符合题意;C.反应中,气体的物质的量会随着反应而变化,故混合气体的总物质的
量不随时间的变化而变化说明反应已达平衡,C符合题意;D.单位时间内消耗2mol 的同时生成1mol
,均指正反应速率,不能说明已达平衡,D不符合题意;故选C。
(4)该反应的生成物总能量低于反应物总能量,为放热反应,由图知:
=-128.8kJ/mol=反应物总键能-生成物总键能,已知断开1mol CO(g)和2mol 中的化学键需要吸收
的能量为1924kJ,则断开1mol 中的化学键所需要吸收1924kJ-(-128.8kJ/mol)=2052.8kJ。
(5)在汽车的排气管上装一个“催化转换器”,可以使CO和NO转化为无毒气体N 和CO,根据得失电
2 2
子守恒和原子守恒配平化学方程式为: 。
17.(15分)(2024·河南·模拟预测)二氧化碳一甲烷重整反应制备合成气(H +CO)是一种生产高附加值
2
化学品的低碳过程。该过程存在如下化学反应:
①
②
③
④
回答下列问题:
(1) ,反应① 正向自发进行(填标号)。
A.低温下能 B.高温下能 C.任何温度下都能 D.任何温度下都不能
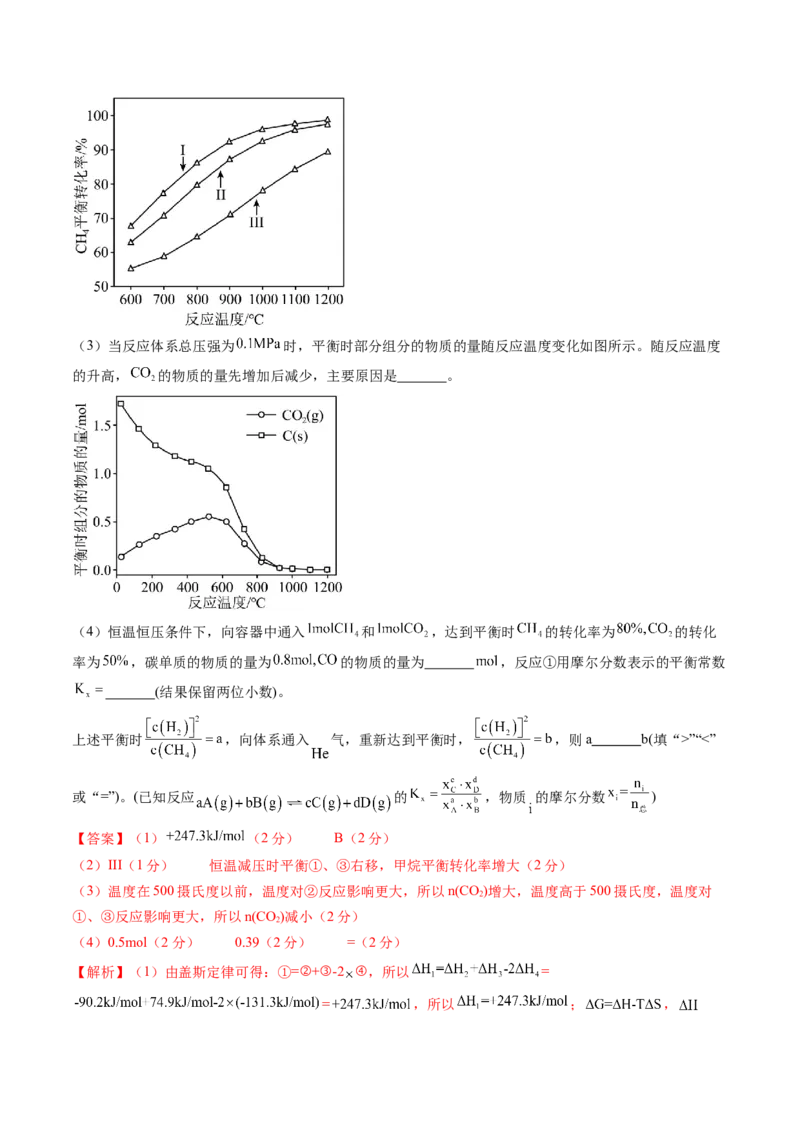
(2)反应体系总压强分别为 和 时, 平衡转化率随反应温度变化如图所
示,则代表反应体系总压强为 的曲线是 (填“Ⅰ”“Ⅱ”或“Ⅲ”),判断依据是
。(3)当反应体系总压强为 时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度
的升高, 的物质的量先增加后减少,主要原因是 。
(4)恒温恒压条件下,向容器中通入 和 ,达到平衡时 的转化率为 的转化
率为 ,碳单质的物质的量为 的物质的量为 ,反应①用摩尔分数表示的平衡常数
(结果保留两位小数)。
上述平衡时 ,向体系通入 气,重新达到平衡时, ,则a b(填“>”“<”
或“=”)。(已知反应 的 ,物质 的摩尔分数 )
【答案】(1) (2分) B(2分)
(2)III(1分) 恒温减压时平衡①、③右移,甲烷平衡转化率增大(2分)
(3)温度在500摄氏度以前,温度对②反应影响更大,所以n(CO)增大,温度高于500摄氏度,温度对
2
①、③反应影响更大,所以n(CO)减小(2分)
2
(4)0.5mol(2分) 0.39(2分) =(2分)
【解析】(1)由盖斯定律可得:①=②+③-2 ④,所以 =
= ,所以 ; ,>0、 >0,所以高温反应①正向自发进行;
(2)图像显示恒温变压(III、II、I的是顺序变化)甲烷平衡转化率增大,而反应①、③恒温减压平衡均
右移,甲烷平衡转化率增大,即同温时压强越大甲烷平衡转化率越小,所以III曲线代表5.00MPa;判断依
据是恒温减压时平衡①、③右移,甲烷平衡转化率增大;
(3)升温②反应左移,使n(CO)有增大的趋势,①、③反应右移,使n(CO)有减小的趋势,温度在500
2 2
摄氏度以前,温度对②反应影响更大,所以n(CO)增大,温度高于500摄氏度,温度对①、③反应影响更
2
大,所以n(CO)减小;
2
(4)三段式表示如下:
平衡时甲烷转化了0.8mol,CO 转化了0.5 mol,C生成了
2
0.8mol,所以x+m=0.8mol、x+y=0.5mol、y+m+n=0.8 mol 、解得n(CO)=2x-n=0.5mol;由氧原子守恒得
n(H O)= ,由氢原子守恒得n(H )=
2 2
,容器气体总物质的量=
, = =0.39;反应③的平衡
常数K= ,恒温恒压条件下向体系通入 气,尽管平衡正向移动,但是温度不变其平衡常数不
变,其他平衡的移动也不能影响该反应的平衡常数,所以b=a。
18.(14分)(2024·辽宁锦州·模拟预测)利用 、 为原料合成 的主要反应如下。
Ⅰ.
Ⅱ.
回答下列问题:
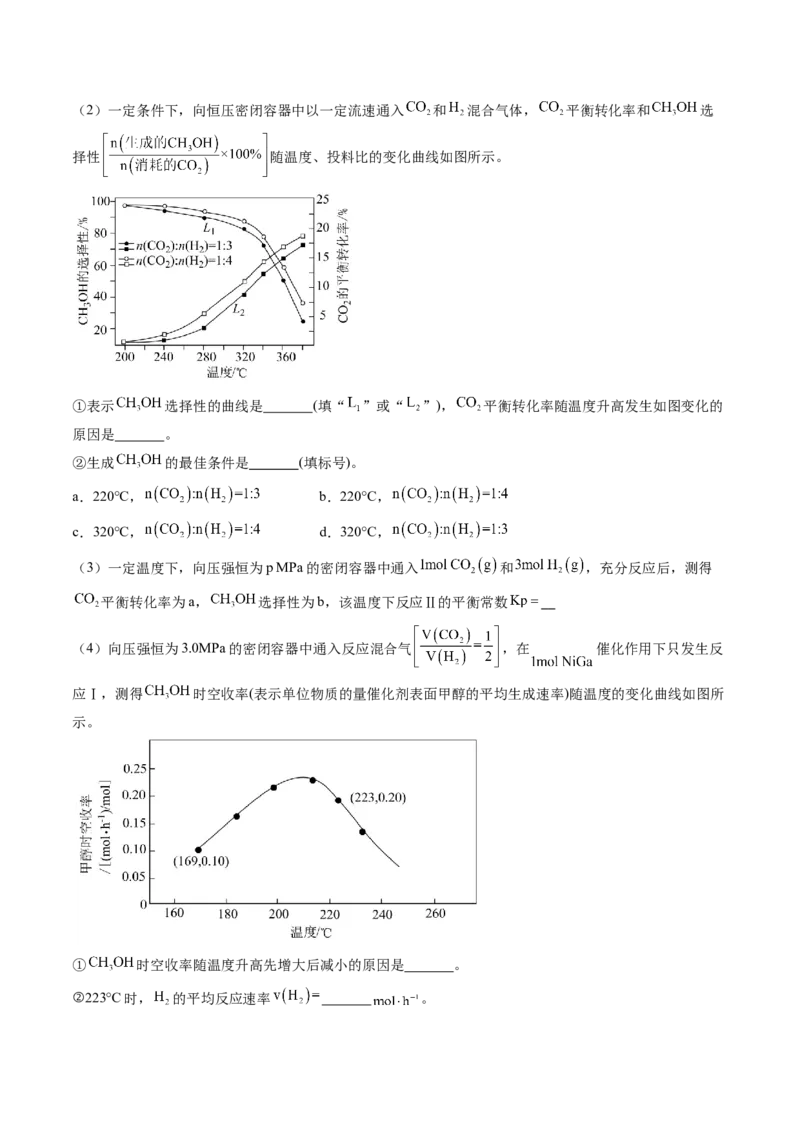
(1)已知反应Ⅲ的平衡常数 ,写出反应Ⅲ的热化学方程式 。(2)一定条件下,向恒压密闭容器中以一定流速通入 和 混合气体, 平衡转化率和 选
择性 随温度、投料比的变化曲线如图所示。
①表示 选择性的曲线是 (填“ ”或“ ”), 平衡转化率随温度升高发生如图变化的
原因是 。
②生成 的最佳条件是 (填标号)。
a.220°C, b.220°C,
c.320°C, d.320°C,
(3)一定温度下,向压强恒为p MPa的密闭容器中通入 和 ,充分反应后,测得
平衡转化率为a, 选择性为b,该温度下反应Ⅱ的平衡常数
(4)向压强恒为3.0MPa的密闭容器中通入反应混合气 ,在 催化作用下只发生反
应Ⅰ,测得 时空收率(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度的变化曲线如图所
示。
① 时空收率随温度升高先增大后减小的原因是 。
②223°C时, 的平均反应速率 。【答案】(1)CO(g)+2H
2
(g)⇌CH
3
OH(g) △H=-92.4kJ/mol(2分)
(2)L(2分) 反应Ⅱ是吸热反应,升高温度,反应Ⅱ正向移动的程度大于反应Ⅰ逆向移动的程
1
度,CO 平衡转化率随温度的升高而增大(2分) c(2分)
2
(3) (2分)
(4)温度较低时,反应速率较慢,反应未达到平衡,升高温度,反应速率加快,CHOH时空收率增大,
3
当温度较高,反应速率较快,反应达到平衡,升高温度,平衡逆向移动,CHOH的转化率减小,CHOH
3 3
时空收率减小(2分) 0.6mol·h-1/mol(2分)
【解析】(1)已知反应Ⅲ的平衡常数 ,由盖斯定律可知反应Ⅰ-反应Ⅱ可得反应Ⅲ的热化学方程式
为:CO(g)+2H(g) CHOH(g) 。
2 3
(2)①反应Ⅰ是放热反应,升高温度,平衡逆向移动,CHOH的转化率减小,选择性减小,则表示
3
CHOH选择性的曲线是L,L 代表CO 平衡转化率随温度变化的曲线,反应Ⅱ是吸热反应,升高温度,反
3 1 2 2
应Ⅱ正向移动的程度大于反应Ⅰ逆向移动的程度,CO 平衡转化率随温度的升高而增大;
2
②由图可知,320°C , 时,CHOH选择性较大,同时CO 的转化率也较大,故选c。
3 2
(3)根据已知条件列出“三段式”
充分反应后,测得 平衡转化率为 =a, 选择性为 =b,解得x=abmol,y=(a-ab)mol,平
衡时n( )=(1-a)mol,n(H )=(3-a-2ab)mol,n(CO)=(a-ab)mol,n(H O)=amol,n(CHOH)=abmol,则该温度
2 2 3
下反应Ⅰ的平衡常数K= 。
x
(4)① 时空收率随温度升高先增大后减小的原因是:温度较低时,反应速率较慢,反应未达到平
衡,升高温度,反应速率加快,CHOH时空收率增大,当温度较高,反应速率较快,反应达到平衡,升高
3
温度,平衡逆向移动,CHOH的转化率减小,CHOH时空收率减小;
3 3
②223°C时, 时空收率为0.2 [(mol·h-1)/mol], 的平均反应速率 0.2
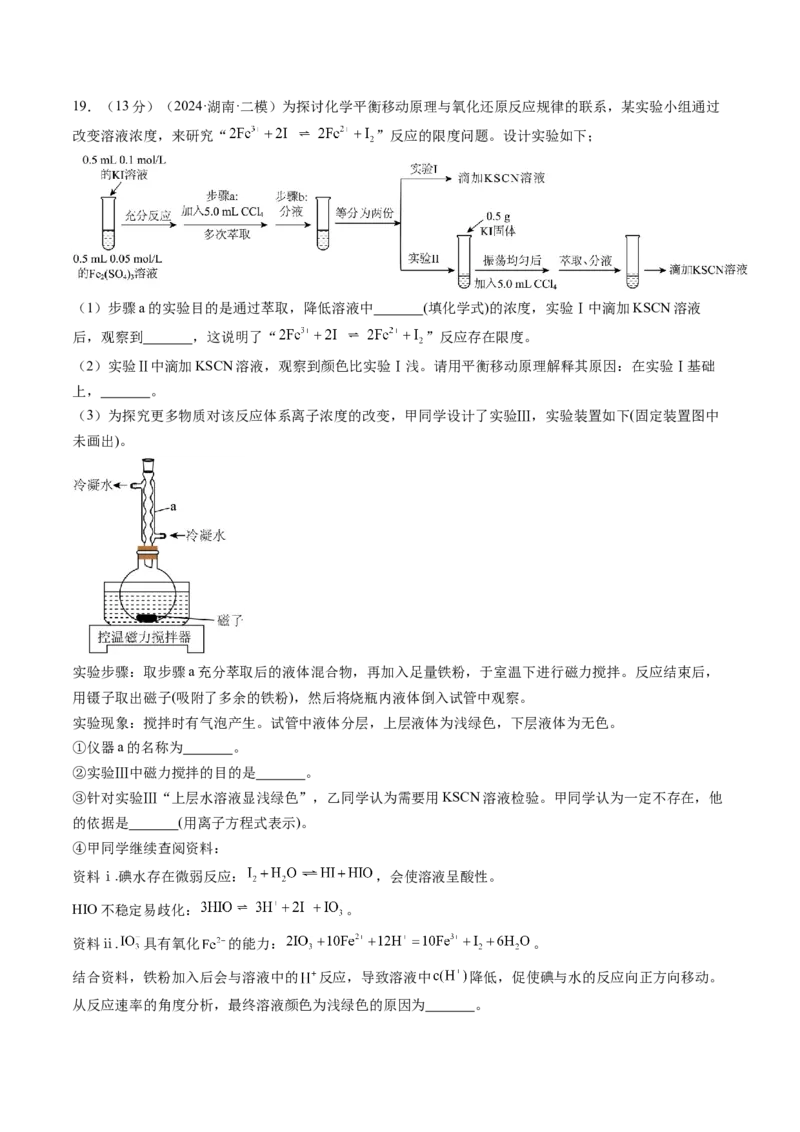
[(mol·h-1)/mol]×1mol×3=0.6 [(mol·h-1)/mol]。19.(13分)(2024·湖南·二模)为探讨化学平衡移动原理与氧化还原反应规律的联系,某实验小组通过
改变溶液浓度,来研究“ ”反应的限度问题。设计实验如下;
(1)步骤a的实验目的是通过萃取,降低溶液中 (填化学式)的浓度,实验Ⅰ中滴加KSCN溶液
后,观察到 ,这说明了“ ”反应存在限度。
(2)实验Ⅱ中滴加KSCN溶液,观察到颜色比实验Ⅰ浅。请用平衡移动原理解释其原因:在实验Ⅰ基础
上, 。
(3)为探究更多物质对该反应体系离子浓度的改变,甲同学设计了实验Ⅲ,实验装置如下(固定装置图中
未画出)。
实验步骤:取步骤a充分萃取后的液体混合物,再加入足量铁粉,于室温下进行磁力搅拌。反应结束后,
用镊子取出磁子(吸附了多余的铁粉),然后将烧瓶内液体倒入试管中观察。
实验现象:搅拌时有气泡产生。试管中液体分层,上层液体为浅绿色,下层液体为无色。
①仪器a的名称为 。
②实验Ⅲ中磁力搅拌的目的是 。
③针对实验Ⅲ“上层水溶液显浅绿色”,乙同学认为需要用KSCN溶液检验。甲同学认为一定不存在,他
的依据是 (用离子方程式表示)。
④甲同学继续查阅资料:
资料ⅰ.碘水存在微弱反应: ,会使溶液呈酸性。
HIO不稳定易歧化: 。
资料ⅱ. 具有氧化 的能力: 。
结合资料,铁粉加入后会与溶液中的 反应,导致溶液中 降低,促使碘与水的反应向正方向移动。
从反应速率的角度分析,最终溶液颜色为浅绿色的原因为 。【答案】(1)I(2分) 溶液颜色为红色(2分)
2
(2)增大反应物 的浓度后,让 平衡向 浓度减小的方向(正向)移动,水溶液中
浓度比实验Ⅰ中 浓度低(2分)
(3)①球形冷凝管(1分) ②磁力搅拌增大了有机相中的溶质碘与水的接触面积 (2分)
③ (2分)
④ 与 反应生成 的速率小于 与足量铁粉反应生成 的速率(2分)
【分析】根据题中所给的浓度与体积可知,三价铁离子与碘离子为等物质的量,根据反应可知等物质的量
的三价铁和碘离子发生氧化还原反应生成二价铁和碘单质,若是反应存在限度,则体系中仍会有三价铁离
子和碘离子,步骤a中加入四氯化碳进行萃取,碘单质进入有机层,其他可溶于水的物质进入无机层,经
过步骤b分液后,留下无机层,实验Ⅰ中加入KSCN溶液检验三价铁离子的存在,实验Ⅱ中加入碘离子促
使产生碘单质,后续再检验三价铁离子。
【解析】(1)根据分析可知步骤a的实验目的是通过萃取,降低溶液中碘单质的浓度;实验Ⅰ中滴加
KSCN溶液后,观察到溶液颜色为红色,说明反应存在限度,故答案为:I;溶液颜色为红色。
2
(2)实验Ⅱ中滴加KSCN溶液,观察到颜色比实验Ⅰ浅。请用平衡移动原理解释其原因:在实验Ⅰ基础
上,增大反应物 的浓度后,促使 平衡向 浓度减小的方向(正向)移动,水溶液中
浓度比实验Ⅰ中 浓度低,故答案为:增大反应物 的浓度后,促使 平衡
向 浓度减小的方向(正向)移动,水溶液中 浓度比实验Ⅰ中 浓度低。
(3)①仪器a的名称为球形冷凝管,故答案为:球形冷凝管;
②实验Ⅲ中磁力搅拌的目的是:磁力搅拌增大了有机相中的溶质碘与水的接触面积,故答案为:磁力搅拌
增大了有机相中的溶质碘与水的接触面积;
③加入足量铁粉后三价铁会与之反应生成二价铁,发生反应为: ,故答案为:
;
④根据所给信息分析可知,最终溶液颜色为浅绿色的原因为 与 反应生成 的速率小于 与足
量铁粉反应生成 的速率,故答案为: 与 反应生成 的速率小于 与足量铁粉反应生成
的速率。