文档内容
INCLUDEPICTURE " 第 七 章 .tif" \*
MERGEFORMAT INCLUDEPICTURE " 第 七
章 .tif" \* MERGEFORMAT
第1讲 化学反应速率及其影响因素
【2020·备考】
最新考纲:1.了解化学反应速率的概念、反应速率的定量表示方法。2.了解催化剂
在生产、生活和科学研究领域中的重大作用。3.理解外界条件(浓度、温度、压强、催
化剂等)对反应速率的影响,认识并能用相关理论解释其一般规律。4.了解反应活
化能的概念。5.了解化学反应速率的调控在生活、生产和科学研究领域中的重要作
用。
核心素养:1.变化观念与平衡思想:能认识化学反应速率是变化的,知道化学反应
速率与外界条件有关,并遵循一定规律;能多角度、动态地分析化学反应速率,运
用化学反应原理解决实际问题。2.科学探究与创新意识:能发现和提出有关化学反
应速率的有探究价值的问题;通过控制变量来探究影响化学反应速率的外界条件。考点一 化学反应速率
(频数:★★☆ 难度:★☆☆)
INCLUDEPICTURE "名师课堂.tif" \* MERGEFORMAT INCLUDEPICTURE
" 名 师 课 堂 .tif" \* MERGEFORMAT
INCLUDEPICTURE " 书名号 .TIF " \* MERGEFORMAT INCLUDEPICTURE
" 书名号 .TIF" \* MERGEFORMAT 名师课堂导语 化学反应速率在高考中主要
在二卷中设项考查,考查角度有以下几个方面:(1)速率影响因素分析。(2)根据图
表信息求算化学反应速率。(3)根据图表信息比较反应速率大小。(4)根据信息求算
某一反应的正逆速率。
1.化学反应速率
INCLUDEPICTURE "5H472.tif" \* MERGEFORMATINCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
计算反应速率时,我们往往忽略溶液的体积,特别是给出的是物质的量的变化量
时,一定要先转化为物质的量浓度的变化量,再进行计算。
2.化学反应速率与化学计量数的关系
(1)内容:对于已知反应mA(g)+nB(g)===pC(g)+qD(g),其化学反应速率可用不同
的反应物或生成物来表示,当单位相同时,化学反应速率的数值之比等于方程式
中各物质的化学计量数之比,即 (A)∶ (B)∶ (C)∶ (D)= m ∶ n ∶ p ∶ q 。
v v v v
(2)实例:一定温度下,在密闭容器中发生反应:3A(g)+B(g) INCLUDEPICTURE
"KN.TIF" \* MERGEFORMAT 2C(g)。已知 (A)=0.6 mol·L-1·s-1,则 (B)
v v
=0.2 mol·L-1·s-1, (C)=0.4 mol·L-1·s-1。
v
INCLUDEPICTURE " 名 师 课 堂 实 录 .tif" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
当比较用不同物质表示同一反应速率的相对大小时,必须做到两个统一:即按照
化学计量数关系换算成同一物质、同一单位表示,再比较数值大小。3.求解反应速率的解题模式:“三段式”法
对 于 反 应 mA(g) + nB(g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
pC(g)+qD(g),起始时A的浓度为a mol·L-1,B的浓度为b mol·L-1,反应
进行至t 时,A消耗了x mol·L-1,则化学反应速率可计算如下:
1
则:(A)=mol·L-1·s-1,(B)=mol·L-1· s-1,(C)=mol·L-1·s-1,(D)=mol·L-1·s-
v v v v
1。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)化学反应速率是指一定时间内任何一种反应物浓度的减少或任何一种生成物
浓度的增加(×)
(2)化学反应速率为0.8 mol·L-1·s-1是指1 s时某物质的浓度为0.8 mol·L-1(×)
(3)由 =计算平均速率,用反应物表示为正值,用生成物表示为负值(×)
v
(4)同一化学反应,相同条件下用不同物质表示的反应速率,其数值可能不同,但表
示的意义相同(√)
(5)对于任何化学反应来说,反应速率越大,反应现象就越明显(×)
2.(教材改编题)(RJ选修4·P 5改编)某温度下,浓度都是1 mol·L-1的两种气体X
19 2
和Y ,在密闭容器中反应生成气体Z,经t min后,测得各物质的浓度分别为c(X )
2 2
=0.4 mol·L-1,c(Y )=0.6 mol·L-1,c(Z)=0.4 mol·L-1,则该反应的化学方程式可
2
表示为( )
A.2X + 3Y INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT 2X Y
2 2 2 3
B.3X + 2Y INCLUDEPICTURE
2 2
"KN.TIF" \* MERGEFORMAT 2X Y
3 2
C.X + 2Y INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT 2XY
2 2 2
D.2X + Y INCLUDEPICTURE
2 2"KN.TIF" \* MERGEFORMAT 2X Y
2
答案 B
3.(思维探究题) 比较化学反应速率大小时,可通过比较化学反应速率与化学计
量数的比值的大小快速判定。
[运用]反应4CO+2NO =====N +4CO 在不同条件下的化学反应速率如下。
2 2 2
① (CO)=1.5 mol·L-1·min-1 ② (NO )=0.7 mol·L-1·min-1
v v 2
③ (N )=0.4 mol·L-1·min-1 ④ (CO )=1.1 mol·L-1·min-1
v 2 v 2
⑤ (NO )=0.01 mol·L-1·s-1
v 2
上述5种情况反应的速率由大到小的顺序为________。
答案 ③①②⑤④
INCLUDEPICTURE "题组诊断.tif" \* MERGEFORMAT INCLUDEPICTURE
" 题 组 诊 断 .tif" \* MERGEFORMAT
[A组 基础知识巩固]
1.(2018·淄博联考)对于可逆反应 A(g)+3B(s) INCLUDEPICTURE "KN.TIF" \*
MERGEFORMAT 2C(g)+2D(g),在不同条件下的化学反应速率如下,其
中表示的反应速率最快的是( )
A. (A)=0.5 mol·L-1·min-1 B. (B)=1.2 mol·L-1·s-1
v v
C. (D)=0.4 mol·L-1·min-1 D. (C)=0.1 mol·L-1·s-1
v v
解析 本题可以采用归一法进行求解,通过方程式的化学计量数将不同物质表示
的反应速率折算成同一物质表示的反应速率进行比较,B物质是固体,不能表示
反应速率;C项中对应的 (A)=0.2 mol·L-1·min-1;D项中对应的 (A)=
v v3 mol·L-1·min-1。
答案 D
2.将等物质的量的A、B混合于2 L的恒容密闭容器中,发生如下反应:3A(g)+
B(g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT xC(g)+2D(g),经
5 min后,测得D的物质的量为1 mol,C的平均反应速率是0.1 mol·L-1·min-1。则
x的值为( )
A.1 B.2
C.3 D.4
解析 先计算出用D表示的该反应的反应速率: (D)=1 mol÷2 L÷5 min=
v
0.1 mol·L-1·min-1,根据C与D的反应速率关系有x∶2=0.1 mol·L-1·min-1∶
0.1 mol·L-1·min-1,则x=2。
答案 B
3.(2018·浙江杭州四校期中联考)一定条件下,在体积为10 L的固定容器中发生反
应:N (g)+3H (g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
2 2
2NH (g) ΔH<0,反应过程如图所示,下列说法正确的是( )
3
INCLUDEPICTURE "10X580.TIF" \* MERGEFORMAT
A.t min时,正、逆反应速率相等
1
B.X曲线表示NH 的物质的量随时间变化的关系
3
C.0~8 min内,H 的平均反应速率 (H )=0.075 mol·L-1· min-1
2 v 2D.10~12 min,升高温度,反应速率减慢
解析 t min后,X、Y的物质的量继续发生变化,则t min时该反应未达到平衡状
1 1
态,故t min时,正、逆反应速率不相等,A错误。由题图可知,8~10 min处于平衡
1
状态,0~8 min内,X、Y的物质的量变化分别为0.6 mol、0.9 mol,二者的比值为
0.6 mol∶0.9 mol=2∶3,结合反应N (g)+3H (g) INCLUDEPICTURE "KN.TIF" \*
2 2
MERGEFORMAT 2NH (g)推知,X曲线表示NH ,Y曲线表示H ,B正确。
3 3 2
0~8 min内,n(H )由1.2 mol减少到0.3 mol,则 (H )==0.011 25 mol·L-1·min-1,
2 v 2
C错误。该反应为放热反应,升高温度,化学反应速率加快,平衡向逆反应方向移
动,n(X)减小,n(Y)增大,与题图不符,D错误。
答案 B
【方法规律】
依据图像求反应速率的步骤
INCLUDEPICTURE "10X581.TIF" \* MERGEFORMAT
[B组 考试能力过关]
4.(全国卷节选)在容积为1.00 L的容器中,通入一定量的N O ,发生反应N O (g)
2 4 2 4
INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT 2NO (g),随温度升高,
2
混合气体的颜色变深。
INCLUDEPICTURE "10X582.TIF" \* MERGEFORMAT在0~60 s时段,反应速率 (N O )为________mol·L-1·s-1。
v 2 4
解析 由题图可知,0~60 s时段,N O 的物质的量浓度变化为0.060 mol·L-1,
2 4
(N O )==0.001 0 mol·L-1·s-1。
v 2 4
答案 0.001 0
5.[2018·课标全国Ⅰ,28(2)]F.Daniels等曾利用测压法在刚性反应器中研究了25
℃时N O (g)分解反应:
2 5
其中NO 二聚为N O 的反应可以迅速达到平衡。体系的总压强p随时间t的变化
2 2 4
如表所示(t=∞时,N O (g)完全分解):
2 5
t/min 0 40 80 160 260 1 300 1 700 ∞
p/kPa 35.8 40.3 42.5 45.9 49.2 61.2 62.3 63.1
研究表明,N O (g)分解的反应速率 =2×10-3×pN O (kPa·min-1)。t=62 min时,
2 5 v 2 5
测得体系中pO =2.9 kPa,则此时的pN O =________kPa, =________
2 2 5 v
kPa·min-1。
解析 t=62 min时,体系中pO =2.9 kPa,根据三段式法得
2
则62 min时pN O =30.0 kPa, =2×10-3×30.0 kPa·min-1=6.0×10-2kPa·min-
2 5 v1。
答案 30.0 6.0×10-2
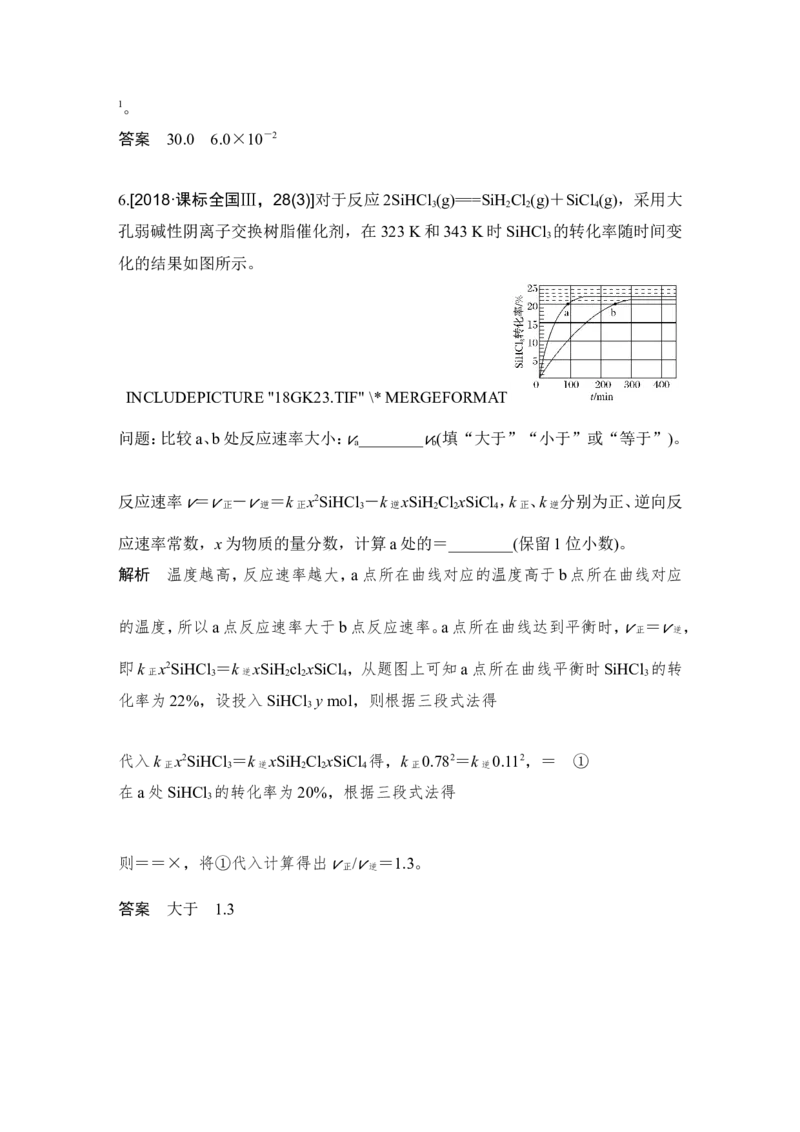
6.[2018·课标全国Ⅲ,28(3)]对于反应2SiHCl (g)===SiH Cl (g)+SiCl (g),采用大
3 2 2 4
孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl 的转化率随时间变
3
化的结果如图所示。
INCLUDEPICTURE "18GK23.TIF" \* MERGEFORMAT
问题:比较a、b处反应速率大小: ________ (填“大于”“小于”或“等于”)。
va vb
反应速率 = - =k x2SiHCl -k xSiH Cl xSiCl ,k 、k 分别为正、逆向反
v v正 v逆 正 3 逆 2 2 4 正 逆
应速率常数,x为物质的量分数,计算a处的=________(保留1位小数)。
解析 温度越高,反应速率越大,a点所在曲线对应的温度高于b点所在曲线对应
的温度,所以a点反应速率大于b点反应速率。a点所在曲线达到平衡时, = ,
v正 v逆
即k x2SiHCl =k xSiH cl xSiCl ,从题图上可知a点所在曲线平衡时SiHCl 的转
正 3 逆 2 2 4 3
化率为22%,设投入SiHCl y mol,则根据三段式法得
3
代入k x2SiHCl =k xSiH Cl xSiCl 得,k 0.782=k 0.112,= ①
正 3 逆 2 2 4 正 逆
在a处SiHCl 的转化率为20%,根据三段式法得
3
则==×,将①代入计算得出 / =1.3。
v正v逆
答案 大于 1.3考点二 影响化学反应速率的因素
(频数:★★★ 难度:★★☆)
INCLUDEPICTURE "名师课堂.tif" \* MERGEFORMAT INCLUDEPICTURE
" 名 师 课 堂 .tif" \* MERGEFORMAT
INCLUDEPICTURE " 书名号 .TIF " \* MERGEFORMAT INCLUDEPICTURE
" 书名号 .TIF" \* MERGEFORMAT 名师课 堂导语 化学反应速率的影响因素是
高频考点,主要考查外界条件改变对速率影响的结论判断;由图像速率的改变判
断外界条件的改变;另外要注意外界条件改变对速率的影响和平衡的影响的关系。
1.内因
反应物本身的性质是影响化学反应速率的主要因素。如相同条件下,Mg、Al与稀
盐酸反应的速率大小关系为: (Mg)> (Al)。
v v
2.外因(其他条件不变,只改变一个条件)
INCLUDEPICTURE "5H474.TIF" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT浓度对化学反应速率的影响的理解
①固体和纯液体对化学反应速率无影响,但要注意水(液态)对溶液的稀释作用。
②浓度的改变必须是真正参加反应离子的浓度,如酸碱中和反应影响速率的是
H+、OH-浓度。
③体系中各组分气体浓度同等程度的改变相当于压强的改变。
3.理论解释——有效碰撞理论
(1)活化分子:能够发生有效碰撞的分子。
(2)活化能:如图
INCLUDEPICTURE "5H475.TIF" \* MERGEFORMAT
图中:E 为正反应的活化能,使用催化剂时的活化能为E ,E 为逆反应的活化能,
1 3 2
反应热为E - E 。
1 2
(3)有效碰撞:活化分子之间能够引发化学反应的碰撞。
(4)活化分子、有效碰撞与反应速率的关系
INCLUDEPICTURE "5H476.TIF" \* MERGEFORMAT
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)升高温度时,不论正反应是吸热还是放热,正、逆反应的速率都增大(√)
(2)可逆反应中减小产物的浓度可增加正反应的速率(×)
(3)增大反应体系的压强,反应速率不一定增大(√)
(4)增大反应物的浓度,能够增大活化分子的百分含量,所以反应速率增大(×)(5)对可逆反应FeCl +3KSCN INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
3
Fe(SCN) +3KCl,增加氯化钾浓度,逆反应速率加快(×)
3
2.(教材改编题)(RJ选修4·P 2改编)中国首条“生态马路”在上海复兴路隧道建
24
成,它运用了“光触媒”技术,在路面涂上一种光催化剂涂料,可将汽车尾气中
45%的NO和CO转化成N 和CO 。下列对此反应的叙述中正确的是( )
2 2
A.使用光催化剂不改变反应速率
B.使用光催化剂能增大NO的转化率
C.升高温度能加快反应速率
D.改变压强对反应速率无影响
答案 C
3.(思维探究题)[小组讨论]有人说压强对化学反应速率的影响是通过改变浓度实
现的。
你对这句话是如何理解的?并完成以下填空:
一 定 温 度 下 , 反 应 N (g) + O (g) INCLUDEPICTURE "KN.TIF" \*
2 2
MERGEFORMAT 2NO(g)在密闭容器中进行,回答下列措施对化学反应速
率的影响(填“增大”、“减小”或“不变”)。
(1)缩小体积使压强增大:________;
(2)恒容充入N :________;
2
(3)恒容充入He:________;
(4)恒压充入He:________。
答案 这句话是正确的。但压强仅对有气体参加的反应起作用。增大压强,所有参
与反应的气体的浓度均增大,如2SO (g)+O (g) INCLUDEPICTURE "KN.TIF" \*
2 2
MERGEFORMAT 2SO (g)增大压强,SO 、O 、SO 的浓度均增大,正、逆反
3 2 2 3
应速率均增大。而增大浓度可只增大反应物或生成物的浓度,若只增大反应物的
浓度, 瞬间增大, 不变。压强对无气体参与的反应无影响,但浓度仍可改变无
v正 v逆
气体参与的反应的化学反应速率。(1)增大 (2)增大 (3)不变 (4)减小
INCLUDEPICTURE "题组诊断.tif" \* MERGEFORMAT INCLUDEPICTURE
" 题 组 诊 断 .tif" \* MERGEFORMAT
[A组 基础知识巩固]
1.(2018·山东临沂一模)在Ag+催化作用下,Cr3+被S O氧化为Cr O的机理为S O
2 2 2
+2Ag+===2SO+2Ag2+ 慢
2Cr3++6Ag2++7H O===6Ag++14H++Cr O 快
2 2
下列有关说法正确的是( )
A.反应速率与Ag+浓度有关
B.Ag2+也是该反应的催化剂
C.Ag+能降低该反应的活化能和焓变
D. (Cr3+)= (S O)
v v 2
解析 Ag+浓度越大,反应速率越快,A正确;Ag2+为中间产物,不是催化剂,故B
错误;Ag+能降低该反应的活化能,但不改变焓变,C错误;反应的总化学方程式为
3S O+2Cr3++7H O===6SO+14H++Cr O,反应速率之比等于化学计量数之比,
2 2 2
则3 (Cr3+)=2 (S O),D错误。
v v 2
答案 A
2. 在 一 定 的 条 件 下 , 某 反 应 X(g) INCLUDEPICTURE "KN.TIF" \*
MERGEFORMAT Y(g)+Z(g)分解的部分实验数据如下:
反应时间/min 0 10 20 30 40 50
c(X)/mol·L-1 0.100 0.090 0.080 0.070 0.060 0.050
反应时间/min 60 70 80 90 100
c(X)/mol·L-1 0.040 0.030 0.020 0.010 0.000
下列有关说法正确的是( )A.X的浓度越大,反应速率越大
B.X的浓度越大,消耗一半时所用的时间越短
C.X分解的速率与其浓度无关
D.X的分解速率先快后慢
解析 X的分解速率是匀速的,与其浓度无关,A、D错误,C正确;X的分解速率
不变;X的浓度越大,消耗一半时所用的时间越长,B项错误。
答案 C
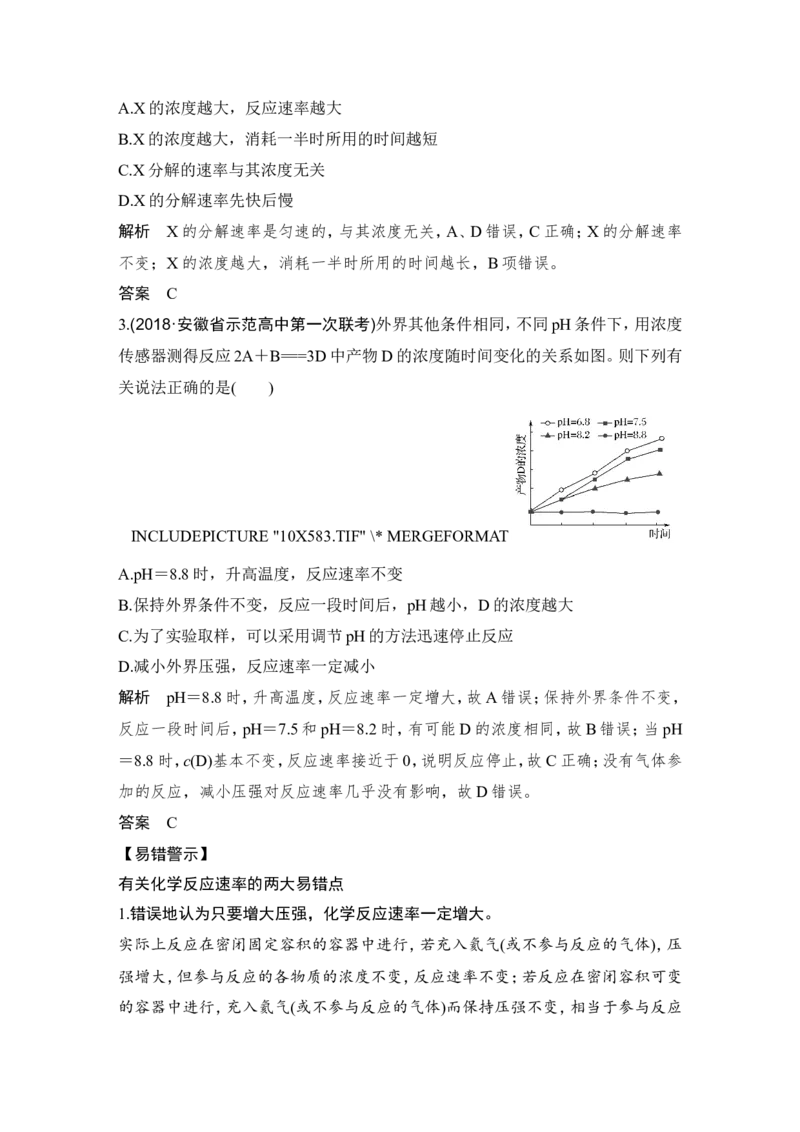
3.(2018·安徽省示范高中第一次联考)外界其他条件相同,不同pH条件下,用浓度
传感器测得反应2A+B===3D中产物D的浓度随时间变化的关系如图。则下列有
关说法正确的是( )
INCLUDEPICTURE "10X583.TIF" \* MERGEFORMAT
A.pH=8.8时,升高温度,反应速率不变
B.保持外界条件不变,反应一段时间后,pH越小,D的浓度越大
C.为了实验取样,可以采用调节pH的方法迅速停止反应
D.减小外界压强,反应速率一定减小
解析 pH=8.8时,升高温度,反应速率一定增大,故A错误;保持外界条件不变,
反应一段时间后,pH=7.5和pH=8.2时,有可能D的浓度相同,故B错误;当pH
=8.8时,c(D)基本不变,反应速率接近于0,说明反应停止,故C正确;没有气体参
加的反应,减小压强对反应速率几乎没有影响,故D错误。
答案 C
【易错警示】
有关化学反应速率的两大易错点
1.错误地认为只要增大压强,化学反应速率一定增大。
实际上反应在密闭固定容积的容器中进行,若充入氦气(或不参与反应的气体),压
强增大,但参与反应的各物质的浓度不变,反应速率不变;若反应在密闭容积可变
的容器中进行,充入氦气(或不参与反应的气体)而保持压强不变,相当于参与反应的各物质的浓度减小,反应速率减小。
2.不能正确区分外界条件对可逆反应的正、逆反应速率的影响趋势。
如对ΔH<0的反应,升高温度,平衡逆向移动,正、逆反应速率都增大,并不是只
增大逆反应速率,只是逆反应速率增大的程度大于正反应速率;工业合成氨中,移
出部分氨气(平衡右移),在移出氨气时刻,正反应速率瞬间不变,逆反应速率减小。
[B组 考试能力过关]
4.(全国卷节选)COCl 的分解反应为 COCl (g)===Cl (g)+CO(g) ΔH=+108
2 2 2
kJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下图所
示(第10 min到14 min的COCl 浓度变化曲线未示出):
2
INCLUDEPICTURE "5H477.TIF" \* MERGEFORMAT
(1)比较第2 min反应温度T(2)与第8 min反应温度T(8)的高低:T(2)________T(8)
(填“<”“>”或“=”)。
(2)比较产物CO在2~3 min、5~6 min和12~13 min时平均反应速率[平均反应
速率分别以 (2~3)、 (5~6)、 (12~13)表示]的大小________。
v v v
(3)比较反应物COCl 在5~6 min和15~16 min时平均反应速率的大小: (5~
2 v
6)________ (15 ~ 16)( 填 “ < ” “ > ” 或 “ = ” ) , 原 因 是
v
______________________________________________________________________
_____________________________________________________________________
。
解析 (1)2 min和8 min时反应都处于平衡状态,在4 min时生成物浓度都增大,反应物浓度减小,则改变的条件是升高温度,故T(2)<T(8)。
(2)分析图像表示的意义,根据图像可得出平均反应速率为 (5~6)> (2~3)=
v v
(12~13)。
v
(3)分析图像可知反应在5~6 min和15~16 min时,反应温度相同,因为在相同温
度时,该反应的反应物浓度越高,反应速率越大,故 (5~6)> (15~16)。
v v
答案 (1)< (2) (5~6)> (2~3)= (12~13)
v v v
(3)> 在相同温度时,该反应的反应物浓度越高,反应速率越大
5.[2018·江苏化学,20(4)]在有氧条件下,新型催化剂M能催化NH 与NO 反应生
3 x
成N 。
2
①NH 与 NO 生成 N 的反应中,当生成 1 mol N 时,转移的电子数为
3 2 2 2
________mol。
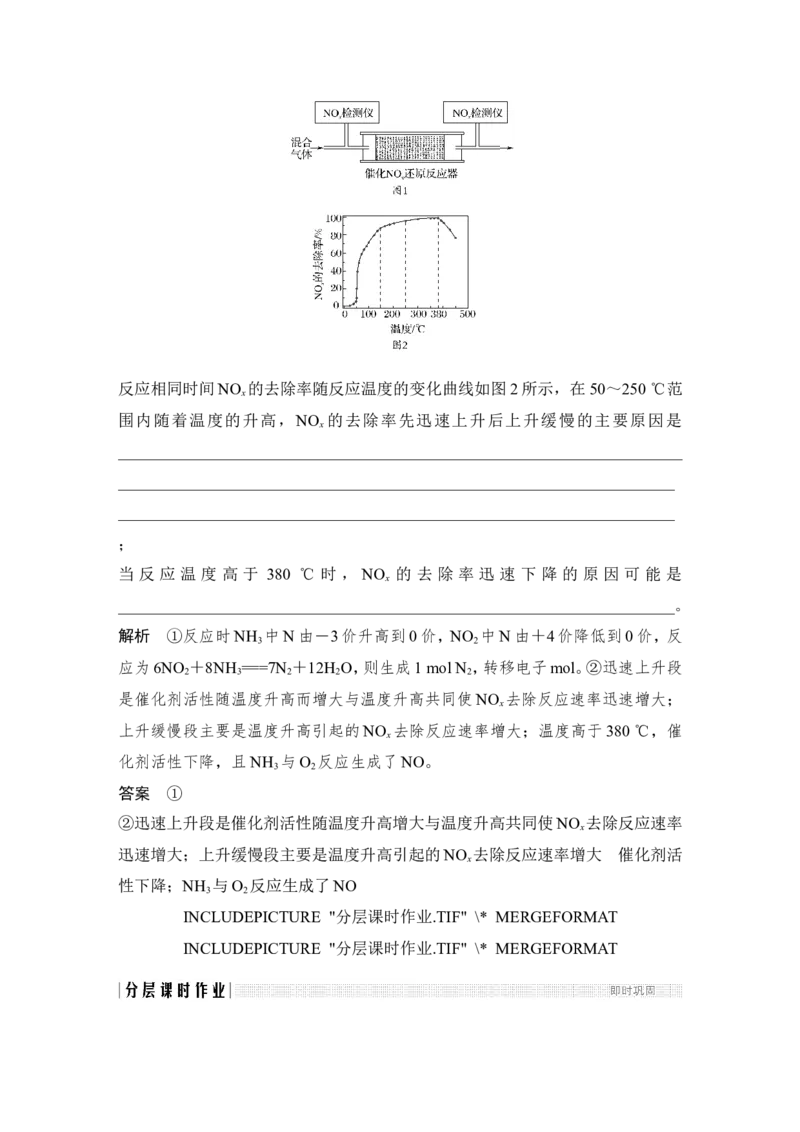
②将一定比例的O 、NH 和NO 的混合气体,匀速通入装有催化剂M的反应器中
2 3 x
反应(装置如图1)。
INCLUDEPICTURE "18GK61.TIF" \* MERGEFORMAT反应相同时间NO 的去除率随反应温度的变化曲线如图2所示,在50~250 ℃范
x
围内随着温度的升高,NO 的去除率先迅速上升后上升缓慢的主要原因是
x
______________________________________________________________________
_____________________________________________________________________
_____________________________________________________________________
;
当 反 应 温 度 高 于 380 ℃ 时 , NO 的 去 除 率 迅 速 下 降 的 原 因 可 能 是
x
_____________________________________________________________________。
解析 ①反应时NH 中N由-3价升高到0价,NO 中N由+4价降低到0价,反
3 2
应为6NO +8NH ===7N +12H O,则生成1 mol N ,转移电子mol。②迅速上升段
2 3 2 2 2
是催化剂活性随温度升高而增大与温度升高共同使NO 去除反应速率迅速增大;
x
上升缓慢段主要是温度升高引起的NO 去除反应速率增大;温度高于380 ℃,催
x
化剂活性下降,且NH 与O 反应生成了NO。
3 2
答案 ①
②迅速上升段是催化剂活性随温度升高增大与温度升高共同使NO 去除反应速率
x
迅速增大;上升缓慢段主要是温度升高引起的NO 去除反应速率增大 催化剂活
x
性下降;NH 与O 反应生成了NO
3 2
INCLUDEPICTURE "分层课时作业.TIF" \* MERGEFORMAT
INCLUDEPICTURE "分层课时作业.TIF" \* MERGEFORMAT[A级 全员必做题]
1.以下是几位同学在学习化学反应速率理论后发表的一些看法,其中不正确的是(
)
A.化学反应速率理论可指导怎样提高原料的转化率和生成物的产率
B.化学反应速率理论可以指导怎样在一定时间内快出产品
C.影响化学反应速率的主要因素是反应物的性质,浓度、温度、催化剂、反应物颗
粒大小等外部因素也会对化学反应速率产生影响
D.正确利用化学反应速率理论可提高化工生产的综合经济效益
解析 化学反应速率理论研究的是化学反应进行的快慢问题,不能指导提高原料
的转化率和生成物的产率。
答案 A
2.(2018·北京六十六中学期中)升高温度时,化学反应速率加快原因的合理解释是(
)
A.该化学反应的过程是吸热的
B.该化学反应的过程是放热的
C.分子运动速率加快,使反应物分子的碰撞机会增多
D.反应物分子的能量增加,活化分子百分数增加,有效碰撞次数增多
解析 无论反应是吸热反应还是放热反应,升高温度,化学反应速率均增大,A、B
两项错误;升高温度,反应物的分子的能量增加,活化分子百分数增加,单位体积
内活化分子总数增加,有效碰撞次数增多,反应速率加快,C项错误,D项正确。
答案 D
3.(2019·太原模拟)在一容积可变的密闭容器中加入WO 和H 进行反应WO (s)+
3 2 3
3H (g)=====W(s)+3H O(g),下列说法不正确的是( )
2 2
A.增加H O(g)的量,消耗H 的速率不变
2 2
B.将容器的体积缩小一半,其反应速率加快
C.保持体积不变,充入氩气,其反应速率不变
D.保持压强不变,充入氖气,H O(g)的生成速率减慢
2
解析 增加H O(g)的量,容器体积会增大,H 的浓度会瞬间减小,则消耗H 的速
2 2 2
率瞬间减小,A项错误;将体积缩小,氢气的浓度增大,反应速率加快,B项正确;
体积不变,充入氩气,H 、H O(g)的浓度不变,反应速率不变,C项正确;压强不变,
2 2充入氖气,体积增大,H 、H O(g)的浓度减小,反应速率减慢,D项正确。
2 2
答案 A
4.(2019·福建厦门质检,7)2SO (g)+O (g)===2SO (g) ΔH=-198 kJ·mol-1,在
2 2 3
V O 存在时,该反应的机理为:V O +SO ===2VO +SO (快),4VO +
2 5 2 5 2 2 3 2
O ===2V O (慢)。
2 2 5
下列说法中正确的是( )
A.反应速率主要取决于V O 的质量
2 5
B.VO 是该反应的催化剂
2
C.逆反应的活化能大于198 kJ·mol-1
D.增大SO 的浓度可显著提高反应速率
2
解析 由反应机理可知,V O 是该反应的催化剂,反应速率与催化剂V O 的质量
2 5 2 5
有一定关系,但主要取决于催化剂V O 的表面积,A、B项错误;ΔH=正反应的活
2 5
化能-逆反应的活化能=-198 kJ·mol-1,所以逆反应的活化能大于198 kJ·mol-
1,C项正确;使用催化剂可以显著提高反应速率,增大SO 的浓度可以提高反应速
2
率(不是显著提高),D项错误。
答案 C
5.NH 和纯净的O 在一定条件下发生如下反应:
3 2
4NH (g)+3O (g 2N (g)+6H O(g)
3 2 2 2
现向一容积不变的2 L密闭容器中充入4 mol NH 和3 mol O ,4 min后,测得生成
3 2
的H O占混合气体体积的40%,则下列表示此段时间内该反应的平均速率不正确
2
的是( )
A. (N )=0.125 mol·L-1·min-1
v 2
B. (H O)=0.375 mol·L-1·min-1
v 2
C. (O )=0.225 mol·L-1·min-1
v 2
D. (NH )=0.250 mol·L-1·min-1
v 3解析 设4 min时,生成6x mol H O(g)
2
据题意,则有:=0.4 解得:x=0.5
则4 min内H O的变化浓度为
2
Δc(H O)==1.5 mol·L-1
2
(H O)==0.375 mol·L-1·min-1,
v 2
再由各物质表示的速率之比等于各物质的化学计量数之比,可得各物质表示的反
应速率分别为
(N )=0.125 mol·L-1·min-1,
v 2
(NH )=0.250 mol·L-1·min-1,
v 3
(O )=0.187 5 mol·L-1·min-1。
v 2
答案 C
6.(2018·合肥模拟)三氯乙烯(C HCl )是地下水中有机污染物的主要成分,研究显
2 3
示,在地下水中加入高锰酸钾溶液可将其中的三氯乙烯除去,发生反应如下:
2KMnO +C HCl ===2KCl+2CO ↑+2MnO ↓+HCl
4 2 3 2 2
常温下,在某密闭容器中进行上述反应,测定c(KMnO )与时间的关系如表所示:
4
时间/min 0 2 4 6 7 …
c(KMnO )/(mol·L-1) 1.0 0.70 0.50 0.40 0.35 …
4
下列推断合理的是( )A.上述反应先慢后快
B.0~4 min时 (Cl-)=mol·L-1·min-1
v
C.若高锰酸钾完全反应,所用时间为8 min
D.随着反应的进行,c(K+)逐渐降低
解析 A项,分析表格中的数据,题述反应先快后慢,错误;B项,每消耗2 mol
KMnO 会生成3 mol Cl-, (Cl-)=×= mol·L-1·min-1,正确;C项,高锰酸钾完
4 v
全反应,其浓度为0,消耗时间大于8 min,错误;D项,钾离子未参与反应,故钾离
子浓度不变,错误。
答案 B
7.(2018·试题调研)在298 K时,实验测得溶液中的反应H O +2HI===2H O+I ,
2 2 2 2
在反应物为不同浓度时的化学反应速率如表所示:
实验编号 1 2 3 4 5 6
c(HI)/ (mol·L-1) 0.100 0.200 0.150 0.100 ? 0.500
c(H O )/ (mol·L-1) 0.100 0.100 0.150 0.200 ? 0.400
2 2
/(mol·L-1·s-1) 0.007 60 0.015 2 0.017 1 0.015 2 0.022 8 0.152
v
根据表中数据可推知第5组实验中c(HI)、c(H O )不可能为( )
2 2
A.0.150 mol·L-1、0.200 mol·L-1
B.0.300 mol·L-1、0.100 mol·L-1
C.0.200 mol·L-1、0.200 mol·L-1
D.0.100 mol·L-1、0.300 mol·L-1
解析 分析表中数据可知,反应速率 与c(HI)和c(H O )的乘积成正比,以实验1
v 2 2
为参照,实验5的反应速率是其反应速率的3倍,故实验5中c(HI)和c(H O )的乘
2 2
积为实验1的3倍,C项符合题意。
答案 C
8.(2019·江西宜春奉新一中月考)为探究Fe3+和Cu2+对H O 分解反应的催化效果,
2 2
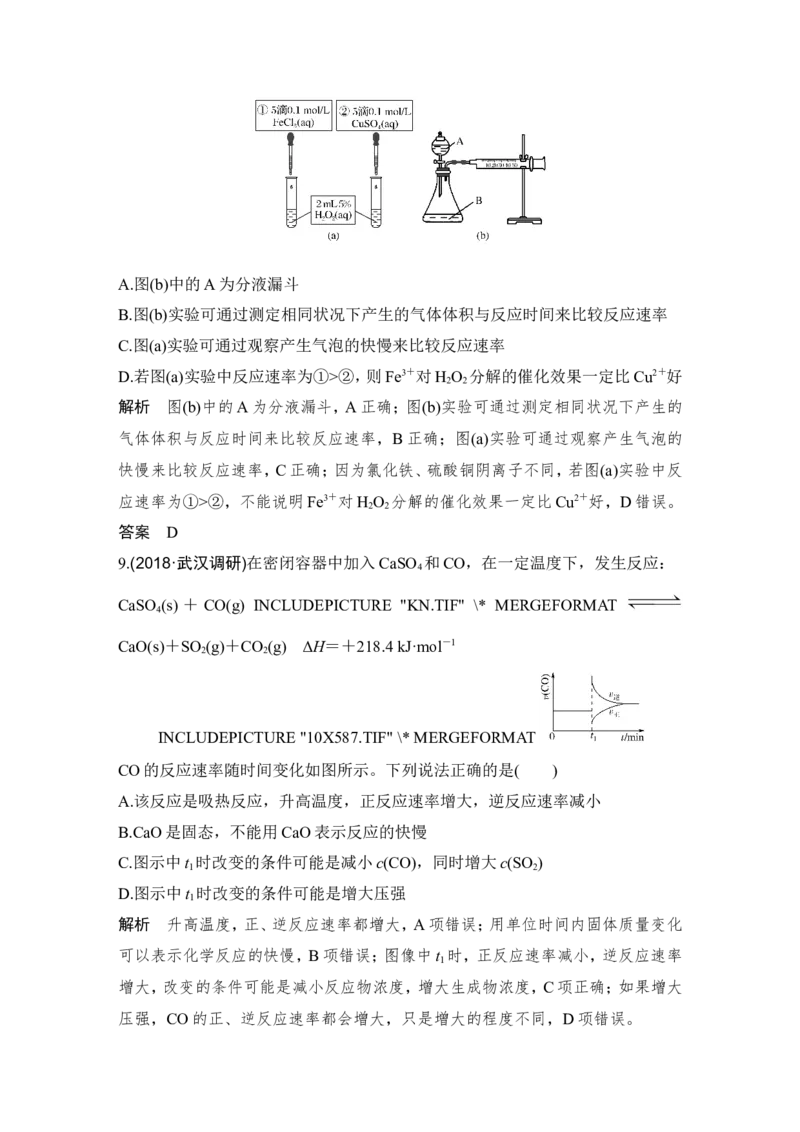
某同学分别设计了图(a)、图(b)所示的实验。下列叙述中不正确的是( )
INCLUDEPICTURE "10X586.TIF" \* MERGEFORMATA.图(b)中的A为分液漏斗
B.图(b)实验可通过测定相同状况下产生的气体体积与反应时间来比较反应速率
C.图(a)实验可通过观察产生气泡的快慢来比较反应速率
D.若图(a)实验中反应速率为①>②,则Fe3+对H O 分解的催化效果一定比Cu2+好
2 2
解析 图(b)中的A为分液漏斗,A正确;图(b)实验可通过测定相同状况下产生的
气体体积与反应时间来比较反应速率,B正确;图(a)实验可通过观察产生气泡的
快慢来比较反应速率,C正确;因为氯化铁、硫酸铜阴离子不同,若图(a)实验中反
应速率为①>②,不能说明Fe3+对H O 分解的催化效果一定比Cu2+好,D错误。
2 2
答案 D
9.(2018·武汉调研)在密闭容器中加入CaSO 和CO,在一定温度下,发生反应:
4
CaSO (s) + CO(g) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
4
CaO(s)+SO (g)+CO (g) ΔH=+218.4 kJ·mol-1
2 2
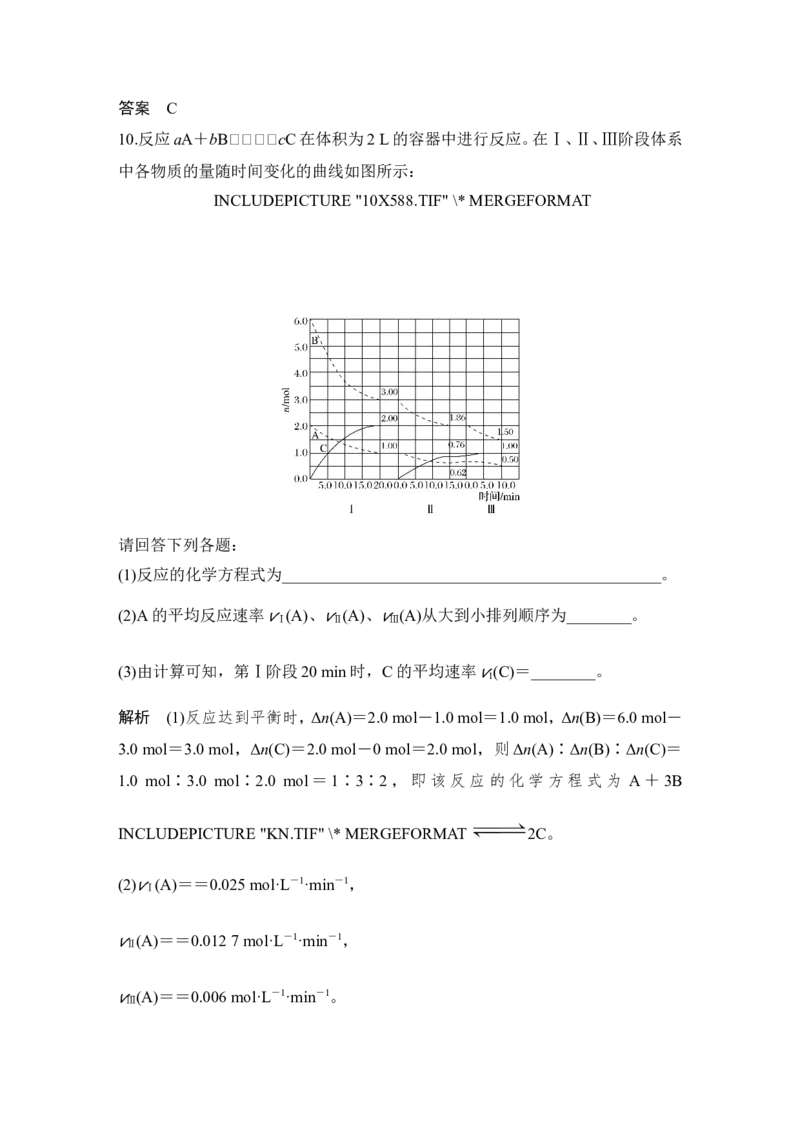
INCLUDEPICTURE "10X587.TIF" \* MERGEFORMAT
CO的反应速率随时间变化如图所示。下列说法正确的是( )
A.该反应是吸热反应,升高温度,正反应速率增大,逆反应速率减小
B.CaO是固态,不能用CaO表示反应的快慢
C.图示中t 时改变的条件可能是减小c(CO),同时增大c(SO )
1 2
D.图示中t 时改变的条件可能是增大压强
1
解析 升高温度,正、逆反应速率都增大,A项错误;用单位时间内固体质量变化
可以表示化学反应的快慢,B项错误;图像中t 时,正反应速率减小,逆反应速率
1
增大,改变的条件可能是减小反应物浓度,增大生成物浓度,C项正确;如果增大
压强,CO的正、逆反应速率都会增大,只是增大的程度不同,D项错误。答案 C
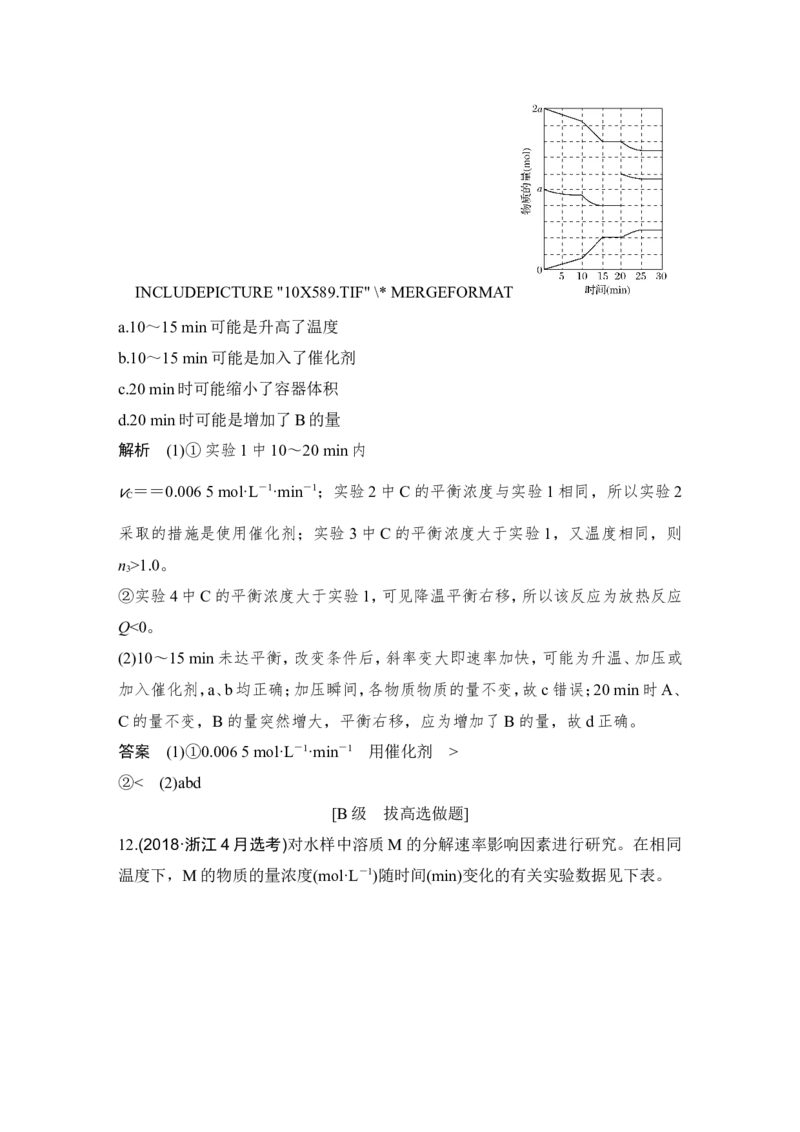
10.反应aA+bBcC在体积为2 L的容器中进行反应。在Ⅰ、Ⅱ、Ⅲ阶段体系
中各物质的量随时间变化的曲线如图所示:
INCLUDEPICTURE "10X588.TIF" \* MERGEFORMAT
请回答下列各题:
(1)反应的化学方程式为_______________________________________________。
(2)A的平均反应速率 (A)、 (A)、 (A)从大到小排列顺序为________。
vⅠ vⅡ vⅢ
(3)由计算可知,第Ⅰ阶段20 min时,C的平均速率 (C)=________。
v1
解析 (1)反应达到平衡时,Δn(A)=2.0 mol-1.0 mol=1.0 mol,Δn(B)=6.0 mol-
3.0 mol=3.0 mol,Δn(C)=2.0 mol-0 mol=2.0 mol,则Δn(A)∶Δn(B)∶Δn(C)=
1.0 mol∶3.0 mol∶2.0 mol=1∶3∶2,即该反应的化学方程式为 A+3B
INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT 2C。
(2) (A)==0.025 mol·L-1·min-1,
vⅠ
(A)==0.012 7 mol·L-1·min-1,
vⅡ
(A)==0.006 mol·L-1·min-1。
vⅢ故 (C)=2 (A)=0.05 mol·L-1·min-1。
vⅠ vⅠ
答案 (1)A+3B INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT 2C
(2) (A)> (A)> (A)
vⅠ vⅡ vⅢ
(3)0.05 mol·L-1·min-1
11.(2019·河南开封高级中学月考)实验室中做如下实验:一定条件下,在容积为
2.0 L 的恒容密闭容器中,发生如下反应:2A(g)+B(g) INCLUDEPICTURE
"KN.TIF" \* MERGEFORMAT 2C(g) ΔH=Q kJ/mol。
(1)若A、B起始物质的量均为零,通入C的物质的量(mol)随反应时间(min)的变化
情况如下表:
根据上表数据,完成下列填空:
①在实验1中反应在10~20 min内反应的平均速率 =________,实验2中采取
vC
的措施是________;实验3中n ________(填“>”“=”或“<”)1.0。
3
②比较实验4和实验1,可推测该反应中Q________0(填“>”“=”或“<”)。
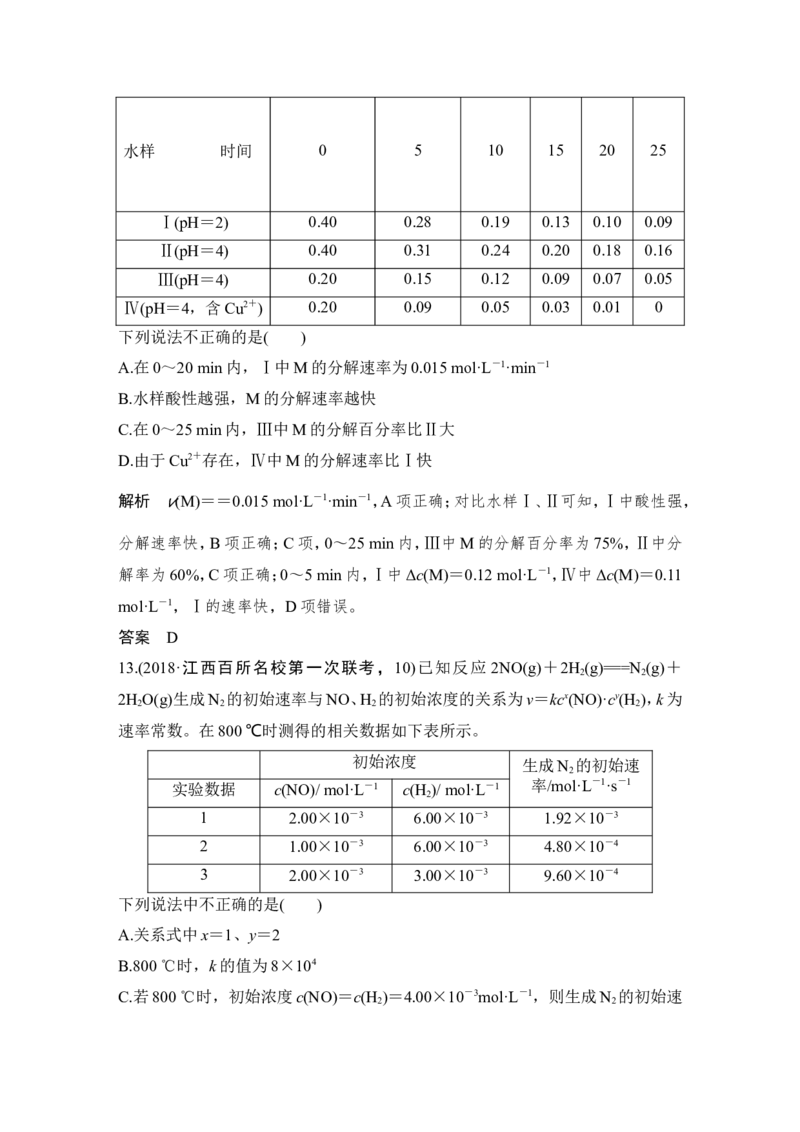
(2)在另一反应过程中A(g)、B(g)、C(g)物质的量变化如图所示,根据图中所示判断
下列说法正确的是________。INCLUDEPICTURE "10X589.TIF" \* MERGEFORMAT
a.10~15 min可能是升高了温度
b.10~15 min可能是加入了催化剂
c.20 min时可能缩小了容器体积
d.20 min时可能是增加了B的量
解析 (1)①实验1中10~20 min内
==0.006 5 mol·L-1·min-1;实验2中C的平衡浓度与实验1相同,所以实验2
vC
采取的措施是使用催化剂;实验3中C的平衡浓度大于实验1,又温度相同,则
n >1.0。
3
②实验4中C的平衡浓度大于实验1,可见降温平衡右移,所以该反应为放热反应
Q<0。
(2)10~15 min未达平衡,改变条件后,斜率变大即速率加快,可能为升温、加压或
加入催化剂,a、b均正确;加压瞬间,各物质物质的量不变,故c错误;20 min时A、
C的量不变,B的量突然增大,平衡右移,应为增加了B的量,故d正确。
答案 (1)①0.006 5 mol·L-1·min-1 用催化剂 >
②< (2)abd
[B级 拔高选做题]
12.(2018·浙江4月选考)对水样中溶质M的分解速率影响因素进行研究。在相同
温度下,M的物质的量浓度(mol·L-1)随时间(min)变化的有关实验数据见下表。水样 时间 0 5 10 15 20 25
Ⅰ(pH=2) 0.40 0.28 0.19 0.13 0.10 0.09
Ⅱ(pH=4) 0.40 0.31 0.24 0.20 0.18 0.16
Ⅲ(pH=4) 0.20 0.15 0.12 0.09 0.07 0.05
Ⅳ(pH=4,含Cu2+) 0.20 0.09 0.05 0.03 0.01 0
下列说法不正确的是( )
A.在0~20 min内,Ⅰ中M的分解速率为0.015 mol·L-1·min-1
B.水样酸性越强,M的分解速率越快
C.在0~25 min内,Ⅲ中M的分解百分率比Ⅱ大
D.由于Cu2+存在,Ⅳ中M的分解速率比Ⅰ快
解析 (M)==0.015 mol·L-1·min-1,A项正确;对比水样Ⅰ、Ⅱ可知,Ⅰ中酸性强,
v
分解速率快,B项正确;C项,0~25 min内,Ⅲ中M的分解百分率为75%,Ⅱ中分
解率为60%,C项正确;0~5 min内,Ⅰ中Δc(M)=0.12 mol·L-1,Ⅳ中Δc(M)=0.11
mol·L-1,Ⅰ的速率快,D项错误。
答案 D
13.(2018·江西百所名校第一次联考,10)已知反应 2NO(g)+2H (g)===N (g)+
2 2
2H O(g)生成N 的初始速率与NO、H 的初始浓度的关系为v=kcx(NO)·cy(H ),k为
2 2 2 2
速率常数。在800 ℃时测得的相关数据如下表所示。
初始浓度
生成N 的初始速
2
实验数据 c(NO)/ mol·L-1 c(H )/ mol·L-1
率/mol·L-1·s-1
2
1 2.00×10-3 6.00×10-3 1.92×10-3
2 1.00×10-3 6.00×10-3 4.80×10-4
3 2.00×10-3 3.00×10-3 9.60×10-4
下列说法中不正确的是( )
A.关系式中x=1、y=2
B.800 ℃时,k的值为8×104
C.若800 ℃时,初始浓度c(NO)=c(H )=4.00×10-3mol·L-1,则生成N 的初始速
2 2率为5.12×10-3mol·L-1·s-1
D.当其他条件不变时,升高温度,速率常数将增大
解析 由实验数据1和2可知,c(H )不变,c(NO)扩大1倍,反应速率扩大为原来
2
的=4倍,则x=2,由实验数据1和3可知,c(NO)不变,c(H )扩大1倍,反应速率
2
扩大为原来的=2倍,则y=1,A项错误;根据数据1可知800 ℃时,k的值为==
8×104,B项正确;若800 ℃时,初始浓度c(NO)=c(H )=4.00×10-3mol·L-1,则生
2
成 N 的初始速率 =k×c2(NO)×c(H )=[8×104×(4.00×10-3)2×(4.00×10-
2 v 2
3)]mol·L-1·s-1=5.12×10-3mol·L-1·s-1,C项正确;温度升高,反应速率加快,则当
浓度和其他条件不变时,升高温度,速率常数一定是增大的,D项正确。
答案 A
14.大气中的部分碘源于O 对海水中I-的氧化。某科学小组进行O 与含I-溶液反
3 3
应相关研究。
(1)O 将I-氧化生成I 的过程由3步反应组成:
3 2
①I-(aq)+O (g)===IO-(aq)+O (g) ΔH
3 2 1
②IO-(aq)+H+(aq) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
HOI(aq) ΔH
2
③HOI(aq)+I-(aq)+H+(aq) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
I (aq)+H O(l) ΔH
2 2 3
用 热 化 学 方 程 式 表 示 O 氧 化 I - 生 成 I 的 反 应
3 2
_____________________________________________________________________
_____________________________________________________________________
。
(2)O 在水中易分解,在一定条件下,O 的浓度减少一半时所需的时间(t)如下表所
3 3
示。已知:O 的起始浓度为0.021 6 mol·L-1。
3①在30 ℃、pH=4.0条件下,O 的分解速率为________mol·L-1·min-1。
3
②pH增大能加速O 分解,表明对O 分解起催化作用的是________。
3 3
③根据表中数据,推测O 在下列条件下分解速率依次增大的顺序为________(填
3
字母代号)。
a.40 ℃、pH=3.0
b.10 ℃、pH=4.0
c.30 ℃、pH=7.0
解析 (1)将所给的三个反应相加,即①+②+③可得总反应:2I-(aq)+O (g)+2H
3
+(aq)===I (aq)+O (g)+H O(l) ΔH=ΔH +ΔH +ΔH 。
2 2 2 1 2 3
(2)① ===1.00×10-4mol·L-1·min-1;②pH增大,则OH-浓度增大,pH增大能
v
加速O 分解,表示对O 分解起催化作用的是OH-;③由表中数据可知,40 ℃、pH
3 3
=3.0时,所需时间在31~158 min之间;10 ℃、pH=4.0时,所需时间>231 min;30
℃、pH=7.0时,所需时间<15 min,则分解速率依次增大的顺序为b、a、c。
答案 (1)O (g)+2I-(aq)+2H+(aq)===I (aq)+H O(l)+O (g) ΔH=ΔH +ΔH +
3 2 2 2 1 2
ΔH
3
(2)①1.00×10-4 ②OH- ③bac