文档内容
第六章 化学反应与能量
测试卷
时间:90分钟 分值:100分
可能用到的相对原子质量:H 1 C 12 O16 Na 23 Cl 35.5
一、选择题(每小题只有一个正确选项,共16×3分)
1.(2023·上海静安·统考二模)2022年6月17日,经中央军委批准,首艘自主设计建造的弹射型航空母
舰命名为“中国人民解放军海军福建舰”, 舷号“18” ,为我国第三艘航空母舰。下列说法正确的是
A.为屏蔽自身不被定位,福建舰的舰体采用的是高强度耐腐蚀低磁钢,其熔点高于纯铁
B.雷达系统相控阵化是福建舰的一大特色,所用碳化硅材料属于新型有机物
C.下水前,福建舰在舰体表面刷漆涂上中国海军灰白色涂装,目的之一是防止金属腐蚀
D.当前,各国常规动力航空母舰的燃料都是重油,为混合物,主要成分属于酯类
2.(2023·北京海淀·统考二模)甲、乙同学分别用如图所示装置验证铁的电化学防腐原理,相同时间后继
续进行实验。
实验①:甲同学分别向Ⅰ、Ⅱ中Fe电极附近滴加K[Fe(CN) ]溶液,Ⅰ中产生蓝色沉淀,Ⅱ中无沉淀。
3 6
实验②:乙同学分别取Ⅰ、Ⅱ中Fe电极附近溶液,滴加K[Fe(CN) ]溶液,Ⅰ、Ⅱ中均无沉淀。
3 6
下列说法正确的是
A.Ⅰ是牺牲阳极保护法,正极反应式为
B.Ⅱ为外加电流阴极保护法,Fe电极与外接电源的正极相连
C.由实验①中Ⅰ、Ⅱ现象的差异,推测K[Fe(CN) ]在Ⅰ中氧化性强于Ⅱ
3 6
D.由实验可知,两种保护法均能保护 ,且Ⅱ保护得更好
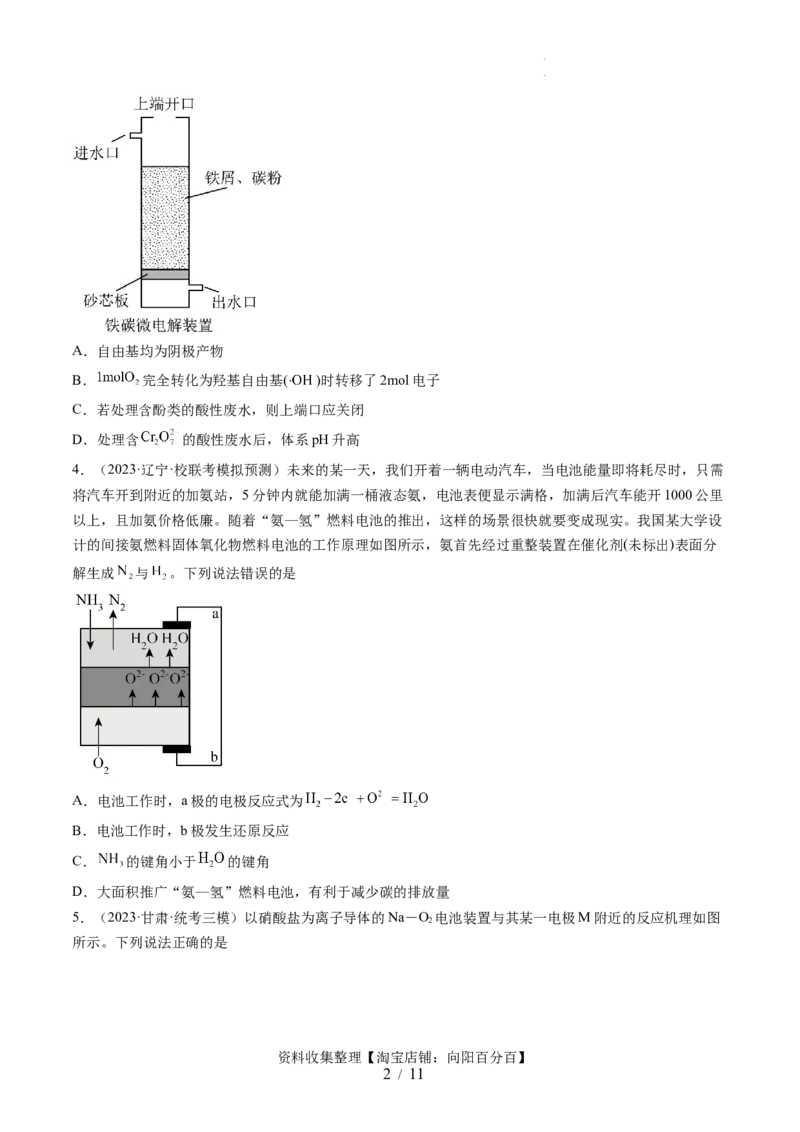
3.(2023·山东济南·山东省实验中学校考模拟预测)铁碳微电解技术是处理酸性废水的一种工艺,装置如
图所示。若上端口打开,并鼓入空气,可得到强氧化性中间体羟基自由基( );若上端口关闭,可得到
强还原性中间体氢原子( )。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】
1 / 11
学科网(北京)股份有限公司A.自由基均为阴极产物
B. 完全转化为羟基自由基( )时转移了2mol电子
C.若处理含酚类的酸性废水,则上端口应关闭
D.处理含 的酸性废水后,体系pH升高
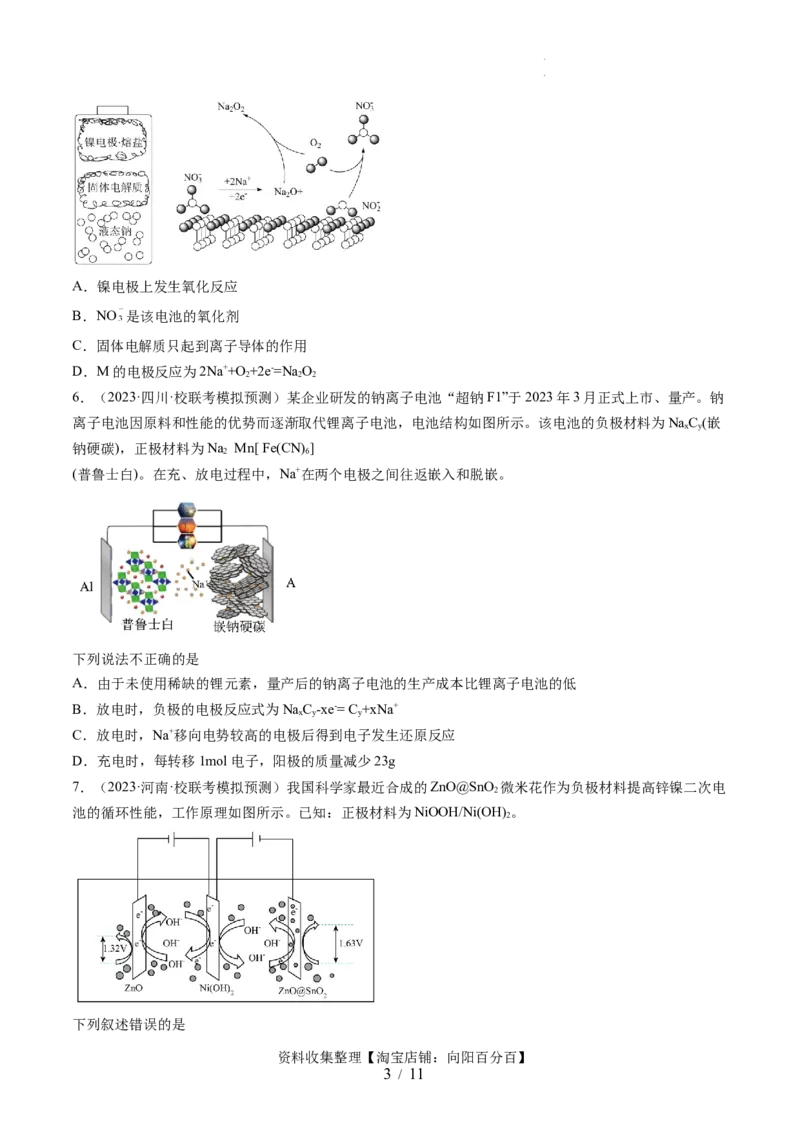
4.(2023·辽宁·校联考模拟预测)未来的某一天,我们开着一辆电动汽车,当电池能量即将耗尽时,只需
将汽车开到附近的加氨站,5分钟内就能加满一桶液态氨,电池表便显示满格,加满后汽车能开1000公里
以上,且加氨价格低廉。随着“氨—氢”燃料电池的推出,这样的场景很快就要变成现实。我国某大学设
计的间接氨燃料固体氧化物燃料电池的工作原理如图所示,氨首先经过重整装置在催化剂(未标出)表面分
解生成 与 。下列说法错误的是
A.电池工作时,a极的电极反应式为
B.电池工作时,b极发生还原反应
C. 的键角小于 的键角
D.大面积推广“氨—氢”燃料电池,有利于减少碳的排放量
5.(2023·甘肃·统考三模)以硝酸盐为离子导体的Na-O 电池装置与其某一电极M附近的反应机理如图
2
所示。下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】
2 / 11
学科网(北京)股份有限公司A.镍电极上发生氧化反应
B.NO 是该电池的氧化剂
C.固体电解质只起到离子导体的作用
D.M的电极反应为2Na++O +2e-=Na O
2 2 2
6.(2023·四川·校联考模拟预测)某企业研发的钠离子电池“超钠F1”于2023年3月正式上市、量产。钠
离子电池因原料和性能的优势而逐渐取代锂离子电池,电池结构如图所示。该电池的负极材料为NaC (嵌
x y
钠硬碳),正极材料为Na Mn[ Fe(CN) ]
2 6
(普鲁士白)。在充、放电过程中,Na+在两个电极之间往返嵌入和脱嵌。
下列说法不正确的是
A.由于未使用稀缺的锂元素,量产后的钠离子电池的生产成本比锂离子电池的低
B.放电时,负极的电极反应式为NaC -xe-= C +xNa+
x y y
C.放电时,Na+移向电势较高的电极后得到电子发生还原反应
D.充电时,每转移1mol电子,阳极的质量减少23g
7.(2023·河南·校联考模拟预测)我国科学家最近合成的ZnO@SnO 微米花作为负极材料提高锌镍二次电
2
池的循环性能,工作原理如图所示。已知:正极材料为NiOOH/Ni(OH) 。
2
下列叙述错误的是
资料收集整理【淘宝店铺:向阳百分百】
3 / 11
学科网(北京)股份有限公司A.放电时,上述装置主要将化学能转化成电能
B.放电时,负极表面副反应可能是Zn+2OH-= +H ↑
2
C.充电时,阴极附近电解质溶液pH降低
D.充电时,1molOH-向阳极迁移时理论上转移1mol电子
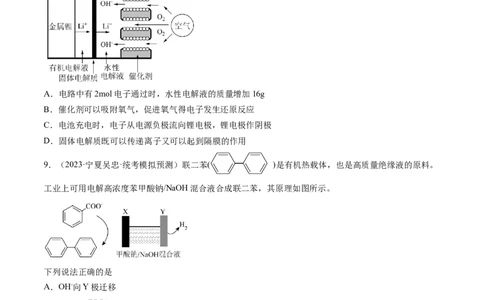
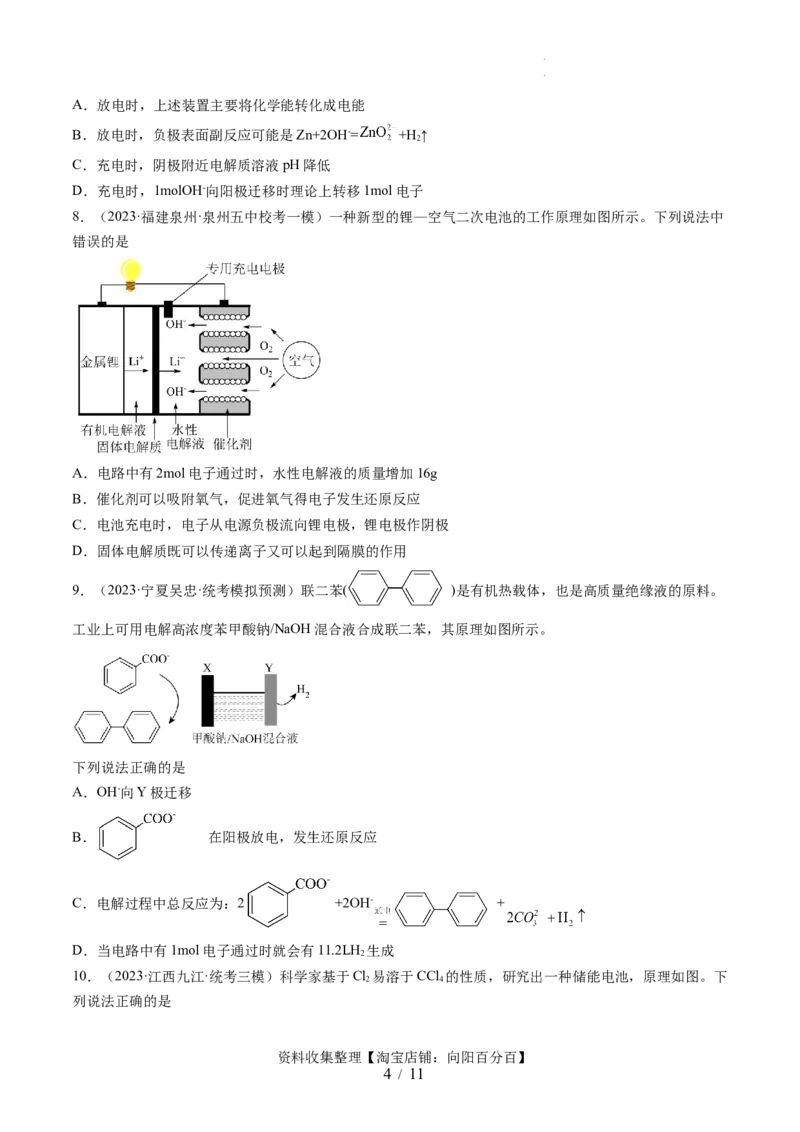
8.(2023·福建泉州·泉州五中校考一模)一种新型的锂—空气二次电池的工作原理如图所示。下列说法中
错误的是
A.电路中有2mol电子通过时,水性电解液的质量增加16g
B.催化剂可以吸附氧气,促进氧气得电子发生还原反应
C.电池充电时,电子从电源负极流向锂电极,锂电极作阴极
D.固体电解质既可以传递离子又可以起到隔膜的作用
9.(2023·宁夏吴忠·统考模拟预测)联二苯( )是有机热载体,也是高质量绝缘液的原料。
工业上可用电解高浓度苯甲酸钠/NaOH混合液合成联二苯,其原理如图所示。
下列说法正确的是
A.OH-向Y极迁移
B. 在阳极放电,发生还原反应
C.电解过程中总反应为:2 +2OH- +
D.当电路中有1mol电子通过时就会有11.2LH 生成
2
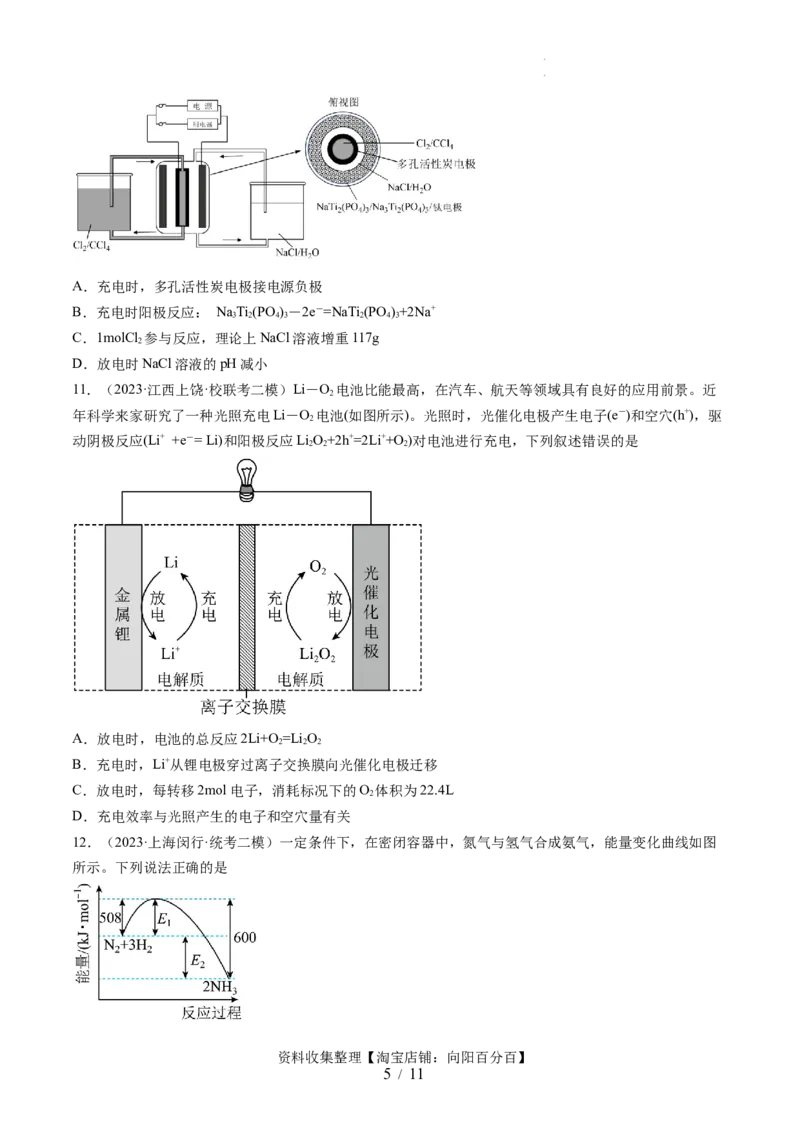
10.(2023·江西九江·统考三模)科学家基于Cl 易溶于CCl 的性质,研究出一种储能电池,原理如图。下
2 4
列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】
4 / 11
学科网(北京)股份有限公司A.充电时,多孔活性炭电极接电源负极
B.充电时阳极反应: NaTi (PO )-2e-=NaTi(PO )+2Na+
3 2 4 3 2 4 3
C.1molCl 参与反应,理论上NaCl溶液增重117g
2
D.放电时NaCl溶液的pH减小
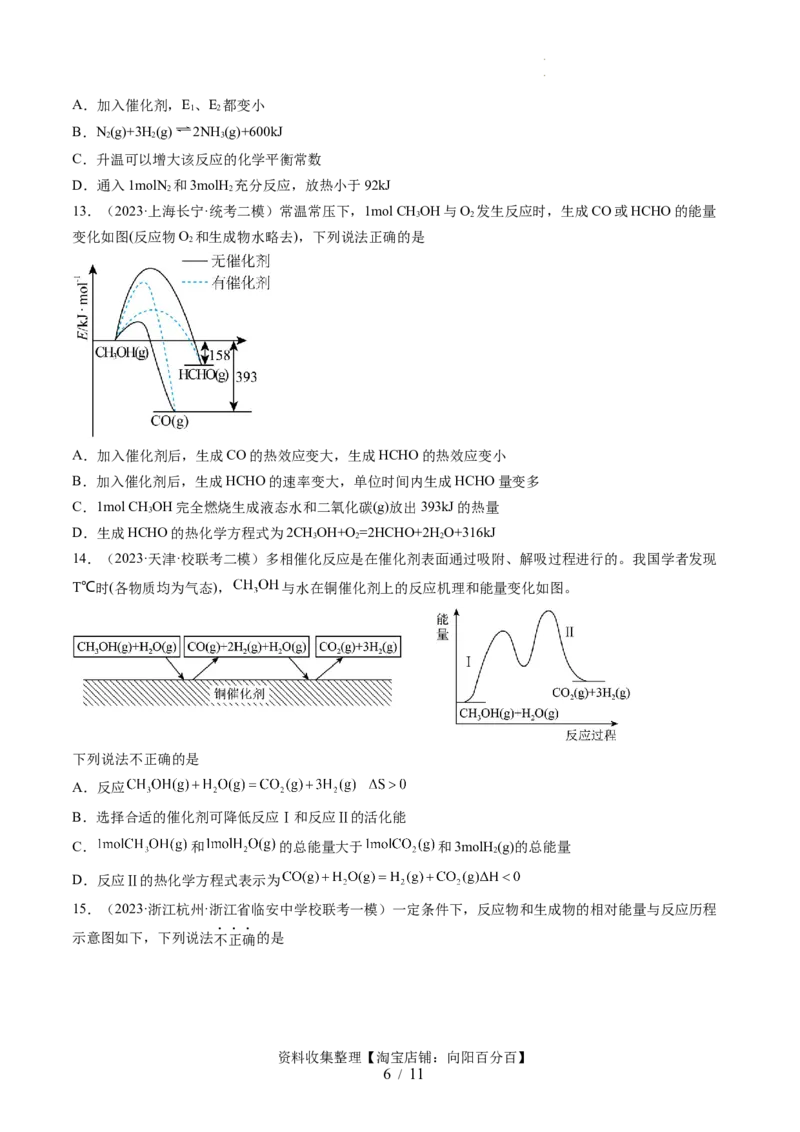
11.(2023·江西上饶·校联考二模)Li-O 电池比能最高,在汽车、航天等领域具有良好的应用前景。近
2
年科学来家研究了一种光照充电Li-O 电池(如图所示)。光照时,光催化电极产生电子(e-)和空穴(h+),驱
2
动阴极反应(Li+ +e-= Li)和阳极反应LiO+2h+=2Li++O )对电池进行充电,下列叙述错误的是
2 2 2
A.放电时,电池的总反应2Li+O=Li O
2 2 2
B.充电时,Li+从锂电极穿过离子交换膜向光催化电极迁移
C.放电时,每转移2mol电子,消耗标况下的O 体积为22.4L
2
D.充电效率与光照产生的电子和空穴量有关
12.(2023·上海闵行·统考二模)一定条件下,在密闭容器中,氮气与氢气合成氨气,能量变化曲线如图
所示。下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】
5 / 11
学科网(北京)股份有限公司A.加入催化剂,E、E 都变小
1 2
B.N(g)+3H(g) 2NH (g)+600kJ
2 2 3
C.升温可以增大该反应的化学平衡常数
D.通入1molN 和3molH 充分反应,放热小于92kJ
2 2
13.(2023·上海长宁·统考二模)常温常压下,1mol CHOH与O 发生反应时,生成CO或HCHO的能量
3 2
变化如图(反应物O 和生成物水略去),下列说法正确的是
2
A.加入催化剂后,生成CO的热效应变大,生成HCHO的热效应变小
B.加入催化剂后,生成HCHO的速率变大,单位时间内生成HCHO量变多
C.1mol CHOH完全燃烧生成液态水和二氧化碳(g)放出393kJ的热量
3
D.生成HCHO的热化学方程式为2CHOH+O =2HCHO+2H O+316kJ
3 2 2
14.(2023·天津·校联考二模)多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现
T℃时(各物质均为气态), 与水在铜催化剂上的反应机理和能量变化如图。
下列说法不正确的是
A.反应
B.选择合适的催化剂可降低反应Ⅰ和反应Ⅱ的活化能
C. 和 的总能量大于 和3molH (g)的总能量
2
D.反应Ⅱ的热化学方程式表示为
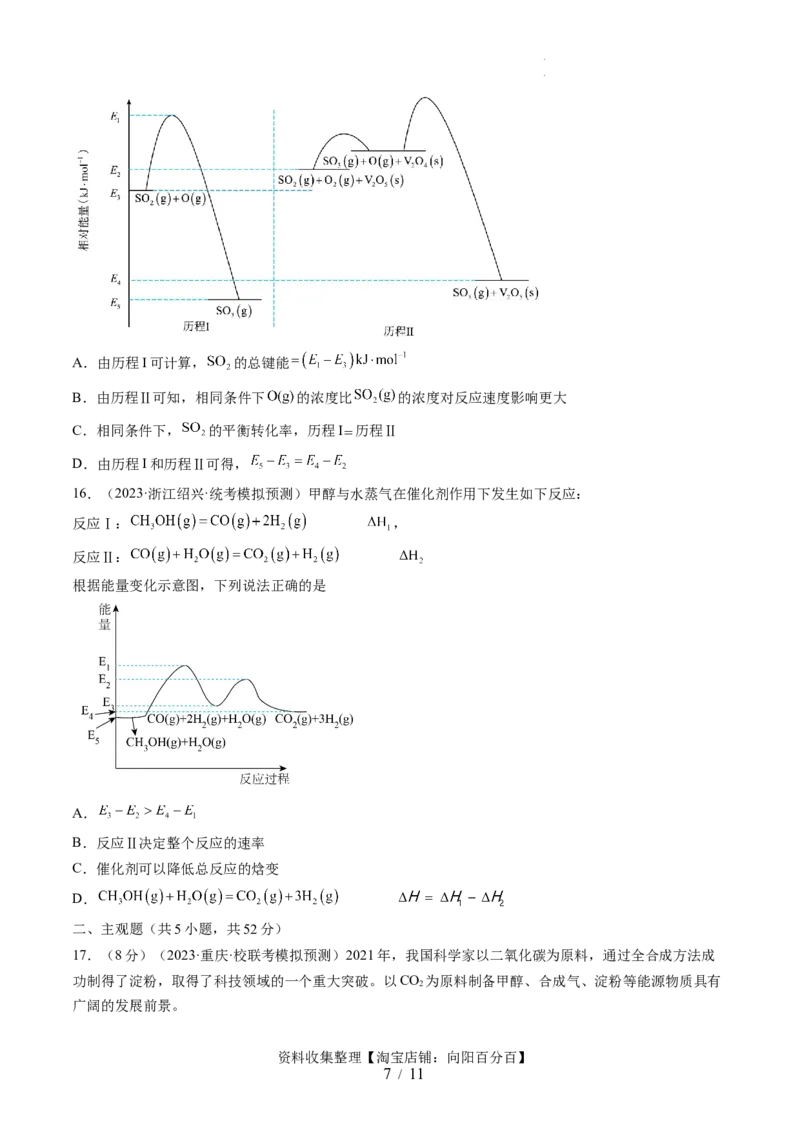
15.(2023·浙江杭州·浙江省临安中学校联考一模)一定条件下,反应物和生成物的相对能量与反应历程
示意图如下,下列说法不正确的是
资料收集整理【淘宝店铺:向阳百分百】
6 / 11
学科网(北京)股份有限公司A.由历程I可计算, 的总键能
B.由历程Ⅱ可知,相同条件下 的浓度比 的浓度对反应速度影响更大
C.相同条件下, 的平衡转化率,历程I 历程Ⅱ
D.由历程I和历程Ⅱ可得,
16.(2023·浙江绍兴·统考模拟预测)甲醇与水蒸气在催化剂作用下发生如下反应:
反应Ⅰ: ,
反应Ⅱ:
根据能量变化示意图,下列说法正确的是
A.
B.反应Ⅱ决定整个反应的速率
C.催化剂可以降低总反应的焓变
D.
二、主观题(共5小题,共52分)
17.(8分)(2023·重庆·校联考模拟预测)2021年,我国科学家以二氧化碳为原料,通过全合成方法成
功制得了淀粉,取得了科技领域的一个重大突破。以CO 为原料制备甲醇、合成气、淀粉等能源物质具有
2
广阔的发展前景。
资料收集整理【淘宝店铺:向阳百分百】
7 / 11
学科网(北京)股份有限公司I.在催化剂的作用下,氢气还原CO 的过程中可同时发生反应①②。
2
①CO(g)+3H(g) CHOH(g)+H O(g) H=-50kJ·mol-1
2 2 3 2 1
②CO(g)+H(g) CO(g)+HO(g) H=+41.1kJ·mol-1
2 2 2 2 △
(1)CO(g)+2H (g) CHOH(g) H= kJ·mol-1。
2 3 3△
(2)已知反应①的△S=-177.2J·mol-1·K-1,在下列哪些温度下反应能自发进行?_______(填标号)。
△
A.0℃ B.5℃ C.25℃ D.500℃
II.固体氧化物电解池(SOEC)利用废热电解水和CO 来制合成气(主要组分为一氧化碳和氢气),因为高温电
2
解可降低内阻,所以相比于低温电解池表现出更高的电解效率。
(3)a为电源的 极(填“正”或“负”)。
(4)生成一氧化碳和氢气物质的量之比为1:3时的电极反应式为 。
18.(12分)(2023·江苏盐城·盐城市伍佑中学校考模拟预测)电催化还原 是当今资源化利用二氧化
碳的重点课题,常用的阴极材料有有机多孔电极材料、铜基复合电极材料等。
(1)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原 的装置示意图如图-1所示。控
制其他条件相同,将一定量的 通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图-2
所示。
①电解前需向电解质溶液中持续通入过量 的原因是 。
②控制电压为0.8V,电解时转移电子的物质的量为 mol。
③科研小组利用 代替原有的 进行研究,其目的是 。
(2)一种铜基复合电极材料 的制备方法:将一定量 分散至水与乙醇的混合溶液中,向溶液中
逐滴滴加 (一种强酸)溶液,搅拌一段时间后离心分离,得 ,溶液呈蓝色。写出 还原
资料收集整理【淘宝店铺:向阳百分百】
8 / 11
学科网(北京)股份有限公司的离子方程式: 。
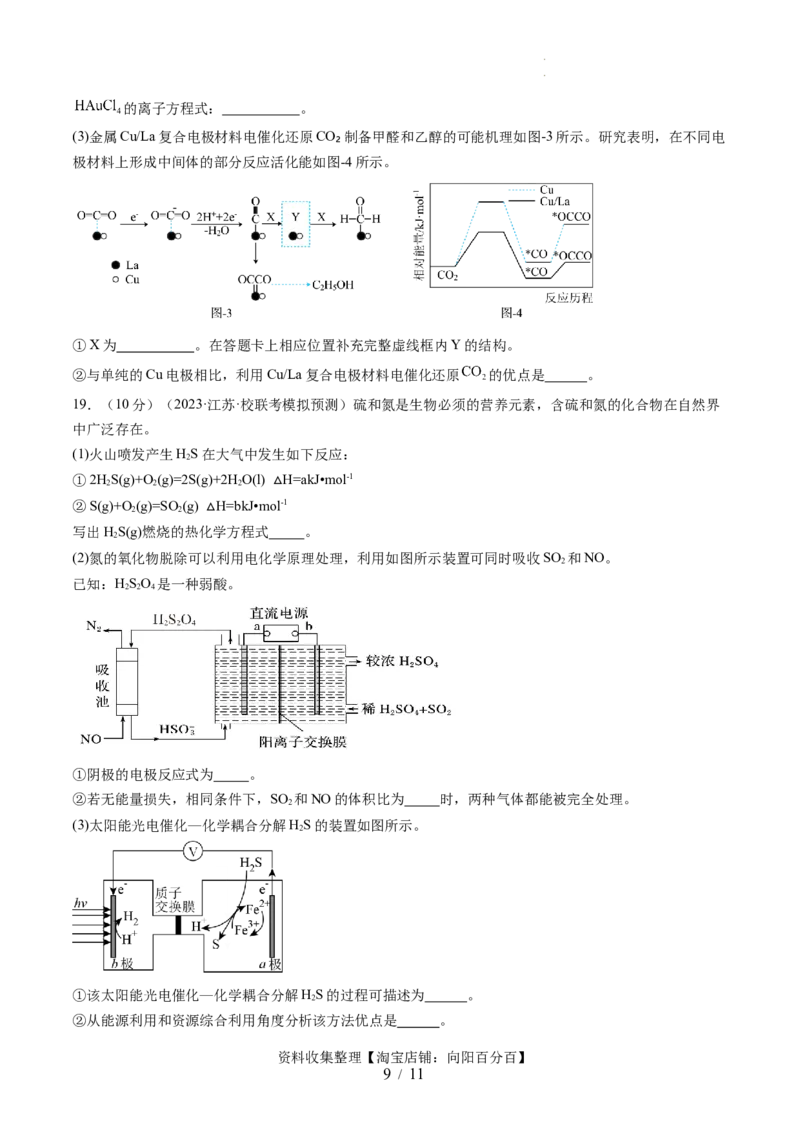
(3)金属Cu/La复合电极材料电催化还原CO₂制备甲醛和乙醇的可能机理如图-3所示。研究表明,在不同电
极材料上形成中间体的部分反应活化能如图-4所示。
①X为 。在答题卡上相应位置补充完整虚线框内Y的结构。
②与单纯的Cu电极相比,利用Cu/La复合电极材料电催化还原 的优点是 。
19.(10分)(2023·江苏·校联考模拟预测)硫和氮是生物必须的营养元素,含硫和氮的化合物在自然界
中广泛存在。
(1)火山喷发产生HS在大气中发生如下反应:
2
①2HS(g)+O(g)=2S(g)+2H O(l) H=akJ•mol-1
2 2 2
②S(g)+O(g)=SO(g) H=bkJ•mol-1
2 2 △
写出HS(g)燃烧的热化学方程式 。
2 △
(2)氮的氧化物脱除可以利用电化学原理处理,利用如图所示装置可同时吸收SO 和NO。
2
已知:HSO 是一种弱酸。
2 2 4
①阴极的电极反应式为 。
②若无能量损失,相同条件下,SO 和NO的体积比为 时,两种气体都能被完全处理。
2
(3)太阳能光电催化—化学耦合分解HS的装置如图所示。
2
①该太阳能光电催化—化学耦合分解HS的过程可描述为 。
2
②从能源利用和资源综合利用角度分析该方法优点是 。
资料收集整理【淘宝店铺:向阳百分百】
9 / 11
学科网(北京)股份有限公司20.(12分)(2023·北京顺义·北京市顺义区第一中学校考模拟预测)环状碳酸酯( )是一种重要
的工业原料,可用作锂离子电池电解质的溶剂。一种由苯乙烯经电解制备环状碳酸酯的实验操作如下:
i.将一定量电解质、苯乙烯、水-二甲亚砜溶剂依次放入塑料烧杯中,搅拌均匀后放入高压反应釜内,充
入一定量 气体;
ii.以石墨和铜片为两个电极,电解至苯乙烯完全消耗后,停止电解;
iii.分离、提纯产品,计算产率。
在相同条件下,采用不同电解质进行实验I~Ⅳ,实验结果如表:
实验序
电解质 产率/% 实验现象
号
I 微量
Ⅱ 68 阴极产生气体,能使湿润的红色石蕊试纸变蓝
Ⅲ a
Ⅳ NaI 0 阴极产生气体;阳极附近有白色固体析出
已知:i.电解效率
ii.环状碳酸酯的产率=n(生成的环状碳酸酯)/n(投入的苯乙烯)
iii. 在碱性环境中会歧化为 和 。
(1)针对实验Ⅲ进行如下分析:
①取反应后石墨电极附近溶液滴加淀粉溶液变蓝,则石墨作 极(填“阳”或“阴”)。
②苯乙烯与石墨电极上生成的 发生加成反应,再发生水解反应,得到中间产物1-苯基-2-碘乙醇(
),在一定条件下进一步转化为苯基环氧乙烷( )后者与 进行
加成反应,得到的环状碳酸酯的结构简式为 。
③实验中加入80mL密度为0.91 的苯乙烯,η(环状碳酸酯)≈63%,则电路中通过2mol电子时,产生
mol环状碳酸酯:a= 。
(2)对比实验I~Ⅲ可知,其他条件相同时,电解质分别选用 、 、 时,环状碳酸酯的产
率依次显著升高,从原子结构角度解释,是因为 ,导致 、 、 的放电能力依次增强。
(3)探究实验Ⅳ中未生成环状碳酸酯的原因,继续实验。
①实验Ⅳ中阴极产生气体为 。
资料收集整理【淘宝店铺:向阳百分百】
10 / 11
学科网(北京)股份有限公司②经X光单晶衍射实验证实,实验Ⅳ中得到的白色固体含 ,用化学用语和必要的文字解释得
到该物质的原理 。
21.(10分)(2023·北京朝阳·统考三模)某研究小组探究镁、铝与 溶液的反应。
实验Ⅰ:将过量镁条、铝条(除去表面氧化膜)分别放入60℃的温水中,观察到开始时镁条表面有气泡,5
分钟后气泡迅速减少直至反应停止;铝条表面无明显现象。
实验Ⅱ:将过量镁条、铝条(除去表面氧化膜)分别放入饱和 溶液( )中,观察到镁条表面有气
泡,且持续时间较长,溶液中产生白色浑浊,铝条表面持续产生气泡。
(1)实验Ⅰ中镁条表面产生气泡的反应为 。
(2)实验Ⅱ中饱和 溶液 的原因 (写离子方程式)。
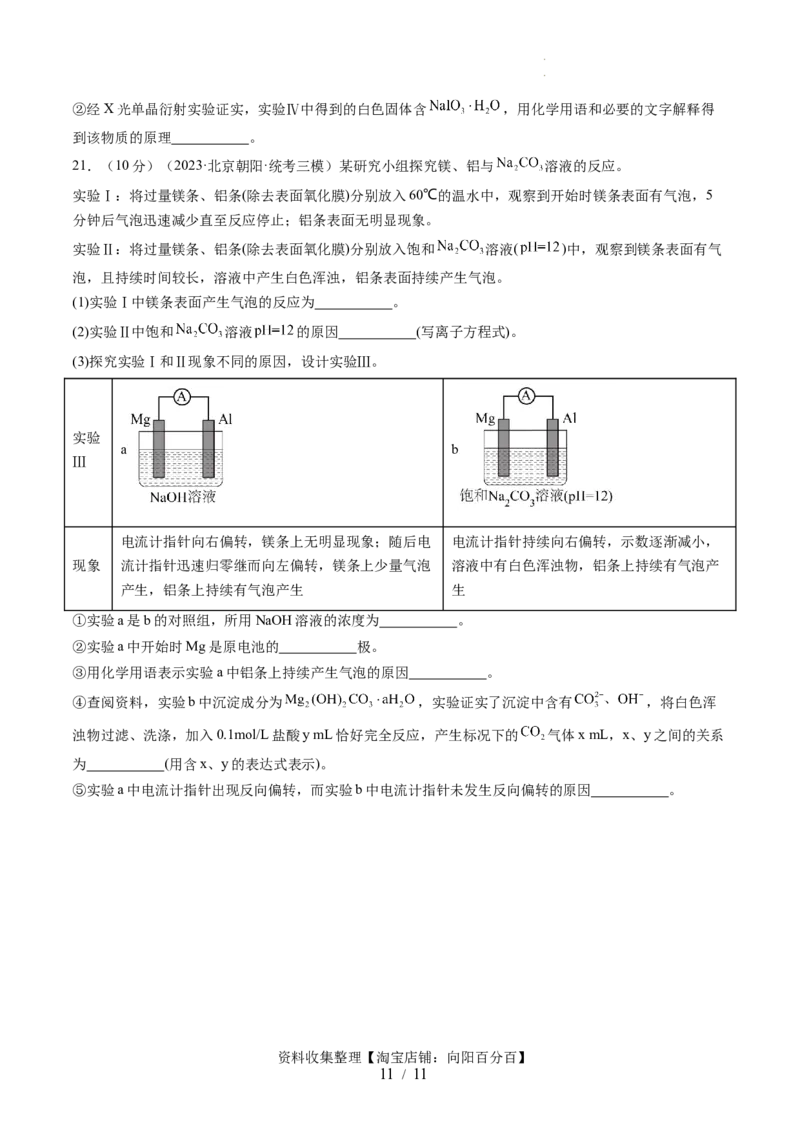
(3)探究实验Ⅰ和Ⅱ现象不同的原因,设计实验Ⅲ。
实验
a b
Ⅲ
电流计指针向右偏转,镁条上无明显现象;随后电 电流计指针持续向右偏转,示数逐渐减小,
现象 流计指针迅速归零继而向左偏转,镁条上少量气泡 溶液中有白色浑浊物,铝条上持续有气泡产
产生,铝条上持续有气泡产生 生
①实验a是b的对照组,所用NaOH溶液的浓度为 。
②实验a中开始时Mg是原电池的 极。
③用化学用语表示实验a中铝条上持续产生气泡的原因 。
④查阅资料,实验b中沉淀成分为 ,实验证实了沉淀中含有 ,将白色浑
浊物过滤、洗涤,加入0.1mol/L盐酸y mL恰好完全反应,产生标况下的 气体x mL,x、y之间的关系
为 (用含x、y的表达式表示)。
⑤实验a中电流计指针出现反向偏转,而实验b中电流计指针未发生反向偏转的原因 。
资料收集整理【淘宝店铺:向阳百分百】
11 / 11
学科网(北京)股份有限公司