文档内容
第六章 化学反应与能量
能力提升检测卷
时间:90分钟 分值:100分
一、选择题(每小题只有一个正确选项,共16*3分)
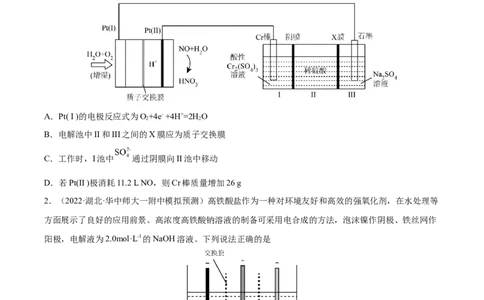
1.(2022·湖北·华中师大一附中模拟预测)某同学设计的利用NO-空气质子交换膜燃料电池通过电解法制
备高纯铬和硫酸的简单装置如图所示。下列说法错误的是
A.Pt( I )的电极反应式为O+4e- +4H+=2H O
2 2
B.电解池中II和III之间的X膜应为质子交换膜
C.工作时,I池中 通过阴膜向II池中移动
D.若Pt(II )极消耗11.2 L NO,则Cr棒质量增加26 g
2.(2022·湖北·华中师大一附中模拟预测)高铁酸盐作为一种对环境友好和高效的强氧化剂,在水处理等
方面展示了良好的应用前景。高浓度高铁酸钠溶液的制备可采用电合成的方法,泡沫镍作阴极、铁丝网作
阳极,电解液为2.0mol·L-1的NaOH溶液。下列说法正确的是
A.工作时,阳极附近的pH增大
B.交换膜为质子交换膜
C.阴极反应式:4OH-+4e-=2H O+O↑
2 2
D.阳极反应式:Fe-6e-+8OH-= +4H O
2
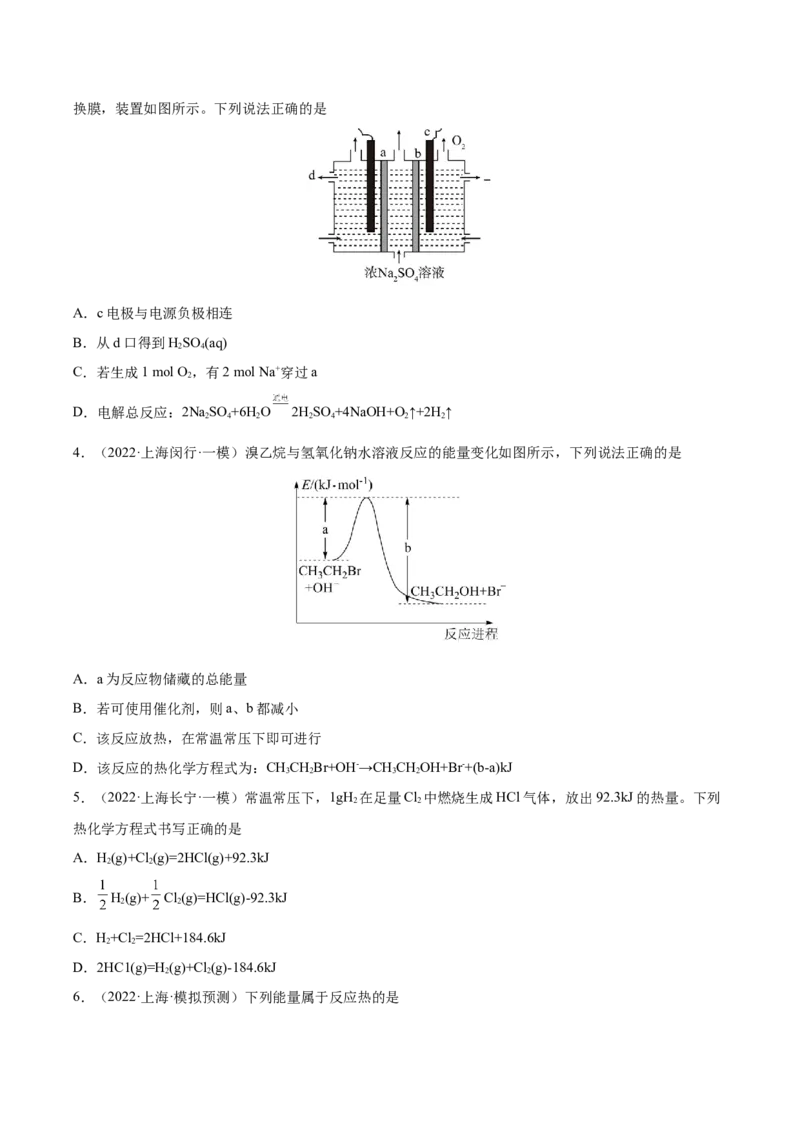
3.(2022·上海金山·二模)工业上通过惰性电极电解NaSO 浓溶液来制备NaOH和HSO ,a、b为离子交
2 4 2 4换膜,装置如图所示。下列说法正确的是
A.c电极与电源负极相连
B.从d口得到HSO (aq)
2 4
C.若生成1 mol O ,有2 mol Na+穿过a
2
D.电解总反应:2NaSO +6H O 2HSO +4NaOH+O↑+2H ↑
2 4 2 2 4 2 2
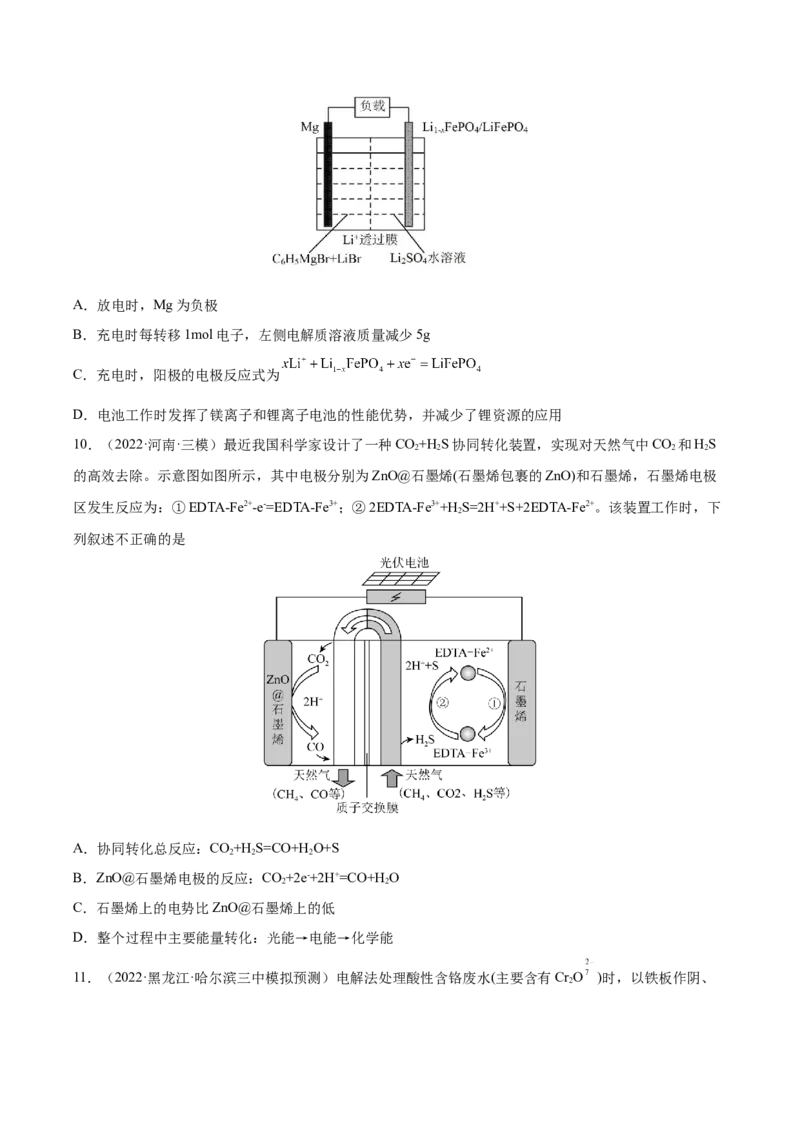
4.(2022·上海闵行·一模)溴乙烷与氢氧化钠水溶液反应的能量变化如图所示,下列说法正确的是
A.a为反应物储藏的总能量
B.若可使用催化剂,则a、b都减小
C.该反应放热,在常温常压下即可进行
D.该反应的热化学方程式为:CHCHBr+OH-→CHCHOH+Br-+(b-a)kJ
3 2 3 2
5.(2022·上海长宁·一模)常温常压下,1gH 在足量Cl 中燃烧生成HCl气体,放出92.3kJ的热量。下列
2 2
热化学方程式书写正确的是
A.H(g)+Cl (g)=2HCl(g)+92.3kJ
2 2
B. H(g)+ Cl(g)=HCl(g)-92.3kJ
2 2
C.H+Cl=2HCl+184.6kJ
2 2
D.2HC1(g)=H(g)+Cl (g)-184.6kJ
2 2
6.(2022·上海·模拟预测)下列能量属于反应热的是A. 分解成H、 时吸收的能量 B.石墨转化成金刚石时吸收的能量
C. 变成 时吸收的能量 D.冰变成水时吸收的能量
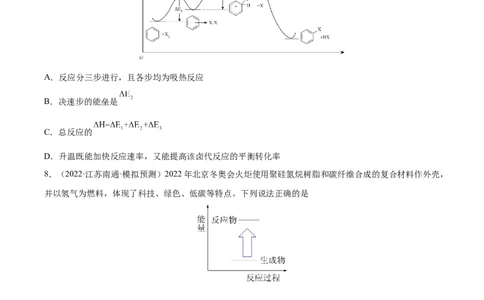
7.(2022·河北保定·一模)苯亲电取代反应中卤代反应的反应进程与能量变化曲线如图所示,下列说法正
确的是
A.反应分三步进行,且各步均为吸热反应
B.决速步的能垒是
C.总反应的
D.升温既能加快反应速率,又能提高该卤代反应的平衡转化率
8.(2022·江苏南通·模拟预测)2022年北京冬奥会火炬使用聚硅氮烷树脂和碳纤维合成的复合材料作外壳,
并以氢气为燃料,体现了科技、绿色、低碳等特点。下列说法正确的是
A.该复合材料有密度大、熔点低的特点
B.聚硅氮烷树脂和碳纤维都属于纯净物
C.燃烧时氢气与氧气发生氧化还原反应
D.可用如图表示氢气燃烧的能量变化
9.(2022·辽宁沈阳·三模)镁-锂双离子二次电池的装置如图所示,下列说法中错误的是A.放电时,Mg为负极
B.充电时每转移1mol电子,左侧电解质溶液质量减少5g
C.充电时,阳极的电极反应式为
D.电池工作时发挥了镁离子和锂离子电池的性能优势,并减少了锂资源的应用
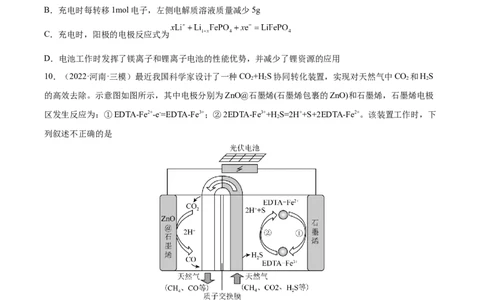
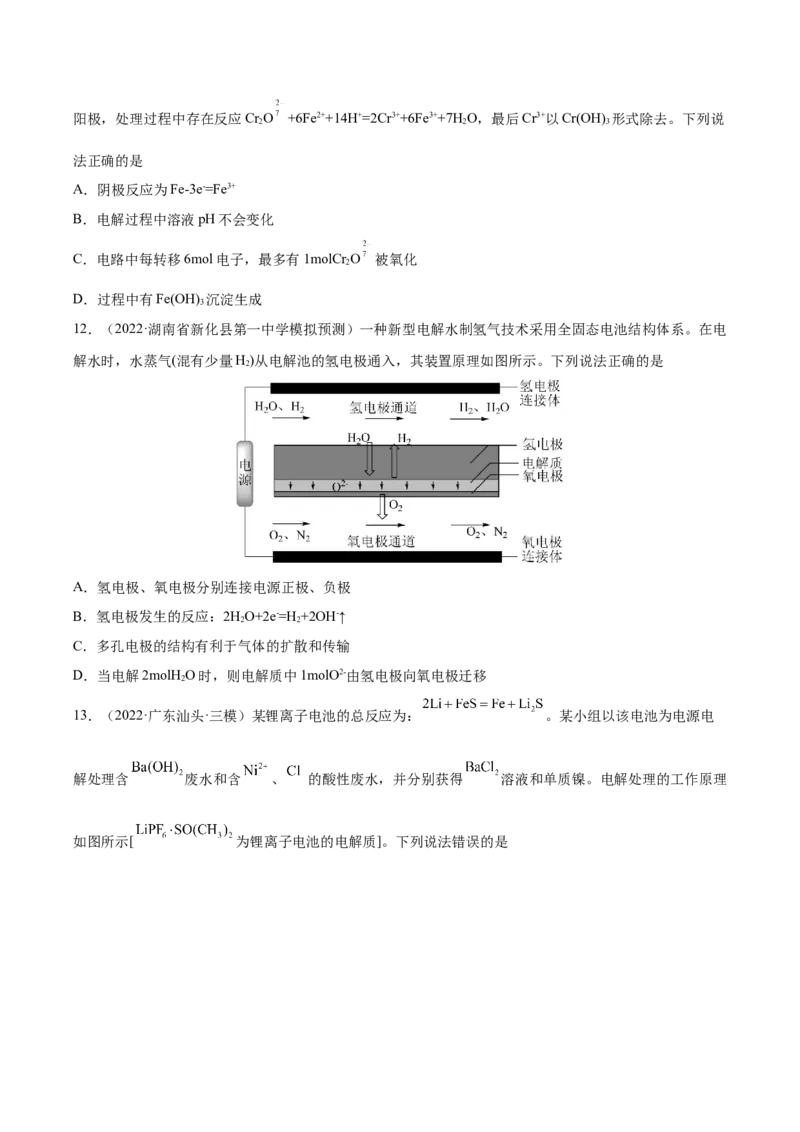
10.(2022·河南·三模)最近我国科学家设计了一种CO+H S协同转化装置,实现对天然气中CO 和HS
2 2 2 2
的高效去除。示意图如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极
区发生反应为:①EDTA-Fe2+-e-=EDTA-Fe3+;②2EDTA-Fe3++H S=2H++S+2EDTA-Fe2+。该装置工作时,下
2
列叙述不正确的是
A.协同转化总反应:CO+H S=CO+H O+S
2 2 2
B.ZnO@石墨烯电极的反应:CO+2e-+2H+=CO+H O
2 2
C.石墨烯上的电势比ZnO@石墨烯上的低
D.整个过程中主要能量转化:光能→电能→化学能
11.(2022·黑龙江·哈尔滨三中模拟预测)电解法处理酸性含铬废水(主要含有Cr O )时,以铁板作阴、
2阳极,处理过程中存在反应Cr O +6Fe2++14H+=2Cr3++6Fe3++7H O,最后Cr3+以Cr(OH) 形式除去。下列说
2 2 3
法正确的是
A.阴极反应为Fe-3e-=Fe3+
B.电解过程中溶液pH不会变化
C.电路中每转移6mol电子,最多有1molCr O 被氧化
2
D.过程中有Fe(OH) 沉淀生成
3
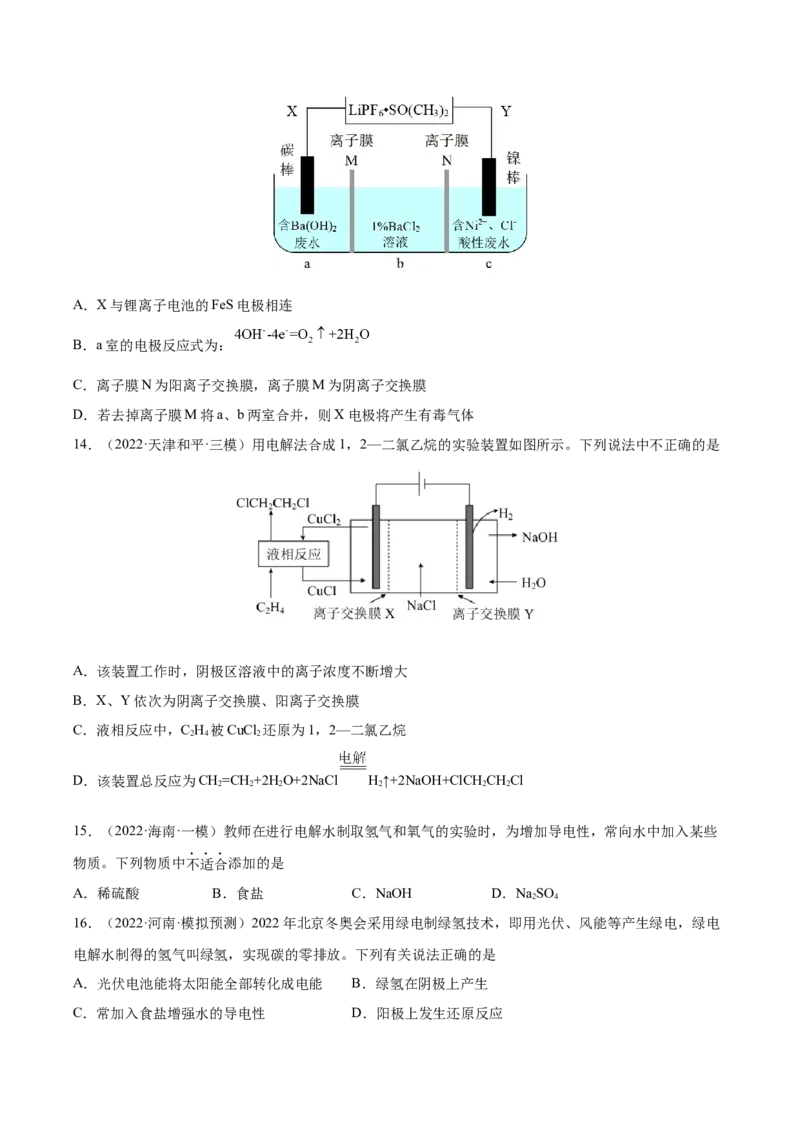
12.(2022·湖南省新化县第一中学模拟预测)一种新型电解水制氢气技术采用全固态电池结构体系。在电
解水时,水蒸气(混有少量H)从电解池的氢电极通入,其装置原理如图所示。下列说法正确的是
2
A.氢电极、氧电极分别连接电源正极、负极
B.氢电极发生的反应:2HO+2e-=H +2OH-↑
2 2
C.多孔电极的结构有利于气体的扩散和传输
D.当电解2molH O时,则电解质中1molO2-由氢电极向氧电极迁移
2
13.(2022·广东汕头·三模)某锂离子电池的总反应为: 。某小组以该电池为电源电
解处理含 废水和含 、 的酸性废水,并分别获得 溶液和单质镍。电解处理的工作原理
如图所示[ 为锂离子电池的电解质]。下列说法错误的是A.X与锂离子电池的FeS电极相连
B.a室的电极反应式为:
C.离子膜N为阳离子交换膜,离子膜M为阴离子交换膜
D.若去掉离子膜M将a、b两室合并,则X电极将产生有毒气体
14.(2022·天津和平·三模)用电解法合成1,2—二氯乙烷的实验装置如图所示。下列说法中不正确的是
A.该装置工作时,阴极区溶液中的离子浓度不断增大
B.X、Y依次为阴离子交换膜、阳离子交换膜
C.液相反应中,C H 被CuCl 还原为1,2—二氯乙烷
2 4 2
D.该装置总反应为CH=CH +2H O+2NaCl H↑+2NaOH+ClCH CHCl
2 2 2 2 2 2
15.(2022·海南·一模)教师在进行电解水制取氢气和氧气的实验时,为增加导电性,常向水中加入某些
物质。下列物质中不适合添加的是
A.稀硫酸 B.食盐 C.NaOH D.NaSO
2 4
16.(2022·河南·模拟预测)2022年北京冬奥会采用绿电制绿氢技术,即用光伏、风能等产生绿电,绿电
电解水制得的氢气叫绿氢,实现碳的零排放。下列有关说法正确的是
A.光伏电池能将太阳能全部转化成电能 B.绿氢在阴极上产生
C.常加入食盐增强水的导电性 D.阳极上发生还原反应二、主观题(共5小题,共52分)
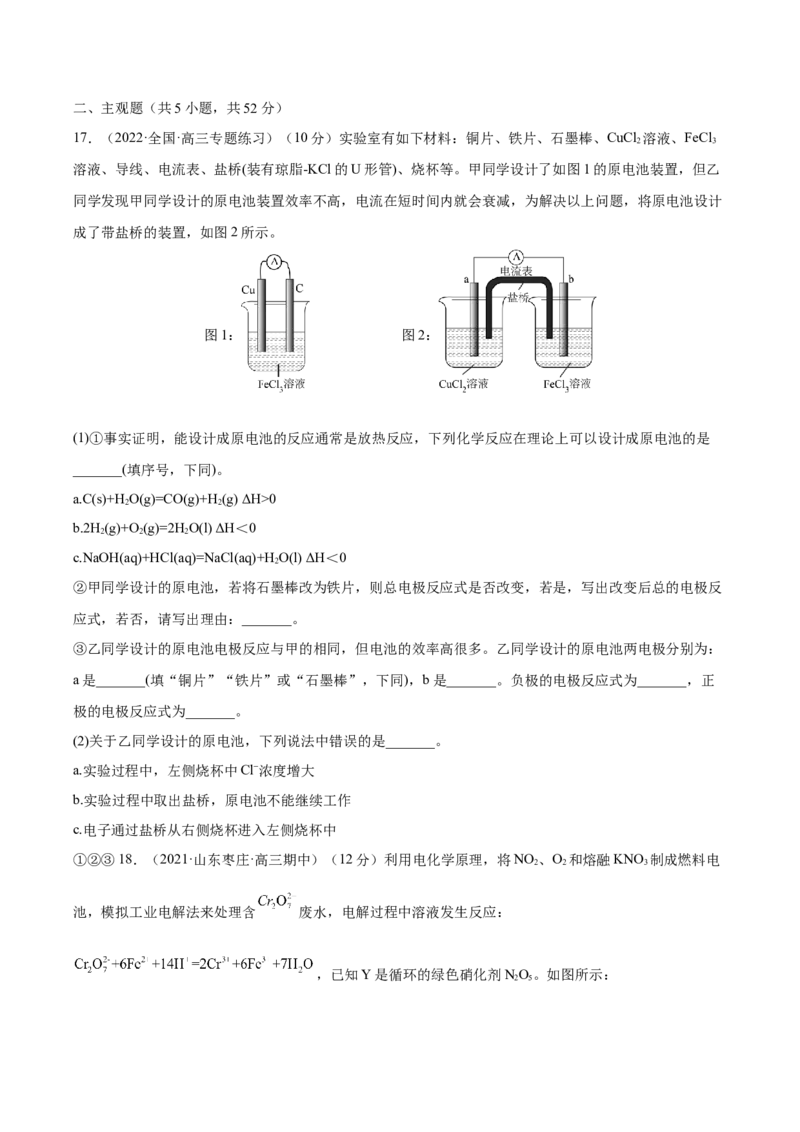
17.(2022·全国·高三专题练习)(10分)实验室有如下材料:铜片、铁片、石墨棒、CuCl 溶液、FeCl
2 3
溶液、导线、电流表、盐桥(装有琼脂-KCl的U形管)、烧杯等。甲同学设计了如图1的原电池装置,但乙
同学发现甲同学设计的原电池装置效率不高,电流在短时间内就会衰减,为解决以上问题,将原电池设计
成了带盐桥的装置,如图2所示。
图1: 图2:
(1)①事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
_______(填序号,下同)。
a.C(s)+H O(g)=CO(g)+H (g) ΔH>0
2 2
b.2H (g)+O(g)=2HO(l) ΔH<0
2 2 2
c.NaOH(aq)+HCl(aq)=NaCl(aq)+H O(l) ΔH<0
2
②甲同学设计的原电池,若将石墨棒改为铁片,则总电极反应式是否改变,若是,写出改变后总的电极反
应式,若否,请写出理由:_______。
③乙同学设计的原电池电极反应与甲的相同,但电池的效率高很多。乙同学设计的原电池两电极分别为:
a是_______(填“铜片”“铁片”或“石墨棒”,下同),b是_______。负极的电极反应式为_______,正
极的电极反应式为_______。
(2)关于乙同学设计的原电池,下列说法中错误的是_______。
a.实验过程中,左侧烧杯中Cl−浓度增大
b.实验过程中取出盐桥,原电池不能继续工作
c.电子通过盐桥从右侧烧杯进入左侧烧杯中
①②③18.(2021·山东枣庄·高三期中)(12分)利用电化学原理,将NO 、O 和熔融KNO 制成燃料电
2 2 3
池,模拟工业电解法来处理含 废水,电解过程中溶液发生反应:
,已知Y是循环的绿色硝化剂NO。如图所示:
2 5(1)以上装置中的反应共涉及___________种还原剂(填阿拉伯数字)。
(2)甲池工作时,电极石墨Ⅰ发生的是___________反应(填“氧化”或“还原”);石墨Ⅱ附近发生的电极反
应式为___________。
(3)工作时,甲池内的 向___________移动(填“左”或“右”);在相同条件下,消耗的O 和NO 的体
2 2
积比为___________。
(4)乙池中Fe(I)棒上消耗1.00 mol Fe,则甲池消耗标况下的氧气的体积为___________。
(5)若外电路中转移了1.0 mol电子,则处理废液中的 的物质的量为___________。
19.(2021·河南·义马市高级中学高三阶段练习)(13分)回答下列问题:
(1)一氧化碳催化加氢制甲醇,反应原理为: 。
①若已知CO、 、 的燃烧热分别为 、 、 ,则
_______。
②已知反应中相关的化学键键能数据如下:
化学键
436 413 343 465
且 ,试计算断开 气体中的 需提供的最低能
量为_______。
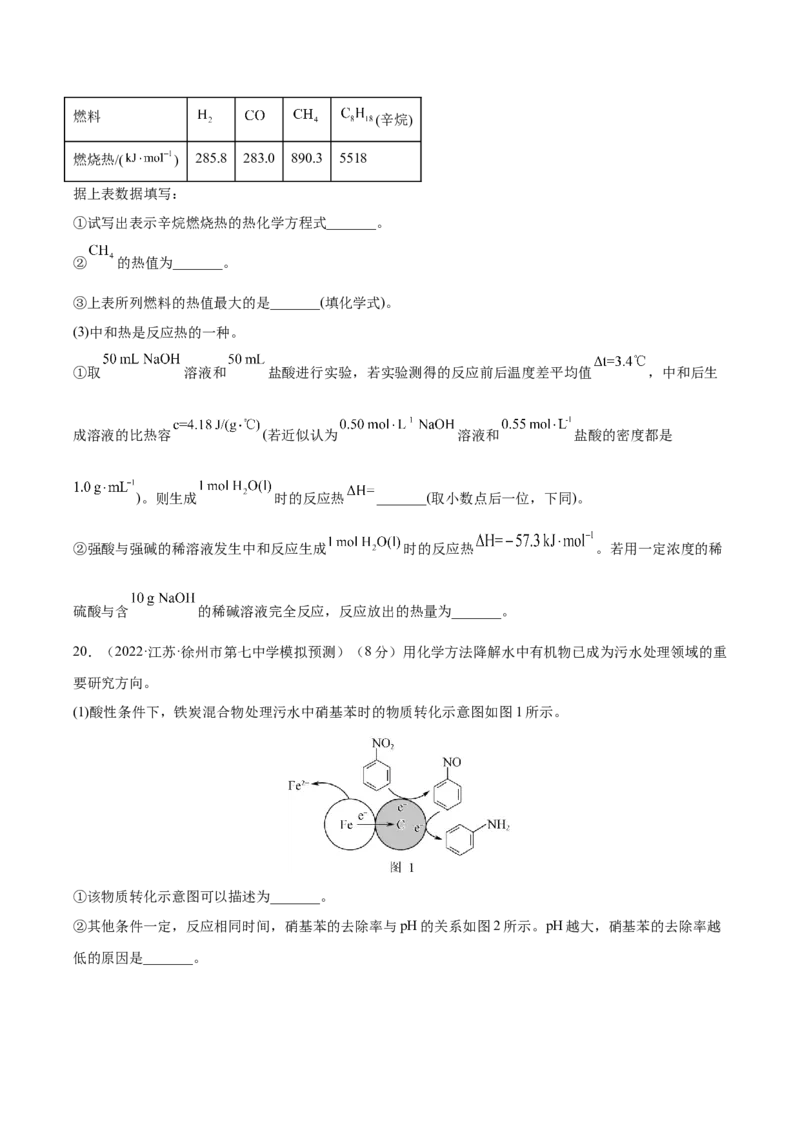
(2)燃料的热值是指单位质量某种燃料完全燃烧放出的热量,其常用单位为 。已知下列物质的燃烧
热(25℃、 ):燃料 (辛烷)
燃烧热/( ) 285.8 283.0 890.3 5518
据上表数据填写:
①试写出表示辛烷燃烧热的热化学方程式_______。
② 的热值为_______。
③上表所列燃料的热值最大的是_______(填化学式)。
(3)中和热是反应热的一种。
①取 溶液和 盐酸进行实验,若实验测得的反应前后温度差平均值 ,中和后生
成溶液的比热容 (若近似认为 溶液和 盐酸的密度都是
)。则生成 时的反应热 _______(取小数点后一位,下同)。
②强酸与强碱的稀溶液发生中和反应生成 时的反应热 。若用一定浓度的稀
硫酸与含 的稀碱溶液完全反应,反应放出的热量为_______。
20.(2022·江苏·徐州市第七中学模拟预测)(8分)用化学方法降解水中有机物已成为污水处理领域的重
要研究方向。
(1)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图1所示。
①该物质转化示意图可以描述为_______。
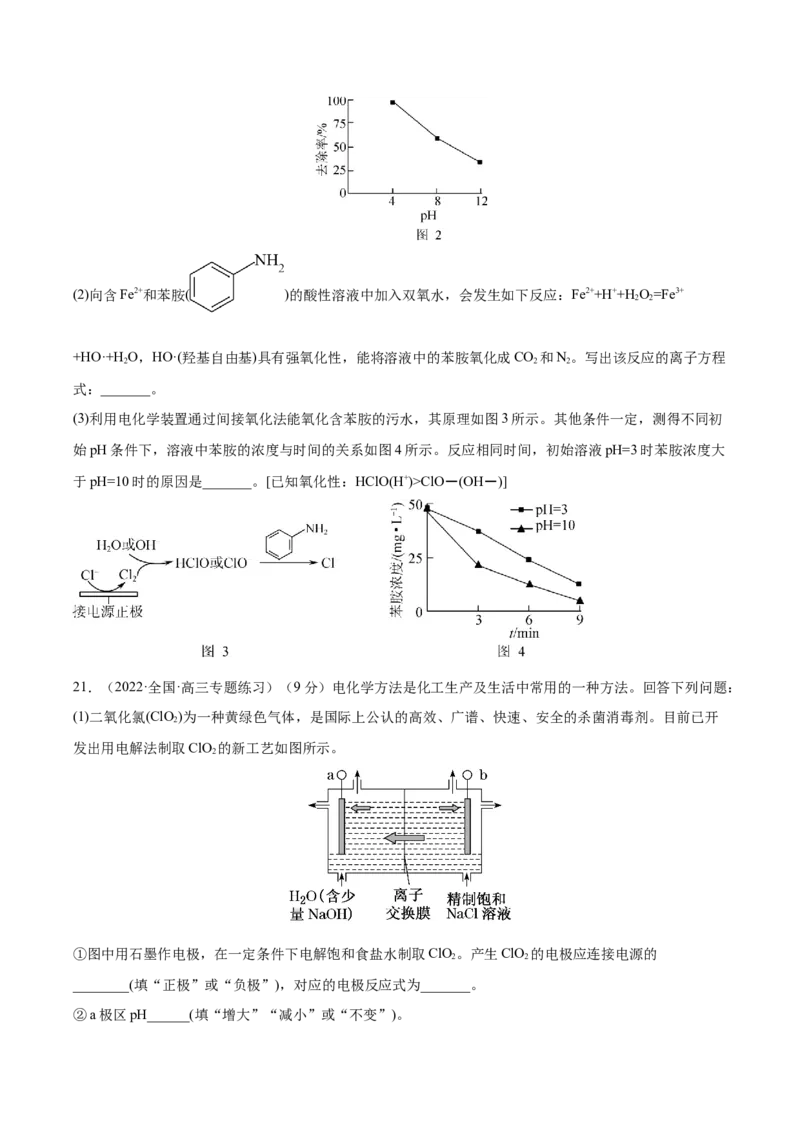
②其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图2所示。pH越大,硝基苯的去除率越
低的原因是_______。(2)向含Fe2+和苯胺( )的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H O=Fe3+
2 2
+HO·+HO,HO·(羟基自由基)具有强氧化性,能将溶液中的苯胺氧化成CO 和N。写出该反应的离子方程
2 2 2
式:_______。
(3)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图3所示。其他条件一定,测得不同初
始pH条件下,溶液中苯胺的浓度与时间的关系如图4所示。反应相同时间,初始溶液pH=3时苯胺浓度大
于pH=10时的原因是_______。[已知氧化性:HClO(H+)>ClO-(OH-)]
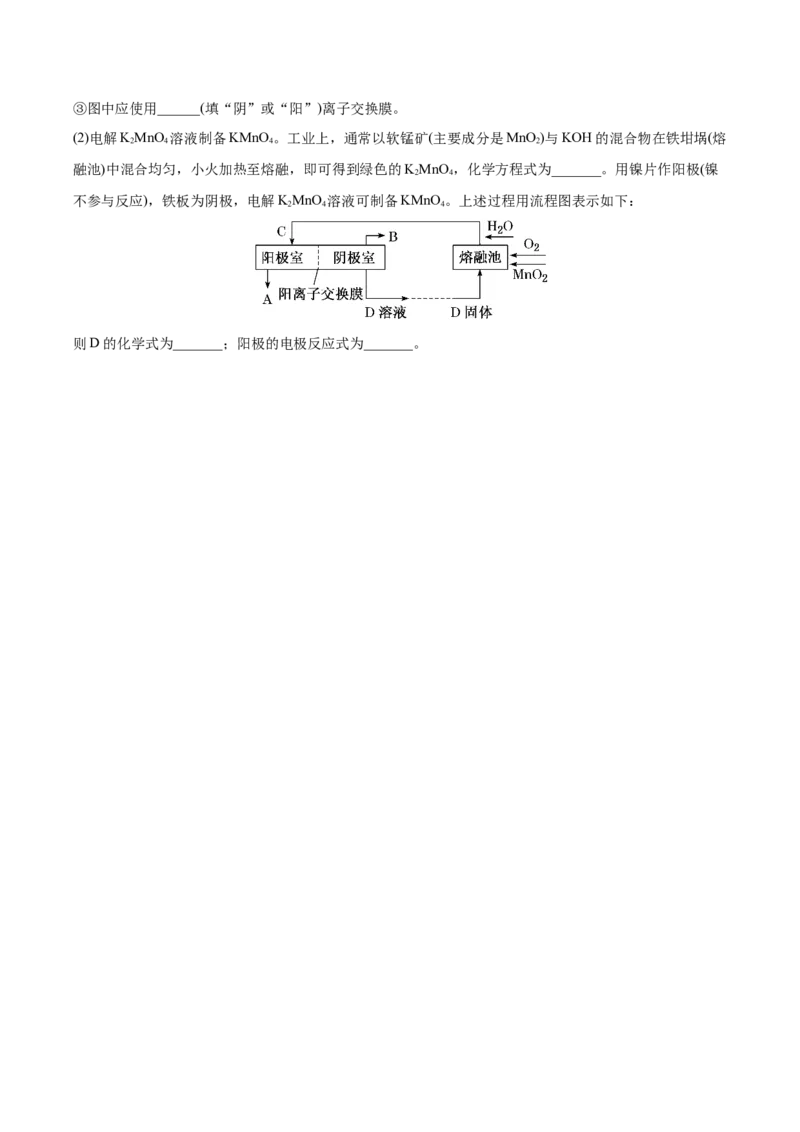
21.(2022·全国·高三专题练习)(9分)电化学方法是化工生产及生活中常用的一种方法。回答下列问题:
(1)二氧化氯(ClO )为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开
2
发出用电解法制取ClO 的新工艺如图所示。
2
①图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO 。产生ClO 的电极应连接电源的
2 2
________(填“正极”或“负极”),对应的电极反应式为_______。
②a极区pH______(填“增大”“减小”或“不变”)。③图中应使用______(填“阴”或“阳”)离子交换膜。
(2)电解KMnO 溶液制备KMnO 。工业上,通常以软锰矿(主要成分是MnO )与KOH的混合物在铁坩埚(熔
2 4 4 2
融池)中混合均匀,小火加热至熔融,即可得到绿色的KMnO ,化学方程式为_______。用镍片作阳极(镍
2 4
不参与反应),铁板为阴极,电解KMnO 溶液可制备KMnO 。上述过程用流程图表示如下:
2 4 4
则D的化学式为_______;阳极的电极反应式为_______。