文档内容
1.(2020·全国卷Ⅱ,9)二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理
如下图所示。下列叙述错误的是( )
A.海水酸化能引起HCO浓度增大、CO浓度减小
B.海水酸化能促进CaCO 的溶解,导致珊瑚礁减少
3
C.CO 能引起海水酸化,其原理为HCOH++CO
2
D.使用太阳能、氢能等新能源可改善珊瑚的生存环境
2.(2018·海南,6)某温度下向含AgCl固体的AgCl饱和溶液中加少量稀盐酸,下列说法正
确的是( )
A.AgCl的溶解度、K 均减小
sp
B.AgCl的溶解度、K 均不变
sp
C.AgCl的溶解度减小、K 不变
sp
D.AgCl的溶解度不变,K 减小
sp
3.往锅炉注入NaCO 溶液浸泡,将水垢中的CaSO 转化为CaCO ,再用盐酸去除,下列叙
2 3 4 3
述正确的是( )
A.温度升高,NaCO 溶液的K 增大,c(OH-)减小
2 3 w
B.CaSO 能转化为CaCO ,说明K (CaCO)>K (CaSO)
4 3 sp 3 sp 4
C.CaCO 溶于盐酸而CaSO 不溶,是因为硫酸酸性强于盐酸
3 4
D.沉淀转化的离子方程式为CO(aq)+CaSO(s)CaCO (s)+SO(aq)
4 3
4.向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资
料得知:Ag++ 2NH ·H O[Ag(NH)]++ 2HO。下列分析不正确的是( )
3 2 3 2 2
A.浊液中存在沉淀溶解平衡:AgCl (s)Ag+(aq)+Cl-(aq)
B.实验可以证明NH 结合Ag+能力比Cl-强
3
C.实验表明实验室可用氨水洗涤银镜反应后的试管
D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
5.大气中CO 含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究
2
小组在实验室测得不同温度下(T ,T)海水中CO浓度与模拟空气中CO 浓度的关系曲线。
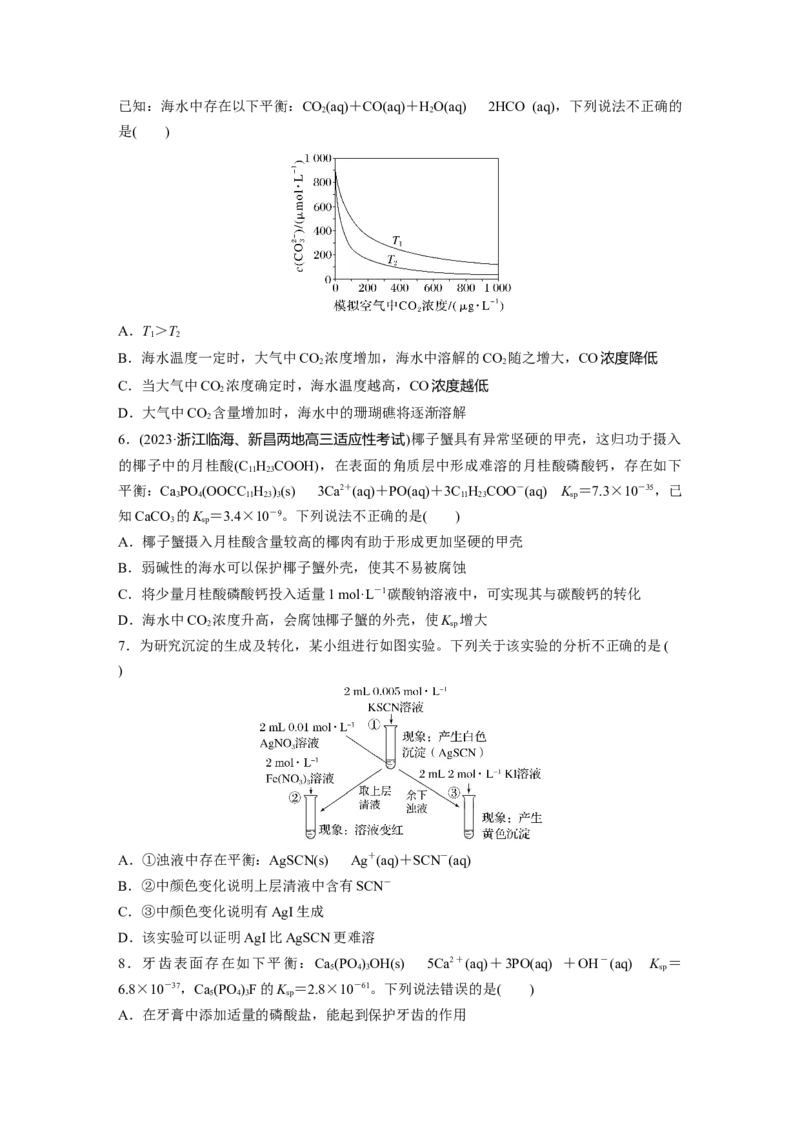
1 2 2已知:海水中存在以下平衡:CO(aq)+CO(aq)+HO(aq)2HCO (aq),下列说法不正确的
2 2
是( )
A.T>T
1 2
B.海水温度一定时,大气中CO 浓度增加,海水中溶解的CO 随之增大,CO浓度降低
2 2
C.当大气中CO 浓度确定时,海水温度越高,CO浓度越低
2
D.大气中CO 含量增加时,海水中的珊瑚礁将逐渐溶解
2
6.(2023·浙江临海、新昌两地高三适应性考试)椰子蟹具有异常坚硬的甲壳,这归功于摄入
的椰子中的月桂酸(C H COOH),在表面的角质层中形成难溶的月桂酸磷酸钙,存在如下
11 23
平衡:Ca PO (OOCC H )(s)3Ca2+(aq)+PO(aq)+3C H COO-(aq) K =7.3×10-35,已
3 4 11 23 3 11 23 sp
知CaCO 的K =3.4×10-9。下列说法不正确的是( )
3 sp
A.椰子蟹摄入月桂酸含量较高的椰肉有助于形成更加坚硬的甲壳
B.弱碱性的海水可以保护椰子蟹外壳,使其不易被腐蚀
C.将少量月桂酸磷酸钙投入适量1 mol·L-1碳酸钠溶液中,可实现其与碳酸钙的转化
D.海水中CO 浓度升高,会腐蚀椰子蟹的外壳,使K 增大
2 sp
7.为研究沉淀的生成及转化,某小组进行如图实验。下列关于该实验的分析不正确的是(
)
A.①浊液中存在平衡:AgSCN(s)Ag+(aq)+SCN-(aq)
B.②中颜色变化说明上层清液中含有SCN-
C.③中颜色变化说明有AgI生成
D.该实验可以证明AgI比AgSCN更难溶
8.牙齿表面存在如下平衡:Ca (PO )OH(s)5Ca2+(aq)+3PO(aq) +OH-(aq) K =
5 4 3 sp
6.8×10-37,Ca (PO )F的K =2.8×10-61。下列说法错误的是( )
5 4 3 sp
A.在牙膏中添加适量的磷酸盐,能起到保护牙齿的作用B.口腔中的食物残渣能产生有机酸,容易导致龋齿,使K 增大
sp
C.正常口腔的pH接近中性,有利于牙齿健康
D.使用含氟牙膏,当Ca (PO )OH(s)与Ca (PO )F(s)共存时,≈2.4×1024
5 4 3 5 4 3
9.探究Mg(OH) 的沉淀溶解平衡时,利用下表三种试剂进行实验,下列说法不正确的是(
2
)
编号 ① ② ③
分散质 Mg(OH) HCl NH Cl
2 4
备注 悬浊液 1 mol·L-1 1 mol·L-1
A.向①中滴加几滴酚酞溶液后,溶液显红色,说明Mg(OH) 是一种弱电解质
2
B.为了使Mg(OH) 悬浊液溶解得更快,加入过量NH Cl浓溶液并充分振荡,效果更好
2 4
C.①③混合后发生反应:Mg(OH) (s)+2NH(aq)Mg2+(aq)+2NH ·H O(aq)
2 3 2
D.向少量Mg(HCO ) 溶液中加入足量NaOH溶液,反应的离子方程式是Mg2++2HCO+
3 2
4OH-===Mg(OH) ↓+2CO+2HO
2 2
10.已知:常温下,K (NiCO)=1.4×10-7,K (PbCO )=1.4×10-13,则向浓度均为0.1 mol·L
sp 3 sp 3
-1的Ni(NO ) 和Pb(NO ) 混合溶液中逐滴加入NaCO 溶液,下列说法错误的是( )
3 2 3 2 2 3
A.常温下在水中的溶解度:NiCO>PbCO
3 3
B.逐滴加入NaCO 溶液,先生成NiCO 沉淀,后生成PbCO 沉淀
2 3 3 3
C.向NiCO 沉淀中加入Pb(NO ) 溶液,会生成PbCO 沉淀
3 3 2 3
D.逐滴加入NaCO 溶液,当两种沉淀共存时,溶液中c(Ni2+)∶c(Pb2+)=106∶1
2 3
11.(2023·湖南,9)处理某铜冶金污水(含Cu2+、Fe3+、Zn2+、Al3+)的部分流程如下:
已知:①溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
物质 Fe(OH) Cu(OH) Zn(OH) Al(OH)
3 2 2 3
开始沉淀pH 1.9 4.2 6.2 3.5
完全沉淀pH 3.2 6.7 8.2 4.6
②K (CuS)=6.4×10-36,K (ZnS)=1.6×10-24。
sp sp
下列说法错误的是( )
A.“沉渣Ⅰ”中含有Fe(OH) 和Al(OH)
3 3
B.NaS溶液呈碱性,其主要原因是S2-+HOHS-+OH-
2 2
C.“沉淀池Ⅱ”中,当Cu2+和Zn2+完全沉淀时,溶液中=4.0×10-12
D.“出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水12.[2021·海南,16(4)(5)](4)25 ℃时,潮湿的石膏雕像表面会发生反应:CaSO(s)+
4
CO(aq)CaCO (s)+SO(aq),其平衡常数K=______________。[已知K (CaSO)=9.1×10-
3 sp 4
6,K (CaCO)=2.8×10-9]
sp 3
(5)溶洞景区限制参观的游客数量,主要原因之一是游客呼吸产生的气体对钟乳石有破坏作
用,从化学平衡的角度说明其原因:______________________________________________
______________________________________________________________________________。
13.[2020·全国卷Ⅲ,27(4)]某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其
氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体
(NiSO ·7H O):
4 2
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Ni2+ Al3+ Fe3+ Fe2+
开始沉淀时(c=0.01 mol·L-1)的pH 7.2 3.7 2.2 7.5
沉淀完全时(c=1.0×10-5 mol·L-1)的pH 8.7 4.7 3.2 9.0
利用上述表格数据,计算Ni(OH) 的K =_________________________________________
2 sp
________________________________________________________________________(列出计
算式)。如果“转化”后的溶液中Ni2+浓度为1.0 mol·L-1,则“调pH”应控制的pH范围是
__________________。
14.氟化钡可用于制造电机电刷、光学玻璃、光导纤维、激光发生器等。以钡矿粉(主要成
分为BaCO ,含有SiO、Fe2+、Mg2+等杂质)为原料制备氟化钡的流程如下:
3 2
已知:常温下Fe3+、Mg2+完全沉淀的pH分别是3.4、12.4。
(1)滤渣A的化学式为____________。
(2)滤液1加HO 氧化的过程中主要反应的离子方程式为_____________________________。
2 2
(3)加20%NaOH溶液调节pH=12.5,得到滤渣C的主要成分是______________。
(4)滤液3加入盐酸酸化后再经__________、冷却结晶、__________、洗涤、真空干燥等一
系列操作后得到BaCl ·2H O。
2 2
(5)常温下,用BaCl ·2H O配制成0.2 mol·L-1水溶液与等浓度的氟化铵溶液反应,可得到氟
2 2化钡沉淀。请写出该反应的离子方程式:__________________________________________
______________________________________________________________________________。
已知K (BaF )=1.84×10-7,当钡离子完全沉淀时(即钡离子浓度≤10-5 mol·L-1),至少需要
sp 2
的氟离子浓度是________ mol·L-1(结果保留三位有效数字,已知=1.36)。