文档内容
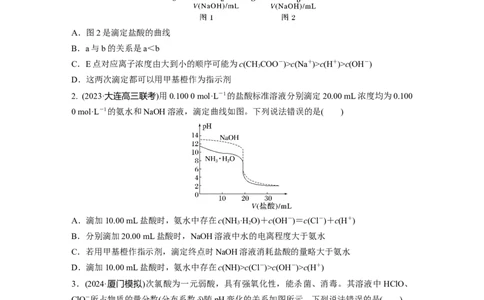
1.常温下,用0.10 mol·L-1 NaOH溶液分别滴定20.00 mL 0.10 mol·L-1盐酸和20.00 mL
0.10 mol·L-1 CHCOOH溶液,得到两条滴定曲线,如图所示,则下列说法正确的是( )
3
A.图2是滴定盐酸的曲线
B.a与b的关系是a<b
C.E点对应离子浓度由大到小的顺序可能为c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3
D.这两次滴定都可以用甲基橙作为指示剂
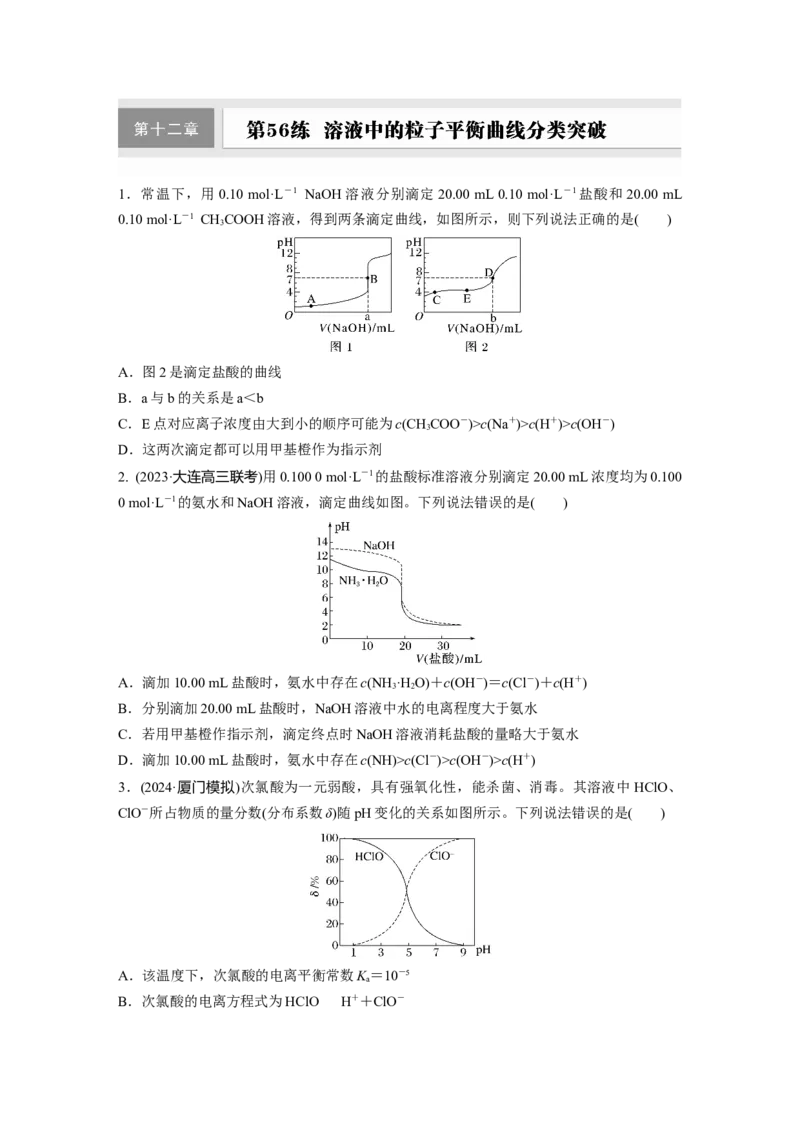
2. (2023·大连高三联考)用0.100 0 mol·L-1的盐酸标准溶液分别滴定20.00 mL浓度均为0.100
0 mol·L-1的氨水和NaOH溶液,滴定曲线如图。下列说法错误的是( )
A.滴加10.00 mL盐酸时,氨水中存在c(NH ·H O)+c(OH-)=c(Cl-)+c(H+)
3 2
B.分别滴加20.00 mL盐酸时,NaOH溶液中水的电离程度大于氨水
C.若用甲基橙作指示剂,滴定终点时NaOH溶液消耗盐酸的量略大于氨水
D.滴加10.00 mL盐酸时,氨水中存在c(NH)>c(Cl-)>c(OH-)>c(H+)
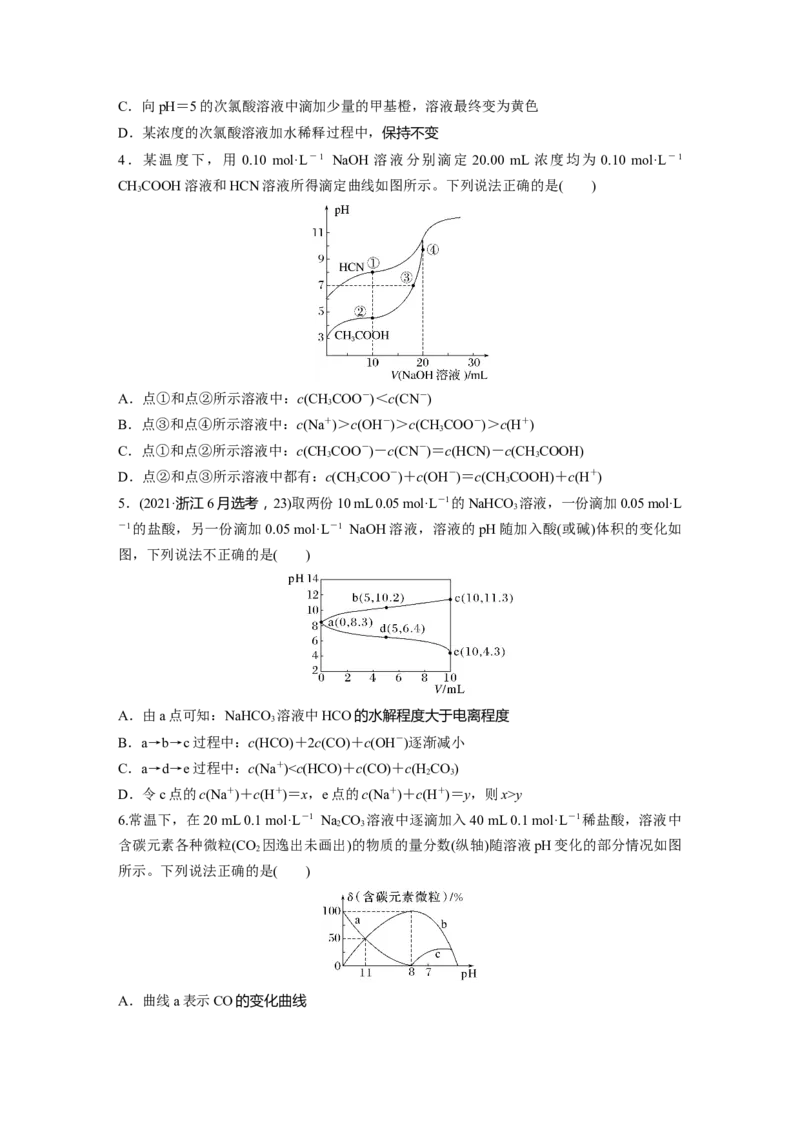
3.(2024·厦门模拟)次氯酸为一元弱酸,具有强氧化性,能杀菌、消毒。其溶液中 HClO、
ClO-所占物质的量分数(分布系数δ)随pH变化的关系如图所示。下列说法错误的是( )
A.该温度下,次氯酸的电离平衡常数K=10-5
a
B.次氯酸的电离方程式为HClOH++ClO-C.向pH=5的次氯酸溶液中滴加少量的甲基橙,溶液最终变为黄色
D.某浓度的次氯酸溶液加水稀释过程中,保持不变
4.某温度下,用 0.10 mol·L-1 NaOH 溶液分别滴定 20.00 mL 浓度均为 0.10 mol·L-1
CHCOOH溶液和HCN溶液所得滴定曲线如图所示。下列说法正确的是( )
3
A.点①和点②所示溶液中:c(CHCOO-)<c(CN-)
3
B.点③和点④所示溶液中:c(Na+)>c(OH-)>c(CHCOO-)>c(H+)
3
C.点①和点②所示溶液中:c(CHCOO-)-c(CN-)=c(HCN)-c(CHCOOH)
3 3
D.点②和点③所示溶液中都有:c(CHCOO-)+c(OH-)=c(CHCOOH)+c(H+)
3 3
5.(2021·浙江6月选考,23)取两份10 mL 0.05 mol·L-1的NaHCO 溶液,一份滴加0.05 mol·L
3
-1的盐酸,另一份滴加0.05 mol·L-1 NaOH溶液,溶液的pH随加入酸(或碱)体积的变化如
图,下列说法不正确的是( )
A.由a点可知:NaHCO 溶液中HCO的水解程度大于电离程度
3
B.a→b→c过程中:c(HCO)+2c(CO)+c(OH-)逐渐减小
C.a→d→e过程中:c(Na+)y
6.常温下,在20 mL 0.1 mol·L-1 Na CO 溶液中逐滴加入40 mL 0.1 mol·L-1稀盐酸,溶液中
2 3
含碳元素各种微粒(CO 因逸出未画出)的物质的量分数(纵轴)随溶液pH变化的部分情况如图
2
所示。下列说法正确的是( )
A.曲线a表示CO的变化曲线B.HCO、HCO、CO可大量共存于同一溶液中
2 3
C.pH=11时,c(HCO)c(A-)
8.25 ℃时,用0.10 mol·L-1的氨水滴定10.00 mL 0.05 mol·L-1 HA溶液,加入氨水的体积
2
(V)与溶液中lg的关系如图所示(忽略溶液体积变化)。下列说法不正确的是( )
A.A点溶液的pH等于1
B.由图中数据可知,HA为强酸
2
C.B点水电离出的H+浓度为1.0×10-6 mol·L-1
D.C点溶液中c(A2-)>c(NH)>c(OH-)>c(H+)
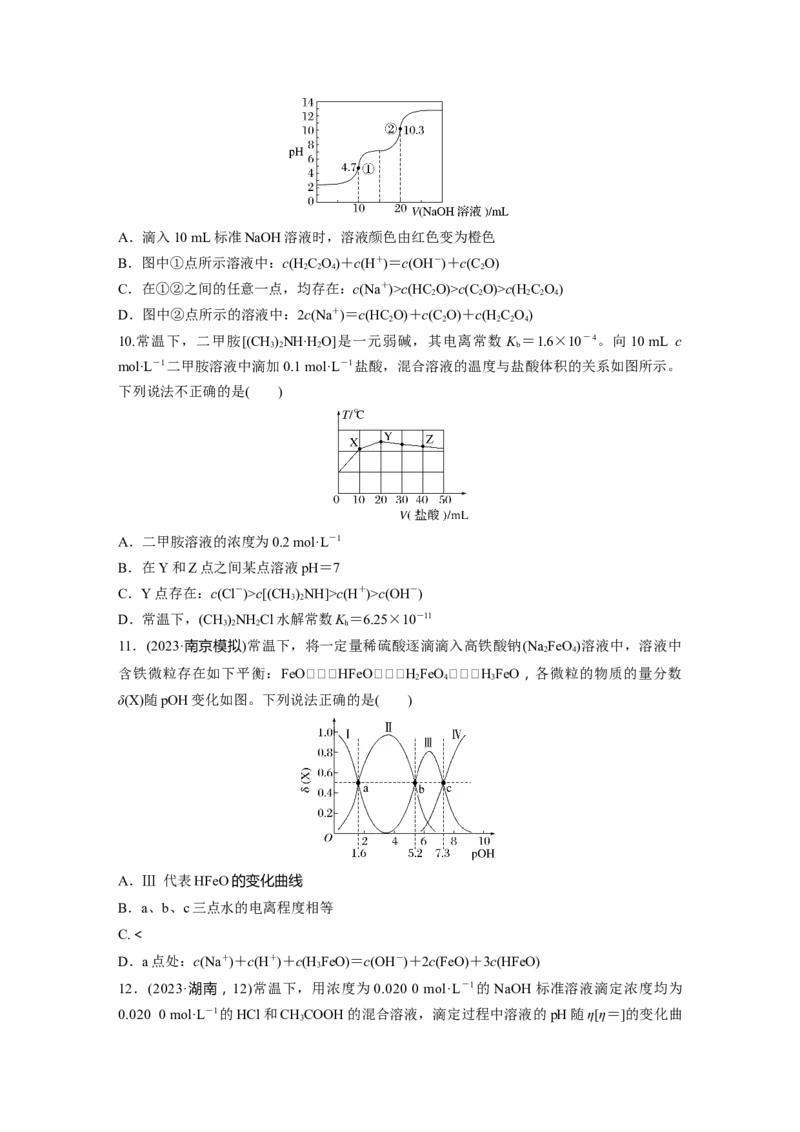
9.(2023·河北衡水高三模拟)常温下,向10 mL 0.1 mol·L-1的草酸(H C O)溶液中逐滴滴入
2 2 4
等浓度的NaOH溶液至过量,用甲基橙(变色范围的pH为3.1~4.4)作指示剂,并用pH计测
定滴定过程的溶液pH变化,其滴定曲线如图所示,则下列分析正确的是( )A.滴入10 mL标准NaOH溶液时,溶液颜色由红色变为橙色
B.图中①点所示溶液中:c(H C O)+c(H+)=c(OH-)+c(C O)
2 2 4 2
C.在①②之间的任意一点,均存在:c(Na+)>c(HC O)>c(C O)>c(H C O)
2 2 2 2 4
D.图中②点所示的溶液中:2c(Na+)=c(HC O)+c(C O)+c(H C O)
2 2 2 2 4
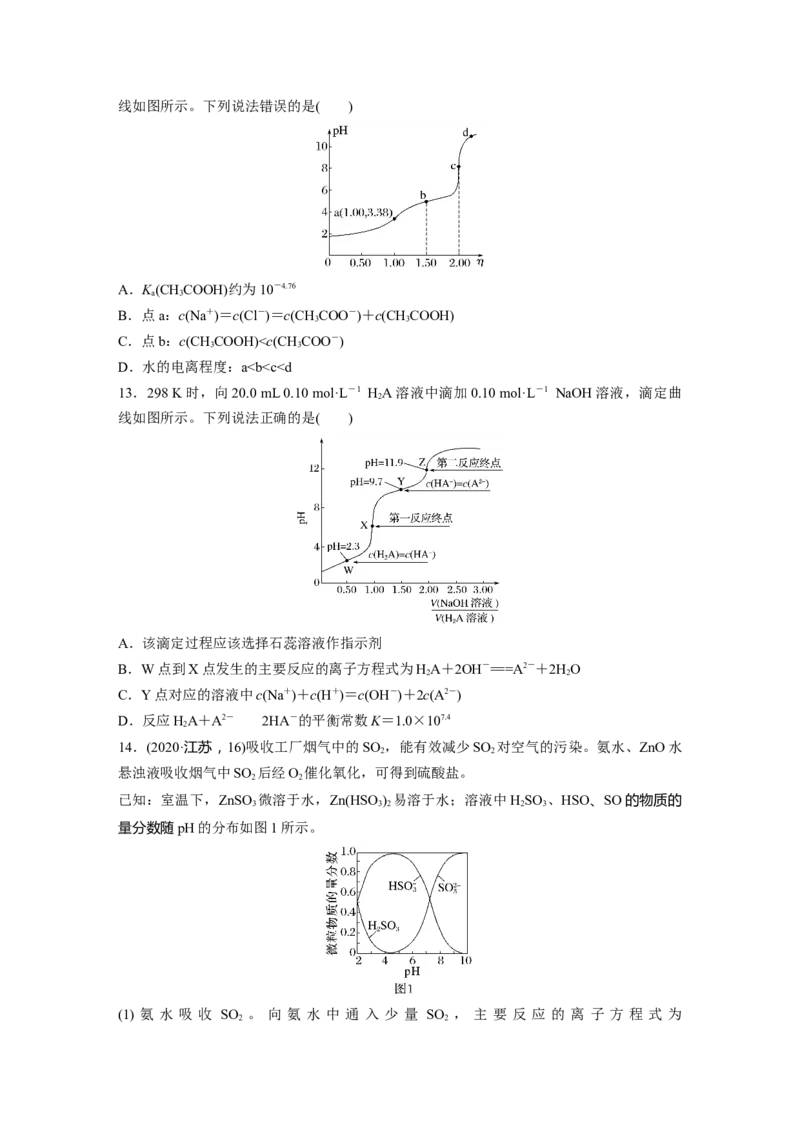
10.常温下,二甲胺[(CH )NH·HO]是一元弱碱,其电离常数 K =1.6×10-4。向 10 mL c
3 2 2 b
mol·L-1二甲胺溶液中滴加0.1 mol·L-1盐酸,混合溶液的温度与盐酸体积的关系如图所示。
下列说法不正确的是( )
A.二甲胺溶液的浓度为0.2 mol·L-1
B.在Y和Z点之间某点溶液pH=7
C.Y点存在:c(Cl-)>c[(CH )NH]>c(H+)>c(OH-)
3 2
D.常温下,(CH)NH Cl水解常数K =6.25×10-11
3 2 2 h
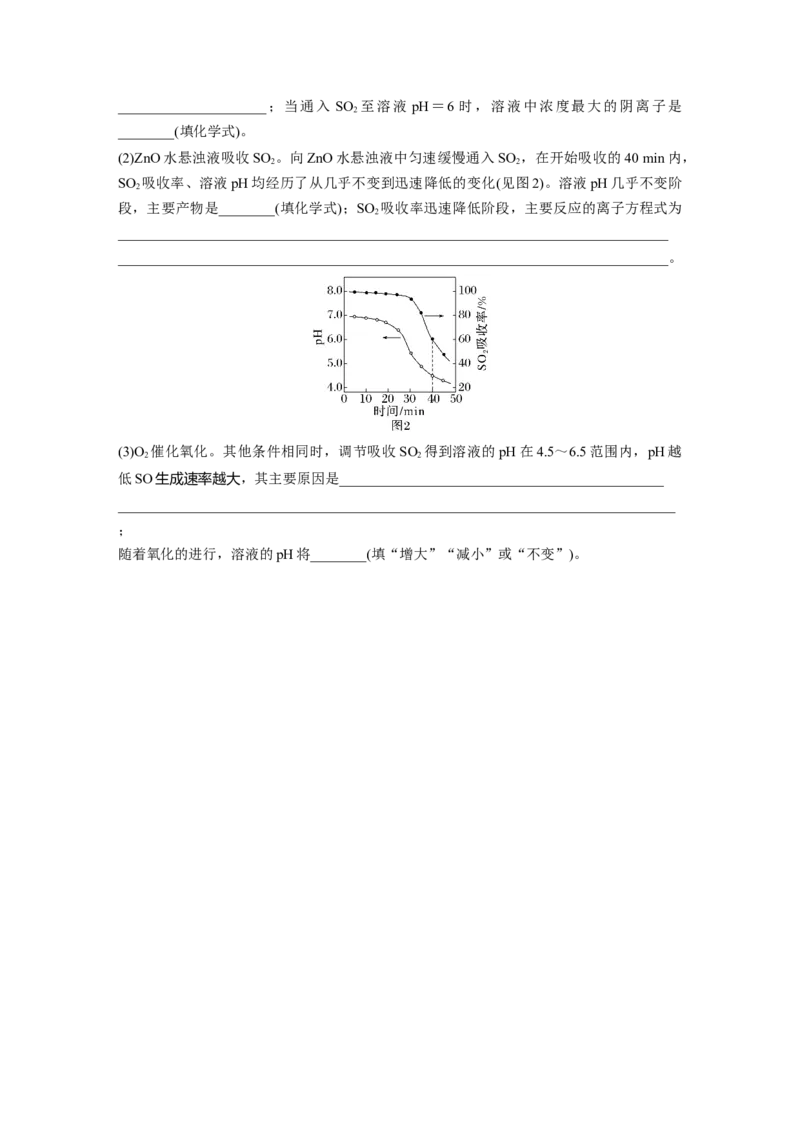
11.(2023·南京模拟)常温下,将一定量稀硫酸逐滴滴入高铁酸钠(Na FeO)溶液中,溶液中
2 4
含铁微粒存在如下平衡:FeOHFeOHFeOHFeO,各微粒的物质的量分数
2 4 3
δ(X)随pOH变化如图。下列说法正确的是( )
A.Ⅲ 代表HFeO的变化曲线
B.a、b、c三点水的电离程度相等
C.<
D.a点处:c(Na+)+c(H+)+c(H FeO)=c(OH-)+2c(FeO)+3c(HFeO)
3
12.(2023·湖南,12)常温下,用浓度为0.020 0 mol·L-1的NaOH标准溶液滴定浓度均为
0.020 0 mol·L-1的HCl和CHCOOH的混合溶液,滴定过程中溶液的pH随η[η=]的变化曲
3线如图所示。下列说法错误的是( )
A.K(CHCOOH)约为10-4.76
a 3
B.点a:c(Na+)=c(Cl-)=c(CHCOO-)+c(CHCOOH)
3 3
C.点b:c(CHCOOH)