文档内容
1.据《本草纲目》记载:“生熟铜皆有青,即是铜之精华,大者即空绿,以次空青也,铜
青则是铜器上绿色者,淘洗用之。”这里的“铜青”是指( )
A.CuO B.Cu O
2
C.Cu D.Cu (OH) CO
2 2 3
2.(2023·哈尔滨模拟)旅游景点售卖的仿银饰品大多是白铜(铜镍合金)。下列说法正确的是(
)
A.硬度比铜的大
B.熔点比铜的高
C.容易被腐蚀
D.通过外观颜色即可区分它和白银
3.下列有关铜的化合物说法正确的是( )
A.根据铁比铜金属性强,在实际应用中可用FeCl 腐蚀Cu刻制印刷电路板
3
B.CuSO 溶液与HS溶液反应的离子方程式为Cu2++S2-===CuS↓
4 2
C.用稀盐酸除去铜锈的离子方程式为CuO+2H+===Cu2++HO
2
D.化学反应:CuO+CO=====Cu+CO 的实验现象为黑色固体变成红色固体
2
4.下列铜及其化合物性质与用途具有对应关系的是( )
A.铜单质具有延展性,可用作传输电流
B.Cu O的熔、沸点较高,可用作催化反应
2
C.Cu(OH) 具有氧化性,可用作检验醛基
2
D.CuSO 能使蛋白质变性,可用于饮用水消毒
4
5.下列古诗或古文中的描述与化学方程式对应关系不正确的是( )
A.丹砂烧之成水银:HgS=====Hg+S
B.爆竹声中一岁除:S+2KNO+3C=====KS+3CO↑+N↑
3 2 2 2
C.炉火照天地,红星乱紫烟:Cu CO+2H=====Cu+CO+3HO
22 3 2 2 2
D.曾青得铁则化为铜:CuSO +Fe===FeSO +Cu
4 4
6.人类最早冶金的历史年代曲线图如图所示(-1000表示公元前1000年)。下列说法正确的
是( )A.金属越活泼,冶炼的年代一定越晚
B.冶炼金属的历史:电解氯化物比电解氧化物早
C.自然界中铜元素以游离态形式存在,故铜的冶炼年代最早
D.金属氧化物(如Al O、Cu O)也属于金属材料
2 3 2
7.(2023·西安模拟)金属的冶炼与生产、生活及国防军事等领域均密切相关。下列有关金属
冶炼的原理错误的是( )
A.用电解法制取金属钠:2NaCl(熔融)=====2Na+Cl↑
2
B.用Mg等活泼金属为还原剂冶炼Ti:2Mg+TiCl (熔融)=====Ti+2MgCl
4 2
C.用Al作还原剂冶炼金属V:3VO+10Al=====6V+5Al O
2 5 2 3
D.用H 作还原剂冶炼金属Ag:Ag O+H=====2Ag+HO
2 2 2 2
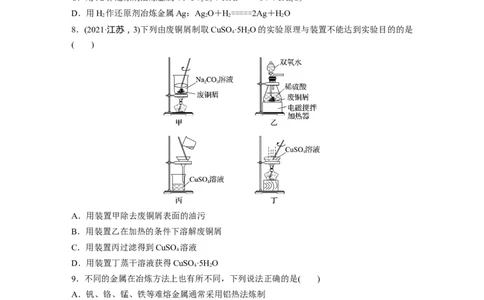
8.(2021·江苏,3)下列由废铜屑制取CuSO ·5H O的实验原理与装置不能达到实验目的的是
4 2
( )
A.用装置甲除去废铜屑表面的油污
B.用装置乙在加热的条件下溶解废铜屑
C.用装置丙过滤得到CuSO 溶液
4
D.用装置丁蒸干溶液获得CuSO ·5H O
4 2
9.不同的金属在冶炼方法上也有所不同,下列说法正确的是( )
A.钒、铬、锰、铁等难熔金属通常采用铝热法炼制
B.铝及其合金是电气、工业、家庭广泛使用的材料,是因为铝的冶炼方法比较简单
C.由于钠、镁、铝等金属化学性质太活泼,人们通常采用电解熔融状态下的氯化物的方式
来获取它们的单质
D.炼铁时加入的焦炭除了提供热量外,还用来制造还原剂一氧化碳
10.为研究废旧电池的再利用,实验室利用废旧电池的铜帽(主要成分为Zn和Cu)回收Cu
并制备ZnO的部分实验过程如图所示。下列叙述错误的是( )A.“溶解”操作中溶液温度不宜过高
B.铜帽溶解后,将溶液加热至沸腾以除去溶液中过量的氧气或HO
2 2
C.与锌粉反应的离子可能为Cu2+、H+
D.“过滤”操作后,将滤液蒸发结晶、过滤、洗涤、干燥后,高温灼烧即可得纯净的ZnO
11.向CuSO 溶液中加入HO 溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色
4 2 2
溶液变为红色浑浊(Cu O),继续加入HO 溶液,红色浑浊又变为蓝色溶液,这个反应可以
2 2 2
反复多次。下列关于上述过程的说法不正确的是( )
A.Cu2+将HO 还原为O
2 2 2
B.HO 既表现氧化性又表现还原性
2 2
C.Cu2+是HO 分解反应的催化剂
2 2
D.发生了反应:Cu O+HO+4H+===2Cu2++3HO
2 2 2 2
12.氯化亚铜(CuCl)是一种微溶于水、不溶于乙醇、易被氧化的白色粉末,以黄铜矿(主要
成分为CuFeS)为原料制取CuCl的流程如图所示:
2
已知:在水溶液中存在平衡:CuCl(s)+2Cl-(aq)[CuCl ]2-(aq)。下列说法错误的是( )
3
A.“浸取”后所得浸取液可用来腐蚀铜制电路板
B.加入浓盐酸的目的是为了实现CuCl的净化
C.[CuCl ]2-中加水可使平衡CuCl(s)+2Cl-(aq)[CuCl ]2-(aq)逆向移动
3 3
D.采用乙醇洗涤和真空干燥有利于提高CuCl的产率和纯度
13.铜器久置,表面会生成一层绿色固体,为探究铜在空气中的腐蚀情况,某化学兴趣小组
收集家中铜器表面的绿色固体进行探究。
①对试管内的绿色固体进行加热,至完全分解,观察到A装置中绿色固体逐渐变成黑色,B
装置中无水硫酸铜变成蓝色,C装置中澄清石灰水变浑浊。
②取少量加热后生成的黑色固体于试管中,加入稀硫酸,观察到黑色固体逐渐溶解,溶液变成蓝色。
③取少量上述蓝色溶液于试管中,浸入一根洁净的铁丝。观察到铁丝表面有红色物质析出。
请回答下列问题:
(1)绿色固体中含有的元素是_____________________________________________________。
(2)加热后试管中剩余的黑色物质是_______________________________________________。
(3)假设该绿色物质是一种纯净物,则其化学式可能是______________________,加热分解
的化学方程式为_________________________________________________________________。
(4)上述实验步骤③中反应的离子方程式为_________________________________________
_____________________________________________________________________________。
(5)实验装置最后的干燥管的作用是_______________________________________________
_____________________________________________________________________________。
(6)如果将B、C两装置对调,能否达到实验目的?________(填“能”或“不能”),为什么?
_____________________________________________________________________________
_____________________________________________________________________________。
14.工业上由黄铜矿(主要成分CuFeS)冶炼铜的主要流程如下:
2
(1)气体A中的大气污染物可选用下列试剂中的________(填字母)吸收。
a.浓HSO b.稀HNO
2 4 3
c.NaOH溶液 d.氨水
(2)用稀HSO 浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在
2 4
______(填离子符号),检验溶液中还存在Fe2+的方法是_______________________________。
(3)由泡铜冶炼粗铜的化学方程式为_______________________________________________
_____________________________________________________________________________。
(4)取一定量的泡铜,加入1 L 0.6 mol·L-1 HNO 溶液恰好完全溶解,同时放出2 240 mL NO
3
气体(标准状况),另取等量的泡铜,用足量的H 还原,得到的铜的质量为________g。
2