文档内容
特色练 5 原子、分子的结构与性质
1.2022年北京冬奥会已经成功落下帷幕,它的成功举办离不开各种科技力量的支撑。下列
说法正确的是( )
A.跨临界直接制冰使用的CO 分子中含有非极性键
2
B.滑冰场上的冰中水分子的稳定性低于甲烷
C.颁奖礼服内胆中添加了石墨烯(结构如图),其中C原子的杂化方式是sp3杂化
D.闭幕式中,鸟巢上空绽放的璀璨焰火与原子核外电子发生跃迁释放能量有关
2.已知NO能被FeSO 溶液吸收生成配合物[Fe(NO)(H O) ]SO 。下列说法正确的是( )
4 2 5 4
A.该配合物中阴离子为平面正方形
B.该配合物的配体为NO,配位数为1
C.Fe2+的价层电子排布式为3d54s1,易被氧化为Fe3+
D.HO的VSEPR模型为四面体形,空间结构为V形
2
3.100多年来,人类首次合成了甲二醇,它的化学式为CH(OH) ,这种有机分子是形成气
2 2
溶胶和大气臭氧层反应的关键中间物。关于甲二醇的说法错误的是( )
A.甲二醇分子中有3个sp3杂化的原子
B.甲二醇是非极性分子
C.甲二醇的沸点高于甲醇
D.相同物质的量的甲二醇和甲醇完全燃烧,甲二醇的耗氧量低
4.离子液体常被用作电化学研究的电解质、有机合成的溶剂和催化剂。如图是离子液体 1-
丁基-3-甲基咪唑六氟磷酸盐的结构简式。下列说法正确的是( )
A.该物质含有的化学键类型是共价键
B.PF的空间结构为三角双锥形
C.该物质中N有2种杂化轨道类型
D.离子液体的沸点较低,容易挥发
5.物质结构决定物质的性质。下列说法错误的是( )A.由于钙离子半径大于镁离子半径,可推测碳酸钙的分解温度高于碳酸镁
B.由于氢键的存在,可推测邻羟基苯甲醛沸点高于对羟基苯甲醛
C.由于N的电负性小于F,可推测NH 具有碱性(可与H+结合)而NF 没有碱性
3 3
D.由于孤电子对排斥作用较大,可推测单个水分子中∠H—O—H小于[Ti(HO) ]2+中∠H—
2 6
O—H
6.下列关于O、S及其化合物的说法错误的是( )
A.O的电负性比S的大,可推断HO分子的极性比HS的极性大
2 2
B.电子云重叠程度O—H比S—H的大,可推断O—H比S—H更稳定
C.HO的相对分子质量比HS的小,可推断HO的沸点比HS的低
2 2 2 2
D.HO的成键电子对排斥力大,可推测HO的键角比HS的大
2 2 2
7.下列说法正确的是( )
A.HCl和Cl 分子中均含有s-p σ键
2
B.甲醛(HCHO)中H—C—H的键角小于光气(COCl )中Cl—C—Cl的键角;NF 键角大于
2 3
NH 键角
3
C.NH Cl中阳离子的键角大于NH 的键角
4 3
D.酸性:HCOOH>CH COOH>CHCl COOH>CCl COOH
3 2 3
8.下列关于卤素及其化合物的说法错误的是( )
A.I的空间结构为直线形
B.顺-1,2-二氯乙烯分子的极性大于反-1,2-二氯乙烯
C.HClO、HClO、HClO、HClO酸性依次减小的主要原因是中心原子的正电性依次减小
4 3 2
D.固态PCl 中含有[PCl ]+[PCl ]-,而PBr 中含有[PBr ]+Br-,存在差异的原因是Br-的半
5 4 6 5 4
径较大
9.下列有关物质结构与性质的说法正确的是( )
A.碳正离子CH呈平面三角形
B.Mn是第四周期未成对电子数最多的元素
C.物质的熔、沸点:MgO>C(金刚石)>O
2
D.冰分子中的化学键即氢键可以表示为O—H…O
10.“液态阳光”由中国科学院液态阳光研究组命名,指的是利用太阳能、风能等可再生能
源分解水制氢,再将空气中的CO 加氢制成CHOH等液体燃料。该过程零污染、零排放,
2 3
并且可形成循环,是迄今为止人类制备CHOH最清洁环保的方式之一,下列说法错误的是(
3
)
A.即使使用高效催化剂,改变反应历程,CO 和HO合成CHOH和O 也为吸热反应
2 2 3 2
B.SiO 的熔点比CO 的高,原因是SiO 的分子间作用力更大
2 2 2
C.CO 是直线形分子
2
D.甲醇的沸点介于水和甲硫醇(CHSH)之间
3
11.尿素[CO(NH)]可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为
2 2[Fe(H NCONH)](NO )。下列说法错误的是( )
2 2 6 3 3
A.电负性:O>N>C>H
B.基态Fe3+核外电子排布式为1s22s22p63s23p63d5
C.NO与尿素分子中的N原子杂化方式相同
D.C、N原子中电子占据能量最高的轨道形状相同
12.实验室中利用 CoCl 制取配合物[Co(NH )]Cl 的反应为 2CoCl +10NH +2NH Cl+
2 3 6 3 2 3 4
HO===2[Co(NH )]Cl +2HO。下列叙述正确的是( )
2 2 3 6 3 2
A.Co2+的价层电子轨道表示式为
B.1 mol [Co(NH)]3+中含σ键为18 mol
3 6
C.HO 中氧原子采取sp3杂化
2 2
D.氨分子间存在氢键,因而NH 易溶于水
3
13.燃煤燃烧过程中易产生CO、SO 气体,下列关于CO、SO 说法正确的是( )
2 2 2 2
A.均为含有极性键的极性分子
B.空间结构相同
C.CO 分子中键角大于SO
2 2
D.C与S杂化类型相同
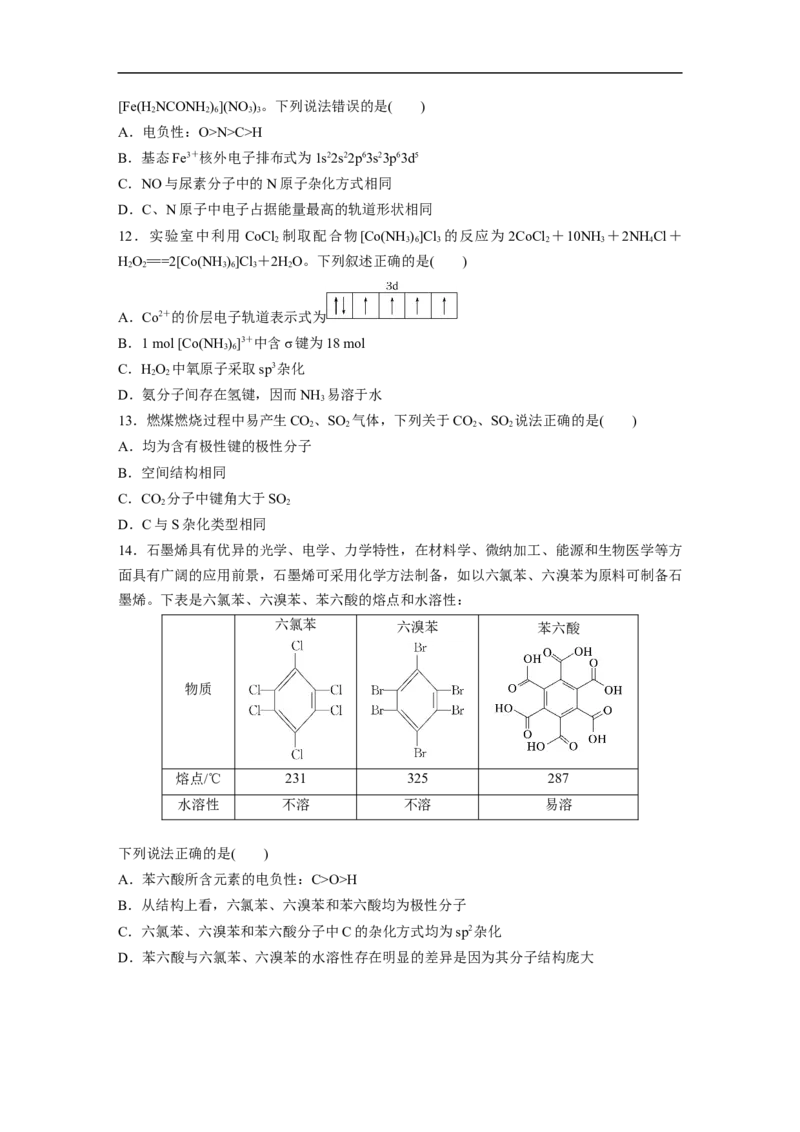
14.石墨烯具有优异的光学、电学、力学特性,在材料学、微纳加工、能源和生物医学等方
面具有广阔的应用前景,石墨烯可采用化学方法制备,如以六氯苯、六溴苯为原料可制备石
墨烯。下表是六氯苯、六溴苯、苯六酸的熔点和水溶性:
六氯苯 六溴苯 苯六酸
物质
熔点/℃ 231 325 287
水溶性 不溶 不溶 易溶
下列说法正确的是( )
A.苯六酸所含元素的电负性:C>O>H
B.从结构上看,六氯苯、六溴苯和苯六酸均为极性分子
C.六氯苯、六溴苯和苯六酸分子中C的杂化方式均为sp2杂化
D.苯六酸与六氯苯、六溴苯的水溶性存在明显的差异是因为其分子结构庞大