文档内容
考点 09 钠及其重要化合物
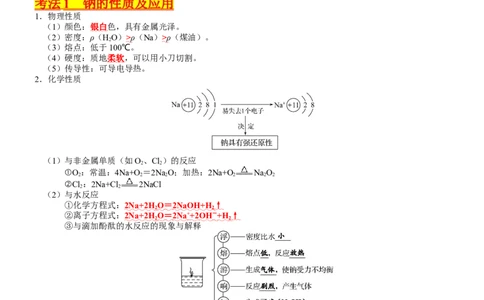
1.3年真题考点分布
考点分布
年份 卷区 钠的性
钠的氧化物的性质 碳酸氢钠和碳酸钠的性质 综合应用
质
广东 √ √
河北 √
江苏 √
天津 √
2022
海南 √
辽宁 √
山东 √
浙江 √ √
北京 √ √
海南 √ √
广东 √ √
2021 河北 √
辽宁 √
湖南 √
湖北 √
海南 √
2020 浙江 √
北京 √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于钠及其化合物主要考查:
1.单质钠的性质及应用
2.钠的氧化物的性质及应用
3.碳酸钠\碳酸氢钠的性质及应用
4.碱金属性质的相似性及递变性
5.焰色试验
【备考策略】熟练掌握钠及其化合物之间的转化关系,熟悉各物质的特特殊性质及其应用;明确元素化合物和
化学反应原理、物质结构和性质之间的联系。
【命题预测】在近几年的高考中,主要以钠、过氧化钠的性质、碳酸钠、碳酸氢钠为知识载体,结合生活、生
产及物质的应用,以选择题、实验题和流程题等形式考查学生的思维能力、实验能力、计算能力。在实验题和
流程题中往往涉及物质制备、分离、检验、含量的计算等;高考题中对碱金属的考查,多与元素周期律相结合,
考查其性质、在生产中的应用及物质的制备等。
资料收集整理【淘宝店铺:向阳百分百】考法 1 钠的性质及应用
1.物理性质
(1)颜色:银白色,具有金属光泽。
(2)密度:ρ(HO)>ρ(Na)>ρ(煤油)。
2
(3)熔点:低于100℃。
(4)硬度:质地柔软,可以用小刀切割。
(5)传导性:可导电导热。
2.化学性质
(1)与非金属单质(如O、Cl)的反应
2 2
①O:常温:4Na+O=2NaO;加热:2Na+O NaO
2 2 2 2 2 2
②Cl :2Na+Cl 2NaCl
2 2
(2)与水反应
①化学方程式:2Na+2H O = 2NaOH+H ↑
2 2
②离子方程式:2Na+2H O = 2Na + +2 OH - +H ↑
2 2
③与滴加酚酞的水反应的现象与解释
(3)与乙醇反应:
①化学方程式:2Na+2CH OH → 2C HONa+H ↑
2 5 2 5 2
②反应现象:钠沉在容器底部,缓慢反应冒气泡
(4)与酸(如盐酸)
①离子方程式: 2Na+2H + = 2Na + +H ↑,
2
②现象:钠与酸的反应比与水的反应更剧烈。
(5)与盐(如CuSO )溶液的反应
4
①离子方程式:2Na+2H O = 2Na + +2OH - +H ↑, Cu 2+ +2OH - = Cu ( OH ) ↓
2 2 2
②现象:有气泡和蓝色沉淀产生
3.钠的制取、保存与用途
(1)制取: 2NaCl (熔融) 2Na+Cl ↑
2
(2)保存:通常保存在石蜡油或煤油中
资料收集整理【淘宝店铺:向阳百分百】(3)用途
①钠、钾合金(液态)用于原子反应堆,作导热剂。
②作强还原剂,熔融状态冶炼某些金属(如钛)。
③作电光源,制作高压钠灯。
【典例1】某同学将金属钠露置于空气中足够长时间,观察到下列现象:银白色→变灰暗→变白色→出现液滴
→白色固体→白色粉末。下列有关叙述不正确的是( )。
A.表面迅速变暗是因为钠与空气中的氧气反应生成了NaO
2
B.出现液滴原因是生成的NaCO 吸收空气中的水蒸气在表面形成了溶液
2 3
C.最后白色粉末为碳酸钠粉末
D.最后白色粉末的质量比金属钠质量大
【解析】选B。小块金属钠露置于空气中发生的变化中,银白色→变灰暗→变白色→出现液滴→白色固体→白
色粉末,是钠被氧化为氧化钠;氧化钠和水反应生成氢氧化钠;氢氧化钠潮解形成氢氧化钠溶液;二氧化碳和
氢氧化钠反应生成十水碳酸钠,最终风化变成的白色粉末为碳酸钠,据此解答。因钠很活泼,易被氧化,则金
属钠在空气中易被氧化形成氧化钠,出现表面变暗现象,故A正确;氧化钠与空气中的水反应生成氢氧化钠,
氢氧化钠吸收空气中的水蒸气在表面形成了溶液,故B错误;生成的氢氧化钠再与空气中的二氧化碳反应生成
碳酸钠的结晶水合物,最终风化变成的白色粉末为碳酸钠,故C正确;最后白色粉末为碳酸钠,质量比金属钠
的质量大,故D正确。
【拓展延伸】钠在空气中的变化过程
1.变化过程
2.相关化学方程式
(1)4Na+O 2NaO
2 2
(2)NaO+HO 2NaOH
2 2
(3)2NaOH+CO NaCO+H O,NaCO+10H O NaCO·10HO
2 2 3 2 2 3 2 2 3 2
(4)NaCO·10HO NaCO+10H O
2 3 2 2 3 2
3.两个变化过程
(1)潮解过程主要发生物理变化
(2)风化过程则发生了化学变化
【典例2】(2023·沈阳模拟)如图,在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO 与
4
熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成,据此判断下列说法中不正确的是( )。
A.上述反应是置换反应
B.上述反应说明钠比铜活泼
C.上述反应证明钠可以从CuSO 溶液中置换出铜
4
D.加热且无水条件下,Na可以与CuSO 反应并生成Cu
4
【解析】选C。实验在无水条件下进行,有红色物质生成,说明熔融的钠将硫酸铜中的铜置换出来,属于置换
反应,钠作还原剂,硫酸铜作氧化剂,说明钠比铜活泼,故A、B项正确;若钠与CuSO 溶液混合,则钠先与
4
水反应生成氢氧化钠,氢氧化钠再与硫酸铜反应生成氢氧化铜,不会置换出铜单质,故C错误;根据以上分析,
在无水条件下,Na可以与CuSO 反应并生成Cu,故D正确。
4
【拓展延伸】Na与盐反应的原理
1.Na与盐的反应
(1)钠与盐溶液反应(以CuSO 为例):先与水反应,生成的碱与盐可能发生复分解反应
4
①现象:有气泡产生,产生蓝色沉淀
②反应:2Na+CuSO+2H O Cu ( OH ) ↓ +N a SO +H ↑
4 2 2 2 4 2
(2)钠与熔融盐反应(以TiCl 为例)
4
①本质:钠与熔融的盐的置换反应
资料收集整理【淘宝店铺:向阳百分百】②反应: 4 Na+ TiCl Ti + 4 Na Cl
4
③Na+KCl NaCl+K↑,Na能够制取K并不能说明Na的还原性比K强,因为K的沸点比Na低,使
K成为蒸气逸出
2.钠与水、酸、醇、羧酸、酚及盐溶液反应的实质都是与H+的反应。
3.钠与乙醇反应的特点——慢、沉
钠与乙醇反应,钠块先沉在液面下,后上下浮动、能看到表面冒出气泡,并不能熔化成小球。
4.钠与酸反应
(1)特点——快,可能燃烧或爆炸。
(2)过量钠和酸的反应:钠直接与酸反应
①先: 2Na+2H Cl 2Na Cl +H ↑
2
②后:2Na+2HO 2NaOH+H ↑
2 2
5.钠和碱溶液的反应:实际上是钠和水的反应
(1)饱和NaOH溶液:有气泡产生,有白色晶体析出
(2)澄清石灰水:有气泡产生,溶液变浑浊
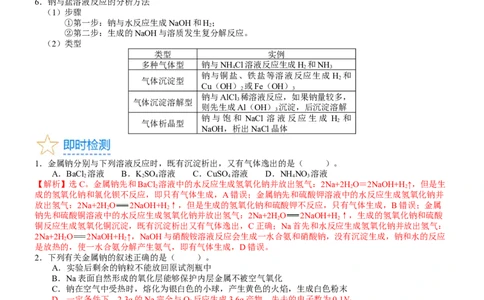
6.钠与盐溶液反应的分析方法
(1)步骤
①第一步:钠与水反应生成NaOH和H;
2
②第二步:生成的NaOH与溶质发生复分解反应。
(2)类型
类型 实例
多种气体型 钠与NH Cl溶液反应生成H 和NH
4 2 3
钠与铜盐、铁盐等溶液反应生成 H 和
气体沉淀型 2
Cu(OH) 或Fe(OH)
2 3
钠与AlCl 稀溶液反应,如果钠量较多,
气体沉淀溶解型 3
则先生成Al(OH) 沉淀,后沉淀溶解
3
钠与饱和 NaCl 溶液反应生成 H 和
气体析晶型 2
NaOH,析出NaCl晶体
1.金属钠分别与下列溶液反应时,既有沉淀析出,又有气体逸出的是( )。
A.BaCl 溶液 B.KSO 溶液 C.CuSO 溶液 D.NH NO 溶液
2 2 4 4 4 3
【解析】选C。金属钠先和BaCl 溶液中的水反应生成氢氧化钠并放出氢气:2Na+2HO=2NaOH+H ↑,但是生
2 2 2
成的氢氧化钠和氯化钡不反应,即只有气体生成,A错误;金属钠先和硫酸钾溶液中的水反应生成氢氧化钠并
放出氢气:2Na+2HO 2NaOH+H ↑,但是生成的氢氧化钠和硫酸钾不反应,只有气体生成,B错误;金属
2 2
钠先和硫酸铜溶液中的水反应生成氢氧化钠并放出氢气:2Na+2HO 2NaOH+H ↑,生成的氢氧化钠和硫酸
2 2
铜反应生成氢氧化铜沉淀,既有沉淀析出又有气体逸出,C正确;Na首先和水反应生成氢氧化钠并放出氢气:
2Na+2HO 2NaOH+H ↑,NaOH与硝酸铵溶液反应会生成一水合氨和硝酸钠,没有沉淀生成,钠和水的反应
2 2
是放热的,使一水合氨分解产生氨气,即有气体生成,D错误。
2.下列有关金属钠的叙述正确的是( )。
A.实验后剩余的钠粒不能放回原试剂瓶中
B.Na表面自然形成的氧化层能够保护内层金属不被空气氧化
C.钠在空气中受热时,熔化为银白色的小球,产生黄色的火焰,生成白色粉末
D.一定条件下,2.3g的Na完全与O 反应生成3.6g产物,失去的电子数为0.1N
2 A
【解析】选D。实验剩余的钠应放回原试剂瓶,A错误;Na表面形成的氧化层不能保护内层金属不被空气氧化,
B错误;钠在空气中加热,生成了淡黄色的过氧化钠,故C错误;2.3g钠的物质的量为0.1mol,而钠无论反应
后产物是氧化钠还是过氧化钠,钠元素化合价均为+1价,故0.1mol钠失去0.1N 个电子,D正确。
A
考法 2 钠的氧化物
物质 氧化钠(NaO) 过氧化钠(NaO)
2 2 2
颜色状态 白色固体 淡黄色固体
氧的价态 - 2 价 - 1 价
电子式
所含离子 2个Na+和1个 O 2 - 2个Na+和1个O2-
2
化学键 离子键 离子键和共价键
氧化物类别 碱性氧化物 过氧化物(不属碱性氧化物)
与水反应 Na O+H O = 2NaOH 2Na O+2H O = 4NaOH+O ↑
2 2 2 2 2 2
资料收集整理【淘宝店铺:向阳百分百】与CO 反应 Na O+CO = N a CO 2Na O+2CO = 2N a CO +O
2 2 2 2 3 2 2 2 2 3 2
NaO+2HCl=
与盐酸反应 2 2NaO+4HCl=4NaCl+2H O+O↑
2NaCl+H O 2 2 2 2
2
保存 密封 密封、远离易燃物
主要用途 制烧碱 漂白剂、消毒剂、供氧剂
【特别提醒】NaO 具有强氧化性,但NaO 与水、CO 反应时,水中的氢与CO 中的碳都处于最高价态,不能
2 2 2 2 2 2
被氧化,反应为NaO 自身的氧化还原反应。
2 2
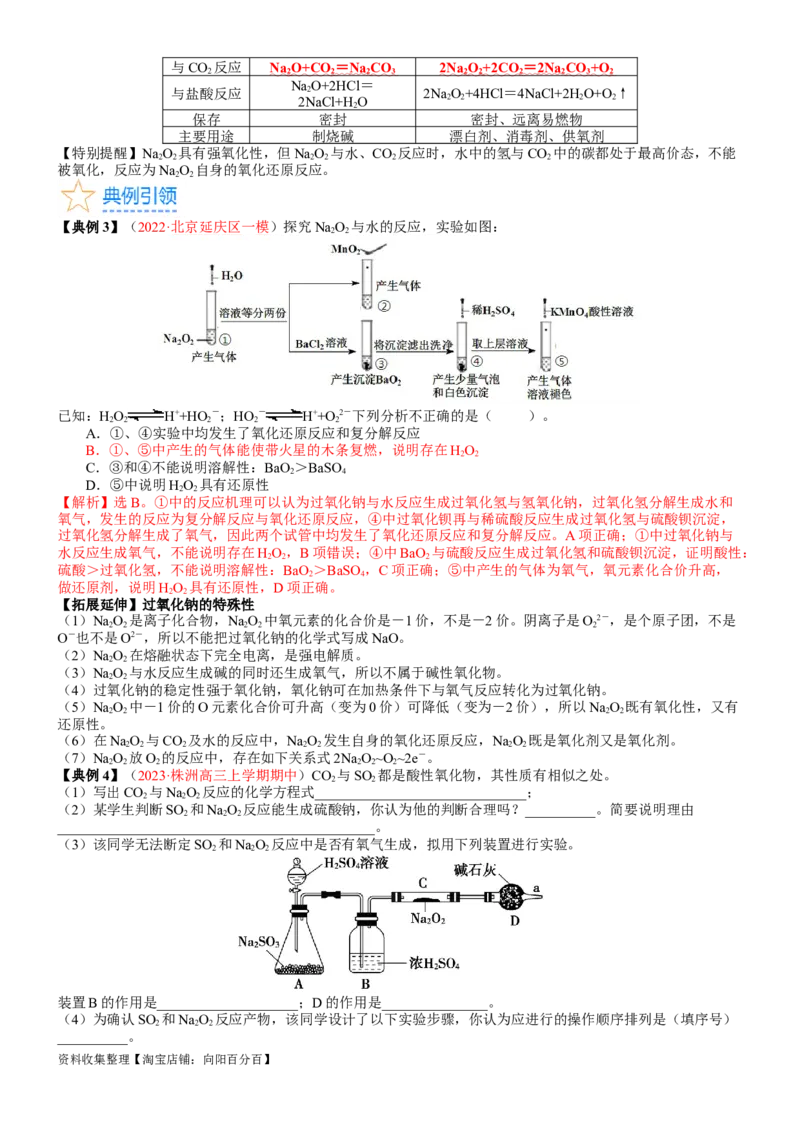
【典例3】(2022·北京延庆区一模)探究NaO 与水的反应,实验如图:
2 2
已知:HO H++HO-;HO - H++O 2-下列分析不正确的是( )。
2 2 2 2 2
A.①、④实验中均发生了氧化还原反应和复分解反应
B.①、⑤中产生的气体能使带火星的木条复燃,说明存在HO
2 2
C.③和④不能说明溶解性:BaO>BaSO
2 4
D.⑤中说明HO 具有还原性
2 2
【解析】选B。①中的反应机理可以认为过氧化钠与水反应生成过氧化氢与氢氧化钠,过氧化氢分解生成水和
氧气,发生的反应为复分解反应与氧化还原反应,④中过氧化钡再与稀硫酸反应生成过氧化氢与硫酸钡沉淀,
过氧化氢分解生成了氧气,因此两个试管中均发生了氧化还原反应和复分解反应。A项正确;①中过氧化钠与
水反应生成氧气,不能说明存在HO,B项错误;④中BaO 与硫酸反应生成过氧化氢和硫酸钡沉淀,证明酸性:
2 2 2
硫酸>过氧化氢,不能说明溶解性:BaO>BaSO,C项正确;⑤中产生的气体为氧气,氧元素化合价升高,
2 4
做还原剂,说明HO 具有还原性,D项正确。
2 2
【拓展延伸】过氧化钠的特殊性
(1)NaO 是离子化合物,NaO 中氧元素的化合价是-1价,不是-2价。阴离子是O2-,是个原子团,不是
2 2 2 2 2
O-也不是O2-,所以不能把过氧化钠的化学式写成NaO。
(2)NaO 在熔融状态下完全电离,是强电解质。
2 2
(3)NaO 与水反应生成碱的同时还生成氧气,所以不属于碱性氧化物。
2 2
(4)过氧化钠的稳定性强于氧化钠,氧化钠可在加热条件下与氧气反应转化为过氧化钠。
(5)NaO 中-1价的O元素化合价可升高(变为0价)可降低(变为-2价),所以NaO 既有氧化性,又有
2 2 2 2
还原性。
(6)在NaO 与CO 及水的反应中,NaO 发生自身的氧化还原反应,NaO 既是氧化剂又是氧化剂。
2 2 2 2 2 2 2
(7)NaO 放O 的反应中,存在如下关系式2NaO~O~2e-。
2 2 2 2 2 2
【典例4】(2023·株洲高三上学期期中)CO 与SO 都是酸性氧化物,其性质有相似之处。
2 2
(1)写出CO 与NaO 反应的化学方程式______________________________;
2 2 2
(2)某学生判断SO 和NaO 反应能生成硫酸钠,你认为他的判断合理吗?__________。简要说明理由
2 2 2
_____________________________________________。
(3)该同学无法断定SO 和NaO 反应中是否有氧气生成,拟用下列装置进行实验。
2 2 2
装置B的作用是____________________;D的作用是_______________。
(4)为确认SO 和NaO 反应产物,该同学设计了以下实验步骤,你认为应进行的操作顺序排列是(填序号)
2 2 2
__________。
资料收集整理【淘宝店铺:向阳百分百】A.用带火星的木条靠近干燥管口,观察木条是否复燃
B.将C装置中反应后的固体物质溶于适量水配成溶液
C.在配成的溶液中加入用硝酸酸化的硝酸钡溶液,观察是否有沉淀生成
D.在配成的溶液中先加入盐酸,再加入氯化钡溶液,观察是否有气泡或沉淀生成
【解析】(1)NaO 与CO 反应的化学方程式2NaO+2CO =2NaCO+O ;(2)由于过氧化钠具有强氧化性,
2 2 2 2 2 2 2 3 2
能将+4价的硫氧化为+6价而生成硫酸钠,故该学生的判断是合理的。(3)B装置用于干燥SO 气体,防止水
2
蒸气进入C装置与NaO 反应:2NaO+2H O=4NaOH+O ↑,影响O 的检验;D装置是为了防止空气中的水蒸
2 2 2 2 2 2 2
气进入C装置与NaO 反应生成氧气,也影响O 的检验,同时吸收过量SO 气体,便于氧气的检验和防止污染
2 2 2 2
空气。(4)通过A操作可以确认有无O 产生。因HNO 具有强氧化性,会把SO 2-氧化为SO 2-,影响实验的
2 3 3 4
测定,故C操作错误,通过B、D操作可以确认反应后固体的成分。因此应进行的操作按顺序排列是A、B、
D。
【答案】(1)2CO+2Na O=2NaCO+O ↑
2 2 2 2 3 2
(2)合理,由于过氧化钠具有强氧化性,能将+4价的硫氧化为+6价的硫而生成硫酸钠。
(3)干燥SO 气体,为防止水蒸气进入C装置与NaO 反应。
2 2 2
为了防止空气中的水蒸气进入C装置与NaO 反应生成氧气,同时吸收过量的SO 气体,便于氧气的检验和防
2 2 2
止污染空气。
(4)ABD
【拓展延伸】NaO 的还原性和强氧化性
2 2
1.遇KMnO 等强氧化剂时,表现出还原性,氧化产物为O
4 2
2.NaO 的强氧化性
2 2
试剂 现象 反应原理并解释
SO 气体 — NaO+SO=NaSO
2 2 2 2 2 4
FeCl 溶液 有红褐色沉淀生成 4NaO+4FeCl +6H O=4Fe(OH)↓+O ↑+8NaCl
2 2 2 2 2 3 2
NaSO 溶
2 3 — NaO+Na SO +H O=NaSO +2NaOH
液 2 2 2 3 2 2 4
氢硫酸 溶液变浑浊 NaO+H S=S↓+2NaOH
2 2 2
酚酞溶液 溶液先变红后褪色 与水反应生成NaOH,NaO 的强氧化性使之褪色
2 2
品红溶液 溶液红色褪去 NaO 的强氧化性使之褪色
2 2
【典例5】(2023·周口模拟)当0.2mol Na 18O 与足量CO 完全反应后,下列说法正确的是( )。
2 2 2
选项生成NaCO 的质量 关于所生成氧气的描述
2 3
A 21.2g 该氧气的摩尔质量是36g·mol-1
B 21.6g 生成的氧气在标准状况下的体积为2.24L
C 21.2g 该氧气的摩尔质量是32g·mol-1
D 22.4g 生成的氧气在标准状况下的体积为2.24L
【解析】选B。NaO 与CO 反应的实质是-1价的氧发生歧化反应,生成物NaCO 中有一个O为18O,摩尔质
2 2 2 2 3
量是108g·mol-1;0.2mol Na 18O 与足量CO 完全反应,生成0.2mol Na C18OO ,质量为108g·mol-1×0.2mol=
2 2 2 2 2
21.6g;生成的氧气为18O,摩尔质量是36g·mol-1,反应生成0.1mol 18O,在标准状况下气体体积为2.24L。
2 2
【拓展延伸】NaO 与CO、HO反应的四个关系
2 2 2 2
1.气体体积的关系
无论是CO 或HO(g)的单一气体还是二者的混合物,通过足量的NaO 时,CO 或HO(g)与放出O
2 2 2 2 2 2 2
的物质的量之比均为2∶1,气体体积的减少量是原来气体体积的 ,等于生成氧气的体积,即ΔV=V(O)=
2
V(混合)。
2.先后顺序关系
由于CO 能够与NaOH反应,所以一定量的NaO 与一定量的HO(g)和CO 的混合物反应,可视为
2 2 2 2 2
NaO 先与CO 反应,剩余的NaO 再与HO(g)反应。
2 2 2 2 2 2
3.转移电子关系
当NaO 与CO、HO反应时,物质的量的关系为2NaO~O~2e-,n(e-)=n(NaO)=2n(O)。
2 2 2 2 2 2 2 2 2 2
4.固体质量关系
(1)基本规律:CO、水蒸气分别与足量NaO 反应时,固体相当于吸收了CO 中的“CO”、水蒸气中的
2 2 2 2
资料收集整理【淘宝店铺:向阳百分百】“H”,所以固体增加的质量Δm(CO)=28g·mol-1×n(CO),Δm(HO)=2g·mol-1×n(HO)。
2 2 2 2 2
(2)特殊应用:凡分子组成符合(CO) ·(H) 的物质,m g该物质在O 中完全燃烧,将其产物[CO 和
m 2 n 2 2
HO(g)]通入足量NaO 后,固体增重必为m g。或者是由C、H、O三种元素组成的物质,只要C、O原子
2 2 2
个数比为1∶1,即可满足上述关系。
无机化合物 H、CO及H 和CO的混合气体
2 2
CHOH(甲醇)、HCHO(甲醛)、CHCOOH(乙
3 3
有机化合物 酸)、
HCOOCH (甲酸甲酯)、C H O(葡萄糖)等
3 6 12 6
1.(2023·河南新乡高三调研)下列有关NaO 的说法不正确的是( )。
2 2
A.向包有NaO 粉末的脱脂棉上滴加几滴水,脱脂棉剧烈燃烧起来,说明NaO 与HO反应放热且有氧气
2 2 2 2 2
生成
B.NaO 与CO 反应时有单质O 生成,该反应属于置换反应
2 2 2 2
C.NaO 在空气中久置变白,涉及的氧化还原反应中,NaO 既是氧化剂,又是还原剂
2 2 2 2
D.NaO 粉末加入Ca(HCO ) 溶液中,会产生气体和浑浊
2 2 3 2
【解析】选B。A项,燃烧的条件是达到着火点和具有助燃物质;B项,反应物中没有单质参加反应,不符合
置换反应的定义;C项,NaO 与CO、HO的反应都是NaO 自身的氧化还原反应;D项,NaO 先和水反应生
2 2 2 2 2 2 2 2
成O 和NaOH,NaOH再与Ca(HCO ) 反应产生沉淀CaCO 。
2 3 2 3
2.(2023·浙江宁波一模)过氧化钠具有强氧化性,遇木炭、铝粉等还原性物质时可燃烧。下列有关说法不正
确的是( )。
A.NaO 与CO 反应时,NaO 是氧化剂,CO 是还原剂
2 2 2 2 2 2
B.熔融过氧化钠时不可使用石英坩埚
C.过氧化钠与木炭、铝粉反应时,过氧化钠均表现出强氧化性
D.过氧化钠与二氧化硫反应时可生成硫酸钠
【解析】选A。NaO 与HO、CO 反应时,都是NaO 自身发生歧化反应,A项错误;石英的主要成分是
2 2 2 2 2 2
SiO ,而NaO 能与SiO 反应生成NaSiO ,故熔融过氧化钠时不可使用石英坩埚,B项正确;NaO 具有强氧
2 2 2 2 2 3 2 2
化性,而C、Al、SO 均具有还原性,故NaO 可与C、Al、SO 发生氧化还原反应,可将C氧化成CO ,将Al
2 2 2 2 2
氧化成Al O,将SO 氧化成SO 2-,C、D项均正确。
2 3 2 4
3.将下列四组物质Wg分别在O 中充分燃烧后,再通过装有足量NaO 的干燥管,干燥管增重的质量大于Wg
2 2 2
的是( )。
A.C HO B.C H O C.C HO D.H 和CO的混合气体
4 8 2 6 12 6 2 4 3 2
【解析】选A。CO 与足量的NaO 反应后固体增重的质量相当于等物质的量的CO的质量,水蒸气与足量的
2 2 2
NaO 反应后固体增重的质量相当于等物质的量的H 的质量。将各物质的化学式变形和增重的质量如下表:
2 2 2
化学式 变形式(Wg) 增重形式(mg) 增重关系
C HO 4H·2CO·2C 4H·2CO·2CO m>W
4 8 2 2 2
C H O 6H·6CO 6H·6CO m=W
6 12 6 2 2
C HO 2H·2CO·O 2H·2CO m<W
2 4 3 2 2
H 和
2 xH·yCO xH·yCO m=W
CO 2 2
考法 3 碳酸钠与碳酸氢钠
1.物理性质
名称 碳酸钠 碳酸氢钠
化学式 NaCO NaHCO
2 3 3
俗名 纯碱或苏打 小苏打
颜色、状态 白色粉末 细小白色晶体
水溶性 易溶于水 水中易溶,但比NaCO 的溶解度小
2 3
2.化学性质
(1)NaCO
2 3
写出上述序号所表示反应的化学方程式
①Na CO +2HCl = 2NaCl+H O+CO ↑
2 3 2 2
②Na CO +Ca ( OH ) = CaCO ↓ +2NaOH
2 3 2 3
资料收集整理【淘宝店铺:向阳百分百】