文档内容
考点 18 元素周期律与元素周期表
1.3年真题考点分布
年 考点分布
卷区
份 元素周期表的结构 元素的性质 元素周期律 综合应用
重庆 √ √
湖北 √ √
浙江 √ √ √
202
江苏 √ √
3
湖南 √ √
辽宁 √ √
全国 √
辽宁 √
天津 √ √
重庆 √
202
福建 √
2
河北 √
江苏 √
广东 √
重庆 √
202 江苏 √
1 湖北 √ √
山东 √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于该专题主要考查:
1.元素周期表的结构
2.电离能和电负性的变化规律
3.元素周期律与元素推断
【备考策略】能从宏观和微观相结合的视角分析原子结构与元素性质的关系,认识元素周期表的结构和原子结
构的关系,了解元素的位置(周期和族);能基于实验现象和事实对物质的组成、结构及其变化分析得出元素周
期律,根据同类元素的性质相似性和递变性理解元素周期律;了解电离能、电负性的概念,并能用以说明元素
的某些性质。
【命题预测】元素周期律与元素周期表是高考每年必考的内容,考查内容主要是元素的推断、元素周期表和元
素周期律的应用、物质结构、元素重要单质及其化合物的主要性质,主要的考查方向为非金属性或金属性强弱、
原子半径大小比较、气态氢化物稳定性强弱、最高价氧化物的水化物的酸性或碱性强弱、元素的电离能及应用、
元素的电负性及应用,常见题型为选择题和填空题,本部分考查内容的规律性强,命题空间广阔,考查方式会
向多方位、多层次发展。考法 1 元素周期表的结构
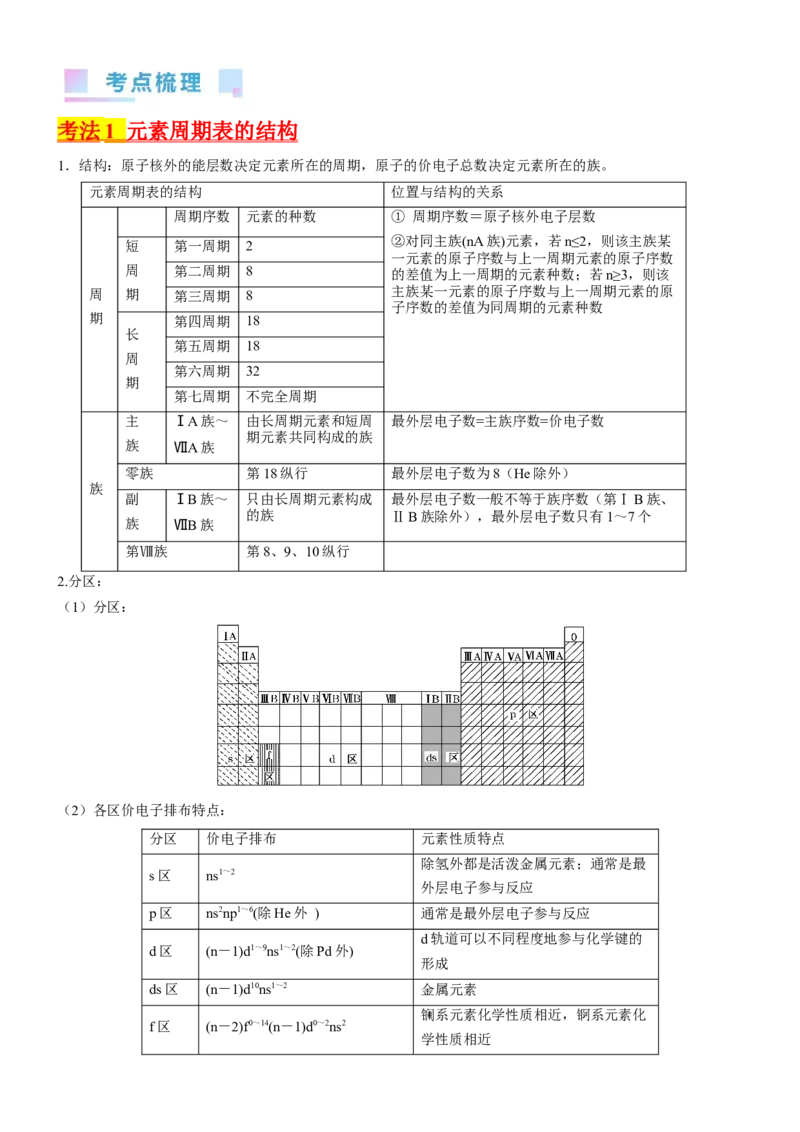
1.结构:原子核外的能层数决定元素所在的周期,原子的价电子总数决定元素所在的族。
元素周期表的结构 位置与结构的关系
周期序数 元素的种数 ① 周期序数=原子核外电子层数
②对同主族(nA族)元素,若n≤2,则该主族某
短 第一周期 2
一元素的原子序数与上一周期元素的原子序数
周 第二周期 8 的差值为上一周期的元素种数;若n≥3,则该
周 期 第三周期 8 主族某一元素的原子序数与上一周期元素的原
子序数的差值为同周期的元素种数
期 第四周期 18
长
第五周期 18
周
第六周期 32
期
第七周期 不完全周期
主 ⅠA族~ 由长周期元素和短周 最外层电子数=主族序数=价电子数
期元素共同构成的族
族 ⅦA族
零族 第18纵行 最外层电子数为8(He除外)
族
副 ⅠB族~ 只由长周期元素构成 最外层电子数一般不等于族序数(第ⅠB族、
的族 ⅡB族除外),最外层电子数只有1~7个
族 ⅦB族
第Ⅷ族 第8、9、10纵行
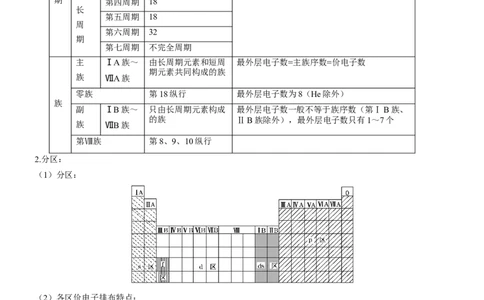
2.分区:
(1)分区:
(2)各区价电子排布特点:
分区 价电子排布 元素性质特点
除氢外都是活泼金属元素;通常是最
s区 ns1~2
外层电子参与反应
p区 ns2np1~6(除He外 ) 通常是最外层电子参与反应
d轨道可以不同程度地参与化学键的
d区 (n-1)d1~9ns1~2(除Pd外)
形成
ds区 (n-1)d10ns1~2 金属元素
镧系元素化学性质相近,锕系元素化
f区 (n-2)f0~14(n-1)d0~2ns2
学性质相近3.规律:
最外层电子数为1的元素有主族(IA族)、副族(IB、VIII族部分等);最外
层电子数为2的元素有主族(IIA族)、副族(IIB、IIIB、IVB、VIIB族)、0
族(He)、VIII族( Fe、 Co等);最外层电子数在3—7之间的元素一定是
26 27
最外层电子数规律 主族元素;最外层电子数为8的元素:0族(He除外)
元素种类最多的是第IIIB族(32种);同周期第IIA族与第IIIA族元素的原
子序数之差有以下三种情况:第2、3周期(短周期)相差1,第4、5周期相
差11,第6、7周期相差25;设n为周期序数,每一周期排布元素的数目为:
数目规律 奇数周期为 (n+1)2/2,偶数周期为(n+2)2/2
分界线规律
位于金属与非金属之间的分界线,右上方的元素为非金属(周期表中的颜色为
深绿色),在此可以找到制造农药的元素(如Cl、P等),左下角为金属元素
(H除外),分界线两边的元素一般既有金属性,又有非金属性;能与酸和碱
反应(如Be、Al等),还可找到制造半导体材料的元素(如Si、Ge等)
对角线规律 金属与非金属分界线对角(左上角与右下角)的两主族元素性质相似,主要表
现在第2、3周期(如Li和Mg、Be和Al、B和Si)
4.应用:预测元素的性质;按周期表的位置在一定区域内寻找新物质(农药、半导体、催化剂等)。
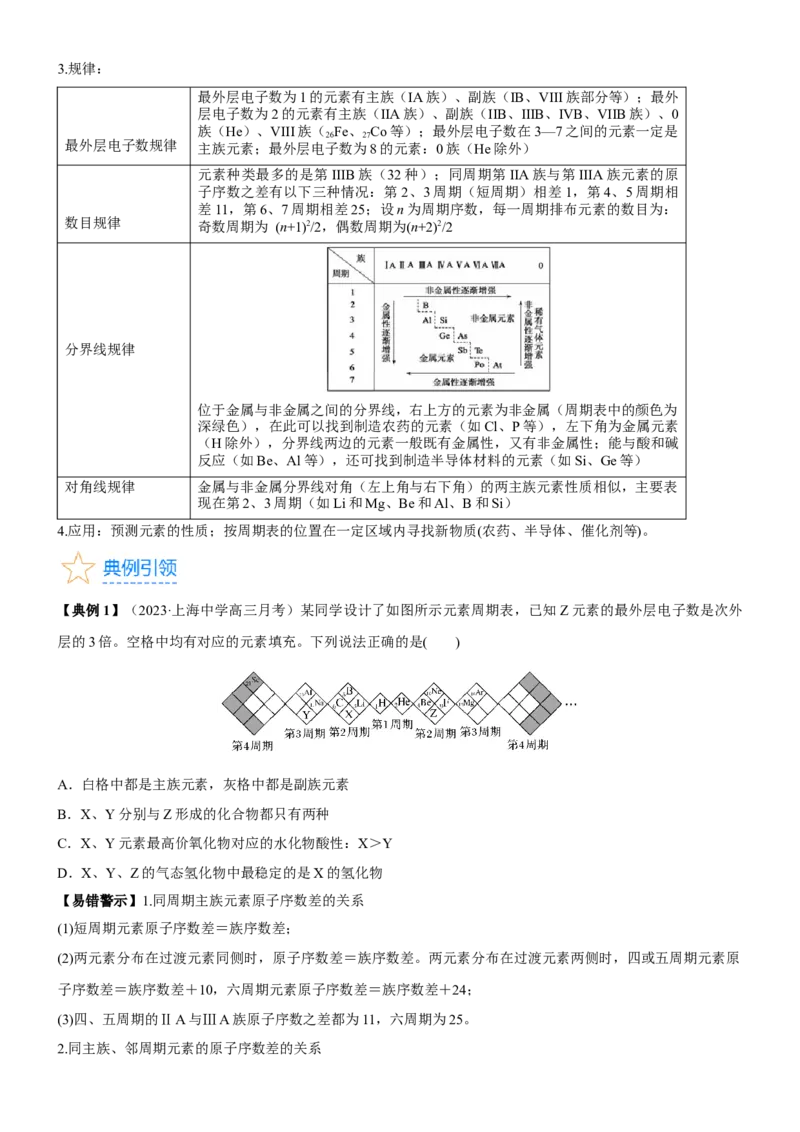
【典例1】(2023·上海中学高三月考)某同学设计了如图所示元素周期表,已知Z元素的最外层电子数是次外
层的3倍。空格中均有对应的元素填充。下列说法正确的是( )
A.白格中都是主族元素,灰格中都是副族元素
B.X、Y分别与Z形成的化合物都只有两种
C.X、Y元素最高价氧化物对应的水化物酸性:X>Y
D.X、Y、Z的气态氢化物中最稳定的是X的氢化物
【易错警示】1.同周期主族元素原子序数差的关系
(1)短周期元素原子序数差=族序数差;
(2)两元素分布在过渡元素同侧时,原子序数差=族序数差。两元素分布在过渡元素两侧时,四或五周期元素原
子序数差=族序数差+10,六周期元素原子序数差=族序数差+24;
(3)四、五周期的ⅡA与ⅢA族原子序数之差都为11,六周期为25。
2.同主族、邻周期元素的原子序数差的关系(1)ⅠA族元素,随电子层数的增加,原子序数依次相差2、8、8、18、18、32;
(2)ⅡA族和0族元素,随电子层数的增加,原子序数依次相差8、8、18、18、32;
(3)ⅢA~ⅦA族元素,随电子层数的增加,原子序数依次相差8、18、18、32。
【典例2】(2023·中山一中高三月考)元素周期表短周期的一部分如表所示。下列有关A、B、C、D、E五种
元素的叙述中,正确的是( )
A.D在过量的B中燃烧的主要产物为DB
3
B.C的氢化物的水溶液酸性比E的强
C.A与B形成的阴离子可能有AB、AB
2
D.E单质中由于形成了氢键,所以很容易液化
1.(2023·浙江·校联考模拟预测)硫酸四氨合铜 可用于织物媒染剂、消毒剂,下列关于硫酸四
氨合铜的说不法确的是
A.硫酸四氨合铜难溶于乙醇 B.Cu元素位于周期表的ds区
C.硫酸四氨合铜中的铜离子为 杂化 D.N-H键电子云轮廓图:
2.(2023·湖北武汉·华中师大一附中校考模拟预测)已知前四周期元素X、Y、Q、R、Z和W在周期表中的位
置如图所示,其中Z位于ds区,基态W原子的价电子中在不同形状的原子轨道中运动的电子数相等。下列说
法正确的是
X Y
Q R
Z W
A.最高正化合价:X=Q<Y=R
B.基态Z原子的价电子排布为3d104s1
C.X和Q的第一电离能都高于同周期相邻元素
D.R最高价氧化物的水化物不能与其最低价氢化物反应
3.(2023·河北沧州·沧县中学校考模拟预测)Y、Z、W、X、M为原子序数依次增大的五种短周期元素,其在
元素周期表中的位置如表所示,Z或M元素的气态氢化物和其气态氧化物可反应生成该元素的单质和水,W元
素是生物体中含量最多的元素。下列说法错误的是Y Z W
X M
A.简单离子半径:M>Z>W
B.含有气态 的体系为无色
C.通过电解熔融的X的常见氧化物可制备X单质
D.最高价氧化物对应的水化物的酸性:M>Y
考法 2 元素的性质
1.电离能:气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量叫做第一电离能(用I 表
1
示)。+1价正离子再失去一个电子所需能量称为第二电离能,依次类推。电离能的大小取决于原子的有效核电荷、
原子半径以及原子的电子层结构。
(1)电离能的变化规律
碱金属元素的第一电离能最小,稀有气体元素的第一电离能最大,从左到
同周期
右,元素的第一电离能在总体上呈现由小到大的趋势
同主族 从上到下第一电离能逐渐减小
同种元素 同一种元素的逐级电离能的大小关系:I”或“<”填空:
第一电离能 离子半径 熔点 酸性
Si____S O2-____Na+ NaCl____Si HSO ____ HClO
2 4 4
Ⅱ.下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
(3)h 的 单 质 在 空 气 中 燃 烧 发 出 耀 眼 的 白 光 , 请 用 原 子 结 构 的 知 识 解 释 发 光 的 原 因 :
________________________________________________________________________。
(4)o、p两元素的部分电离能数据列于下表:
元素 o p
I 717 759
1
电离能/
I 1 509 1 561
2
(kJ·mol-1)
I 3 248 2 957
3
比较两元素的 I 、I 可知,气态 o2+再失去一个电子比气态 p2+再失去一个电子难。对此,你的解释是
2 3
__________________________________________。
(5)已知稀有气体熔、沸点均为同周期的最低者,第三周期8种元素按单质熔点由低到高的顺序排列如图甲所示,
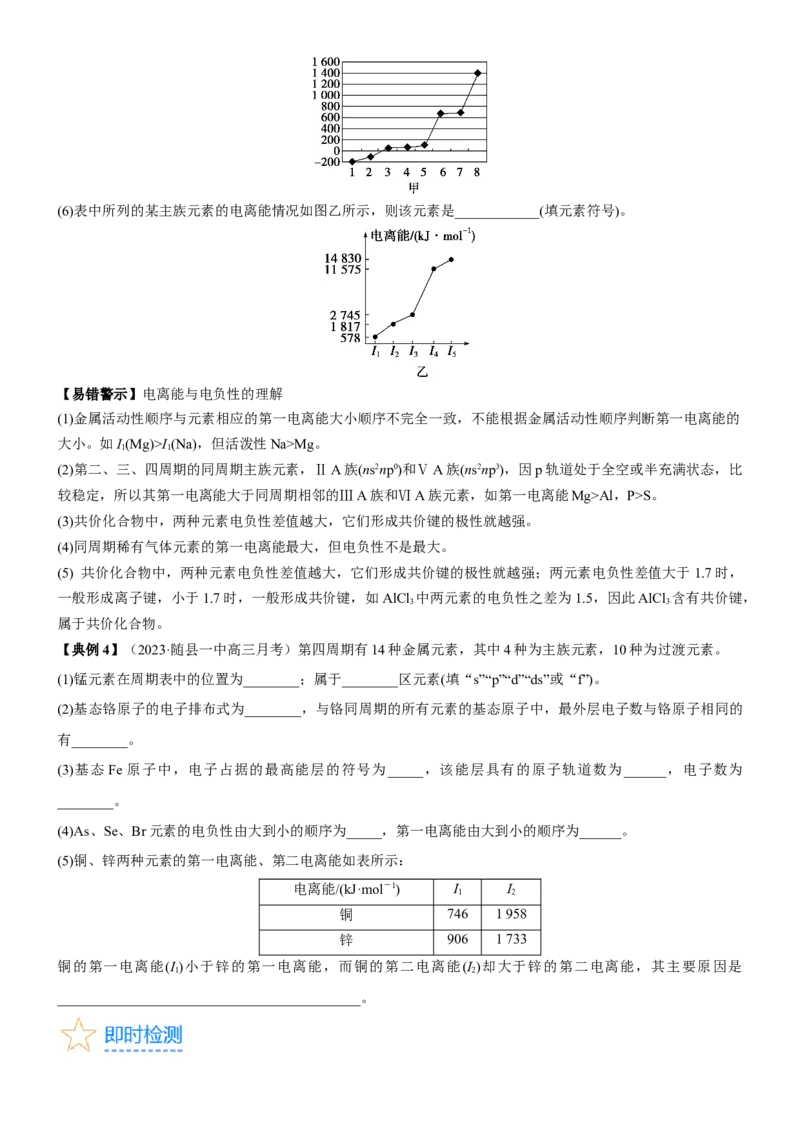
其中电负性最大的是________(填图中的序号)。(6)表中所列的某主族元素的电离能情况如图乙所示,则该元素是____________(填元素符号)。
【易错警示】电离能与电负性的理解
(1)金属活动性顺序与元素相应的第一电离能大小顺序不完全一致,不能根据金属活动性顺序判断第一电离能的
大小。如I(Mg)>I(Na),但活泼性Na>Mg。
1 1
(2)第二、三、四周期的同周期主族元素,ⅡA族(ns2np0)和ⅤA族(ns2np3),因p轨道处于全空或半充满状态,比
较稳定,所以其第一电离能大于同周期相邻的ⅢA族和ⅥA族元素,如第一电离能Mg>Al,P>S。
(3)共价化合物中,两种元素电负性差值越大,它们形成共价键的极性就越强。
(4)同周期稀有气体元素的第一电离能最大,但电负性不是最大。
(5) 共价化合物中,两种元素电负性差值越大,它们形成共价键的极性就越强;两元素电负性差值大于1.7时,
一般形成离子键,小于1.7时,一般形成共价键,如AlCl 中两元素的电负性之差为1.5,因此AlCl 含有共价键,
3 3
属于共价化合物。
【典例4】(2023·随县一中高三月考)第四周期有14种金属元素,其中4种为主族元素,10种为过渡元素。
(1)锰元素在周期表中的位置为________;属于________区元素(填“s”“p”“d”“ds”或“f”)。
(2)基态铬原子的电子排布式为________,与铬同周期的所有元素的基态原子中,最外层电子数与铬原子相同的
有________。
(3)基态 Fe 原子中,电子占据的最高能层的符号为_____,该能层具有的原子轨道数为______,电子数为
________。
(4)As、Se、Br元素的电负性由大到小的顺序为_____,第一电离能由大到小的顺序为______。
(5)铜、锌两种元素的第一电离能、第二电离能如表所示:
电离能/(kJ·mol-1) I I
1 2
铜 746 1 958
锌 906 1 733
铜的第一电离能(I)小于锌的第一电离能,而铜的第二电离能(I)却大于锌的第二电离能,其主要原因是
1 2
___________________________________________。1.(2023·河北唐山·统考模拟预测)中科院发现深海处的含硫物质在微生物作用下会发生如下图所示变化(已略
去部分不含硫物质)。有关转化过程的说法错误的是
A.第一电离能由弱到强的顺序是:CX B.离子半径:Z>Y
C.W与X可组成多种共价化合物 D.简单氢化物的键角:X>Y
3.(2023·福建泉州·福建省永春第一中学校考模拟预测)我国科学家制备的NiO/Al O/Pt催化剂能实现氨硼烷
2 3
(H NBH )高效制备氢气的目的,制氢原理:HNBH +4CH OH NH B(OCH )+3H ↑。请回答下列问
3 3 3 3 3 4 3 4 2
题:
(1)基态氮原子的价电子排布式为 。
(2)硼烷又称硼氢化合物,随着硼原子数的增加,硼烷由气态经液态至固态,其原因为 。
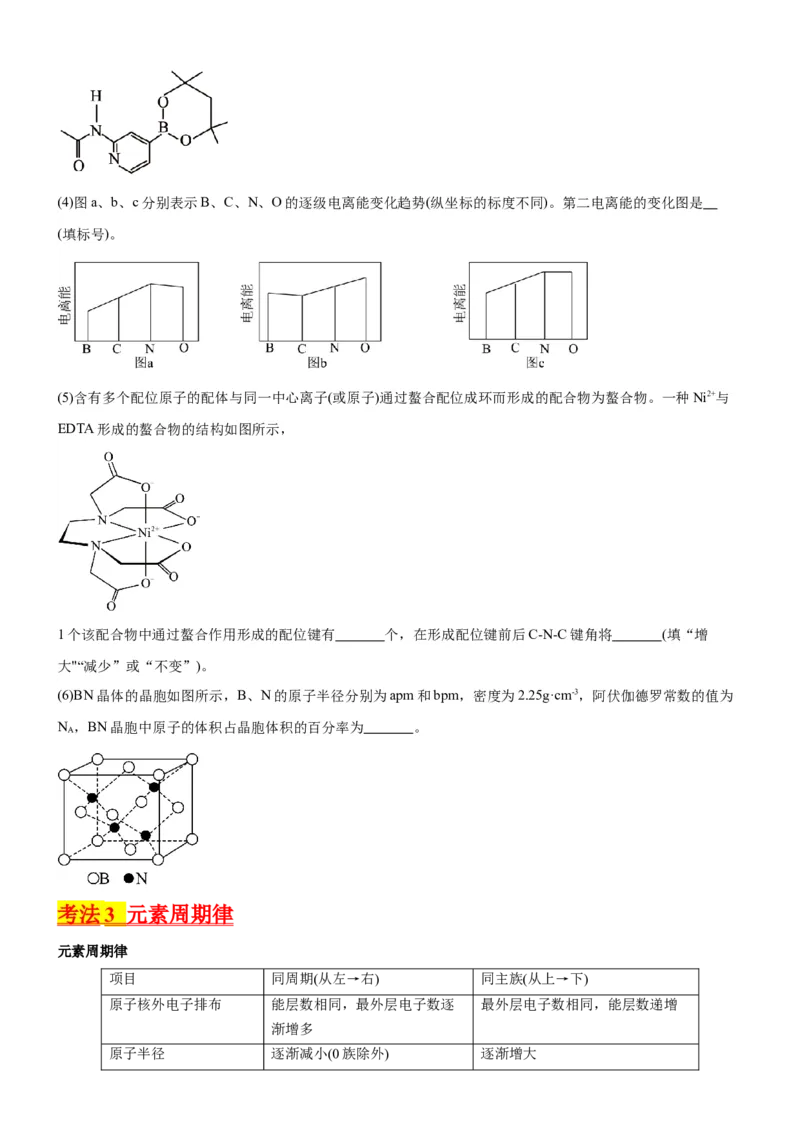
(3)某有机硼化合物的结构简式如图所示,其中氮原子的杂化轨道类型为 。(4)图a、b、c分别表示B、C、N、O的逐级电离能变化趋势(纵坐标的标度不同)。第二电离能的变化图是
(填标号)。
(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Ni2+与
EDTA形成的螯合物的结构如图所示,
1个该配合物中通过螯合作用形成的配位键有 个,在形成配位键前后C-N-C键角将 (填“增
大"“减少”或“不变”)。
(6)BN晶体的晶胞如图所示,B、N的原子半径分别为apm和bpm,密度为2.25g·cm-3,阿伏伽德罗常数的值为
N ,BN晶胞中原子的体积占晶胞体积的百分率为 。
A
考法 3 元素周期律
元素周期律
项目 同周期(从左→右) 同主族(从上→下)
原子核外电子排布 能层数相同,最外层电子数逐 最外层电子数相同,能层数递增
渐增多
原子半径 逐渐减小(0族除外) 逐渐增大元素主要化合价 最高正价由+1→+7(O,F除 最高正价=主族序数(O,F除
外),最低负价由-4→-1 外),非金属最低负价=主族序数
-8
原子得、失电子能力 得电子能力逐渐增强; 得电子能力逐渐减弱;
失电子能力逐渐减弱 失电子能力逐渐增强
第一电离能 增大的趋势 逐渐减小
电负性 逐渐增大 逐渐减小
元素金属性、非金属性 金属性逐渐减弱;非金属性逐 金属性逐渐增强;非金属性逐渐
渐增强 减弱
(1)在周期表中,元素的化学性质遵循以下递变规律:同周期元素,从左到右,金属性依次减弱,非金属性依
次增强。同主族元素,从上到下,金属性依次增强,非金属性依次减弱。金属性越强,单质的还原性越强,对
应离子的氧化性越弱,单质与水或酸反应越剧烈,越容易置换出氢,最高价氧化物的水化物的碱性越强,热稳
定性越强;非金属性越强,单质的氧化性越强,对应离子的还原性越弱,单质与氢气反应越剧烈,氢化物越稳
定,最高价氧化物的水化物的酸性越强。
(2)微粒半径大小比较中的规律
同周期 随原子序数递增,原子半径减小。如:r(Na)>r( Mg)>r(Al)>r(Si)>r(P)
M
>r(S)>r(Cl)
随原子序数递增,原子或离子半径减小。如:r(Li)<r(Na)<r(k)<r(Rb)<r
(Cs),r(Li+)<r(Na+)<r(k+)<r(Rb+)<r(Cs+),r(F—)<r(Cl—)<r(Br
同主族
—)<r(I—)
同电子层 核电荷数越大,离子半径越小。如:r(O2—)>r(F—)>r(Na+)>r(Mg2+)>r
(Al3+)
同元素 阴离子大于原子,原子大于阳离子,低价阳离子大于高价阳离子。如:r(Cl-)>r(Cl),r
(Fe)>r(Fe2+)>r(Fe3+)
(3)元素金属性(非金属性)相对强弱的判断规律
元素的性质 本质 判断的一般依据
元素的原子失电子的 与水或酸(非氧化性)反应置换出氢的难易
能力(与失电子的数
最高价氧化物对应水化物的碱性强弱
目无关),原子越容
易失去电子,元素金 水溶液中单质间的置换反应
元素金属性
属性越强;反之则
弱。
原电池中的正负极(Mg—Al---NaOH溶液例外)
阳离子在电解池中阴极上的放电顺序
元素的原子得电子的 与氢气化合的难易
能力(与得电子的数
气态氢化物的稳定性
目无关),原子越容
易得到电子,元素非 最高价氧化物对应水化物的酸性强弱
元素的非金属性
金属性越强;反之则
水溶液中单质间的置换反应(单质作氧化剂)
弱。
阴离子的还原性
【典例5】一种用作锂电池电解液的锂盐结构如图所示。其中,X位于第三周期,X原子的电子数为Z原子的两
倍,W、Z、Y位于同一周期。下列叙述正确的是( )A.原子半径:X>Z>W
B.非金属性:X>Z>W
C.Y的氢化物可用于刻蚀玻璃
D.X的氧化物对应的水化物均为强酸
【典例6】X、Y、Z、W为原子序数递增的四种短周期元素,其中Z为金属元素,W的单质为常见的半导体材
料,X、W为同一主族元素。X、Z、W分别与Y形成的最高价化合物为甲、乙、丙。结合如图转化关系,下列
判断正确的是( )
A.X的氢化物沸点低于Y的氢化物沸点
B.W的单质可以用作计算机芯片,太阳能电池,丙是玛瑙的主要成分
C.甲、丙、丁均为酸性化合物
D.工业上用X的单质和乙来制取Z单质
1.(2023·全国·校联考一模)X、Y、Z、W、Q为原子序数依次增大的短周期主族元素,已知X、Q为同主族
元素且这两种元素能组成离子化合物;Y元素的气态氢化物水溶液显碱性。下列说法正确的是
A.简单离子半径:
B. 分子的空间结构为平面三角形
C.X分别与Y、Z、W组成的常见化合物均为极性分子
D.由Y、Z、Q组成的化合物的水溶液一定显中性
2.(2023·河北唐山·统考模拟预测)我国科学家在寻找“点击反应”的砌块过程中,发现一种新的化合物,结
构如下图所示,其中X、Y、Z和W是原子序数依次增大的短周期主族元素,Y与Z是同一主族元素。下列说
法正确的是
A.简单离子半径:W>Z>Y>XB.X、Y、Z和W形成的简单氢化物中,X沸点最高
C.X、Z、W氧化物的水化物均为强酸
D.X+采用的是sp杂化方式成键
3.(2023·四川绵阳·统考模拟预测)短周期主族元素X、Y、Z、W的原子序数依次增大,Z、W同周期,且W
原子的半径在同周期中最小,由这些元素组成的常见化合物(部分含有氢元素)之间能发生如图转化,其中G是
生活中应用广泛的一种金属单质,A、C分别为X、Y的氢化物。下列说法正确的是
A.简单离子半径:r(X)AsH
3 3
2.(2023·江苏连云港·连云港高中校考模拟预测)黑火药爆炸时发生反应 。
下列说法正确的是
A.半径大小: B.熔点:
C.电离能大小: D.电负性大小:
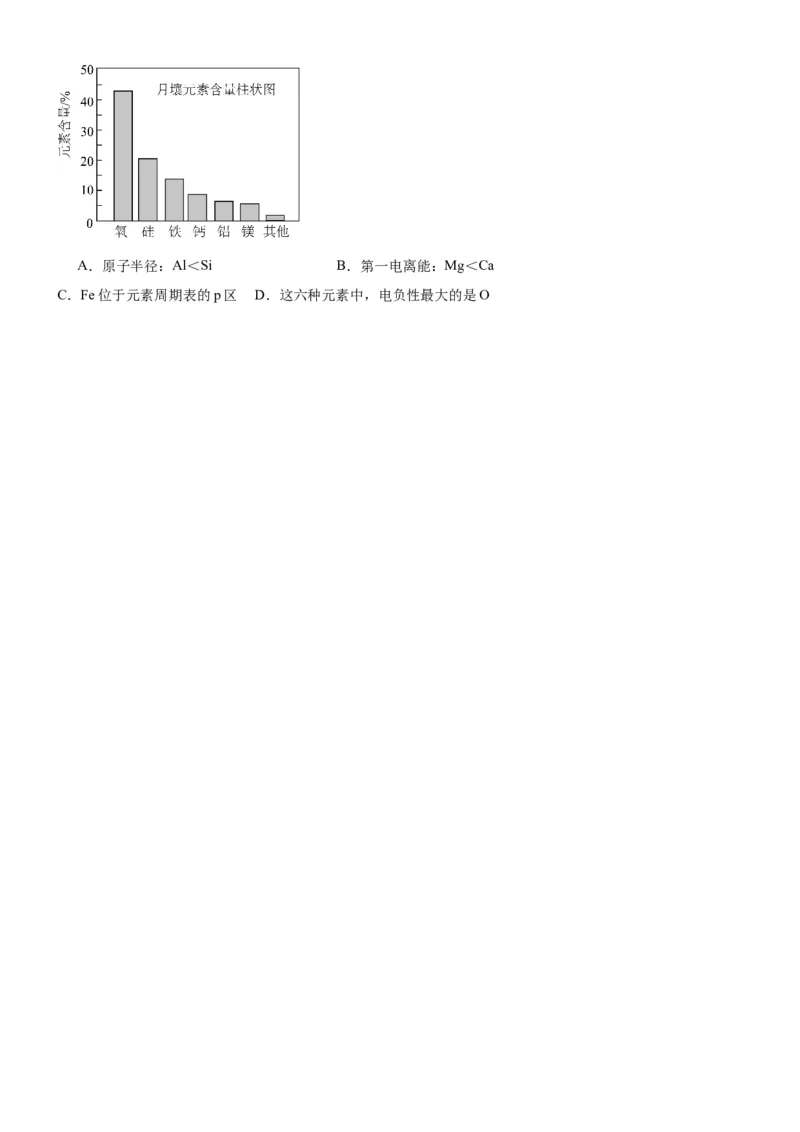
3.(2023·重庆渝中·重庆巴蜀中学校考模拟预测)荣昌陶器为中国四大名陶,其主要成分为O、Si、Al、Fe,
还含有少量Ca、Ti等元素。对于上述有关元素,下列说法正确的是
A.基态Fe原子的价层电子轨道表示式为
B.基态Ca原子最高能级的轨道形状为哑铃形
C.Ti最稳定的化合价为 价
D.第一电离能:O>Si>Al4.(2023·河北衡水·衡水市第二中学校考三模)X、Y、Z、J、Q是原子序数依次增大,且分布在三个短周期的
主族元素,Y元素原子的核外未成对电子数在同周期中最多,Y、Z同周期,Z、J同主族.下列说法错误的是
A.电负性:Q>J;第一电离能:Y>Z B.最高价含氧酸的酸性:Q>J
C. 、 的中心原子杂化方式相同 D.简单离子半径:Y>Z、J>Q
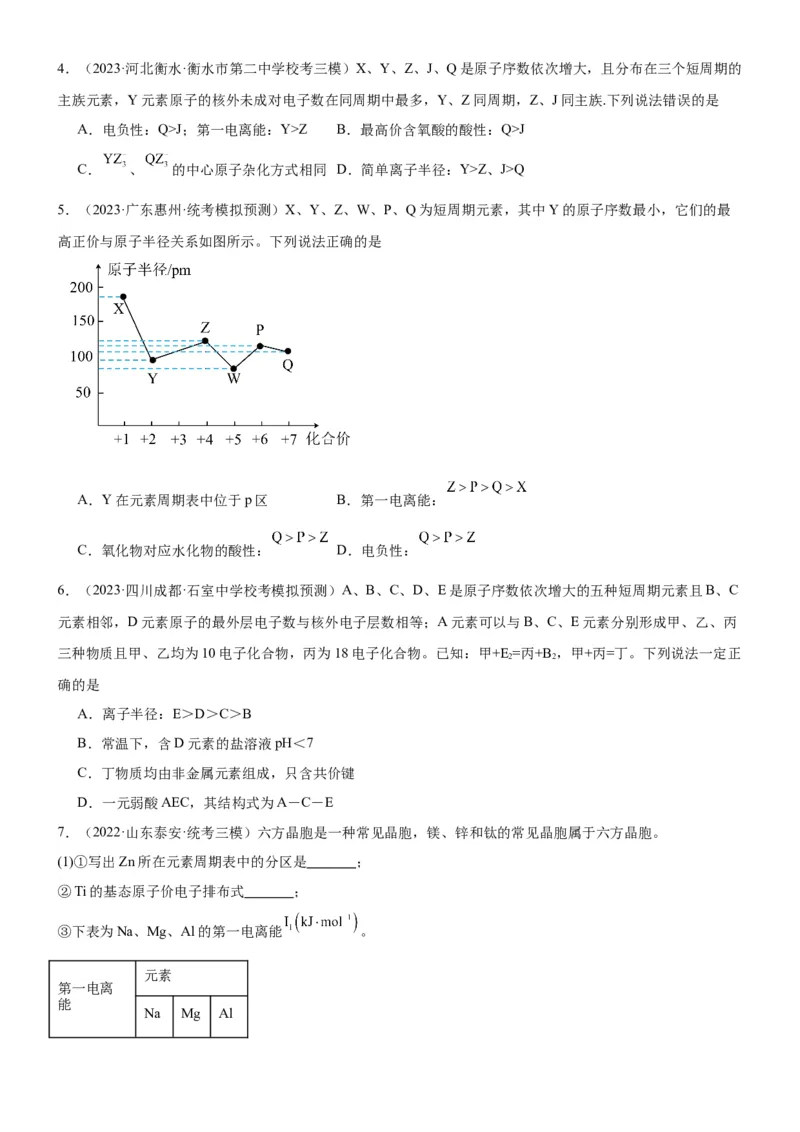
5.(2023·广东惠州·统考模拟预测)X、Y、Z、W、P、Q为短周期元素,其中Y的原子序数最小,它们的最
高正价与原子半径关系如图所示。下列说法正确的是
A.Y在元素周期表中位于p区 B.第一电离能:
C.氧化物对应水化物的酸性: D.电负性:
6.(2023·四川成都·石室中学校考模拟预测)A、B、C、D、E是原子序数依次增大的五种短周期元素且B、C
元素相邻,D元素原子的最外层电子数与核外电子层数相等;A元素可以与B、C、E元素分别形成甲、乙、丙
三种物质且甲、乙均为10电子化合物,丙为18电子化合物。已知:甲+E=丙+B ,甲+丙=丁。下列说法一定正
2 2
确的是
A.离子半径:E>D>C>B
B.常温下,含D元素的盐溶液pH<7
C.丁物质均由非金属元素组成,只含共价键
D.一元弱酸AEC,其结构式为A-C-E
7.(2022·山东泰安·统考三模)六方晶胞是一种常见晶胞,镁、锌和钛的常见晶胞属于六方晶胞。
(1)①写出Zn所在元素周期表中的分区是 ;
②Ti的基态原子价电子排布式 ;
③下表为Na、Mg、Al的第一电离能 。
元素
第一电离
能
Na Mg Al496 738 577
请解释其变化规律的原因 。
(2)已知以上三种金属的盐的熔沸点(℃)如下表:
氯化物
物理性质
熔点 712 290 -24.1
沸点 1412 732 136.4
已知: 熔融状态下能够导电。请解释三种氯化物熔沸点差异的原因 。 的熔沸点明显偏低的
另一个原因是该分子空间构型是 ,分子高度对称,没有极性,分子间作用力很弱。
(3)某晶体属于六方晶系,其晶胞参数 , 。晶胞沿着不同方向投影如下,其中深色小球
代表A原子,浅色大球代表B原子(化学环境完全等同)。已知A2原子坐标为 ,B1原子
沿c方向原子坐标参数 。
①该物质的化学式为 。
②晶胞中原子A1—A2在ab面投影的距离为 (保留四位有效数字)。
③B1原子坐标参数为 。
8.(2023·天津·校联考一模)近日,我国研究人员利用硫氰酸甲基铵{[CH NH ]+[SCN]-}气相辅助生长技术,成
3 3
功制得稳定的钙钛矿型甲脒铅碘(FAPbI )。请回答下列问题:
3
(1)基态S原子的价电子排布图为 。
(2)甲脒(FA)的结构简式为
①其组成元素的电负性由小到大的排序为 ,其中碳原子的杂化方式为 。
②甲脒比丙烷的熔点更高的原因是 。
(3)FAPbI 的晶体结构单元如图所示,图中Y表示Pb,位于八面体中心,则甲脒的碘配位数为 。
3【能力提升】
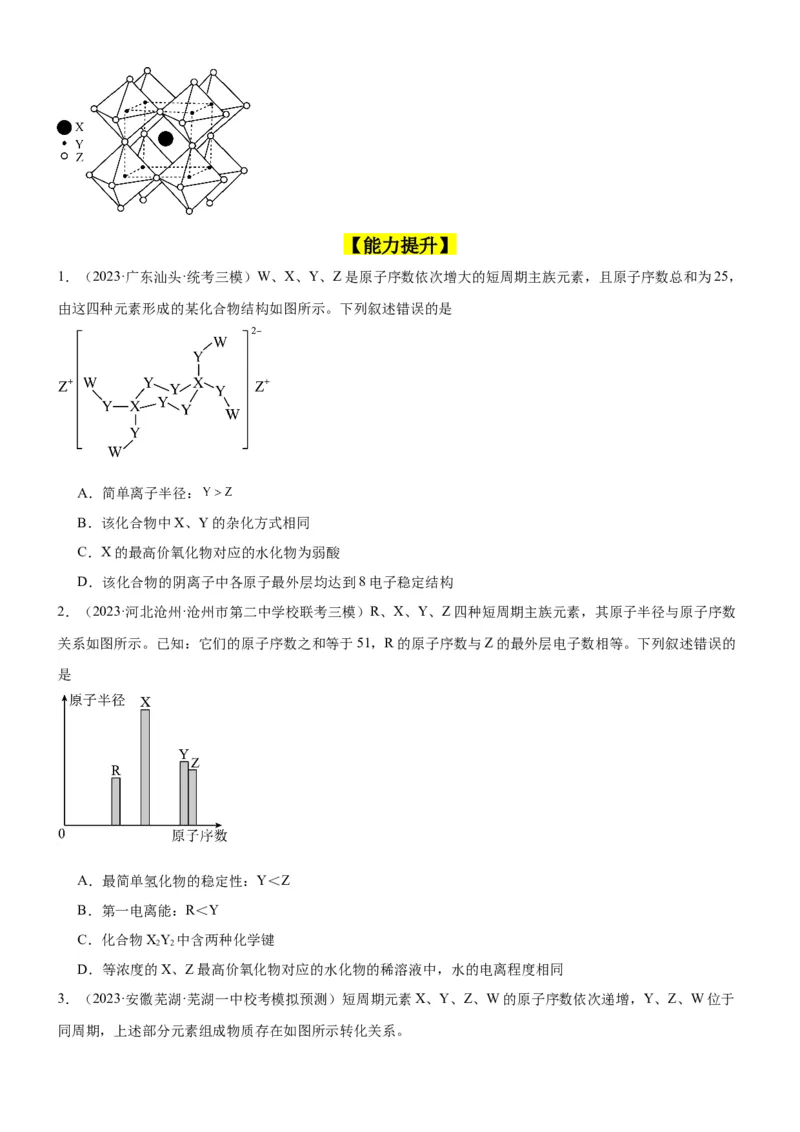
1.(2023·广东汕头·统考三模)W、X、Y、Z是原子序数依次增大的短周期主族元素,且原子序数总和为25,
由这四种元素形成的某化合物结构如图所示。下列叙述错误的是
A.简单离子半径:
B.该化合物中X、Y的杂化方式相同
C.X的最高价氧化物对应的水化物为弱酸
D.该化合物的阴离子中各原子最外层均达到8电子稳定结构
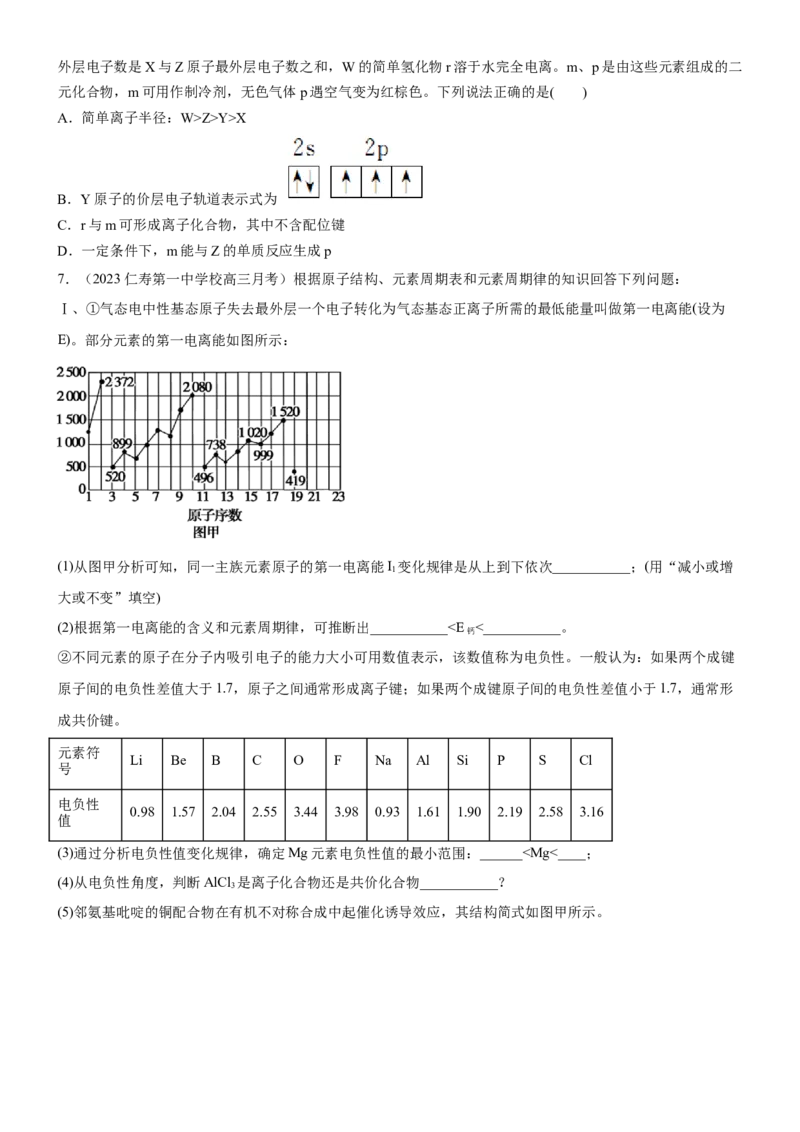
2.(2023·河北沧州·沧州市第二中学校联考三模)R、X、Y、Z四种短周期主族元素,其原子半径与原子序数
关系如图所示。已知:它们的原子序数之和等于51,R的原子序数与Z的最外层电子数相等。下列叙述错误的
是
A.最简单氢化物的稳定性:Y<Z
B.第一电离能:R<Y
C.化合物XY 中含两种化学键
2 2
D.等浓度的X、Z最高价氧化物对应的水化物的稀溶液中,水的电离程度相同
3.(2023·安徽芜湖·芜湖一中校考模拟预测)短周期元素X、Y、Z、W的原子序数依次递增,Y、Z、W位于
同周期,上述部分元素组成物质存在如图所示转化关系。下列说法错误的是
A.第一电离能: Z>W> Y
B.简单氢化物的沸点: W>Z
C.键角: XW>ZX
2 3
D.转化关系中Y原子的杂化方式有sp、sp2、sp3
4.(2023·河北邢台·邢台市第二中学校联考三模)近年来,光催化剂的研究是材料领域的热点。一种Ru配合
物(如图所示)复合光催化剂可将 转化为HCOOH。下列说法错误的是
A.Ru配合物中第二周期元素的电负性:O>N>C
B.吡啶( ,原子在同一平面)中C、N原子的杂化方式分别为 、
C.该配合物中Ru的配位数是6
D. 中P的价层电子对数为4,空间结构为正四面体形
5.(2023·潍坊一中高三月考)短周期元素a、b、c、d的原子序数依次增大,在下列转化关系中,甲、乙、丙、
丁、戊为上述四种元素组成的二元或三元化合物。其中A为d元素组成的单质,常温下乙为液体,丁物质常用
于消毒、漂白。下列说法错误的是( )
A.简单离子半径:c>b
B.丙中既有离子键又有极性共价键
C.b、c形成的化合物中阴、阳离子数目之比为1∶2
D.a、b、d形成的化合物adb 中,d的杂化方式是sp3
4
6.(2023·江苏·南京外国语学校高三阶段练习)短周期元素X、Y、Z、W的原子序数依次增大。W原子的最外层电子数是X与Z原子最外层电子数之和,W的简单氢化物r溶于水完全电离。m、p是由这些元素组成的二
元化合物,m可用作制冷剂,无色气体p遇空气变为红棕色。下列说法正确的是( )
A.简单离子半径:W>Z>Y>X
B.Y原子的价层电子轨道表示式为
C.r与m可形成离子化合物,其中不含配位键
D.一定条件下,m能与Z的单质反应生成p
7.(2023仁寿第一中学校高三月考)根据原子结构、元素周期表和元素周期律的知识回答下列问题:
Ⅰ、①气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫做第一电离能(设为
E)。部分元素的第一电离能如图所示:
(1)从图甲分析可知,同一主族元素原子的第一电离能I 变化规律是从上到下依次___________;(用“减小或增
1
大或不变”填空)
(2)根据第一电离能的含义和元素周期律,可推断出___________3d>3p>3s B.6s>5p>4d>3d C.5f>4d>3p>2s D.7d>6d>5d>4d
Ⅱ、元素周期表前四周期A、B、C、D、E五种元素,A元素的原子最外层电子排布式为ns1;B元素的原子价
电子排布式为ns2np2;C元素位于第二周期且原子中p能级与s能级电子总数相等;D元素原子的M能层的p能
级中有3个未成对电子;E元素原子有5个未成对电子。
(1)写出元素名称:E___________。
(2)C基态原子的电子排布图为___________。
(3)当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是:___________。
(4)若A元素的原子最外层电子排布式为2s1,B元素的原子价电子排布式为3s23p2,A、B、C、D四种元素的第
一电离能由大到小的顺序是___________(用元素符号表示)。
(5)E元素原子的电子排布简写式是___________,在元素周期表中的位置是___________。
8.(2023定兴第三中学高三月考)有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。
其中A为非金属元素;A和E属同一族,它们的原子最外层电子排布为ns1,B和D也属同一族,它们的原子最
外层的p能级电子数均是s能级电子数的两倍。C原子最外层电子数等于D原子最外层电子数的一半。请回答
下列问题:
(1)C是_______,D是_______,E是_______。
(2)由这五种元素组成的一种化合物是_______(写化学式)。写出该物质的一种主要用途:_______。
(3)写出C元素基态原子的电子排布式:_______。
(4)用电子排布图表示D元素原子的价电子排布为_______。
(5)元素B与D的电负性的大小关系是B_______D,C与E的第一电离能的大小关系是C_______E(填“>”“<”或
“=”)。
【真题感知】
1.(2023·广东·统考高考真题)化合物 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,
E在地壳中含量最多。下列说法正确的是
A.元素电负性: B.氢化物沸点:
C.第一电离能: D. 和 的空间结构均为三角锥形
2.(2023·浙江·统考高考真题)X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与Z位于同一
周期,且只有X、 Y元素相邻。X基态原子核外有2个未成对电子,W原子在同周期中原子半径最大。下列说
法不正确的是
A.第一电离能:
B.电负性:
C.Z、W原子形成稀有气体电子构型的简单离子的半径:
D. 与水反应生成产物之一是非极性分子
3.(2023·湖南·统考高考真题)日光灯中用到的某种荧光粉的主要成分为3W(ZX)·WY。已知:X、Y、Z和
3 4 2 2
W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,
基态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是
A.电负性:X>Y>Z>W
B.原子半径:X