文档内容
考点 18 原电池 化学电源
(核心考点精讲精练)
一、3年真题考点分布
考点内容 考题统计
2023广东卷6题,2分;2023山东卷11题,4分;2022全国甲卷12
原电池原理综合应用 题,6分;2022山东卷13题,4分;2021广东卷9题,2分;2021山
东卷10题,2分;
2023辽宁卷11题,3分;2023全国甲卷10题,6分;2022辽宁卷14
题,3分;2022福建卷9题,4分;2021河北卷9题,3分;2021辽
新型二次电池
宁卷10题,3分;2021浙江1月选考22题,2分;2021浙江6月选
考22题,2分;2021湖南卷10题,3分;
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,一般从原电池工作原理的应用、二次电池和多池串联等角度考向进行考查。
考查点主要集中:一是电极反应式或总方程式的正误判断;二是粒子或粒子的移动方向判断;三是工作过
程中及工作后电解质、电极质量的变化的判断;四是隔膜的类型及作用;五是定量计算,已知转移电子的
物质的量求产物或反应物的物质的量,或者已知产物或反应物的物质的量的变化求转移电子的物质的量。
【备考策略】
(1)回归教材,以教材为重点,而不是一味地机械刷题。不论多么复杂陌生的情境,多么复杂新颖的装
置,都离不开教材中原电池的模型。
(2)重视常考点的备考,如电极名称的判断、电极反应式或总反应式的书写或正误判断、电子或粒子
移动方向判断、电解质溶液变化的判断、离子交换膜的使用和相关定量计算等。
(3)重视近几年高考试题的探究,通过做高考真题感知高考考查要求,查找对知识掌握和能力要求上的
不足,在此基础上探究高考命题动向,有针对性地提高解题能力。
【命题预测】
电化学的考查注重联系实际生活,关注电化学在生活、生产方面具体应用,很好地将实际问题与理论
知识联系起来,培养学生的科学精神和社会责任感素养。 关注燃料电池和新型高能电池(如高铁电池、锂
电池)充电或放电的过程;关注电极反应式或总反应式中出现“x”等代数形式。
资料收集整理【淘宝店铺:向阳百分百】考法 1 原电池的工作原理
1.概念和反应本质
原电池是把化学能转化为电能的装置,其反应本质是氧化还原反应。
2.构成条件
(1)一看反应:看是否有能自发进行的氧化还原反应发生(一般是活泼性强的金属与电解质溶液反应)。
(2)二看两电极:一般是活泼性不同的两电极。
(3)三看是否形成闭合回路,形成闭合回路需三个条件:①电解质溶液;②两电极直接或间接接触;③
两电极插入电解质溶液中。
3.工作原理
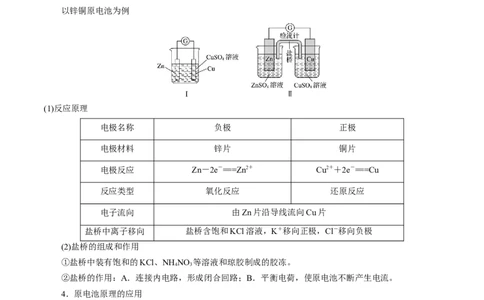
以锌铜原电池为例
(1)反应原理
电极名称 负极 正极
电极材料 锌片 铜片
电极反应 Zn-2e-===Zn2+ Cu2++2e-===Cu
反应类型 氧化反应 还原反应
电子流向 由Zn片沿导线流向Cu片
盐桥中离子移向 盐桥含饱和KCl溶液,K+移向正极,Cl-移向负极
(2)盐桥的组成和作用
①盐桥中装有饱和的KCl、NH NO 等溶液和琼胶制成的胶冻。
4 3
②盐桥的作用:A.连接内电路,形成闭合回路;B.平衡电荷,使原电池不断产生电流。
4.原电池原理的应用
(1)比较金属的活动性强弱:原电池中,负极一般是活动性较强的金属,正极一般是活动性较弱的金属
(或非金属)。
(2)加快化学反应速率:氧化还原反应形成原电池时,反应速率加快。
(3)用于金属的防护:将需要保护的金属制品作原电池的正极而受到保护。
(4)设计制作化学电源
①首先将氧化还原反应分成两个半反应。
②根据原电池的工作原理,结合两个半反应,选择正、负电极材料以及电解质溶液。
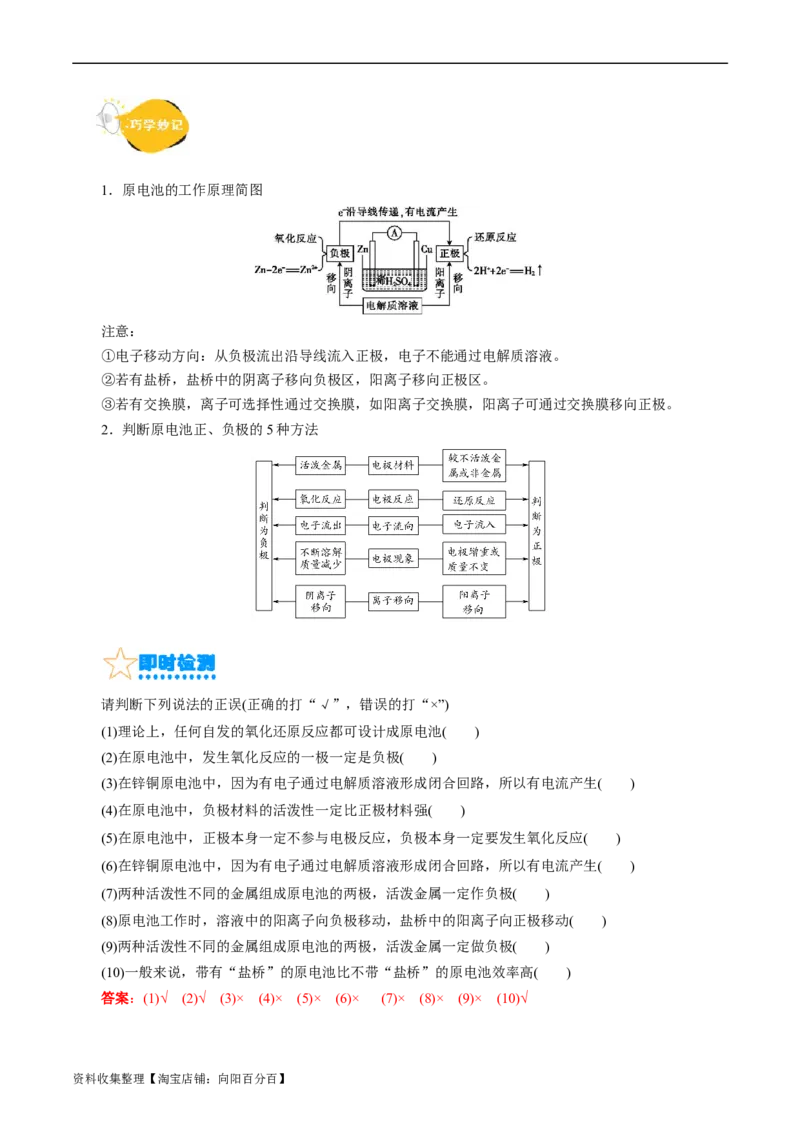
资料收集整理【淘宝店铺:向阳百分百】1.原电池的工作原理简图
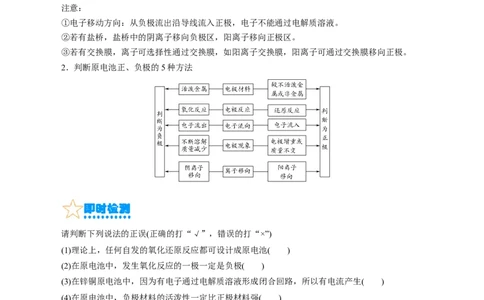
注意:
①电子移动方向:从负极流出沿导线流入正极,电子不能通过电解质溶液。
②若有盐桥,盐桥中的阴离子移向负极区,阳离子移向正极区。
③若有交换膜,离子可选择性通过交换膜,如阳离子交换膜,阳离子可通过交换膜移向正极。
2.判断原电池正、负极的5种方法
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)理论上,任何自发的氧化还原反应都可设计成原电池( )
(2)在原电池中,发生氧化反应的一极一定是负极( )
(3)在锌铜原电池中,因为有电子通过电解质溶液形成闭合回路,所以有电流产生( )
(4)在原电池中,负极材料的活泼性一定比正极材料强( )
(5)在原电池中,正极本身一定不参与电极反应,负极本身一定要发生氧化反应( )
(6)在锌铜原电池中,因为有电子通过电解质溶液形成闭合回路,所以有电流产生( )
(7)两种活泼性不同的金属组成原电池的两极,活泼金属一定作负极( )
(8)原电池工作时,溶液中的阳离子向负极移动,盐桥中的阳离子向正极移动( )
(9)两种活泼性不同的金属组成原电池的两极,活泼金属一定做负极( )
(10)一般来说,带有“盐桥”的原电池比不带“盐桥”的原电池效率高( )
答案:(1)√ (2)√ (3)× (4)× (5)× (6)× (7)× (8)× (9)× (10)√
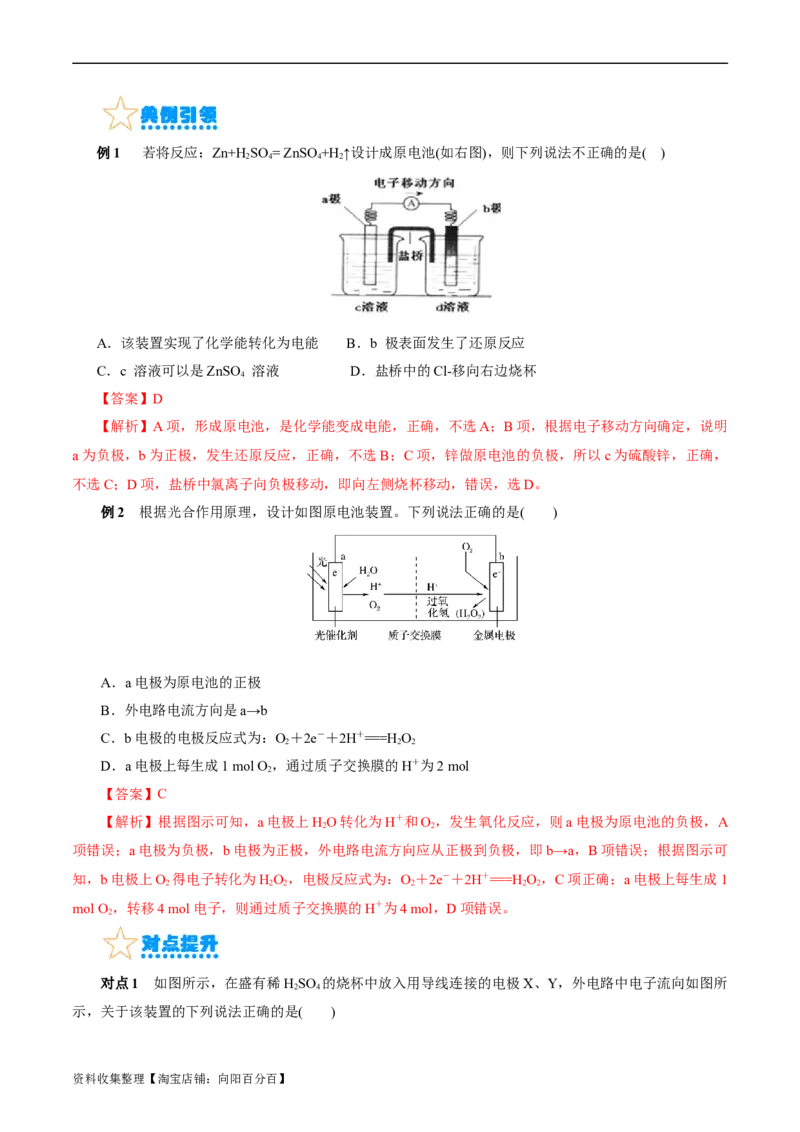
资料收集整理【淘宝店铺:向阳百分百】例1 若将反应:Zn+H SO = ZnSO+H ↑设计成原电池(如右图),则下列说法不正确的是( )
2 4 4 2
A.该装置实现了化学能转化为电能 B.b 极表面发生了还原反应
C.c 溶液可以是ZnSO 溶液 D.盐桥中的Cl-移向右边烧杯
4
【答案】D
【解析】A项,形成原电池,是化学能变成电能,正确,不选A;B项,根据电子移动方向确定,说明
a为负极,b为正极,发生还原反应,正确,不选B;C项,锌做原电池的负极,所以c为硫酸锌,正确,
不选C;D项,盐桥中氯离子向负极移动,即向左侧烧杯移动,错误,选D。
例2 根据光合作用原理,设计如图原电池装置。下列说法正确的是( )
A.a电极为原电池的正极
B.外电路电流方向是a→b
C.b电极的电极反应式为:O+2e-+2H+===H O
2 2 2
D.a电极上每生成1 mol O ,通过质子交换膜的H+为2 mol
2
【答案】C
【解析】根据图示可知,a电极上HO转化为H+和O ,发生氧化反应,则a电极为原电池的负极,A
2 2
项错误;a电极为负极,b电极为正极,外电路电流方向应从正极到负极,即b→a,B项错误;根据图示可
知,b电极上O 得电子转化为HO,电极反应式为:O+2e-+2H+===H O,C项正确;a电极上每生成1
2 2 2 2 2 2
mol O,转移4 mol电子,则通过质子交换膜的H+为4 mol,D项错误。
2
对点1 如图所示,在盛有稀HSO 的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所
2 4
示,关于该装置的下列说法正确的是( )
资料收集整理【淘宝店铺:向阳百分百】A.外电路的电流方向为:X→外电路→Y
B.若两电极分别为Fe和碳棒,则X为碳棒,Y为Fe
C.X极上发生的是还原反应,Y极上发生的是氧化反应
D.若两电极都是金属,则它们的活动性顺序为X>Y
【答案】D
【解析】外电路的电子流向为X→外电路→Y,电流方向与其相反,A项错误;若两电极分别为Fe和
碳棒,则Y为碳棒,X为Fe,B项错误;X极失电子,作负极,Y极上发生的是还原反应,X极上发生的
是氧化反应,C项错误;电解质溶液为稀硫酸,两金属作电极,谁活泼谁作负极,D项正确。
对点2 与甲、乙两套装置有关的下列说法正确的是( )
A.甲、乙装置中,锌棒均作负极,发生氧化反应
B.甲中锌棒直接与稀HSO 接触,故甲生成气泡的速率更快
2 4
C.甲、乙装置的电解质溶液中,阳离子均向碳棒定向迁移
D.乙中盐桥设计的优点是迅速平衡电荷,提高电池效率
【答案】D
【解析】A项,根据上述分析,甲不是原电池,故A错误;B项,甲中锌棒直接与稀HSO 接触,发
2 4
生化学腐蚀,乙中构成了原电池,负极失去电子的速率加快,因此正极放出氢气的速率增大,故B错误;
C项,甲不是原电池,电解质溶液中的阳离子向锌移动,故C错误;D项,盐桥中离子的定向迁移构成了
电流通路,盐桥既可沟通两方溶液,又能阻止反应物的直接接触,迅速平衡电荷,使由它连接的两溶液保
持电中性,提高电池效率,故D正确。
考法 2 化学电源
1.一次电池:只能使用一次,不能充电复原继续使用
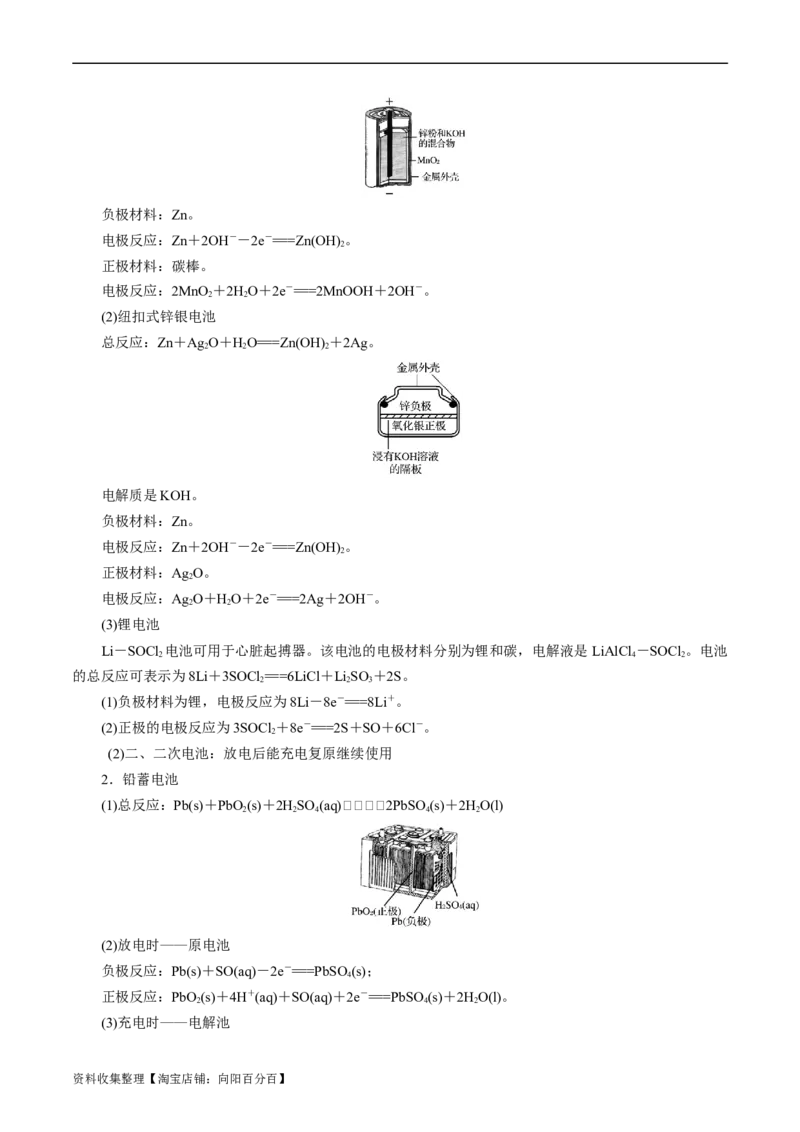
(1)碱性锌锰干电池
总反应:Zn+2MnO +2HO===2MnOOH+Zn(OH) 。
2 2 2
资料收集整理【淘宝店铺:向阳百分百】负极材料:Zn。
电极反应:Zn+2OH--2e-===Zn(OH) 。
2
正极材料:碳棒。
电极反应:2MnO +2HO+2e-===2MnOOH+2OH-。
2 2
(2)纽扣式锌银电池
总反应:Zn+Ag O+HO===Zn(OH) +2Ag。
2 2 2
电解质是KOH。
负极材料:Zn。
电极反应:Zn+2OH--2e-===Zn(OH) 。
2
正极材料:Ag O。
2
电极反应:Ag O+HO+2e-===2Ag+2OH-。
2 2
(3)锂电池
Li-SOCl 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl -SOCl 。电池
2 4 2
的总反应可表示为8Li+3SOCl ===6LiCl+LiSO +2S。
2 2 3
(1)负极材料为锂,电极反应为8Li-8e-===8Li+。
(2)正极的电极反应为3SOCl +8e-===2S+SO+6Cl-。
2
(2)二、二次电池:放电后能充电复原继续使用
2.铅蓄电池
(1)总反应:Pb(s)+PbO (s)+2HSO (aq)2PbSO (s)+2HO(l)
2 2 4 4 2
(2)放电时——原电池
负极反应:Pb(s)+SO(aq)-2e-===PbSO(s);
4
正极反应:PbO (s)+4H+(aq)+SO(aq)+2e-===PbSO(s)+2HO(l)。
2 4 2
(3)充电时——电解池
资料收集整理【淘宝店铺:向阳百分百】阴极反应:PbSO (s)+2e-===Pb(s)+SO(aq);
4
阳极反应:PbSO (s)+2HO(l)-2e-===PbO(s)+4H+(aq)+SO(aq)。
4 2 2
(4)图解二次电池的充放电
3.二次电池的充放电规律
(1)充电时电极的连接:充电的目的是使电池恢复其供电能力,因此负极应与电源的负极相连以获得电
子,可简记为负接负后做阴极,正接正后做阳极。
(2)工作时的电极反应式:同一电极上的电极反应式,在充电与放电时,形式上恰好是相反的;同一电
极周围的溶液,充电与放电时pH的变化趋势也恰好相反。
4.“高效、环境友好”的燃料电池
氢氧燃料电池是目前最成熟的燃料电池,可分为酸性和碱性两种。
种类 酸性 碱性
负极反应式 2H-4e-===4H+ 2H+4OH--4e-===4H O
2 2 2
正极反应式 O+4e-+4H+===2H O O+2HO+4e-===4OH-
2 2 2 2
电池总反应式 2H+O===2H O
2 2 2
备注 燃料电池的电极不参与反应,有很强的催化活性,起导电作用
燃料电池电极反应式的书写(以氢氧燃料电池为例)
(1)注意介质环境
(2)掌握书写程序
资料收集整理【淘宝店铺:向阳百分百】请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)最早使用的化学电池是锌锰电池( )
(2)在干电池中,碳棒只起导电作用,并不参加化学反应( )
(3)干电池根据电池内的电解质分为酸性电池和碱性电池( )
(4)干电池中碳棒为正极( )
(5)铅蓄电池是可充电电池( )
(6)铅蓄电池中的PbO 为负极( )
2
(7)太阳能电池不属于原电池( )
(8)手机、电脑中使用的锂电池属于一次电池( )
(9)铅蓄电池放电时,正极与负极质量均增加( )
(10)燃料电池是一种高效、环保的新型化学电源( )
(11)燃料电池工作时燃料在电池中燃烧,然后热能转化为电能( )
(12)以葡萄糖为燃料的微生物燃料电池,放电过程中,H+从正极区向负极区迁移( )
(13)二次电池的充、放电为可逆反应( )
(14)碱性锌锰干电池是一次电池,其中MnO 是催化剂,可使锌锰干电池的比能量高、可储存时间长(
2
)
(15)铅蓄电池工作过程中,每通过2 mol电子,负极质量减轻207 g( )
(16)镍镉电池不能随意丢弃的主要原因是镍、镉的资源有限,价格昂贵( )
答案:(1)√ (2)√ (3)√ (4)√ (5)√ (6)× (7)√ (8)× (9)√ (10)√ (11)× (12)× (13)× (14)×
(15)× (16)×
资料收集整理【淘宝店铺:向阳百分百】