文档内容
考点 18 原电池 化学电源
【基础过关】
1.下列选项描述的过程能实现化学能转化为电能的是( )
A. 电池充电 B.光合作用 C.手机电池工作 D.太阳能板充电
【答案】C
【解析】A项,电池充电,是将电能转化为化学能,故A错误;B项,光合作用是太阳能转变化为化
学能,故B错误;C项,手机电池工作是化学能转化为电能,故C正确;D项,太阳能板充电是光能转化
为电能,并向蓄电池充电,将电能转化为化学能储存起来,故D错误。
2.(2023·浙江省诸暨市高三适应性考试)可充放电锂硫电池与传统锂电池相比,在能量密度、工作温
度、电压稳定方面都有一定的优势。一种锂硫电池正极材料为被碳材料包装起来的硫单质,放电时Li与S
8
化合成LiS固体,下列说法不正确的是( )
2
A.负极失电子,发生氧化反应
B.充电时,Li+向碳材料电极移动
C.正极的电极反应:S+16Li++16 e-=8Li S
8 2
D.该电池通常不选择水系电解液
【答案】B
【解析】可充放电锂硫电池放电时,Li为负极,Li失去电子被氧化,正极材料为被碳材料包装起来的
硫单质,硫单质得到电子被还原,充电时为电解池,阴极上锂离子得电子被还原,阳极上LiS失去电子被
2
氧化。A项, 放电时为原电池,负极失电子,发生氧化反应,A正确;B项,充电时为电解池,Li+向阴极
Li移动,放电时为原电池,Li+向碳材料电极移动,B不正确;C项,放电时正极发生还原反应,结合题干
信息可知,电极反应:S+16Li++16 e-=8Li S,C正确;D项,Li能与水反应,则该电池通常不选择水系电
8 2
解液,D正确;故选B。
3.(2023·辽宁省锦州市高三统考)我国科学家设计的“海泥电池”,既可用于深海水下仪器的电源补
给,又有利于海洋环境污染治理,其中微生物代谢产物显酸性,电池工作原理如图所示。下列说法错误的
是( )
资料收集整理【淘宝店铺:向阳百分百】A.A电极的电势高于B电极
B.质子从海底沉积层通过交接面向海水层移动
C.负极的电极反应式为CHO-4e-+H O=CO+4H+
2 2 2
D.海水和海泥作为电解质的一部分,富含盐分,导电性高,有利于输出电能
【答案】C
【解析】由图可知,A极物质由氧气转化为水,化合价降低,所以 A极是正极,B极是负极。A项,
A极是正极,B极是负极,正极的电势高于负极电势,所以A电极的电势高于B电极,故A正确;B项,
A极是正极,B极是负极,质子带正电荷,放电时向正极移动,所以质子从海底沉积层通过交接面向海水
层移动,故B正确;C项,CHO在微生物作用下与硫酸根离子反应生成CO 和HS-,并不是在负极的电极
2 2
反应,负极上HS-失去电子发生氧化反应生成硫单质,电极反应式为:HS--2e-=S↓+H+,故C错误;D项,
海水和海泥作为电解质一部分,富含盐分,可增强水的导电性,有利于电池电能的输出,故 D正确;故选
C。
4.一种高达94.2%能效的可充电铝胺电池工作原理如图所示,用Ph表示苯基,三苯基胺(Ph N)失去
3
一个电子后形成的Ph N∙+结构较为稳定。下列说法不正确的是( )
3
A.与锂电池比,铝电池比能量略低,但铝含量丰富价格低廉
B.放电时,负极的电极反应式为Al-3e-+7AlCl -=4AlCl-
4 2 7
资料收集整理【淘宝店铺:向阳百分百】C.充电时,AlCl -向铝电极移动
4
D.理论上每生成1mol Ph N,外电路通过1mol电子
3
【答案】C
【解析】A项,铝电池比能量略低,且含量丰富价格低廉,A项错误;B项,放电时,负极上Al失电
子和AlCl -反应生成Al Cl-,电极反应式为Al-3e-+7AlCl -=4AlCl-,B项正确;C项,充电时Ph N失电子
4 2 7 4 2 7 3
生成Ph N+ , Ph N阳极、Al为阴极,阴离子向阳极移动,所以AlCl -向阳极Ph N移动,C项错误;D项,
3 3 4 3
充电时Ph N失电子生成Ph N+,则生成1个Ph N转移1个电子,所以理论上每生成1molPh N,外电路通
3 3 3 3
过1mol电子,D项正确。故选C。
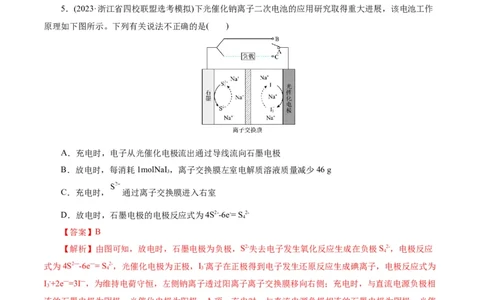
5.(2023·浙江省四校联盟选考模拟)下光催化钠离子二次电池的应用研究取得重大进展,该电池工作
原理如下图所示。下列有关说法不正确的是( )
A.充电时,电子从光催化电极流出通过导线流向石墨电极
B.放电时,每消耗1molNaI ,离子交换膜左室电解质溶液质量减少46 g
3
C.充电时, 通过离子交换膜进入右室
D.放电时,石墨电极的电极反应式为4S2--6e-= S 2-
4
【答案】B
【解析】由图可知,放电时,石墨电极为负极,S2-失去电子发生氧化反应生成在负极S2-,电极反应
4
式为4S2—-6e—= S 2-,光催化电极为正极,I-离子在正极得到电子发生还原反应生成碘离子,电极反应式为
4 3
I-+2e—=3I—,为维持电荷守恒,左侧钠离子透过阳离子离子交换膜移向右侧;充电时,与直流电源负极相
3
连的石墨电极为阴极,光催化电极为阳极。A项,充电时,与直流电源负极相连的石墨电极为阴极,光催
化电极为阳极,则电子从光催化电极流出,通过导线流向石墨电极,故A正确;B项,放电时,石墨电极
为负极,光催化电极为正极,为维持电荷守恒,左侧钠离子透过离子交换膜移向右侧,每消耗1molNaI 时,
3
2mol钠离子从左室迁移到右室,则离子交换膜左室电解质溶液质量减少46g,故B正确;C项,放电时,
为维持电荷守恒,左侧钠离子透过阳离子离子交换膜移向右侧,则充电时,钠离子透过阳离子离子交换膜
移向左侧,故C错误;D项,放电时,石墨电极为负极,S2-失去电子发生氧化反应生成在负极S2-,电极
4
反应式为4S2--6e-= S 2-,故D正确;故选C。
4
6.如图,甲、乙是两个完全相同的光伏并网发电模拟装置,利用它们对煤浆进行脱硫处理。下列叙
资料收集整理【淘宝店铺:向阳百分百】述中错误的是( )
A.光伏并网发电装置中b为正极
B.石墨1电极上消耗1molMn2+,甲、乙中各转移0.5mol电子
C.脱硫反应原理为:15Mn3++FeS +8H O=15Mn2++Fe3++2SO2-+16H+
2 2 4
D.处理60gFeS,石墨2电极上消耗7.5molH+
2
【答案】B
【解析】由图可知,石墨1电极上Mn元素价态升高失电子,故石墨1为阳极,电极反应式为Mn2+-e-
=Mn3+,Mn3+与FeS 反应实现脱硫,反应为15Mn3++FeS +8H O═15Mn2++Fe3++2 SO 2-+16H+,石墨2为阴极,
2 2 2 4
电极反应式为2H++2e-=H ↑。A项,石墨1为阳极极,则b极为电源的正极,A正确;B项,石墨1为阳极,
2
电极反应式为Mn2+-e-=Mn3+,消耗1molMn2+,电路中转移1mol电子,B错误;C项,阳极生成的Mn3+与
FeS 反应实现脱硫,反应为15Mn3++FeS +8H O═15Mn2++Fe3++2 SO 2-+16H+,C正确;D项,处理
2 2 2 4
60gFeS,消耗阳极生成的Mn3+的物质的量为 ×15=7.5mol,转移电子7.5mol,石墨2为阴极,电
2
极反应式为2H++2e-=H ↑,石墨2上消耗7.5molH+,D正确;故选B。
2
7.(2023·浙江省精诚联盟高三三模)内部重整式高温燃料电池具有良好的商业化前景,其基本工作原
理(以CH 为原料,熔融碳酸盐为电解质)如图所示。下列说法正确的是( )
4
资料收集整理【淘宝店铺:向阳百分百】A.b极为正极,发生还原反应
B.电子流向:a极→导线→b极→电解质→a极
C.a极电极反应为CH- 8e- +4CO 2-=5CO +2H O
4 3 2 2
D.该电池所用的隔膜一定属于阳离子交换膜
【答案】A
【解析】由装置可知a电极上CO和H 失电子生成CO 和HO,则a极为负极,b极为正极,b电极上
2 2 2
O 得电子结合CO 生成CO2-,CH 和水反应生成CO和H。A项,由以上分析可知b极为正极,得电子发
2 2 3 4 2
生还原反应,故A正确;B项,电子不经过电解质,故B错误;C项, a极反应物不是甲烷,故C错误;
D项,熔融碳酸盐为电解质,故隔膜允许碳酸根离子通过,为阴离子交换膜,故D错误;故选A。
8.(2023·山东省济南市高三期中)基于硫化学的金属硫电池是有望替代当前锂离子电池技术,满足人
类社会快速增长的能源需求,该电池的结构及原理如图所示。下列有关叙述正确的是( )
A.该电池可采用含K+的水溶液或有机物为电解质溶液
B.放电时,电子的移动方向:电极a→电极b→隔膜→电极a
C.充电时,正极区可能发生的反应有xKS-(2x-6)e-=3S 2-+2xK+
2 3 x
D.充电时,电路中转移 时,负极质量减少78g
【答案】C
【解析】该装置的电化学装置,根据原电池工作原理,K电极为负极,b电极为正极。A项, 该装置
为电化学装置,金属钾作负极,金属钾是活泼金属,能与水发生反应,因此电解质溶液不能是水溶液,故
A错误;B项,放电属于电化学,根据原电池工作原理,电子从负极经外电路流向正极,即电子从电极a→
灯泡→电极b,电池内部没有电子通过,故B错误;C项,充电电池充电时,电池正极接电源正极,电池
负极接电源负极,充电时,电池正极上失去电子,化合价升高,根据装置图可知,正极反应式为xKS-
2 3
(2x-6)e-=3S 2-+2xK+,故C正确;D项,充电时,负极(阴极)反应式为K++e-=K,电路中转移2mole-,生成
x
2molK,负极质量增重2mol×39g/mol=78g,故D错误;故选C。
9.(2023·河北省邯郸市部分学校高三联考)香港城市大学化学工作者首次提出了Al-N 电池(如图),该
2
电池使用N 为原料,以离子液体(Al Cl--AlCl-)为电解质,既实现了能量的存储,又实现了AlN的生产,
2 2 7 4
资料收集整理【淘宝店铺:向阳百分百】和碱反应能产生NH ,可进一步生产氮肥。下列说法错误的是( )
3
A.Al极为负极,发生氧化反应
B.电池总反应为2Al+N =2
2
C.石墨烯电极反应式为8Al Cl-+N +6e- =2AlN+14AlCl-
2 7 2 4
D.生成标准状况下33.6LNH ,电池中转移3mol电子
3
【答案】D
【解析】A项, 根据图中原电池的结构,Al极为负极,Al极电极反应式为2Al+14AlCl--6e-=8AlCl-,
4 2 7
发生氧化反应,故A正确;B项,石墨烯电极为正极,正极反应式为8Al Cl-+N +6e- =2AlN+14AlCl-,Al极
2 7 2 4
电极反应式为2Al+14AlCl--6e-=8AlCl-,所以电池总反应为2Al+N =2AlN,故B正确; C项,石墨烯电极
4 2 7 2
为正极,正极发生还原反应,正极反应式为8Al Cl-+N +6e- =2AlN+14AlCl-,故C正确;D项,标准状况下
2 7 2 4
33.6LNH 的物质的量为1.5mol,AlN和碱反应产生NH 的反应离子方程式为AlN+OH-+H O=AlO-+NH↑,
3 3 2 2 3
生成1.5mol氨气消耗1.5molAlN,根据2Al+N =2AlN,电池中转移了4.5mol电子,故D错误;故选D。
2
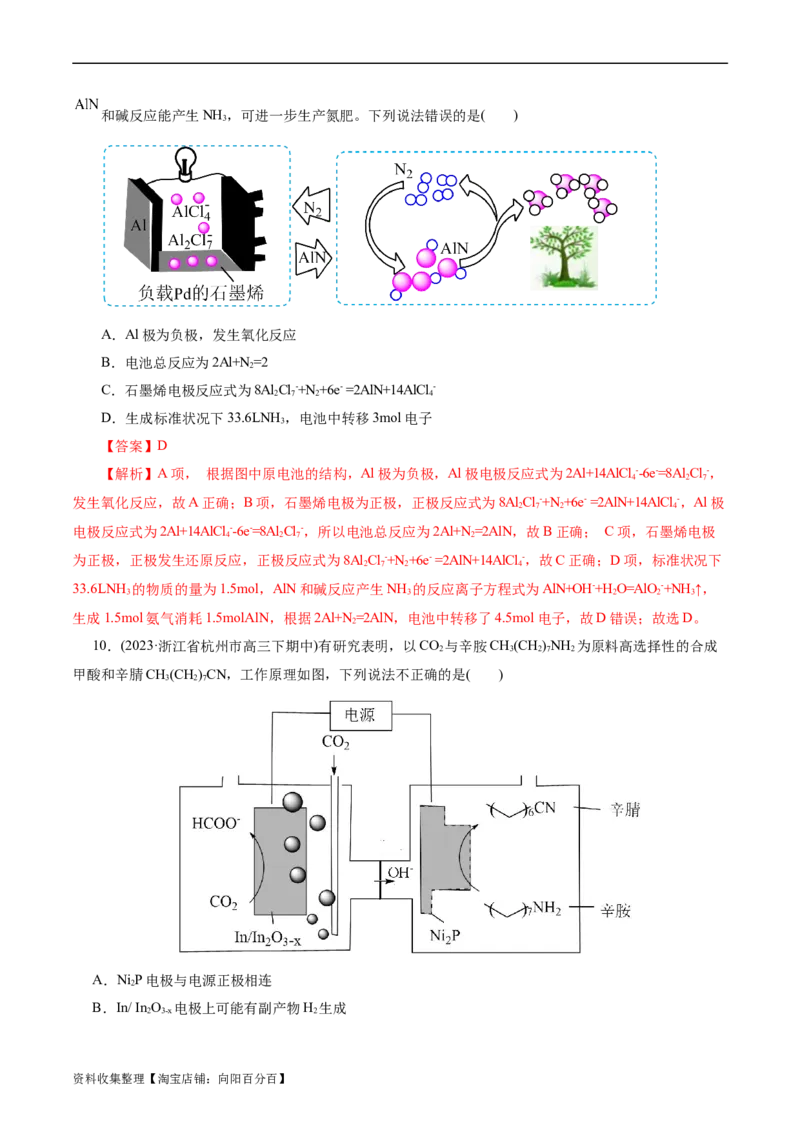
10.(2023·浙江省杭州市高三下期中)有研究表明,以CO 与辛胺CH(CH)NH 为原料高选择性的合成
2 3 2 7 2
甲酸和辛腈CH(CH)CN,工作原理如图,下列说法不正确的是( )
3 2 7
A.NiP电极与电源正极相连
2
B.In/ In O 电极上可能有副产物H 生成
2 3-x 2
资料收集整理【淘宝店铺:向阳百分百】C.在In/ In O 电极上发生的反应为:CO+H O+2e-=HCOO-+OH-
2 3-x 2 2
D.标准状况下33.6LCO 参与反应时NiP电极有1.5mol辛腈生成
2 2
【答案】D
【解析】由图示知,该装置为电解池,In/ In O 电极发生反应CO 转化为HCOO-,电极方程式为:
2 3-x 2
CO+H O+2e-=HCOO-+OH-;NiP电极CH(CH)NH 转化为CH(CH)CN,电极方程式为:CH(CH)NH -
2 2 2 3 2 7 2 3 2 7 3 2 7 2
4e-+4OH-=CH (CH)CN+ 4H O。A项,由图示知,该装置为电解池,In/ In O 电极发生反应CO 转化为
3 2 7 2 2 3-x 2
HCOO-,C元素化合价由+4价降到+2价,得电子被还原,故In/ In O 电极为阴极,则NiP为阳极与电源
2 3-x
正极相连,故A正确;B项,In/ In O 电极为阴极,溶液中H+可能在阴极放电产生副产物H,故B正确;
2 3-x 2
C项,In/ In O 电极发生反应CO 转化为HCOO-,C元素化合价由+4价降到+2价,根据得失电子守恒和
2 3-x 2
电荷守恒配平电极方程式为:CO+H O+2e-=HCOO-+OH-,故C正确;D项,标准状况下33.6L CO 的物质
2 2 2
的量为1.5mol,In/ In O 电极方程式为:CO+H O+2e-=HCOO-+OH-,失去3mol电子;NiP电极电极方程
2 3-x 2 2 2
式为:CH(CH)NH -4e-+4OH-=CH (CH)CN+ 4H O,得到3mol电子时,生成0.75molCH(CH)CN,故D
3 2 7 2 3 2 7 2 3 2 7
错误;故选D。
11.(2023·浙江省重点中学拔尖学生培养联盟适应性考试)直接HO-H O 燃料电池是一种新型化学电
2 2 2 2
源,其工作原理如图所示。电池放电时,下列说法不正确的是( )
A.电池工作时,电极I电势低
B.电极Ⅱ的反应式为:HO+2e- +2H+=2HO
2 2 2
C.电池总反应为:2HO=2HO+O↑
2 2 2 2
D.当电路中转移0.1mol电子时,通过阳离子交换膜的 为3.9g
【答案】C
【解析】电池工作时,电势低的是负极,电子从负极流向正极,故电极I为负极,电极Ⅱ为正极,负
极:HO-2e-+2OH-=O ↑+2H O,正极: H O+2e- +2H+=2HO。A项,电池工作时,电势低的是负极,电子从
2 2 2 2 2 2 2
负极流向正极,故电极I电势低,A正确;B项,电极Ⅱ为正极,电极反应式为:HO+2e- +2H+=2HO,B
2 2 2
资料收集整理【淘宝店铺:向阳百分百】