文档内容
考点 20 金属的腐蚀与防护
【基础过关】
1.(2023·辽宁省名校联盟高考模拟调研卷)“北溪”天然气管道至少泄漏8万吨天然气,近20年间甲烷
的温室效应率是 的84倍。已知管道接口处有钢铁材料等,海水的pH约为8.0。设 为阿伏伽德罗常
数的值。下列有关叙述不正确的是( )
A.损坏的钢铁材料在海水中主要发生吸氧腐蚀
B.制造管道时表面涂层能起到抗腐蚀作用
C.w g铁在海水中完全发生电化学腐蚀时转移电子数一定为
D.修复管道时在钢管表面镶嵌锌块,这种方法叫牺牲阳极法
【答案】C
【解析】A项,钢铁在弱碱性环境中主要发生吸氧腐蚀,A项正确;B项,表面涂层能防止钢铁管道
和水、O 等物质接触,从而起到抗腐蚀作用,B项正确;C项,钢铁腐蚀时负极电极反应式为Fe-2e-
2
=Fe2+,w g铁在海水中完全发生电化学腐蚀时转移电子数为 ,后续发生
,不属于电化学腐蚀,C项错误;D项,锌比铁活泼,在海水中构成原
电池,锌为负极,铁为正极,这种保护钢铁的方法叫牺牲阳极法,D项正确。故选C。
2.(2023·河北省沧州市三模)出土于陕西的两千多年前的越王剑(主要成分为铁),现藏于广州博物馆,
该剑剑格左右侧皆以鸟虫书体铸刻“王戊”二字,剑色为水银古,时至如今,依然锋利。剑脊含铜量较多,
韧性好,不易折断;刃部含锡高,硬度强,可见其性能优异,锻造技术优良。下列叙述错误的是
已知:剑在地下因构成原电池发生了腐蚀,导致生锈(Fe O)。
2 3
A.铁与铜、锡构成原电池时,铁为负极
B.铁发生的电极反应为Fe-3e-=Fe3+
C.酸性环境下剑腐蚀的过程中会产生氢气
资料收集整理【淘宝店铺:向阳百分百】D.生成80gFe O 时理论上转移3mol电子
2 3
【答案】B
【解析】A项,铁与铜、锡构成原电池时,铁的活泼性强于铜和锡,铁作负极,A正确;B项,铁电
极反应为Fe-2e-=Fe2+,B错误;C项,酸性环境下剑腐蚀的过程为析氢腐蚀,正极会产生氢气:2H++2e-
=H ↑,C正确;D项,生成 Fe O 时理论上转移电子 3mol,D正确;故
2 2 3
选B。
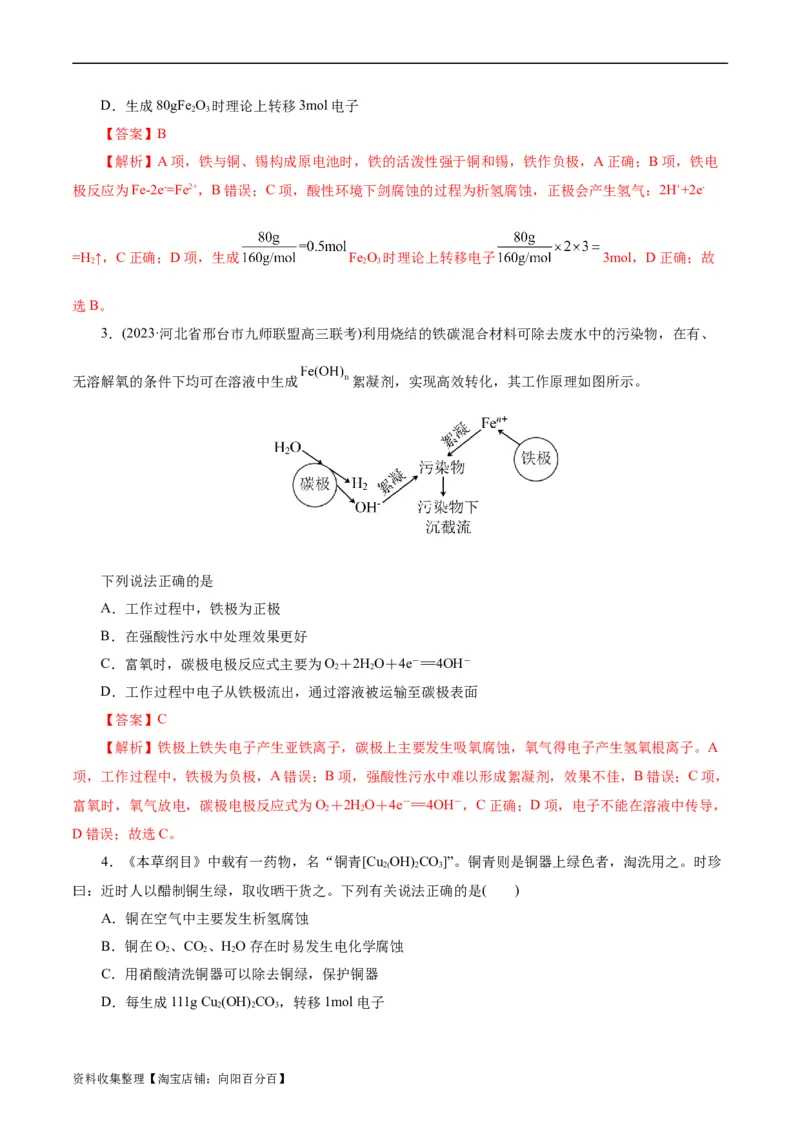
3.(2023·河北省邢台市九师联盟高三联考)利用烧结的铁碳混合材料可除去废水中的污染物,在有、
无溶解氧的条件下均可在溶液中生成 絮凝剂,实现高效转化,其工作原理如图所示。
下列说法正确的是
A.工作过程中,铁极为正极
B.在强酸性污水中处理效果更好
C.富氧时,碳极电极反应式主要为O+2HO+4e-=4OH-
2 2
D.工作过程中电子从铁极流出,通过溶液被运输至碳极表面
【答案】C
【解析】铁极上铁失电子产生亚铁离子,碳极上主要发生吸氧腐蚀,氧气得电子产生氢氧根离子。A
项,工作过程中,铁极为负极,A错误;B项,强酸性污水中难以形成絮凝剂,效果不佳,B错误;C项,
富氧时,氧气放电,碳极电极反应式为O+2HO+4e-=4OH-,C正确;D项,电子不能在溶液中传导,
2 2
D错误;故选C。
4.《本草纲目》中载有一药物,名“铜青[Cu OH) CO]”。铜青则是铜器上绿色者,淘洗用之。时珍
2( 2 3
曰:近时人以醋制铜生绿,取收晒干货之。下列有关说法正确的是( )
A.铜在空气中主要发生析氢腐蚀
B.铜在O、CO、HO存在时易发生电化学腐蚀
2 2 2
C.用硝酸清洗铜器可以除去铜绿,保护铜器
D.每生成111g Cu (OH) CO,转移1mol电子
2 2 3
资料收集整理【淘宝店铺:向阳百分百】【答案】B
【解析】A项,铜在空气中被腐蚀的化学方程式为2Cu+O +CO +H O=Cu OH) CO,则铜在空气中主
2 2 2 2( 2 3
要发生吸氧腐蚀,A错误;B项,铜在空气中被腐蚀的化学方程式为2Cu+O +CO +H O=Cu (OH) CO,铜
2 2 2 2 2 3
在O、CO、HO存在时易发生电化学腐蚀,B正确;C项,铜可以和硝酸反应,用硝酸清洗铜器可以除
2 2 2
去铜绿,但也会破坏铜器,C错误;D项,由化学方程式2Cu+O +CO +H O=Cu (OH) CO 可知,每生成
2 2 2 2 2 3
1mol Cu (OH) CO,转移4mol电子,则生成111g Cu (OH) CO(物质的量为0.5mol)时,转移2mol电子,D
2 2 3 2 2 3
错误;故选B。
5.实验室利用如下装置模拟探究铝制品表面出现白斑的腐蚀现象。下列说法正确的是( )
A.活性炭上发生氧化反应
B.电子从活性炭经电流表流向铝箔
C.NaCl既是离子导体又是电极反应物
D.总反应为4Al +3O + 6H O =4Al( OH) ,生成的Al(OH) 进一步脱水形成白斑
2 2 3 3
【答案】D
【解析】该装置为原电池,铝易失电子发生氧化反应而作负极,碳作正极,发生吸氧腐蚀,电子从负
极流向正极,阴离子向负极移动。A项,碳作正极,正极上氧气得电子生成氢氧根离子,则正极的反应为
2HO+O+4e-═4OH-,发生还原反应,故A错误;B项,铝易失电子做负极,碳作正极,电子从负极流向正
2 2
极,则电子从铝箔经电流表流向活性炭,故B错误;C项,负极电极反应式为Al-3e-=Al3+,正极反应式
O+2H O+4e-═4OH-,NaCl不是电极反应物,故C错误;D项,负极电极反应式为Al-3e-=Al3+,正极反应
2 2
式O+2H O+4e-═4OH-,总反应方程式为:4Al+3O +6H O═4Al(OH) ,生成的Al(OH) 分解生成Al O,则
2 2 2 2 3 3 2 3
白斑的主要成分可能是Al O,故D正确;故选D。
2 3
6.金属的腐蚀除化学腐蚀和普通的电化学腐蚀外,还有“氧浓差腐蚀”,如在管道或缝隙等处的不
同部位氧的浓度不同,在氧浓度低的部位是原电池的负极。下列说法正确的是( )
A.纯铁的腐蚀属于电化学腐蚀
B.钢铁吸氧腐蚀时,负极的电极反应式为Fe-3e-===Fe3+
C.海轮在浸水部位镶一些铜锭可起到抗腐蚀作用
D.在图示氧浓差腐蚀中,M极处发生的电极反应为O+2HO+4e-===4OH-
2 2
资料收集整理【淘宝店铺:向阳百分百】【答案】D
【解析】纯铁发生腐蚀时,没有正极材料,不能构成原电池,所以发生化学腐蚀,A错误;钢铁发生
吸氧腐蚀时,负极的电极反应式为Fe-2e-===Fe2+,B错误;铜不如铁活泼,铜、铁在海水中形成原电池,
Fe作负极,加快了海轮的腐蚀,C错误;因氧浓度低的部位是原电池的负极,由图示可知,M处O 浓度
2
高,该处O 得到电子,其电极反应式为O+2HO+4e-===4OH-,D正确。
2 2 2
7.糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相
同。下列分析正确的是( )
A.脱氧过程是吸热反应,可降低温度,延长糕点保质期
B.脱氧过程中铁作原电池正极,电极反应为Fe-3e-===Fe3+
C.脱氧过程中碳作原电池负极,电极反应为2HO+O+4e-===4OH-
2 2
D.含有1.12 g铁粉的脱氧剂,理论上最多能吸收氧气336 mL(标准状况)
【答案】D
【解析】在脱氧过程中,由铁、碳作电极,氯化钠溶液作电解质溶液形成原电池,发生吸氧腐蚀,该
过程为放热反应;在脱氧过程中,碳作正极,铁作负极,铁失电子发生氧化反应,生成 Fe2+;在脱氧过程
中,Fe失电子被氧化为Fe2+,Fe2+最终还是被氧气氧化为Fe3+,由电子得失守恒知消耗氧气的体积(标准
状况下)V(O )=22.4 L·mol-1×=336 mL。
2
8.(2023·广东省深圳市高三期中)某航天发生器的点火接头金属由合金钢加工成型。该金属接头端面
发生锈蚀的原理如图所示。下列说法错误的是( )
A.合金钢中Fe作负极,长条状硫化物作正极
B.合金钢腐蚀速度与空气相对湿度无关
C.正极的电极反应有O+2HO+4e-=4OH-
2 2
D.可使用酒精棉球擦拭清洗并均匀涂抹润滑脂防锈
【答案】B
【解析】A项, Fe失电子,被氧化,为负极,所以长条状硫化物作正极,A正确;B项,正极为氧气
和水得电子的反应,说明湿度越大,参加反应的物质的量越大,得电子越多,腐蚀速度越快,B错误;C
项,通入空气的一端为正极,氧气得电子,与水反应生成氢氧根离子,故C正确;D项,使用酒精棉球擦
拭清洗并均匀涂抹润滑脂,通过防止金属与氧气和水接触,从而防锈,D正确;故选B。
9.全世界每年因钢铁锈蚀造成巨大损失,钢铁吸氧腐蚀原理如图所示。下列说法正确的是( )
资料收集整理【淘宝店铺:向阳百分百】A.钢铁腐蚀过程不只发生化学能与电能的转化
B.钢铁腐蚀的正极反应为:Fe-2e-=Fe2+
C.电解质溶液浓度可影响钢铁腐蚀的速率
D.将地下铁管与铜块连接,可保护铁管
【答案】C
【解析】A项,钢铁腐蚀过程不仅发生化学能与电能的转化,钢铁的锈蚀过程属于缓慢氧化,还放出
热量,所以还发生化学能与热能的转化,A正确;B项,钢铁发生的腐蚀为吸氧腐蚀,负极上金属铁失电
子,发生氧化反应,正极上氧气得到电子,发生还原反应,电极反应为:2HO+O+4e-=4OH-,B错误;C
2 2
项,因为反应速率与离子浓度正相关,所以电解质溶液浓度可影响钢铁腐蚀的速率, C正确; D项,将
地下铁管与铜块连接会构成原电池,铁作负极,铜作正极,所以不能保护铁管,反而会加快铁管的腐蚀,
D错误;故选 C。
10.利用如图所示装置可以模拟钢铁的电化学防护。下列说法正确的是( )。
A.若X为锌棒,开关K置于M处,铁极发生还原反应
B.若X为碳棒,开关K置于N处,X极发生还原反应
C.若X为碳棒,开关K置于N处,可加快铁的腐蚀
D.若X为锌棒,开关K置于M处,可加快铁的腐蚀
【答案】A
【解析】若X为锌棒,开关K置于M处,形成原电池,此时金属锌为负极,金属铁为正极,金属铁
被保护,铁极发生还原反应,A项正确,D项不正确;若X为碳棒,开关K置于N处,形成电解池,X极
为阳极,发生氧化反应,B项不正确;若X为碳棒,开关K置于N处,形成电解池,此时金属铁为阴极,
铁被保护,C项不正确。
11.炒过菜的铁锅未及时洗净(残液中含NaCl),不久便会因被腐蚀而出现红褐色锈斑。腐蚀原理如图
所示,下列说法正确的是( )
资料收集整理【淘宝店铺:向阳百分百】A.腐蚀过程中,负极是C
B.Fe失去电子经电解质溶液转移给C
C.正极的电极反应式为4OH--4e-===2H O+O↑
2 2
D.C是正极,O 在C表面上发生还原反应
2
【答案】D
【解析】A项,铁锅中含有的Fe、C,和电解质溶液构成原电池,活泼金属作负极,Fe易失电子,故
腐蚀过程中,负极是Fe,错误;B项,原电池中电子由负极Fe经外电路向正极C流动,在电解质溶液中
依靠离子的移动导电,错误;C项,该原电池中,C做正极,正极上氧气得电子发生还原反应,电极反应
式为O+2HO+4e-===4OH-,错误;D项,C是正极,O 在C表面上发生还原反应,正确。
2 2 2
12.钢铁的防护有多种方法,下列对于图中的方法描述错误的是( )
A.a、b以导线连接,辅助电极发生氧化反应
B.a、b以导线连接或以电源连接,辅助电极的材料可能都含有Zn
C.a、b分别连接直流电源,通电后外电路电子被强制从辅助电极流向钢铁闸门
D.a、b分别连接直流电源的负极、正极,该方法是牺牲阳极的阴极保护法
【答案】D
【解析】a、b以导线连接,即为牺牲阳极的阴极保护法,则辅助电极要作负极,发生氧化反应,A项
正确;a、b以导线连接或以电源连接,辅助电极都是发生氧化反应,Zn比较活泼,要失去电子,B项正确;
通电后,被保护的钢铁闸门作阴极,辅助电极作阳极,因此通电后外电路电子被强制从辅助电极流向钢铁
闸门,C项正确;由于有外加电源,故此方法为外加电流的阴极保护法,D项错误。
13.硫酸盐还原菌SRB在地球上分布很广泛,通过多种相互作用发挥诸多潜力。但在水体中,会促使
许多金属及合金发生腐蚀。某种Fe合金在硫酸盐还原菌存在条件下腐蚀的机理如图所示。对于该反应机理
相关信息分析错误的是 ( )
资料收集整理【淘宝店铺:向阳百分百】①升高温度有利于硫酸盐还原菌(SRB)对金属的腐蚀;
②硫酸盐还原菌(SRB)对金属的腐蚀作用是在有氧环境下进行的;
③在硫酸盐还原菌(SRB)作用下,Fe腐蚀后最终会生成Fe O·xH O;
2 3 2
④电化学腐蚀中负极电极反应为 Fe-2e-=Fe2+;
⑤当1mol SO 2-在SRB的作用下转化为硫离子时,理论上正极反应会消耗8 mol水
4
A.①②③ B.①②⑤ C.②③④ D.②③⑤
【答案】A
【解析】①高温下容易使蛋白质发生变性,因此升高温度不有利于硫酸盐还原菌(SRB)对金属的腐蚀,
①错误;②根据示意图可判断硫酸盐还原菌(SRB)对金属的腐蚀作用是在无氧环境下进行的,②错误;③
在硫酸盐还原菌(SRB)作用下,Fe腐蚀后最终会生成FeS,③错误;④电化学腐蚀中负极铁失去电子,电
极反应为 Fe-2e-=Fe2+,④正确;⑤当1mol SO 2-在SRB的作用下转化为硫离子时需要8mol[H],1mol水能
4
产生1mol[H],所以理论上正极反应会消耗8 mol水,⑤正确;故选A。
14.下列根据实验操作及现象进行的分析和推断中,不正确的是( )
操
作
现 一段时间后:①中,铁钉裸露在外的附近区域变红;
象 ②中……
A.NaCl的琼脂水溶液为离子迁移的通路
B.①中变红是因为发生反应2H++2e-= H ↑,促进了水的电离
2
C.②中可观察到铁钉裸露在外的附近区域产生蓝色沉淀,铜丝附近区域变红
D.①和②中发生的氧化反应均可表示为M-2e-=M2+ (M代表锌或铁)
【答案】B
【解析】A项,①和②中,Zn和Fe分别发生了电化学腐蚀,NaCl的琼脂水溶液的作用是形成闭合回
资料收集整理【淘宝店铺:向阳百分百】路,即NaCl的琼脂水溶液为离子迁移的通路,A正确;B项,①中,由于Zn的活动性比Fe强,故Zn作
负极,Fe作正极,正极的电极反应式为O+2H O+4e-=4OH-,正极附近区域OH-使酚酞变红,B错误;C项,
2 2
②中,由于Fe的活动性比Cu强,故Fe作负极,Cu作正极,负极的电极反应式为Fe-2e-=Fe2+,正极的电
极反应式为O+2H O+4e-=4OH-,负极附近区域Fe2+和Fe(CN) 3-反应生成蓝色沉淀,正极附近区域OH-使酚
2 2 6
酞变红,C正确;D项,①中Zn作负极,电极反应式为Zn-2e-=Zn2+,②中Fe作负极,电极反应式为Fe-2e-
=Fe2+,D正确;故选B。
15.某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,设计下表实验。将混合均匀
的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞。从胶头滴管中一次性滴入醋酸溶液,同时测量容器中的压
强变化。下列说法不正确的是( )
编号 实验目的 碳粉/g 铁粉/g 醋酸/ 醋酸/
① 为以下实验作参照 0.5 2.0 90.0 2.0
② 醋酸浓度的影响 0.5 a 36.0 2.0
③ M 0.2 2.0 90.0 2.0
A.
B.M为“碳粉质量的影响”
C.该实验一共探究了4种影响因素
D.铁发生电化学腐蚀负极反应为Fe-2e-=Fe2+
【答案】C
【解析】A项,由表格数据可知,①②的实验目的为探究醋酸浓度对铁发生电化学腐蚀类型的影响,
由变量唯一化原则可知,实验中①和②的醋酸浓度不同,所以铁粉的质量应该相同,所以a为2.0,故A正
确;B项,由表格数据可知,①和③的碳粉质量不同,其他条件完全相同,所以实验目的是探究碳粉质量
对铁发生电化学腐蚀类型的影响,故B正确;C项,由表格数据可知,该实验只探究了醋酸浓度、碳粉质
量对铁发生电化学腐蚀类型的影响,故C错误;D项,铁发生电化学腐蚀时,铁做负极失去电子被损耗,
电极反应式为Fe-2e-=Fe2+,故D正确;故选C。
16.研究发现,CuCl在青铜器的腐蚀过程中起催化作用,下图是青铜器在潮湿环境中发生电化学腐蚀
资料收集整理【淘宝店铺:向阳百分百】