文档内容
考点 20 金属的腐蚀与防护
【基础过关】
1.(2023·辽宁省名校联盟高考模拟调研卷)“北溪”天然气管道至少泄漏8万吨天然气,近20年间甲烷
的温室效应率是 的84倍。已知管道接口处有钢铁材料等,海水的pH约为8.0。设 为阿伏伽德罗常
数的值。下列有关叙述不正确的是( )
A.损坏的钢铁材料在海水中主要发生吸氧腐蚀
B.制造管道时表面涂层能起到抗腐蚀作用
C.w g铁在海水中完全发生电化学腐蚀时转移电子数一定为
D.修复管道时在钢管表面镶嵌锌块,这种方法叫牺牲阳极法
2.(2023·河北省沧州市三模)出土于陕西的两千多年前的越王剑(主要成分为铁),现藏于广州博物馆,
该剑剑格左右侧皆以鸟虫书体铸刻“王戊”二字,剑色为水银古,时至如今,依然锋利。剑脊含铜量较多,
韧性好,不易折断;刃部含锡高,硬度强,可见其性能优异,锻造技术优良。下列叙述错误的是
已知:剑在地下因构成原电池发生了腐蚀,导致生锈(Fe O)。
2 3
A.铁与铜、锡构成原电池时,铁为负极
B.铁发生的电极反应为Fe-3e-=Fe3+
C.酸性环境下剑腐蚀的过程中会产生氢气
D.生成80gFe O 时理论上转移3mol电子
2 3
3.(2023·河北省邢台市九师联盟高三联考)利用烧结的铁碳混合材料可除去废水中的污染物,在有、
无溶解氧的条件下均可在溶液中生成 絮凝剂,实现高效转化,其工作原理如图所示。
资料收集整理【淘宝店铺:向阳百分百】 1下列说法正确的是
A.工作过程中,铁极为正极
B.在强酸性污水中处理效果更好
C.富氧时,碳极电极反应式主要为O+2HO+4e-=4OH-
2 2
D.工作过程中电子从铁极流出,通过溶液被运输至碳极表面
4.《本草纲目》中载有一药物,名“铜青[Cu OH) CO]”。铜青则是铜器上绿色者,淘洗用之。时珍
2( 2 3
曰:近时人以醋制铜生绿,取收晒干货之。下列有关说法正确的是( )
A.铜在空气中主要发生析氢腐蚀
B.铜在O、CO、HO存在时易发生电化学腐蚀
2 2 2
C.用硝酸清洗铜器可以除去铜绿,保护铜器
D.每生成111g Cu (OH) CO,转移1mol电子
2 2 3
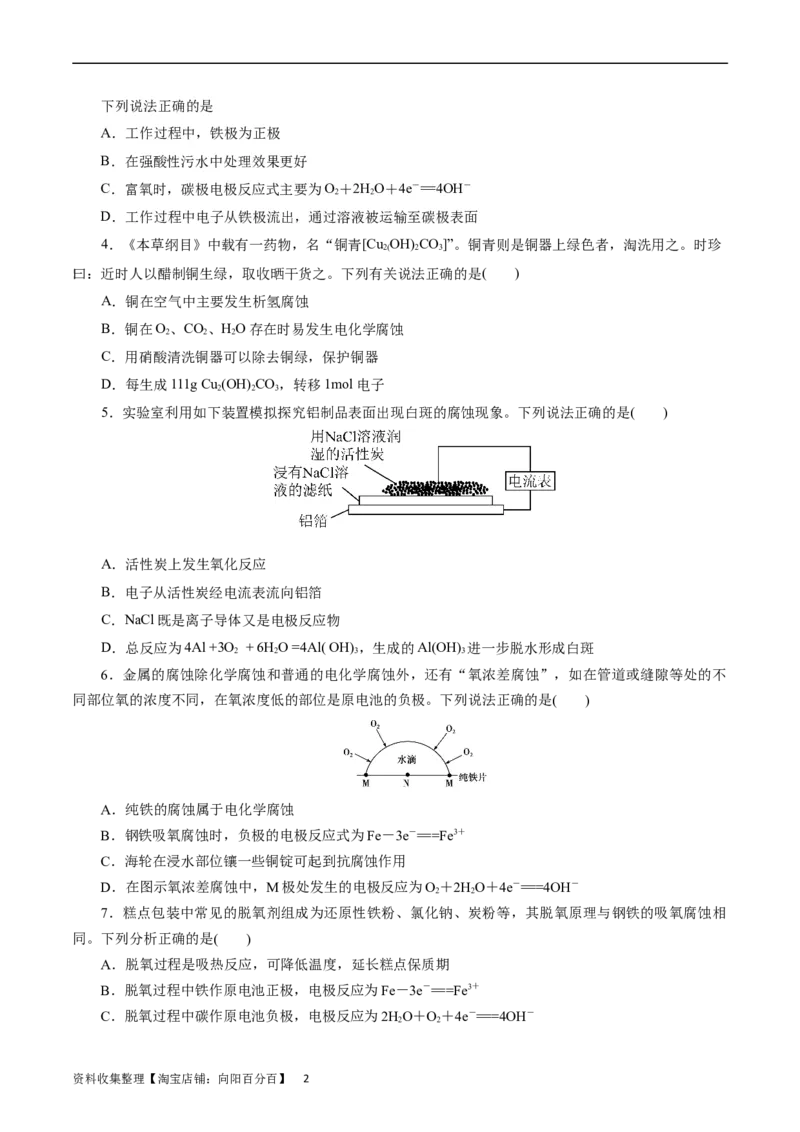
5.实验室利用如下装置模拟探究铝制品表面出现白斑的腐蚀现象。下列说法正确的是( )
A.活性炭上发生氧化反应
B.电子从活性炭经电流表流向铝箔
C.NaCl既是离子导体又是电极反应物
D.总反应为4Al +3O + 6H O =4Al( OH) ,生成的Al(OH) 进一步脱水形成白斑
2 2 3 3
6.金属的腐蚀除化学腐蚀和普通的电化学腐蚀外,还有“氧浓差腐蚀”,如在管道或缝隙等处的不
同部位氧的浓度不同,在氧浓度低的部位是原电池的负极。下列说法正确的是( )
A.纯铁的腐蚀属于电化学腐蚀
B.钢铁吸氧腐蚀时,负极的电极反应式为Fe-3e-===Fe3+
C.海轮在浸水部位镶一些铜锭可起到抗腐蚀作用
D.在图示氧浓差腐蚀中,M极处发生的电极反应为O+2HO+4e-===4OH-
2 2
7.糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相
同。下列分析正确的是( )
A.脱氧过程是吸热反应,可降低温度,延长糕点保质期
B.脱氧过程中铁作原电池正极,电极反应为Fe-3e-===Fe3+
C.脱氧过程中碳作原电池负极,电极反应为2HO+O+4e-===4OH-
2 2
资料收集整理【淘宝店铺:向阳百分百】 2D.含有1.12 g铁粉的脱氧剂,理论上最多能吸收氧气336 mL(标准状况)
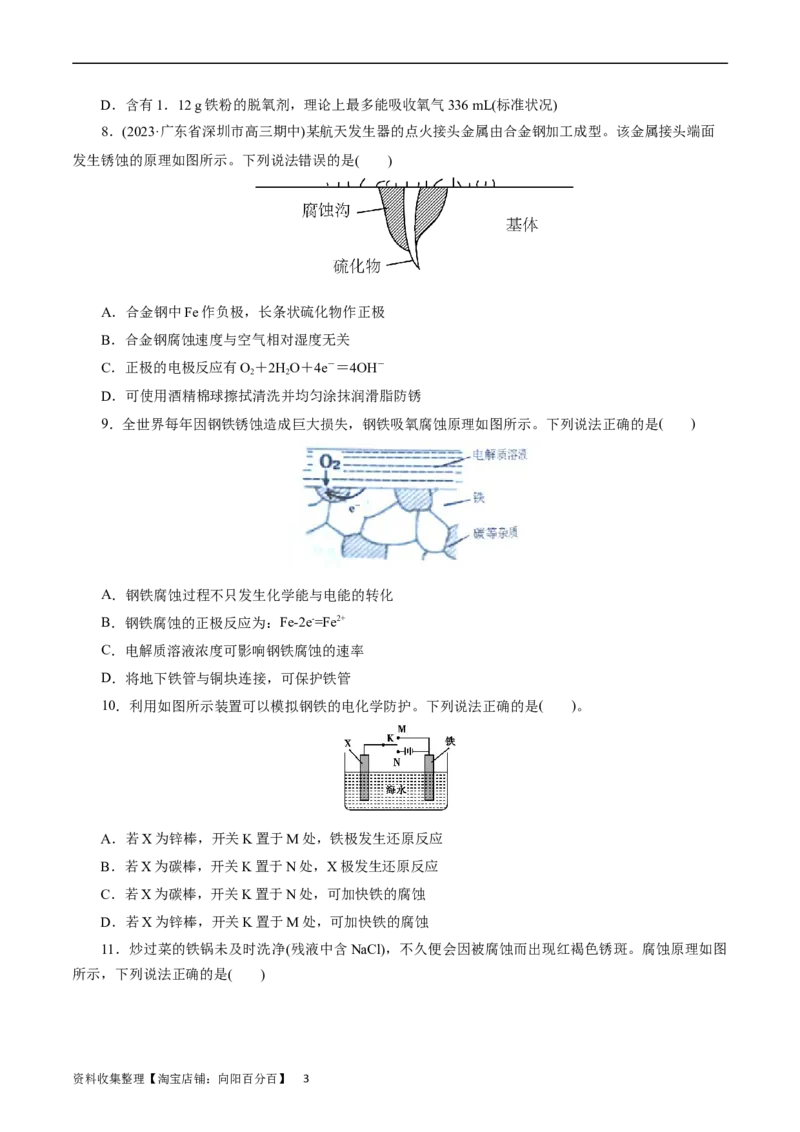
8.(2023·广东省深圳市高三期中)某航天发生器的点火接头金属由合金钢加工成型。该金属接头端面
发生锈蚀的原理如图所示。下列说法错误的是( )
A.合金钢中Fe作负极,长条状硫化物作正极
B.合金钢腐蚀速度与空气相对湿度无关
C.正极的电极反应有O+2HO+4e-=4OH-
2 2
D.可使用酒精棉球擦拭清洗并均匀涂抹润滑脂防锈
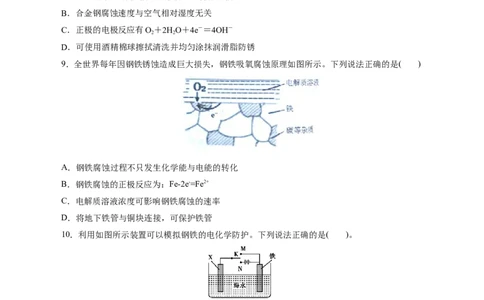
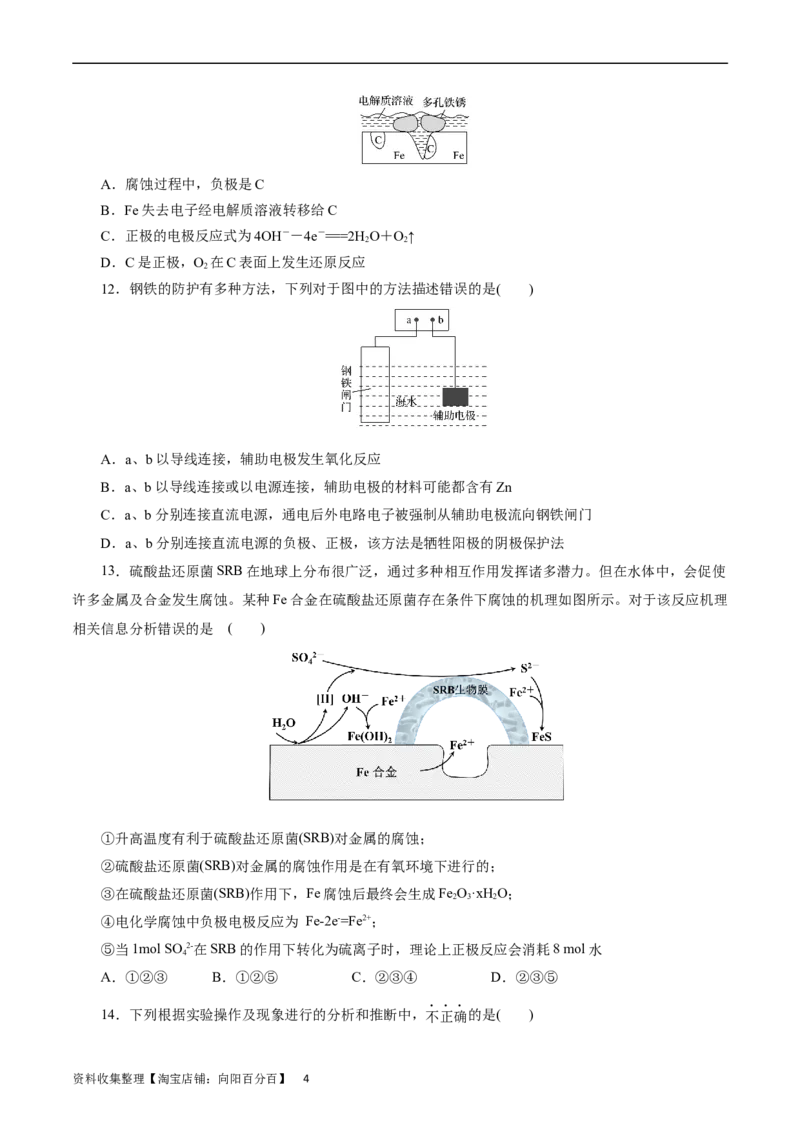
9.全世界每年因钢铁锈蚀造成巨大损失,钢铁吸氧腐蚀原理如图所示。下列说法正确的是( )
A.钢铁腐蚀过程不只发生化学能与电能的转化
B.钢铁腐蚀的正极反应为:Fe-2e-=Fe2+
C.电解质溶液浓度可影响钢铁腐蚀的速率
D.将地下铁管与铜块连接,可保护铁管
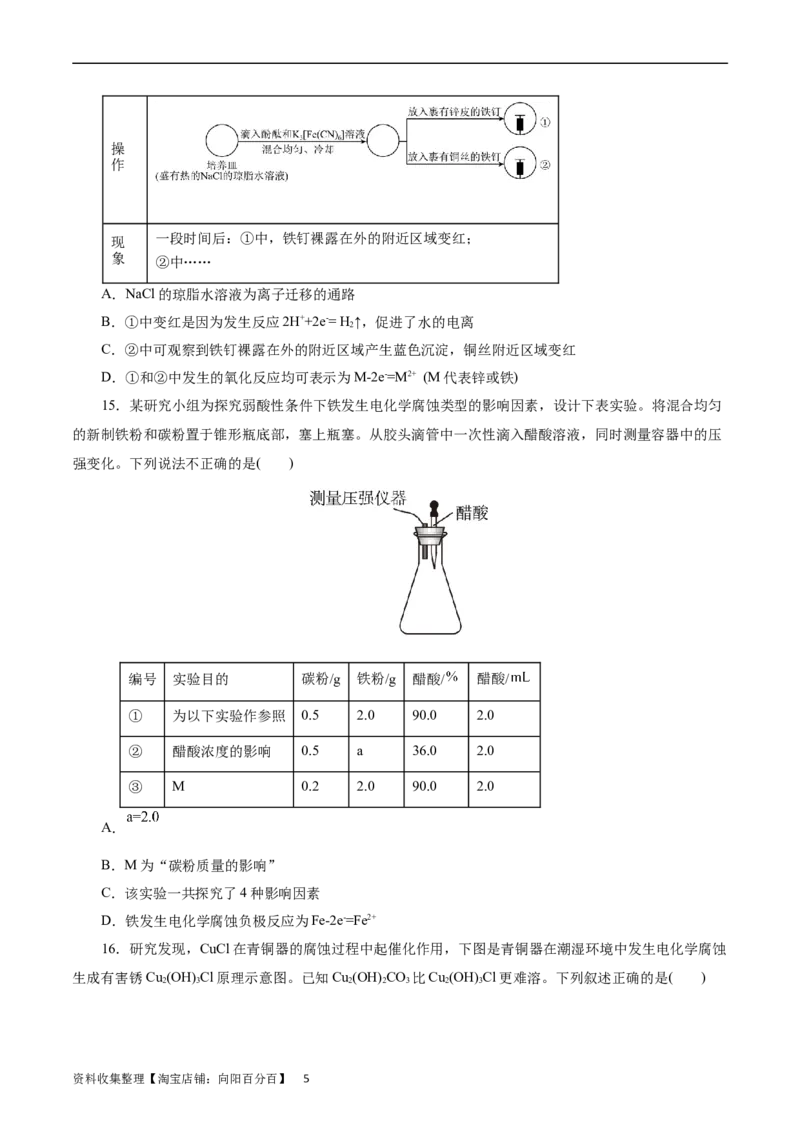
10.利用如图所示装置可以模拟钢铁的电化学防护。下列说法正确的是( )。
A.若X为锌棒,开关K置于M处,铁极发生还原反应
B.若X为碳棒,开关K置于N处,X极发生还原反应
C.若X为碳棒,开关K置于N处,可加快铁的腐蚀
D.若X为锌棒,开关K置于M处,可加快铁的腐蚀
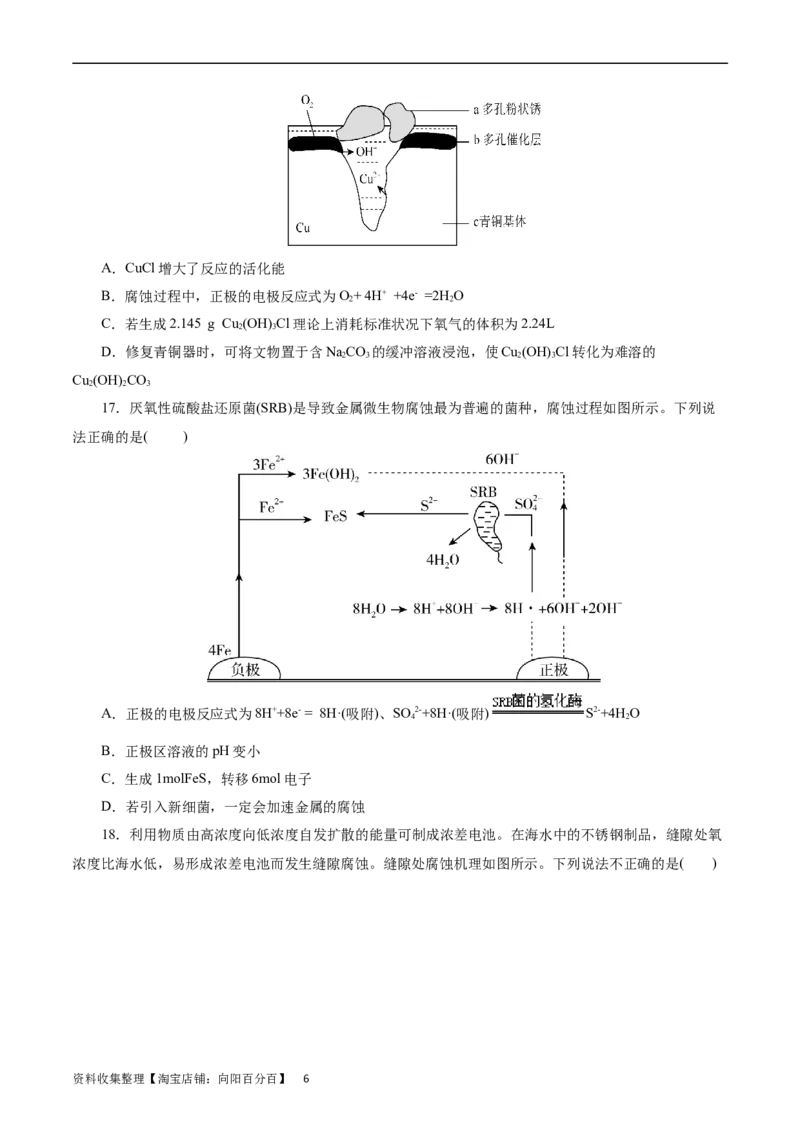
11.炒过菜的铁锅未及时洗净(残液中含NaCl),不久便会因被腐蚀而出现红褐色锈斑。腐蚀原理如图
所示,下列说法正确的是( )
资料收集整理【淘宝店铺:向阳百分百】 3A.腐蚀过程中,负极是C
B.Fe失去电子经电解质溶液转移给C
C.正极的电极反应式为4OH--4e-===2H O+O↑
2 2
D.C是正极,O 在C表面上发生还原反应
2
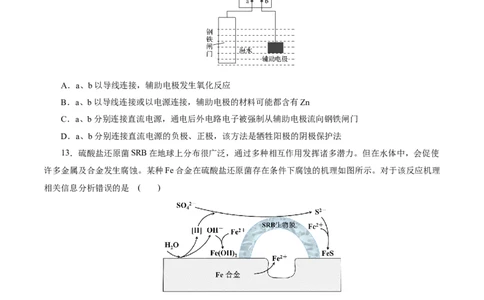
12.钢铁的防护有多种方法,下列对于图中的方法描述错误的是( )
A.a、b以导线连接,辅助电极发生氧化反应
B.a、b以导线连接或以电源连接,辅助电极的材料可能都含有Zn
C.a、b分别连接直流电源,通电后外电路电子被强制从辅助电极流向钢铁闸门
D.a、b分别连接直流电源的负极、正极,该方法是牺牲阳极的阴极保护法
13.硫酸盐还原菌SRB在地球上分布很广泛,通过多种相互作用发挥诸多潜力。但在水体中,会促使
许多金属及合金发生腐蚀。某种Fe合金在硫酸盐还原菌存在条件下腐蚀的机理如图所示。对于该反应机理
相关信息分析错误的是 ( )
①升高温度有利于硫酸盐还原菌(SRB)对金属的腐蚀;
②硫酸盐还原菌(SRB)对金属的腐蚀作用是在有氧环境下进行的;
③在硫酸盐还原菌(SRB)作用下,Fe腐蚀后最终会生成Fe O·xH O;
2 3 2
④电化学腐蚀中负极电极反应为 Fe-2e-=Fe2+;
⑤当1mol SO 2-在SRB的作用下转化为硫离子时,理论上正极反应会消耗8 mol水
4
A.①②③ B.①②⑤ C.②③④ D.②③⑤
14.下列根据实验操作及现象进行的分析和推断中,不正确的是( )
资料收集整理【淘宝店铺:向阳百分百】 4操
作
现 一段时间后:①中,铁钉裸露在外的附近区域变红;
象 ②中……
A.NaCl的琼脂水溶液为离子迁移的通路
B.①中变红是因为发生反应2H++2e-= H ↑,促进了水的电离
2
C.②中可观察到铁钉裸露在外的附近区域产生蓝色沉淀,铜丝附近区域变红
D.①和②中发生的氧化反应均可表示为M-2e-=M2+ (M代表锌或铁)
15.某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,设计下表实验。将混合均匀
的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞。从胶头滴管中一次性滴入醋酸溶液,同时测量容器中的压
强变化。下列说法不正确的是( )
编号 实验目的 碳粉/g 铁粉/g 醋酸/ 醋酸/
① 为以下实验作参照 0.5 2.0 90.0 2.0
② 醋酸浓度的影响 0.5 a 36.0 2.0
③ M 0.2 2.0 90.0 2.0
A.
B.M为“碳粉质量的影响”
C.该实验一共探究了4种影响因素
D.铁发生电化学腐蚀负极反应为Fe-2e-=Fe2+
16.研究发现,CuCl在青铜器的腐蚀过程中起催化作用,下图是青铜器在潮湿环境中发生电化学腐蚀
生成有害锈Cu (OH) Cl原理示意图。已知Cu (OH) CO 比Cu (OH) Cl更难溶。下列叙述正确的是( )
2 3 2 2 3 2 3
资料收集整理【淘宝店铺:向阳百分百】 5A.CuCl增大了反应的活化能
B.腐蚀过程中,正极的电极反应式为O+ 4H+ +4e- =2H O
2 2
C.若生成2.145 g Cu (OH) Cl理论上消耗标准状况下氧气的体积为2.24L
2 3
D.修复青铜器时,可将文物置于含NaCO 的缓冲溶液浸泡,使Cu (OH) Cl转化为难溶的
2 3 2 3
Cu (OH) CO
2 2 3
17.厌氧性硫酸盐还原菌(SRB)是导致金属微生物腐蚀最为普遍的菌种,腐蚀过程如图所示。下列说
法正确的是( )
A.正极的电极反应式为8H++8e- = 8H·(吸附)、SO 2-+8H·(吸附) S2-+4H O
4 2
B.正极区溶液的pH变小
C.生成1molFeS,转移6mol电子
D.若引入新细菌,一定会加速金属的腐蚀
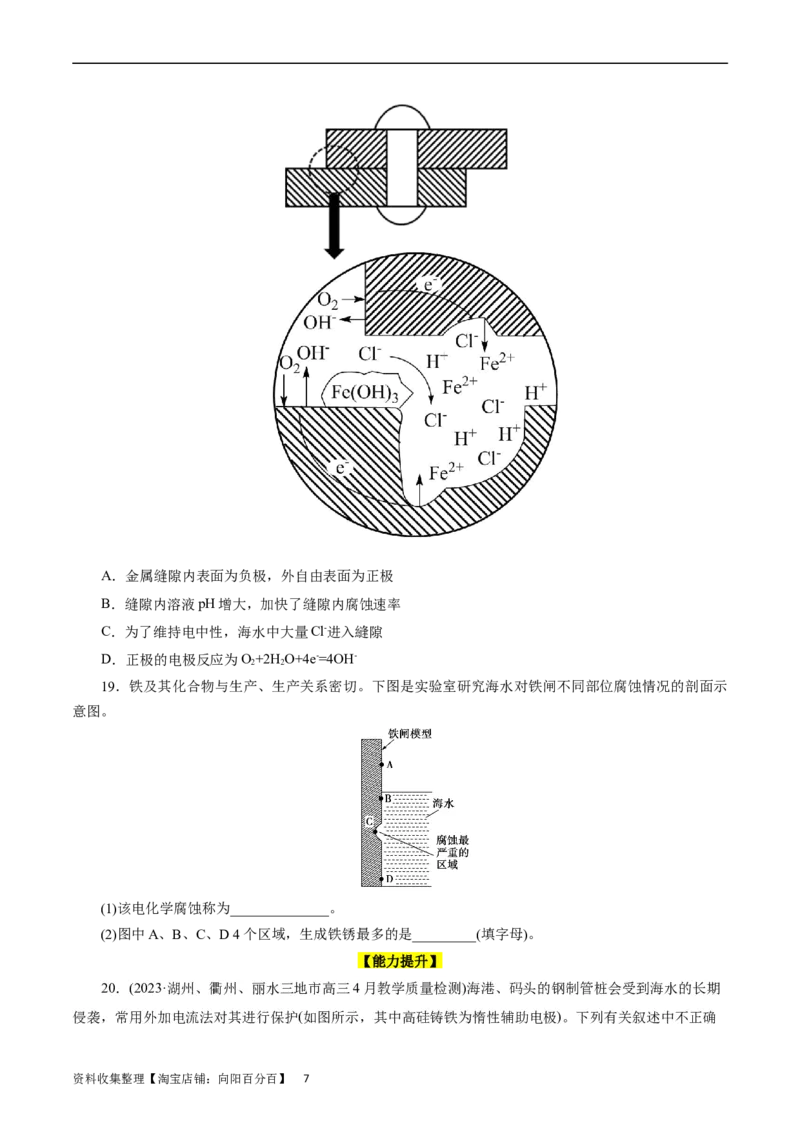
18.利用物质由高浓度向低浓度自发扩散的能量可制成浓差电池。在海水中的不锈钢制品,缝隙处氧
浓度比海水低,易形成浓差电池而发生缝隙腐蚀。缝隙处腐蚀机理如图所示。下列说法不正确的是( )
资料收集整理【淘宝店铺:向阳百分百】 6A.金属缝隙内表面为负极,外自由表面为正极
B.缝隙内溶液pH增大,加快了缝隙内腐蚀速率
C.为了维持电中性,海水中大量Cl-进入縫隙
D.正极的电极反应为O+2H O+4e-=4OH-
2 2
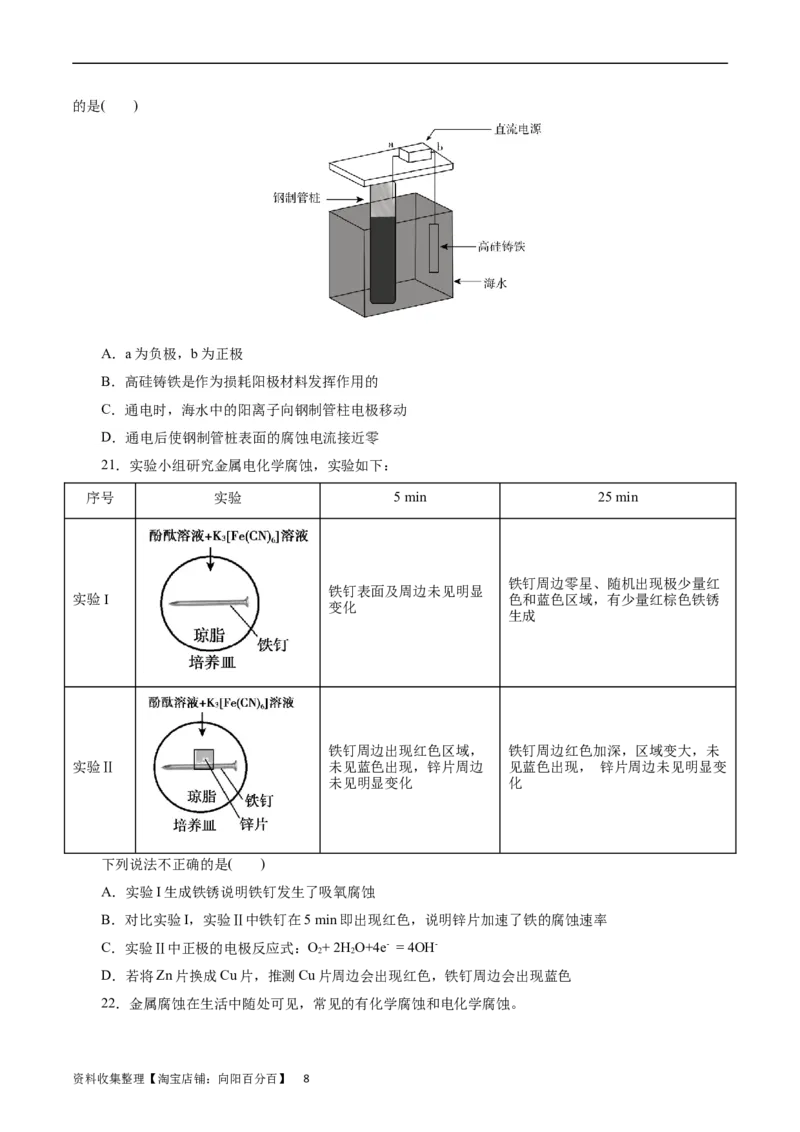
19.铁及其化合物与生产、生产关系密切。下图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示
意图。
(1)该电化学腐蚀称为______________。
(2)图中A、B、C、D 4个区域,生成铁锈最多的是_________(填字母)。
【能力提升】
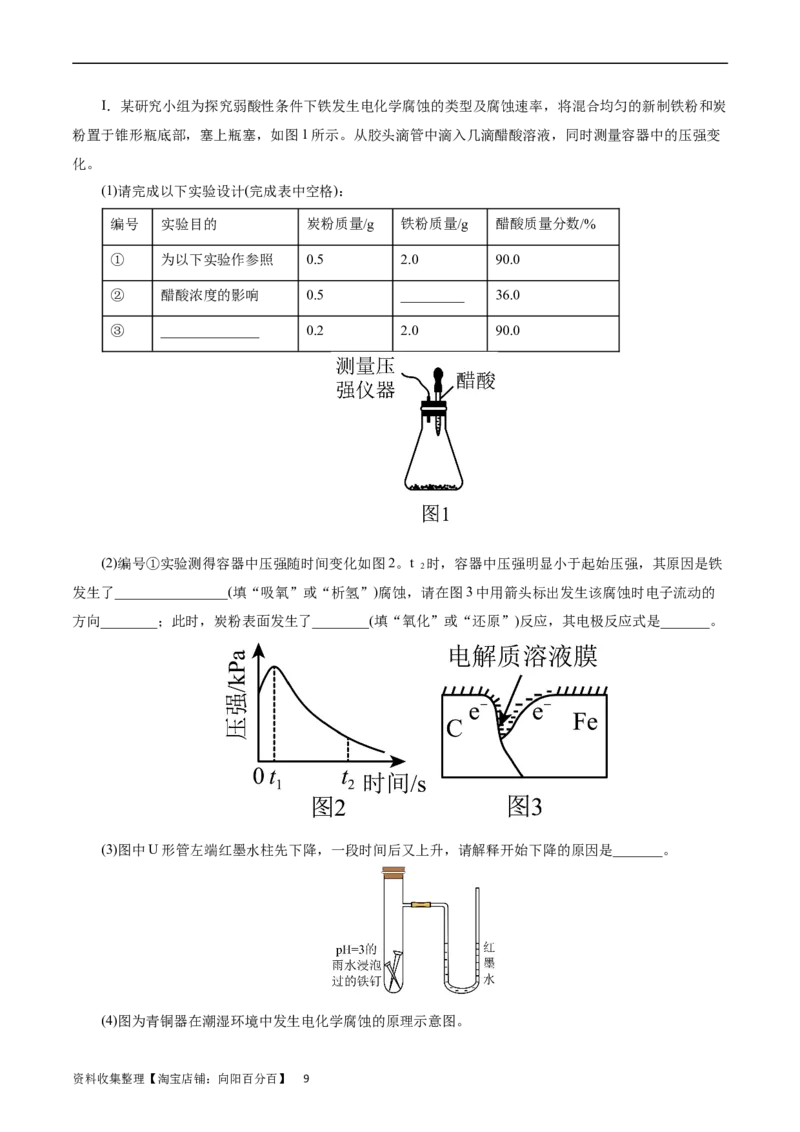
20.(2023·湖州、衢州、丽水三地市高三4月教学质量检测)海港、码头的钢制管桩会受到海水的长期
侵袭,常用外加电流法对其进行保护(如图所示,其中高硅铸铁为惰性辅助电极)。下列有关叙述中不正确
资料收集整理【淘宝店铺:向阳百分百】 7的是( )
A.a为负极,b为正极
B.高硅铸铁是作为损耗阳极材料发挥作用的
C.通电时,海水中的阳离子向钢制管柱电极移动
D.通电后使钢制管桩表面的腐蚀电流接近零
21.实验小组研究金属电化学腐蚀,实验如下:
序号 实验 5 min 25 min
铁钉周边零星、随机出现极少量红
铁钉表面及周边未见明显
实验I 色和蓝色区域,有少量红棕色铁锈
变化
生成
铁钉周边出现红色区域, 铁钉周边红色加深,区域变大,未
实验Ⅱ 未见蓝色出现,锌片周边 见蓝色出现, 锌片周边未见明显变
未见明显变化 化
下列说法不正确的是( )
A.实验I生成铁锈说明铁钉发生了吸氧腐蚀
B.对比实验I,实验Ⅱ中铁钉在5 min即出现红色,说明锌片加速了铁的腐蚀速率
C.实验Ⅱ中正极的电极反应式:O+ 2H O+4e- = 4OH-
2 2
D.若将Zn片换成Cu片,推测Cu片周边会出现红色,铁钉周边会出现蓝色
22.金属腐蚀在生活中随处可见,常见的有化学腐蚀和电化学腐蚀。
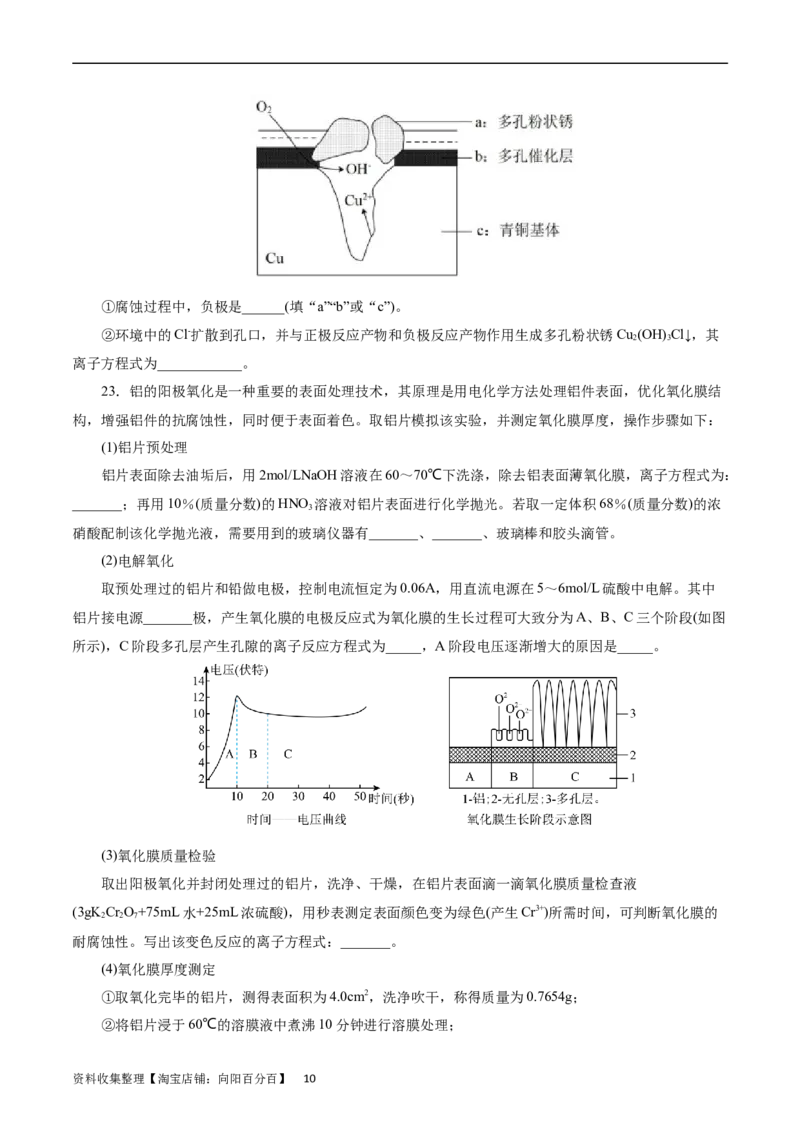
资料收集整理【淘宝店铺:向阳百分百】 8I.某研究小组为探究弱酸性条件下铁发生电化学腐蚀的类型及腐蚀速率,将混合均匀的新制铁粉和炭
粉置于锥形瓶底部,塞上瓶塞,如图1所示。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变
化。
(1)请完成以下实验设计(完成表中空格):
编号 实验目的 炭粉质量/g 铁粉质量/g 醋酸质量分数/%
① 为以下实验作参照 0.5 2.0 90.0
② 醋酸浓度的影响 0.5 _________ 36.0
③ ______________ 0.2 2.0 90.0
(2)编号①实验测得容器中压强随时间变化如图2。t 时,容器中压强明显小于起始压强,其原因是铁
2
发生了________________(填“吸氧”或“析氢”)腐蚀,请在图3中用箭头标出发生该腐蚀时电子流动的
方向________;此时,炭粉表面发生了________(填“氧化”或“还原”)反应,其电极反应式是_______。
(3)图中U形管左端红墨水柱先下降,一段时间后又上升,请解释开始下降的原因是_______。
(4)图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。
资料收集整理【淘宝店铺:向阳百分百】 9①腐蚀过程中,负极是______(填“a”“b”或“c”)。
②环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu (OH) Cl↓,其
2 3
离子方程式为____________。
23.铝的阳极氧化是一种重要的表面处理技术,其原理是用电化学方法处理铝件表面,优化氧化膜结
构,增强铝件的抗腐蚀性,同时便于表面着色。取铝片模拟该实验,并测定氧化膜厚度,操作步骤如下:
(1)铝片预处理
铝片表面除去油垢后,用2mol/LNaOH溶液在60~70℃下洗涤,除去铝表面薄氧化膜,离子方程式为:
_______;再用10%(质量分数)的HNO 溶液对铝片表面进行化学抛光。若取一定体积68%(质量分数)的浓
3
硝酸配制该化学抛光液,需要用到的玻璃仪器有_______、_______、玻璃棒和胶头滴管。
(2)电解氧化
取预处理过的铝片和铅做电极,控制电流恒定为0.06A,用直流电源在5~6mol/L硫酸中电解。其中
铝片接电源_______极,产生氧化膜的电极反应式为氧化膜的生长过程可大致分为A、B、C三个阶段(如图
所示),C阶段多孔层产生孔隙的离子反应方程式为_____,A阶段电压逐渐增大的原因是_____。
(3)氧化膜质量检验
取出阳极氧化并封闭处理过的铝片,洗净、干燥,在铝片表面滴一滴氧化膜质量检查液
(3gK Cr O+75mL水+25mL浓硫酸),用秒表测定表面颜色变为绿色(产生Cr3+)所需时间,可判断氧化膜的
2 2 7
耐腐蚀性。写出该变色反应的离子方程式:_______。
(4)氧化膜厚度测定
①取氧化完毕的铝片,测得表面积为4.0cm2,洗净吹干,称得质量为0.7654g;
②将铝片浸于60℃的溶膜液中煮沸10分钟进行溶膜处理;
资料收集整理【淘宝店铺:向阳百分百】 10③取出铝片,洗净吹干,称得除膜后铝片质量为0.7442g。
已知氧化膜的密度为2.7g/cm3,可以计算得出氧化膜厚度为_____μm(1μm=1×10-4cm)。
资料收集整理【淘宝店铺:向阳百分百】 11