文档内容
考点 25 化学反应速率与平衡图象
(核心考点精讲精练)
一、3年真题考点分布
考点内容 考题统计
2023辽宁卷12题,3分;2023山东卷14题,4分;2022浙江1月选考
19题,2分;2022湖南卷14题,4分;2022广东卷15题,4分;2022
化学反应速率图象
河北卷11题,4分;2021广东卷14题,4分;2021辽宁卷11题,3
分;2021河北卷11题,4分;
2023湖南卷13题,4分;2023浙江6月选考14题,3分;2022江苏卷
化学平衡图象
13题,3分;2022广东卷13题,4分;2021湖南卷11题,4分;
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,识图是化学反应速率和化学平衡的难点,图像、数据信息是高考考查难点和
区分点,高考通过信息给予多样化,往往根据工业生产实际,并结合陌生图象,分析投料比、转化率、产
率的变化,考查接受、加工、同化新信息能力。
【备考策略】
(1)处理好已学知识与题目中提供新信息之间的关系;
(2)提高陌生文本的阅读能力,不断提高获取有效信息;
(3)不同的省份应根据本省命题规律进行有针对性地备考。
【命题预测】
预计2024年的高考仍然会以物质(或微粒)变化示意图、能量变化图象或化学平衡图象的形式呈现,另
选择有机反应、溶液中进行的反应考查化学平衡问题成为命题热点,尤其是化学平衡图象的绘制,应此起
关注。
考法 1 化学反应速率图象
常见速率—时间图像(vt图像)类型如下:
由图像变化分析外界条件对其影响,已知反应为mA(g)+nB(g) pC(g)+qD(g) ΔH=Q kJ·mol-1。
(1)“渐变”类vt图像
图像 分析 结论
资料整理【淘宝店铺:向阳百分百】t 时v′ 突然增大,v′ 逐渐增大;v′ >v′ ,平 t 时其他条件不变,增大反应物
1 正 逆 正 逆 1
衡向正反应方向移动 的浓度
t 时v′ 突然减小,v′ 逐渐减小;v′ >v′ ,平 t 时其他条件不变,减小反应物
1 正 逆 逆 正 1
衡向逆反应方向移动 的浓度
t 时v′ 突然增大,v′ 逐渐增大;v′ >v′ ,平 t 时其他条件不变,增大生成物
1 逆 正 逆 正 1
衡向逆反应方向移动 的浓度
t 时v′ 突然减小,v′ 逐渐减小;v′ >v′ ,平 t 时其他条件不变,减小生成物
1 逆 正 正 逆 1
衡向正反应方向移动 的浓度
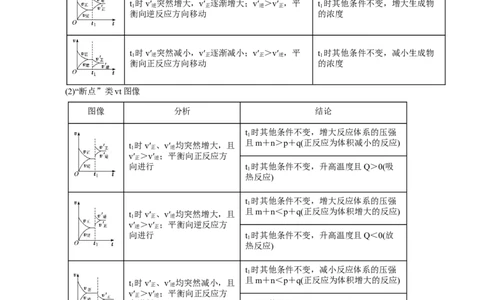
(2)“断点”类vt图像
图像 分析 结论
t 时其他条件不变,增大反应体系的压强
1
t 时v′ 、v′ 均突然增大,且
且m+n>p+q(正反应为体积减小的反应)
1 正 逆
v′ >v′ ;平衡向正反应方
正 逆
向进行 t 时其他条件不变,升高温度且Q>0(吸
1
热反应)
t 时其他条件不变,增大反应体系的压强
1
t 时v′ 、v′ 均突然增大,且
且m+n<p+q(正反应为体积增大的反应)
1 正 逆
v′ >v′ ;平衡向逆反应方
逆 正
向进行 t 时其他条件不变,升高温度且Q<0(放
1
热反应)
t 时其他条件不变,减小反应体系的压强
1
t 时v′ 、v′ 均突然减小,且
且m+n<p+q(正反应为体积增大的反应)
1 正 逆
v′ >v′ ;平衡向正反应方
正 逆
向进行 t 时其他条件不变,降低温度且Q<0(放
1
热反应)
t 时其他条件不变,减小反应体系的压强
1
t 时v′ 、v′ 均突然减小,且
且m+n>p+q(正反应为体积减小的反应)
1 逆 正
v′ >v′ ;平衡向逆反应方
逆 正
向进行 t 时其他条件不变,降低温度且Q>0(吸
1
热反应)
(3)“平台”类vt图像
图像 分析 结论
资料整理【淘宝店铺:向阳百分百】t 时其他条件不变使用催化剂
1
t 时v′ 、v′ 均突然增大
1 正 逆
且v′ 正 =v′ 逆 ,平衡不移动 t 1 时其他条件不变增大反应体系的压强且m+
n=p+q(反应前后气体体积无变化)
t 时v′ 、v′ 均突然减小 t 时其他条件不变,减小反应体系的压强且m
1 正 逆 1
且v′ =v′ ,平衡不移动 +n=p+q(反应前后气体体积无变化)
正 逆
化学速率与平衡图像的解题思路和方法
例1 (2023•湖南卷,13)向一恒容密闭容器中加入1molCH 和一定量的HO,发生反应:CH(g)+
4 2 4
HO(g) CO (g)+ 3H (g)。CH 的平衡转化率按不同投料比 随温度的变化曲线如图所示。
2 2 4
下列说法错误的是( )
资料整理【淘宝店铺:向阳百分百】A.x<x
1 2
B.反应速率:v <vc
正b 正
C.点a、b、c对应的平衡常数:K<K =K
a b c
D.反应温度为T,当容器内压强不变时,反应达到平衡状态
1
【答案】B
【解析】A项,一定条件下,增大水的浓度,能提高CH 的转化率,即x值越小,CH 的转化率越大,
4 4
则x<x,故A正确;B项,b点和c点温度相同,CH 的起始物质的量都为1mol,b点x值小于c点,则
1 2 4
b点加水多,反应物浓度大,则反应速率:v >vc ,故B错误;C项,由图像可知,x一定时,温度升
正b 正
高CH 的平衡转化率增大,说明正反应为吸热反应,温度升高平衡正向移动,K增大;温度相同,K不变,
4
则点a、b、c对应的平衡常数:K<K =K,故C正确;D项,该反应为气体分子数增大的反应,反应进
a b c
行时压强发生改变,所以温度一定时,当容器内压强不变时,反应达到平衡状态,故D正确;故选B。
例2 (2021•辽宁选择性考试,12)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化
剂浓度及时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是( )
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为0.012 mol·L-1·min-1
资料整理【淘宝店铺:向阳百分百】D.条件②,降冰片烯起始浓度为3.0 mol·L-1时,半衰期为62.5 min
【答案】B
【解析】A项,由题干图中曲线①②可知,其他条件相同时,催化剂浓度越大,反应所需要的时间更
短,故反应速率越大,A正确;B项,由题干图中曲线①③可知,其他条件相同时,降冰片烯浓度①是③
的两倍,所用时间①也是③的两倍,反应速率相等,故说明反应速率与降冰片烯浓度无关,B错误;C项,
由题干图中数据可知,条件①,反应速率为 =0.012 mol·L-1·min-1,C正确;D
项,反应物消耗一半所需的时间称为半衰期,由题干图中数据可知,条件②,降冰片烯起始浓度为3.0
mol·L-1时,半衰期为125min÷2=62.5 min,D正确;故选B。
对点1 T 温度下,向2L真空密闭容器中加入NO 固体,发生反应:NO(s) NO (g)+X(g) (未
0 2 3 2 3 2
配平),反应过程如图,下列说法正确的是( )
A.X可能为N
2
B.0~2 min用NO 表示的反应速率为1mol·min-1
2 3
C.第2min时逆反应速率大于第4min时逆反应速率
D.第4min时,保持温度和容积不变,向容器中再加入NO,混合气体颜色加深
2 3
【答案】B
【解析】A项,由图像可知,2min时NO 物质的量变化为2mol、NO 的物质的量变化为2mol,
2 3 2
NO、NO 系数比为1:1,根据元素守恒,X为NO,故A错误;B项,0~2 min内NO 物质的量变化为
2 3 2 2 3
2mol ,所以0~2 min用NO 表示的反应速率为1mol·min-1,故B正确;C项,第2min时NO 的浓度小于
2 3 2
第4min时NO 的浓度,所以第2min时逆反应速率小于第4min时逆反应速率,故C错误;D项,NO 是
2 2 3
固体,第4min时,保持温度和容积不变,向容器中再加入NO,平衡不移动,混合气体颜色不变,故D
2 3
错误;故选B。
资料整理【淘宝店铺:向阳百分百】对 点 2 丙 酮 是 重 要 的 有 机 合 成 原 料 , 可 以 由 过 氧 化 氢 异 丙 苯 合 成 。 其 反 应 为 :
,为了提高过氧化氢异丙苯的转化率,反应进行时需及时从溶液体系
中移出部分苯酚。过氧化氢异丙苯的转化率随反应时间的变化如图所示。设过氧化氢异丙苯的初始浓度为
x mol·L-1,反应过程中的液体体积变化忽略不计。下列说法不正确的是( )
A.a、c 两点丙酮的物质的量浓度相等
B.b、c两点的逆反应速率:v(b)>v(c)
C.100 ℃时,0~5 h 之间丙酮的平均反应速率为 0.14x mol·L-1·h-1
D.若b点处于化学平衡,则120℃时反应的平衡常数
【答案】D
【解析】A项,由于起始反应物浓度相同且a、c点转化率相同,故生成的丙酮浓度相等,A正确;B
项,由于反应物转化率b点(98%)>c点(70%),故生成物浓度:b点>c点,且b点温度大于c点,故逆反
应速率:b点>c点,B正确;C项,由图示知,100℃时,5 h时反应物的转化率为70%,故生成丙酮的浓
度=0.7x mol/L,则0~5 h丙酮的平均反应速率= ,C正确;D项,b点对应
反应物转化率为98%,故两种生成物浓度均为0.98x mol/L,但在反应过程中有部分苯酚被移出反应体系,
故平衡时体系中苯酚的浓度未知,故无法求算平衡常数,D错误; 故选D。
考法 2 化学平衡图象
化学平衡图像的三种类型
对于反应mA(g)+nB(g) pC(g)+qD(g),m+n>p+q,且ΔH>0。
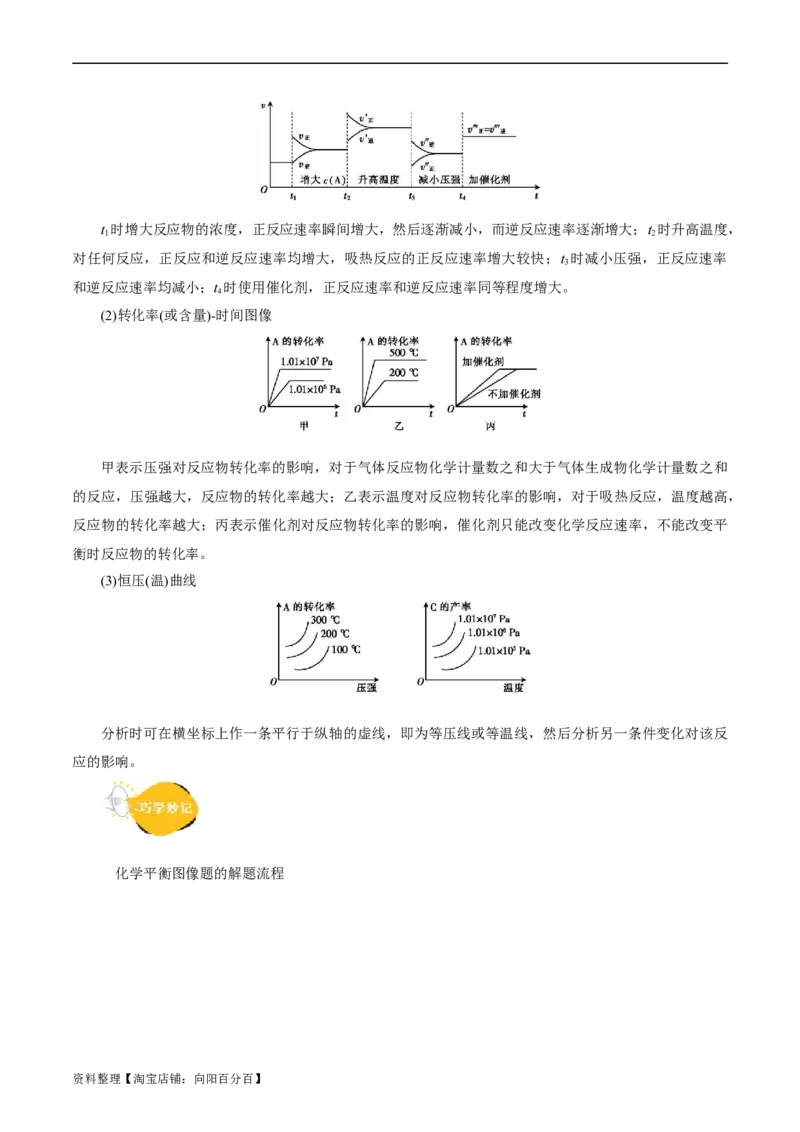
(1)速率-时间图像
资料整理【淘宝店铺:向阳百分百】t 时增大反应物的浓度,正反应速率瞬间增大,然后逐渐减小,而逆反应速率逐渐增大;t 时升高温度,
1 2
对任何反应,正反应和逆反应速率均增大,吸热反应的正反应速率增大较快;t 时减小压强,正反应速率
3
和逆反应速率均减小;t 时使用催化剂,正反应速率和逆反应速率同等程度增大。
4
(2)转化率(或含量)-时间图像
甲表示压强对反应物转化率的影响,对于气体反应物化学计量数之和大于气体生成物化学计量数之和
的反应,压强越大,反应物的转化率越大;乙表示温度对反应物转化率的影响,对于吸热反应,温度越高,
反应物的转化率越大;丙表示催化剂对反应物转化率的影响,催化剂只能改变化学反应速率,不能改变平
衡时反应物的转化率。
(3)恒压(温)曲线
分析时可在横坐标上作一条平行于纵轴的虚线,即为等压线或等温线,然后分析另一条件变化对该反
应的影响。
化学平衡图像题的解题流程
资料整理【淘宝店铺:向阳百分百】