考点 25 化学反应速率与平衡图象
【基础过关】
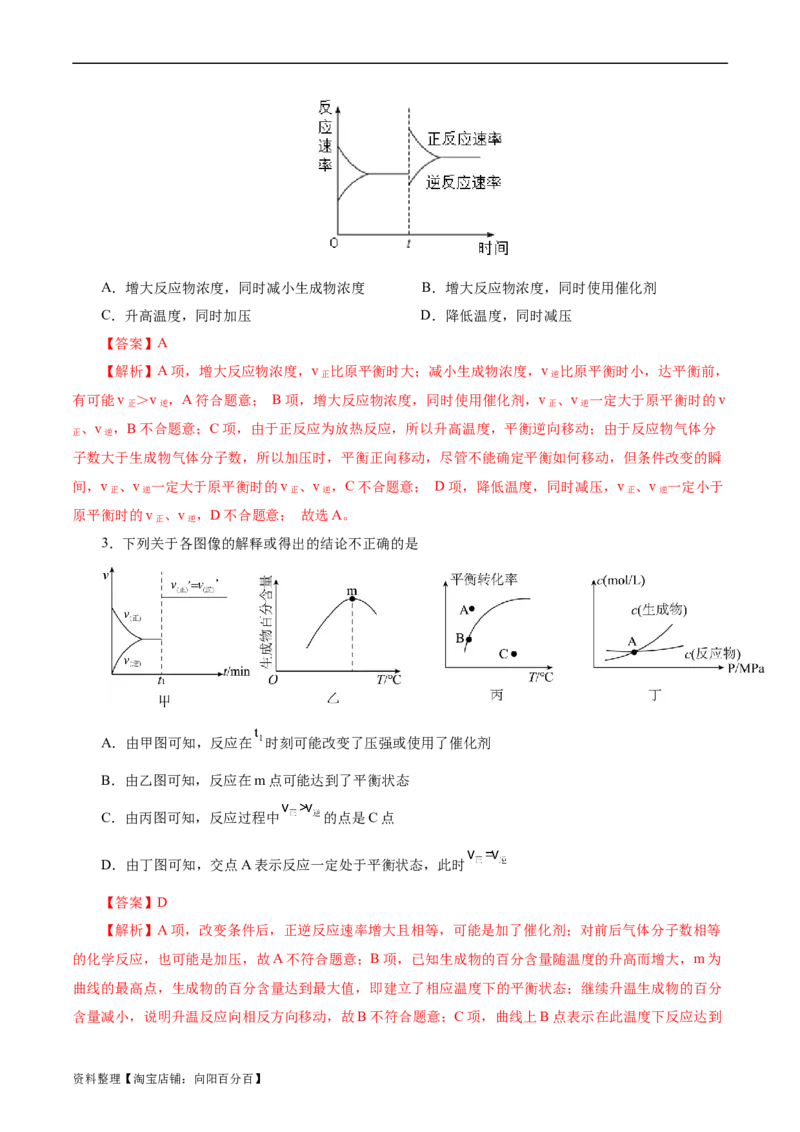
1.(2023·湘豫名校联考一轮复习诊断考试)某温度下,将2mol H 和2molI 充入密闭的刚性容器中发生
2 2
反应H(g)+I(g) 2HI(g),该反应的v-t图象如图所示,t 时刻测定容器内HI的物质的量为1mol,t 时
2 2 1 2
刻保持等温等容,抽走0.5mol HI。下列有关叙述正确的是( )
A.该温度下H(g)+I(g) 2HI(g)的平衡常数
2 2
B.反应过程中,可以利用气体的总压强保持不变来判断是否达到平衡
C.t 时刻,抽取HI的瞬间,v′(逆)在图象上的变化应该是c点
2
D.t 时刻,抽取HI后达到平衡后H 的百分含量减少
2 2
【答案】C
【解析】A项,t 时刻测定容器内HI的物质的量为1mol,根据反应方程式的系数可知,H 和I 各剩下
1 2 2
1.5mol,该反应前后气体物质的系数之和不变,可以用物质的量代替浓度计算平衡常数,故该温度下H(g)
2
+I(g) 2HI(g)的平衡常数 ,故A错误;B项,该反应前后气体总物质的量不变,恒
2
温恒容下,气体的总压强始终不变,故反应过程中,不能利用气体的总压强保持不变来判断是否达到平衡,
故B错误;C项,t 时刻,抽取HI的瞬间,生成物的浓度瞬间减小,则v′(逆)瞬间减小,则在图象上的变
2
化应该是c点,故C正确;D项,t 时刻,抽取HI后H 的百分含量增大,平衡正向移动,根据勒夏特列原
2 2
理可知,达到平衡后H 的百分含量还是增大,故D错误;故选C。
2
2.如图是关于反应A(g)+3B (g) 2C(g) ΔH<0的平衡移动图像,影响平衡移动的原因可能是
2 2
资料整理【淘宝店铺:向阳百分百】A.增大反应物浓度,同时减小生成物浓度 B.增大反应物浓度,同时使用催化剂
C.升高温度,同时加压 D.降低温度,同时减压
【答案】A
【解析】A项,增大反应物浓度,v 比原平衡时大;减小生成物浓度,v 比原平衡时小,达平衡前,
正 逆
有可能v >v ,A符合题意; B项,增大反应物浓度,同时使用催化剂,v 、v 一定大于原平衡时的v
正 逆 正 逆
、v ,B不合题意;C项,由于正反应为放热反应,所以升高温度,平衡逆向移动;由于反应物气体分
正 逆
子数大于生成物气体分子数,所以加压时,平衡正向移动,尽管不能确定平衡如何移动,但条件改变的瞬
间,v 、v 一定大于原平衡时的v 、v ,C不合题意; D项,降低温度,同时减压,v 、v 一定小于
正 逆 正 逆 正 逆
原平衡时的v 、v ,D不合题意; 故选A。
正 逆
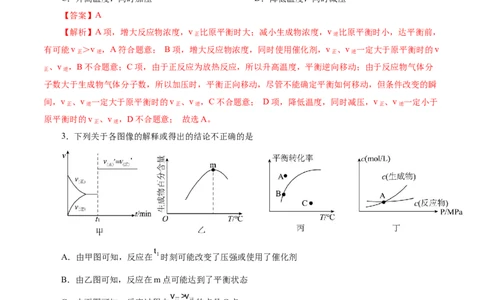
3.下列关于各图像的解释或得出的结论不正确的是
A.由甲图可知,反应在 时刻可能改变了压强或使用了催化剂
B.由乙图可知,反应在m点可能达到了平衡状态
C.由丙图可知,反应过程中 的点是C点
D.由丁图可知,交点A表示反应一定处于平衡状态,此时
【答案】D
【解析】A项,改变条件后,正逆反应速率增大且相等,可能是加了催化剂;对前后气体分子数相等
的化学反应,也可能是加压,故A不符合题意;B项,已知生成物的百分含量随温度的升高而增大,m为
曲线的最高点,生成物的百分含量达到最大值,即建立了相应温度下的平衡状态;继续升温生成物的百分
含量减小,说明升温反应向相反方向移动,故B不符合题意;C项,曲线上B点表示在此温度下反应达到
资料整理【淘宝店铺:向阳百分百】平衡时所能达到的最大转化率,A位于曲线以上,表示超过该温度下的最大转化率,此时平衡会向逆反应
方向移动,v逆>v正;C点位于曲线以下,表示未达到该温度下的最大转化率 ,此时平衡会向正反应方向
移动,v正>v逆,故C不符合题意;D项,A点时c(反应物)=c(生成物),不一定达到平衡状态,故D符合
题意;故选D。
4.一定温度下,X、Y、Z三种气体在某恒容密闭容器中发生反应,其中气体的物质的量变化曲线如
图所示。下列说法正确的是( )
A.Q点Y的正反应速率和逆反应速率相等
B.从开始到达到平衡时用X表示的平均反应速率是0.2mol·L-1·min-1
C.该反应的化学方程式可表示为:3X(g)+Z(g) 2Y(g)
D.达到平衡后,再充入氩气,反应速率增大
【答案】C
【解析】A项,Q点没有到平衡,Y的正反应速率和逆反应速率不相等,A错误;B项,从开始到达
到平衡时X的物质的量改变量为6-3=3mol,没有说明容器的体积,不能用X表示的平均反应速率,B错误;
C项,从开始到平衡,X、Z的物质的量减少,减少量分别为6-3=3mol,2-1=1mol,为反应物,Y的物质的
量增加为生成物,增加量为2-0=2mol,故方程式为3X(g)+Z(g) 2Y(g),C正确;D项,到平衡后,
充入氩气,各物质的浓度不变,反应速率不变,D错误;故选C。
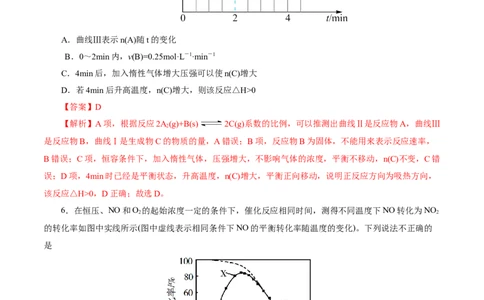
5.(2023·广东省茂名市电白区高三联考)在2L恒容密闭容器中发生反应2A(g)+B(s) 2C(g),各
2
物质的物质的量随反应时间t的部分变化曲线如图所示,下列说法正确的是( )
资料整理【淘宝店铺:向阳百分百】A.曲线Ⅲ表示n(A)随t的变化
B.0~2min内,v(B)=0.25mol·L-1·min-1
C.4min后,加入惰性气体增大压强可以使n(C)增大
D.若4min后升高温度,n(C)增大,则该反应△H>0
【答案】D
【解析】A项,根据反应2A(g)+B(s) 2C(g)系数的比例,可以推测出曲线Ⅱ是反应物A,曲线Ⅲ
2
是反应物B,曲线Ⅰ是生成物C的物质的量,A错误;B项,反应物B为固体,不能用来表示反应速率,
B错误;C项,恒容条件下,加入惰性气体,压强增大,不影响气体的浓度,平衡不移动,n(C)不变,C错
误;D项,4min时已经是平衡状态,升高温度,n(C)增大,平衡正向移动,说明正反应方向为吸热方向,
该反应△H>0,D正确;故选D。
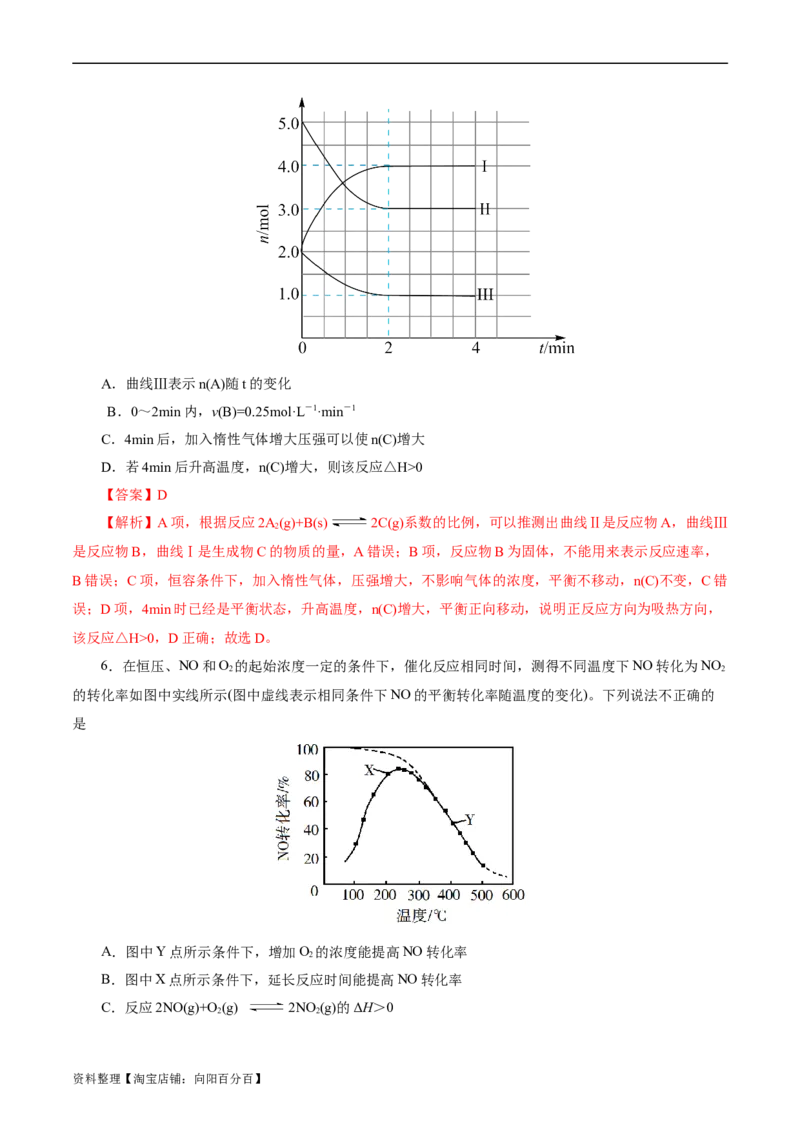
6.在恒压、NO和O 的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO
2 2
的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法不正确的
是
A.图中Y点所示条件下,增加O 的浓度能提高NO转化率
2
B.图中X点所示条件下,延长反应时间能提高NO转化率
C.反应2NO(g)+O (g) 2NO (g)的ΔH>0
2 2
资料整理【淘宝店铺:向阳百分百】D.380℃下,c (O )=5.0×10−4 mol·L−1,NO平衡转化率为50%,则平衡常数K>2000
起始 2
【答案】C
【解析】A项,Y点所示条件下达到平衡状态,增大氧气浓度平衡正向移动,NO转化率提高,A正确;
B项,X点没有达到平衡状态,平衡正向进行,延长时间导致消耗的NO量增多,导致NO转化率提高,B
正确;C项,升高温度NO平衡转化率降低,说明升高温度,化学平衡逆向移动,根据平衡移动原理:升
高温度,化学平衡向吸热方向移动,逆反应为吸热反应,则该反应的正反应为放热反应,所以△H<0,C
错误;D项,380℃下c (O )=5.0×10-4mol/L,反应正向移动,则c (O )<5.0×10-4mol/L,NO平衡转化率
起始 2 平衡 2
为50%,则平衡时c(NO)=c(NO ),化学平衡常数K= =2000,D正确。
2
7.一定温度下,向三个容积不等的恒容密闭容器(a<b<c)中分别投入2 mol NOCl,发生反应:
2NOCl(g) 2NO(g)+Cl(g)。t min后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述
2
正确的是( )
A.A点延长反应时间,可以提高NOCl的转化率
B.A、B两点的压强之比为25︰28
C.A点的平均反应速率大于C点的平均反应速率
D.容积为a L的容器达到平衡后再投入1 mol NOCl、1 mol NO,平衡不移动
【答案】D
【解析】A项,容器体积越大,反应速率越小,容积为a L的容器反应速率大于容积为b L的容器,t
min后, A点的转化率小于B,说明A点达到平衡状态,A点延长反应时间,NOCl的转化率不变,故A
错误;B项,A、B两点的气体物质的量比为25︰28,容器的体积不同,所以压强之比不是25︰28,故B
错误;C项,A为平衡点,A点的平均反应速率为0,C没有达到平衡,C点的平均反应速率大于0,故C
资料整理【淘宝店铺:向阳百分百】错误;D项,A点为平衡点,根据A点数据,K= ,再投入1 mol NOCl、1 mol NO,Q=
,Q=K,平衡不移动,故D正确;故选D。
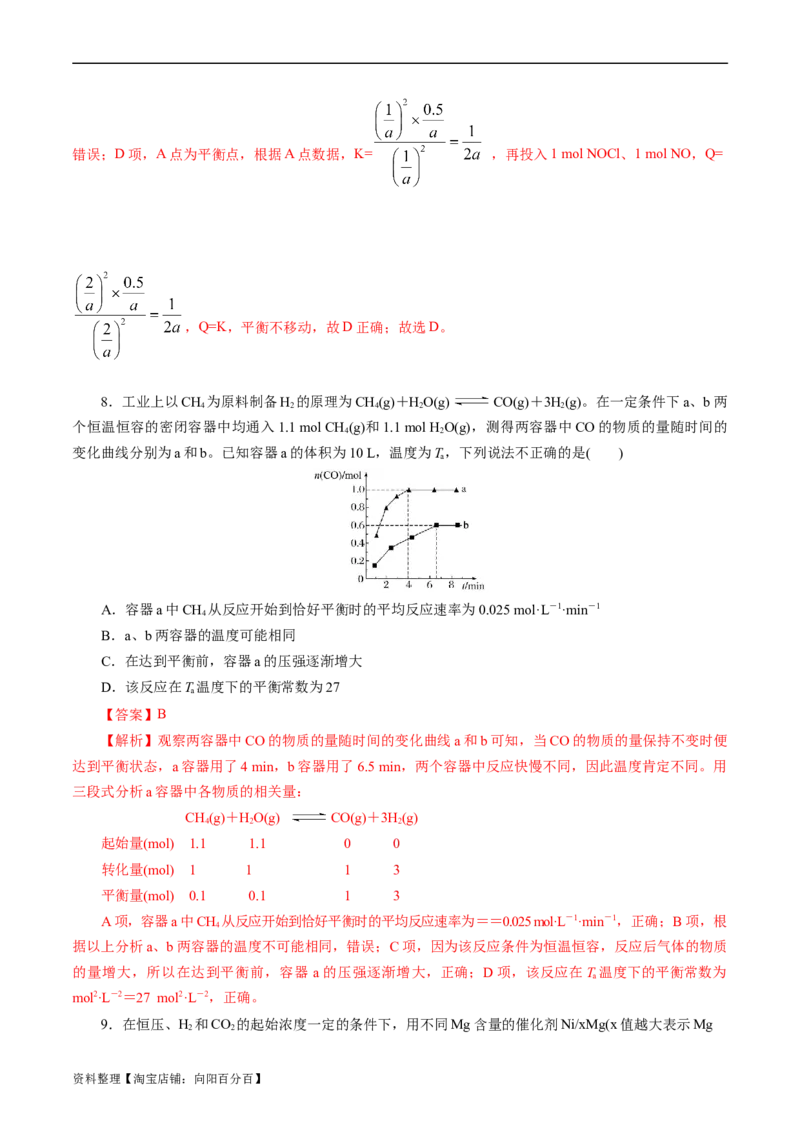
8.工业上以CH 为原料制备H 的原理为CH(g)+HO(g) CO(g)+3H(g)。在一定条件下a、b两
4 2 4 2 2
个恒温恒容的密闭容器中均通入1.1 mol CH (g)和1.1 mol H O(g),测得两容器中CO的物质的量随时间的
4 2
变化曲线分别为a和b。已知容器a的体积为10 L,温度为T,下列说法不正确的是( )
a
A.容器a中CH 从反应开始到恰好平衡时的平均反应速率为0.025 mol·L-1·min-1
4
B.a、b两容器的温度可能相同
C.在达到平衡前,容器a的压强逐渐增大
D.该反应在T温度下的平衡常数为27
a
【答案】B
【解析】观察两容器中CO的物质的量随时间的变化曲线a和b可知,当CO的物质的量保持不变时便
达到平衡状态,a容器用了4 min,b容器用了6.5 min,两个容器中反应快慢不同,因此温度肯定不同。用
三段式分析a容器中各物质的相关量:
CH(g)+HO(g) CO(g)+3H(g)
4 2 2
起始量(mol) 1.1 1.1 0 0
转化量(mol) 1 1 1 3
平衡量(mol) 0.1 0.1 1 3
A项,容器a中CH 从反应开始到恰好平衡时的平均反应速率为==0.025 mol·L-1·min-1,正确;B项,根
4
据以上分析a、b两容器的温度不可能相同,错误;C项,因为该反应条件为恒温恒容,反应后气体的物质
的量增大,所以在达到平衡前,容器 a的压强逐渐增大,正确;D项,该反应在T 温度下的平衡常数为
a
mol2·L-2=27 mol2·L-2,正确。
9.在恒压、H 和CO 的起始浓度一定的条件下,用不同Mg含量的催化剂Ni/xMg(x值越大表示Mg
2 2
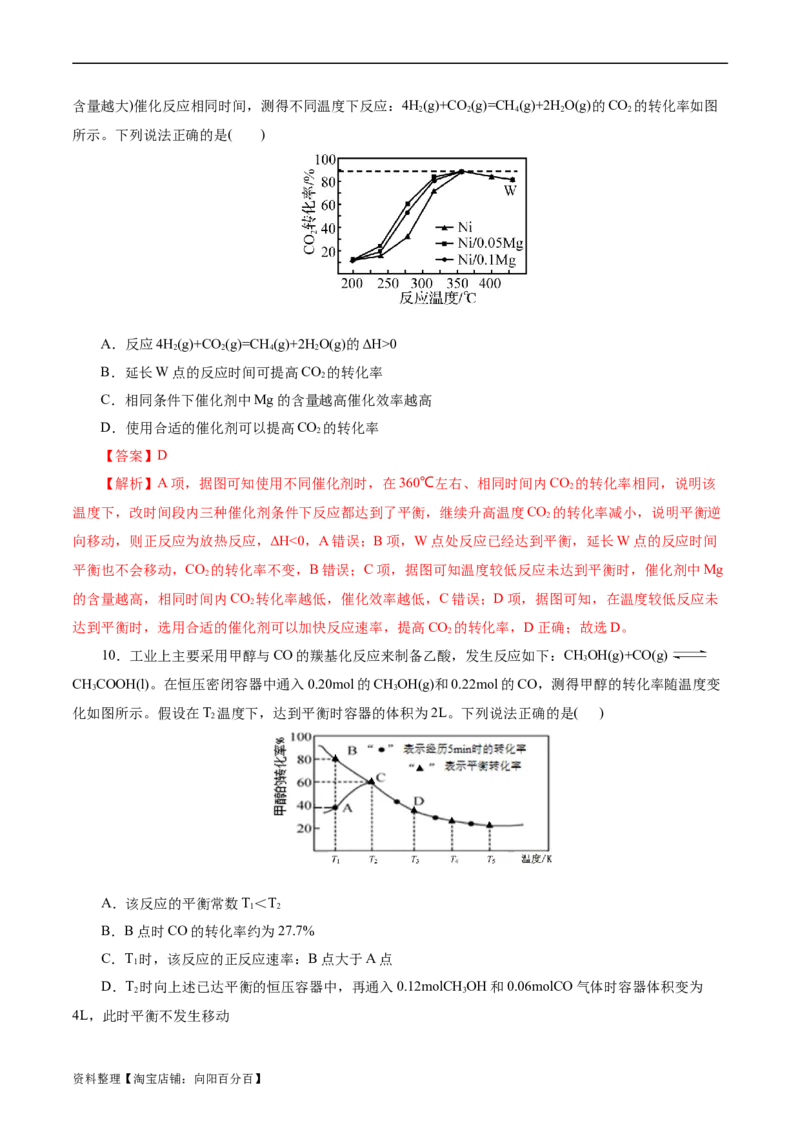
资料整理【淘宝店铺:向阳百分百】含量越大)催化反应相同时间,测得不同温度下反应:4H(g)+CO (g)=CH (g)+2HO(g)的CO 的转化率如图
2 2 4 2 2
所示。下列说法正确的是( )
A.反应4H(g)+CO (g)=CH (g)+2HO(g)的ΔH>0
2 2 4 2
B.延长W点的反应时间可提高CO 的转化率
2
C.相同条件下催化剂中Mg的含量越高催化效率越高
D.使用合适的催化剂可以提高CO 的转化率
2
【答案】D
【解析】A项,据图可知使用不同催化剂时,在360℃左右、相同时间内CO 的转化率相同,说明该
2
温度下,改时间段内三种催化剂条件下反应都达到了平衡,继续升高温度CO 的转化率减小,说明平衡逆
2
向移动,则正反应为放热反应,ΔH<0,A错误;B项,W点处反应已经达到平衡,延长W点的反应时间
平衡也不会移动,CO 的转化率不变,B错误;C项,据图可知温度较低反应未达到平衡时,催化剂中Mg
2
的含量越高,相同时间内CO 转化率越低,催化效率越低,C错误;D项,据图可知,在温度较低反应未
2
达到平衡时,选用合适的催化剂可以加快反应速率,提高CO 的转化率,D正确;故选D。
2
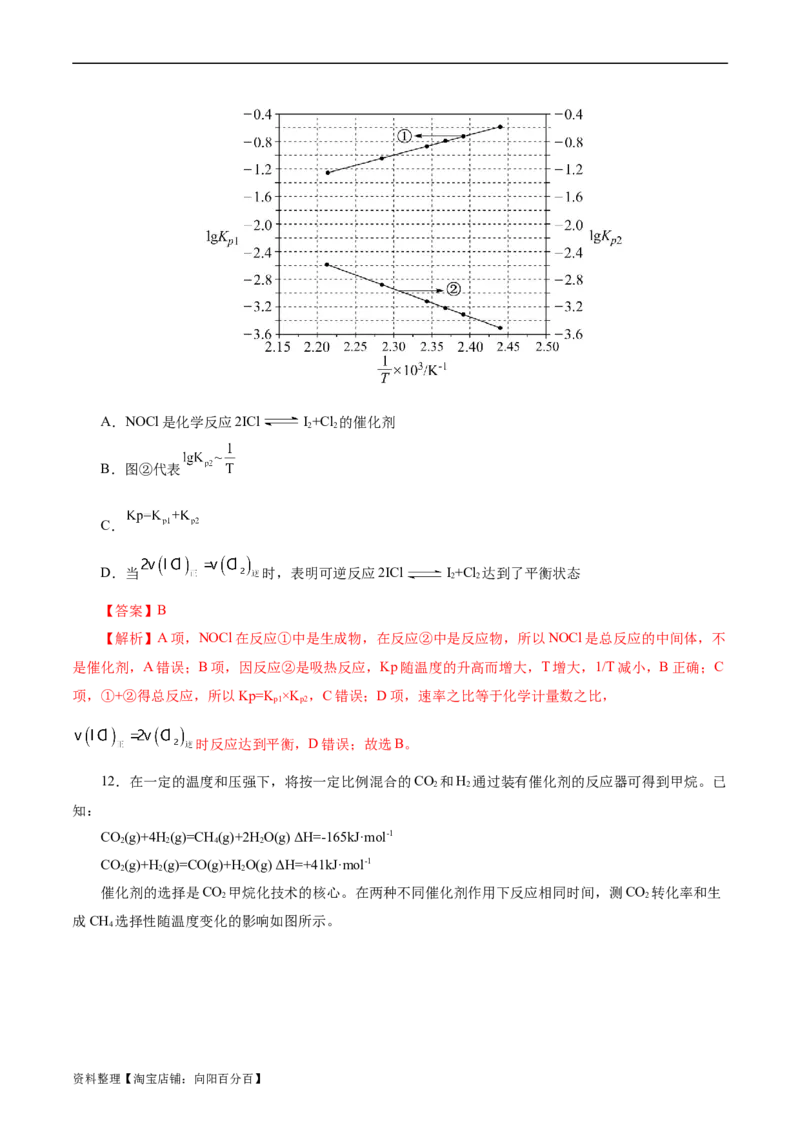
10.工业上主要采用甲醇与CO的羰基化反应来制备乙酸,发生反应如下:CHOH(g)+CO(g)
3
CHCOOH(l)。在恒压密闭容器中通入0.20mol的CHOH(g)和0.22mol的CO,测得甲醇的转化率随温度变
3 3
化如图所示。假设在T 温度下,达到平衡时容器的体积为2L。下列说法正确的是( )
2
A.该反应的平衡常数T<T
1 2
B.B点时CO的转化率约为27.7%
C.T 时,该反应的正反应速率:B点大于A点
1
D.T 时向上述已达平衡的恒压容器中,再通入0.12molCHOH和0.06molCO气体时容器体积变为
2 3
4L,此时平衡不发生移动
资料整理【淘宝店铺:向阳百分百】【答案】D
【解析】A项,根据图可知,甲醇的转化率随着温度的升高而减小,说明升高温度,平衡逆向移动,
平衡常数减小,因此平衡常数T>T,故A错误;B项,根据图像,B点时CHOH的转化率为80%,即反
1 2 3
应的甲醇为0.16mol,则反应的CO为0.16mol,CO的转化率= ×100%=72.7%,故B错误;C项,
T 时,A点未达到平衡,此时甲醇的浓度大于B点甲醇的浓度,浓度越大,反应速率越快,因此温度为T
1 1
时,该反应的正反应速率:B点小于A点,故C错误;D项,根据图像,温度为T 时, CHOH的转化率
2 3
为60%,即反应的甲醇为0.12mol,则反应的CO为0.12mol,平衡时甲醇为0.08mol,则反应的CO为
0.10mol,平衡时容器的体积为2L,平衡浓度分别为甲醇为0.04mol/L,CO为0.05mol/L。再通入0.12 mol
CHOH和0.06 mol CO的混合气体,容器体积变为4L,此时浓度分别为甲醇为
3
=0.05mol/L,CO为 =0.04mol/L,Q= =K= ,平衡不移动,故D
c
正确;故选D。
11.化学反应2ICl I+Cl,Kp可分为以下两步:
2 2
① ;
② 。
经测定和计算,得到 和 均为线性关系,如下图所示,已知反应②是吸热反应。则下
列说法正确的是( )
资料整理【淘宝店铺:向阳百分百】A.NOCl是化学反应2ICl I+Cl 的催化剂
2 2
B.图②代表
C.
D.当 时,表明可逆反应2ICl I+Cl 达到了平衡状态
2 2
【答案】B
【解析】A项,NOCl在反应①中是生成物,在反应②中是反应物,所以NOCl是总反应的中间体,不
是催化剂,A错误;B项,因反应②是吸热反应,Kp随温度的升高而增大,T增大,1/T减小,B正确;C
项,①+②得总反应,所以Kp=K ×K ,C错误;D项,速率之比等于化学计量数之比,
p1 p2
时反应达到平衡,D错误;故选B。
12.在一定的温度和压强下,将按一定比例混合的CO 和H 通过装有催化剂的反应器可得到甲烷。已
2 2
知:
CO(g)+4H(g)=CH (g)+2HO(g) ΔH=-165kJ·mol-1
2 2 4 2
CO(g)+H(g)=CO(g)+HO(g) ΔH=+41kJ·mol-1
2 2 2
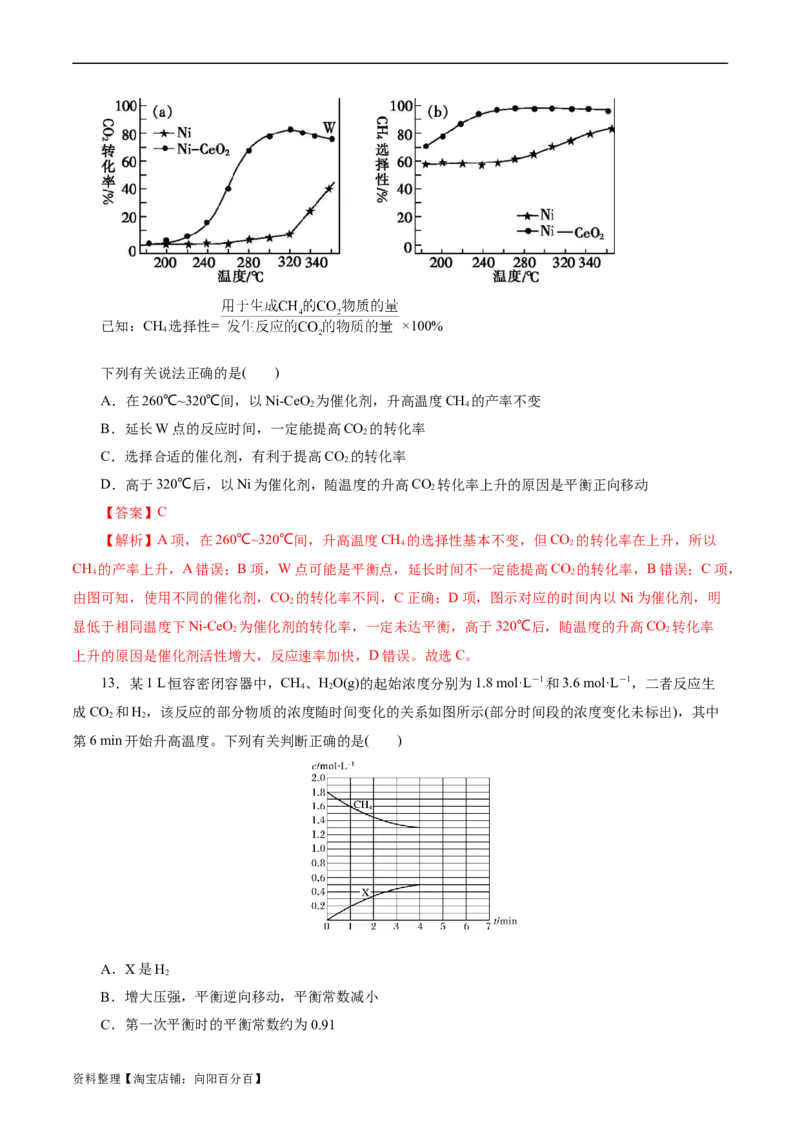
催化剂的选择是CO 甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测CO 转化率和生
2 2
成CH 选择性随温度变化的影响如图所示。
4
资料整理【淘宝店铺:向阳百分百】已知:CH 选择性= ×100%
4
下列有关说法正确的是( )
A.在260℃~320℃间,以Ni-CeO 为催化剂,升高温度CH 的产率不变
2 4
B.延长W点的反应时间,一定能提高CO 的转化率
2
C.选择合适的催化剂,有利于提高CO 的转化率
2
D.高于320℃后,以Ni为催化剂,随温度的升高CO 转化率上升的原因是平衡正向移动
2
【答案】C
【解析】A项,在260℃~320℃间,升高温度CH 的选择性基本不变,但CO 的转化率在上升,所以
4 2
CH 的产率上升,A错误;B项,W点可能是平衡点,延长时间不一定能提高CO 的转化率,B错误;C项,
4 2
由图可知,使用不同的催化剂,CO 的转化率不同,C正确;D项,图示对应的时间内以Ni为催化剂,明
2
显低于相同温度下Ni-CeO 为催化剂的转化率,一定未达平衡,高于320℃后,随温度的升高CO 转化率
2 2
上升的原因是催化剂活性增大,反应速率加快,D错误。故选C。
13.某1 L恒容密闭容器中,CH、HO(g)的起始浓度分别为1.8 mol·L-1和3.6 mol·L-1,二者反应生
4 2
成CO 和H,该反应的部分物质的浓度随时间变化的关系如图所示(部分时间段的浓度变化未标出),其中
2 2
第6 min开始升高温度。下列有关判断正确的是( )
A.X是H
2
B.增大压强,平衡逆向移动,平衡常数减小
C.第一次平衡时的平衡常数约为0.91
资料整理【淘宝店铺:向阳百分百】D.若5 min时向容器中再加入0.7 mol的CH 和0.7 mol的CO,则平衡正向移动
4 2
【答案】C
【解析】根据图像0~4 min CH 减少0.5 mol·L-1,X增加0.5 mol·L-1,则X为CO ,A项错误;温度
4 2
不变时,增大压强,平衡常数不变,B项错误;4 min时,反应第一次达到平衡状态:
CH(g)+2HO(g) CO(g)+4H(g)
4 2 2 2
起始/mol·L-1 1.8 3.6 0 0
转化/mol·L-1 0.5 1.0 0.5 2.0
平衡/mol·L-1 1.3 2.6 0.5 2.0
平衡常数K= mol2·L-2≈0.91 mol2·L-2,C项正确;若5 min时向容器中再加入0.7 mol的CH 和0.7 mol
4
的CO,则浓度商Q= mol2·L-2≈1.42 mol2·L-2>0.91 mol2·L-2,反应逆向移动,D项错误。
2
14.已知:乙二醛可被催化氧化为乙醛酸,其反应为2OHC—CHO(g)+O(g) 2OHC—COOH(g)
2
ΔH。一定条件下,按照=的投料比进行上述反应,乙二醛的平衡转化率(α)和催化剂的催化效率随温度的
变化如图所示。下列叙述正确的是( )
A.ΔH>0
B.b点时,乙二醛的体积分数为33.33%
C.生成乙醛酸的速率:v(a)>v(b)>v(c)
D.a、b、c三点中,a点乙醛酸的体积分数最小
【答案】B
【解析】A项,随着温度的升高,转化率降低,这说明升高温度平衡向逆反应方向移动,则ΔH<0,
错误;B项,b点时转化率是60%,则根据方程式可知
2OHC—CHO(g)+O(g) 2OHC—COOH(g)
2
起始量/mol 2 1 0
转化量/mol 1.2 0.6 1.2
平衡量/mol 0.8 0.4 1.2
因此乙二醛的体积分数为×100%≈33.33%,正确;C项,温度越高,催化效率越高,化学反应速率越快,
而b点的温度低、催化效率高,c点的温度高、催化效率低,所以无法比较速率大小,错误;D项,a、b、
c三点中,a点转化率最大,则乙醛酸的体积分数最大,错误。
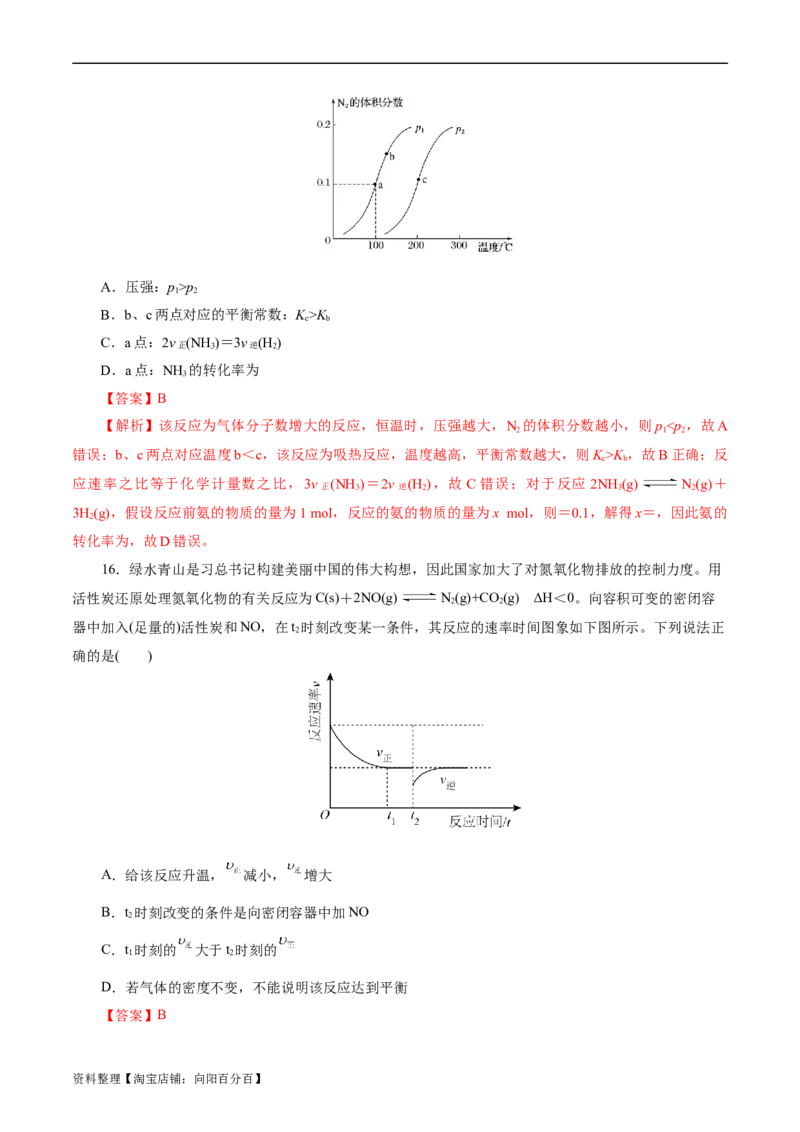
15.一定条件下,反应2NH (g) N(g)+3H(g) ΔH>0,达到平衡时N 的体积分数与温度、压
3 2 2 2
强的关系如图所示。下列说法正确的是( )
资料整理【淘宝店铺:向阳百分百】A.压强:p>p
1 2
B.b、c两点对应的平衡常数:K>K
c b
C.a点:2v (NH )=3v (H )
正 3 逆 2
D.a点:NH 的转化率为
3
【答案】B
【解析】该反应为气体分子数增大的反应,恒温时,压强越大,N 的体积分数越小,则p
K ,故B正确;反
c b
应速率之比等于化学计量数之比,3v (NH )=2v (H ),故 C 错误;对于反应 2NH (g) N(g)+
正 3 逆 2 3 2
3H(g),假设反应前氨的物质的量为1 mol,反应的氨的物质的量为x mol,则=0.1,解得x=,因此氨的
2
转化率为,故D错误。
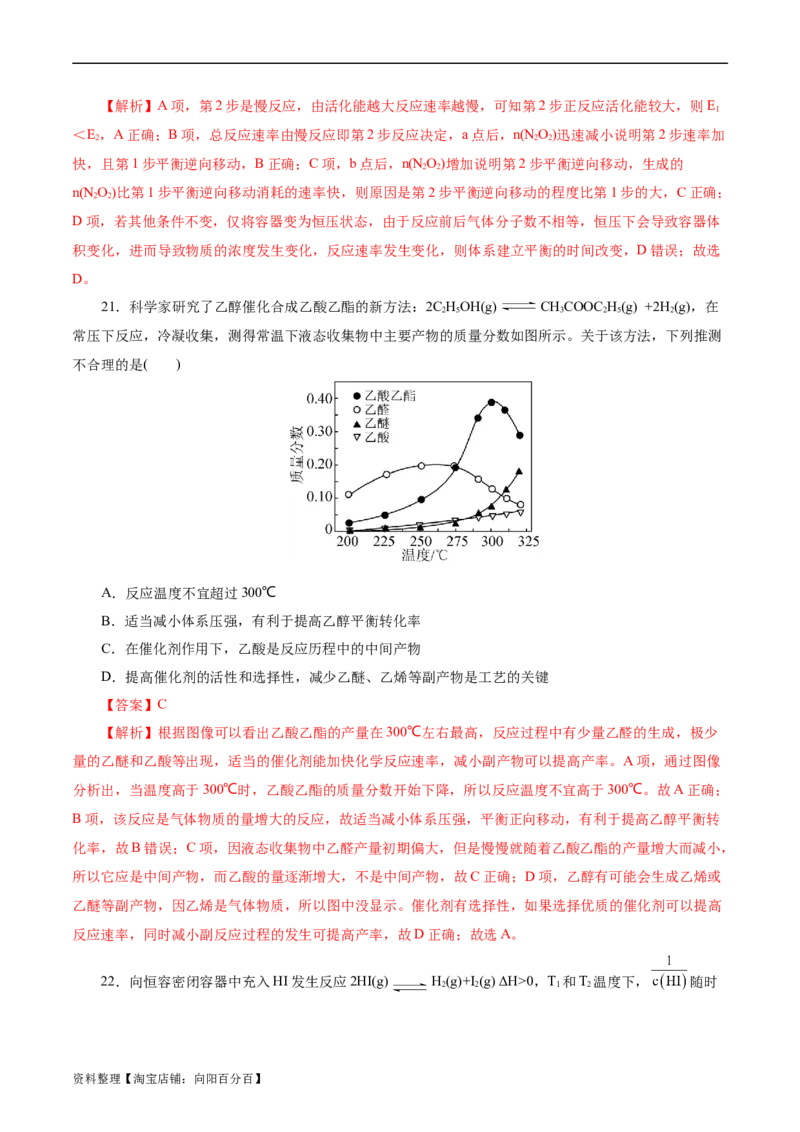
16.绿水青山是习总书记构建美丽中国的伟大构想,因此国家加大了对氮氧化物排放的控制力度。用
活性炭还原处理氮氧化物的有关反应为C(s)+2NO(g) N(g)+CO (g) ΔH<0。向容积可变的密闭容
2 2
器中加入(足量的)活性炭和NO,在t 时刻改变某一条件,其反应的速率时间图象如下图所示。下列说法正
2
确的是( )
A.给该反应升温, 减小, 增大
B.t 时刻改变的条件是向密闭容器中加NO
2
C.t 时刻的 大于t 时刻的
1 2
D.若气体的密度不变,不能说明该反应达到平衡
【答案】B
资料整理【淘宝店铺:向阳百分百】【解析】A项,升高温度,任何反应的反应速率均增大,故给该反应升温, 增大, 增大,A错
误;B项,由图像可知,压强一定条件下,t 时刻改变条件以后,逆反应速率突然减小,达到新平衡时,
2
与原反应速率相同,故改变的条件是向密闭容器中加NO,B正确;C项,由B项分析可知,t2时刻改变的
条件是向密闭容器中加NO,正反应速率增大,逆反应速率减小,则t 时刻的 小于t 时刻的 ,C错误;
1 2
D项,由题干反应方程式可知,反应前后气体的物质的量保持不变,即恒温下容器的体积保持不变,反应
正向气体质量增加,故若气体的密度不变,则气体质量不变,说明该反应达到平衡,D错误;故选B。
17.T℃时,向容积为2L的恒容密闭容器中充入SO 和O 发生反应2SO (g)+O(g) 2SO (g),容
1 2 2 2 2 3
器中各组分的物质的量随时间变化如图所示。下列说法正确的是( )
A.a、b两点反应速率υ<υ
a b
B.0~t 时间段,反应速率υ(SO )= mol∙L−1∙min−1
2 3
C.t 时刻,向容器中充入一定体积的气体氦,使容器中气体总的压强增大,则υ 、υ 均增大
2 正 逆
D.若反应在T℃进行(T <T),反应进行t 分钟后,n(SO )<0.8mol
2 2 1 1 2
【答案】B
【解析】A项,根据浓度越大,反应速率越大,因此a、b两点反应速率υ<υ,故A错误;B项,根
b a
据图中改变量之比等于计量系数之比得到0~t 时间段SO 物质的量改变量为0.8mol,则0~t 时间段,反
2 3 2
应速率υ(SO )= mol∙L−1∙min−1,故B正确;C项,t 时刻,向容器中充入一定体积的气体氦,
3 2
使容器中气体总的压强增大,但反应各物质浓度没有改变,因此υ 、υ 均不变,故C错误;D项,若反
正 逆
应在T℃进行(T <T),根据温度越高,反应速率越快,T℃的速率比T℃的速率慢,因此反应进行t 分钟
2 2 1 2 1 1
后,SO 物质的量改变量小于0.2mol,因此n(SO ) >0.8mol,故D错误。故选B。
2 2
18.25℃时,将20mL3x mol·L-1NaAsO、20mL3x mol·L-1I 和20mL NaOH溶液混合,发生反应:
3 3 2
资料整理【淘宝店铺:向阳百分百】AsO3−(aq)+I(aq)+ 2OH−(aq)= AsO3−(aq)+2I(aq)+HO(l)。溶液中c(AsO3−)与反应时间(t)的关系如图所示。
3 2 4 - 2 4
下列说法正确的是
A.0~ t min用HO表示的平均反应速率为
1 2
B.当2v (AsO3−)=v (I-)时,反应达到平衡状态
正 3 逆
C.a点的逆反应速率小于b点的正反应速率
D.平衡时溶液的pH=13,则该反应的平衡常数
【答案】C
【解析】A项,一般不用纯固体、纯液体表示反应速率,不能用HO表示该反应的平均反应速率,故
2
A错误;B项,依据反应速率之比等于化学计量数之比,当2v (AsO3−)=v (I-)时,正逆反应速率相等,反
正 3 逆
应达到平衡状态,故B错误;C项,由图可知,a到b的过程中,反应一直正向进行,正反应速率一直减
小,逆反应速率一直增大,直到增大到与正反应速率相等,反应达到平衡状态,在反应达到平衡前,逆反
应速率均小于正反应速率,a点和b点均未达到平衡状态,且a到b反应逐渐趋于平衡,a点的逆反应速率
小于b点的正反应速率,故C正确;D项,根据题意,溶液混合后起始时,c(AsO3−)= c(I-)= x mol·L-1,由
3
图可知, 平衡时c(AsO3−)=y mol·L-1,c(I)= 2y mol·L-1,c(AsO3−)= c(I)=(x- y) mol·L-1,平衡时溶液的
4 2 3 2
pH=13,则c(OH-)=0.1mol·L-1,反应的平衡常数 ,故D错误;故选
C。
19.已知:N(g)+3H(g) 2NH (g) ΔH= -m kJ·mol-1.在 2 L 容积不变的密闭容器中通入 1 mol N
2 2 3 2
和3 molH ,在温度分别为T T 下,测得NH 的产率随时间变化如图。下列说法正确的是( )
2 1 、 2 3
资料整理【淘宝店铺:向阳百分百】A.T﹥T,ΔH﹥0
2 1
B.a,b两点的反应速率: >
a b
C.平衡时,通入氩气平衡正向移动
D.达到平衡时,放出热量为 m kJ
【答案】B
【解析】A项,由题干图示信息可知,T 条件下先达到平衡,说明T 时反应速率快,故有T﹥T,温
2 2 2 1
度越高,NH 的百分含量越小,说明升高温度,平衡逆向移动,故ΔH<0,A错误;B项,a,b两点对应
3
的温度分别是T、T,由A项分析可知,T﹥T,故反应速率:v >v ,B正确;C项,由题干信息可知,
2 1 2 1 a b
容器为恒温恒容,故平衡时,通入氩气反应体系各物质的浓度均不改变,正逆反应速率仍然相等,故平衡
不移动,C错误;D项,由于该反应是一个可逆反应,在 2 L 容积不变的密闭容器中通入 1 mol N 和3
2
molH ,达到平衡时,不可能完全进行,则放出热量小于 m kJ,D错误;故选B。
2
20.已知:2NO(g)+CO(g) 2NO (g)的反应历程分两步:
2 2
第1步:2NO(g) NO(g) (快) ΔH<0
2 2 1
第2步:NO(g)+O(g) 2NO (g) (慢) ΔH<0
2 2 2 2 2
在固定容积的容器中充入一定量NO和O 发生上述反应,测得体系中部分物质的物质的量(n)随温度
2
(T)的变化如图所示。下列说法错误的是( )
A.第1步、第2步正反应活化能分别为E、E,则E<E
1 2 1 2
B.a点后,n(N O)迅速减小的原因是第1步平衡逆向移动,第2步速率加快
2 2
C.b点后,n(N O)增加的原因是第2步平衡逆向移动的程度比第1步的大
2 2
D.若其他条件不变,仅将容器变为恒压状态,则体系建立平衡的时间不变
【答案】D
资料整理【淘宝店铺:向阳百分百】【解析】A项,第2步是慢反应,由活化能越大反应速率越慢,可知第2步正反应活化能较大,则E
1
<E,A正确;B项,总反应速率由慢反应即第2步反应决定,a点后,n(N O)迅速减小说明第2步速率加
2 2 2
快,且第1步平衡逆向移动,B正确;C项,b点后,n(N O)增加说明第2步平衡逆向移动,生成的
2 2
n(N O)比第1步平衡逆向移动消耗的速率快,则原因是第2步平衡逆向移动的程度比第1步的大,C正确;
2 2
D项,若其他条件不变,仅将容器变为恒压状态,由于反应前后气体分子数不相等,恒压下会导致容器体
积变化,进而导致物质的浓度发生变化,反应速率发生变化,则体系建立平衡的时间改变,D错误;故选
D。
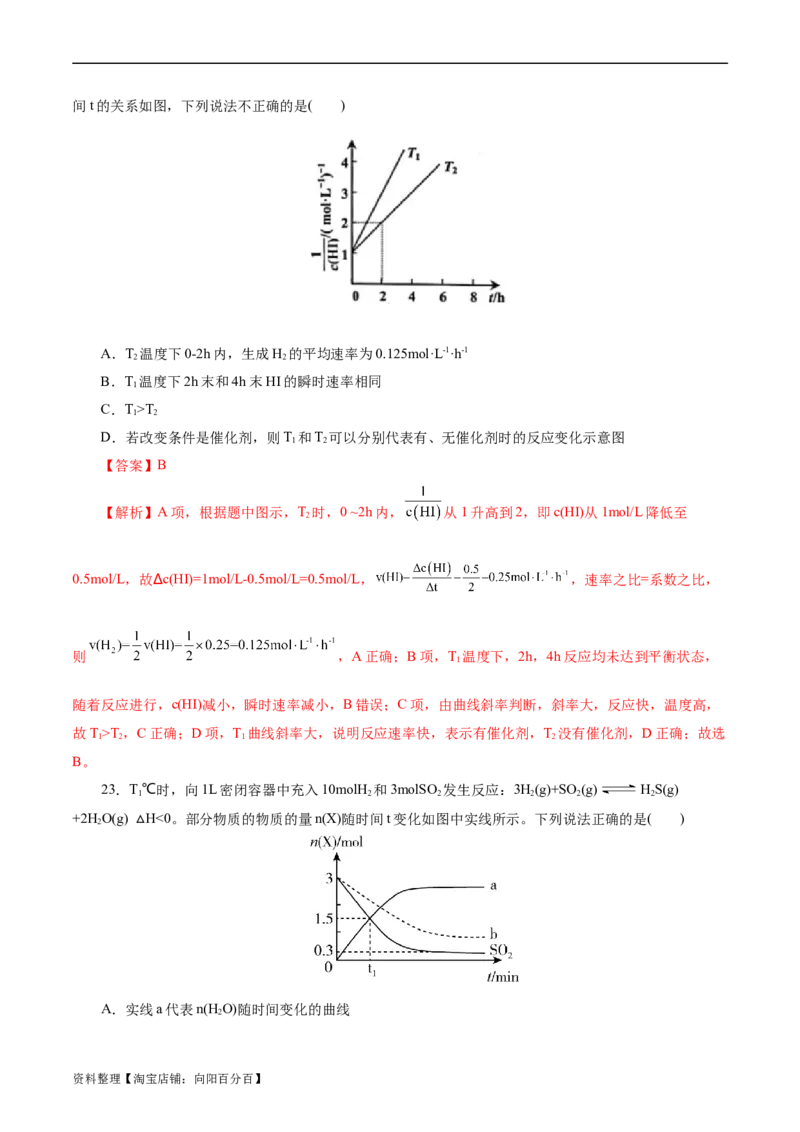
21.科学家研究了乙醇催化合成乙酸乙酯的新方法:2C HOH(g) CHCOOC H(g) +2H (g),在
2 5 3 2 5 2
常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。关于该方法,下列推测
不合理的是( )
A.反应温度不宜超过300℃
B.适当减小体系压强,有利于提高乙醇平衡转化率
C.在催化剂作用下,乙酸是反应历程中的中间产物
D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键
【答案】C
【解析】根据图像可以看出乙酸乙酯的产量在300℃左右最高,反应过程中有少量乙醛的生成,极少
量的乙醚和乙酸等出现,适当的催化剂能加快化学反应速率,减小副产物可以提高产率。A项,通过图像
分析出,当温度高于300℃时,乙酸乙酯的质量分数开始下降,所以反应温度不宜高于300℃。故A正确;
B项,该反应是气体物质的量增大的反应,故适当减小体系压强,平衡正向移动,有利于提高乙醇平衡转
化率,故B错误;C项,因液态收集物中乙醛产量初期偏大,但是慢慢就随着乙酸乙酯的产量增大而减小,
所以它应是中间产物,而乙酸的量逐渐增大,不是中间产物,故C正确;D项,乙醇有可能会生成乙烯或
乙醚等副产物,因乙烯是气体物质,所以图中没显示。催化剂有选择性,如果选择优质的催化剂可以提高
反应速率,同时减小副反应过程的发生可提高产率,故D正确;故选A。
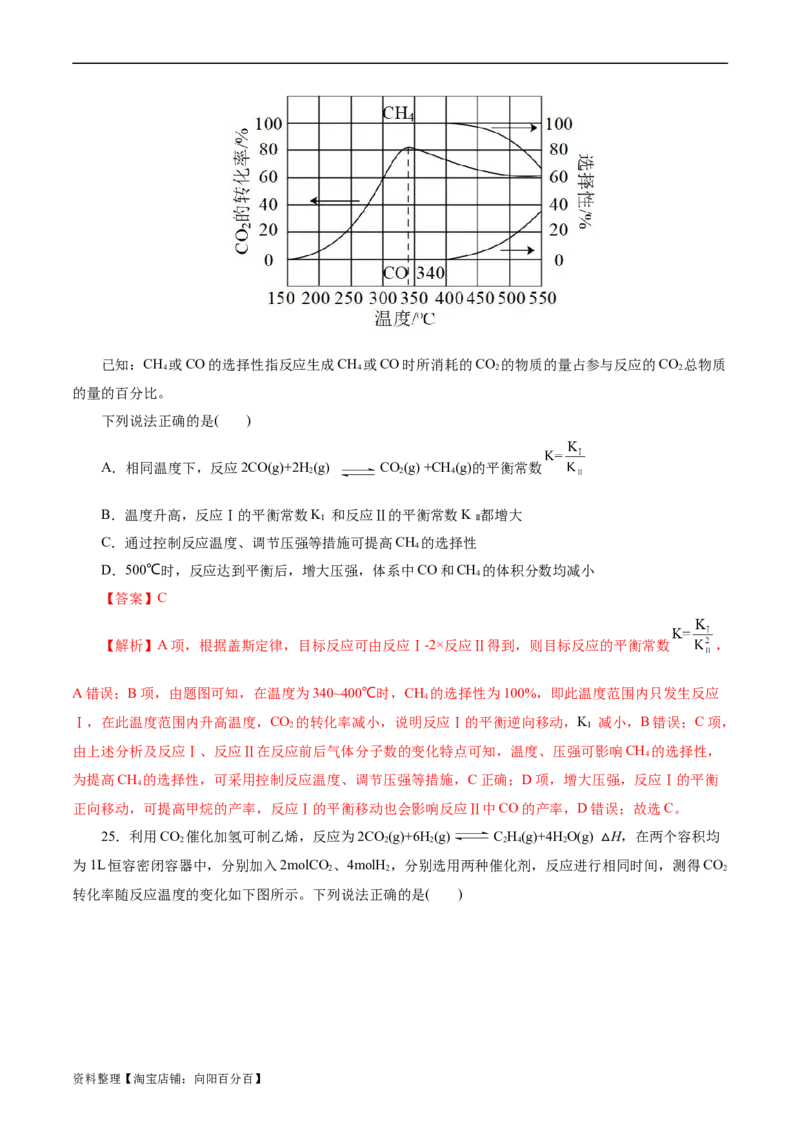
22.向恒容密闭容器中充入HI发生反应2HI(g) H(g)+I (g) ΔH>0,T 和T 温度下, 随时
2 2 1 2
资料整理【淘宝店铺:向阳百分百】间t的关系如图,下列说法不正确的是( )
A.T 温度下0-2h内,生成H 的平均速率为0.125mol·L-1·h-1
2 2
B.T 温度下2h末和4h末HI的瞬时速率相同
1
C.T>T
1 2
D.若改变条件是催化剂,则T 和T 可以分别代表有、无催化剂时的反应变化示意图
1 2
【答案】B
【解析】A项,根据题中图示,T 时,0 ~2h内, 从1升高到2,即c(HI)从1mol/L降低至
2
0.5mol/L,故∆c(HI)=1mol/L-0.5mol/L=0.5mol/L, ,速率之比=系数之比,
则 ,A正确;B项,T 温度下,2h,4h反应均未达到平衡状态,
1
随着反应进行,c(HI)减小,瞬时速率减小,B错误;C项,由曲线斜率判断,斜率大,反应快,温度高,
故T>T,C正确;D项,T 曲线斜率大,说明反应速率快,表示有催化剂,T 没有催化剂,D正确;故选
1 2 1 2
B。
23.T℃时,向1L密闭容器中充入10molH 和3molSO 发生反应:3H(g)+SO(g) HS(g)
1 2 2 2 2 2
+2H O(g) H<0。部分物质的物质的量n(X)随时间t变化如图中实线所示。下列说法正确的是( )
2
△
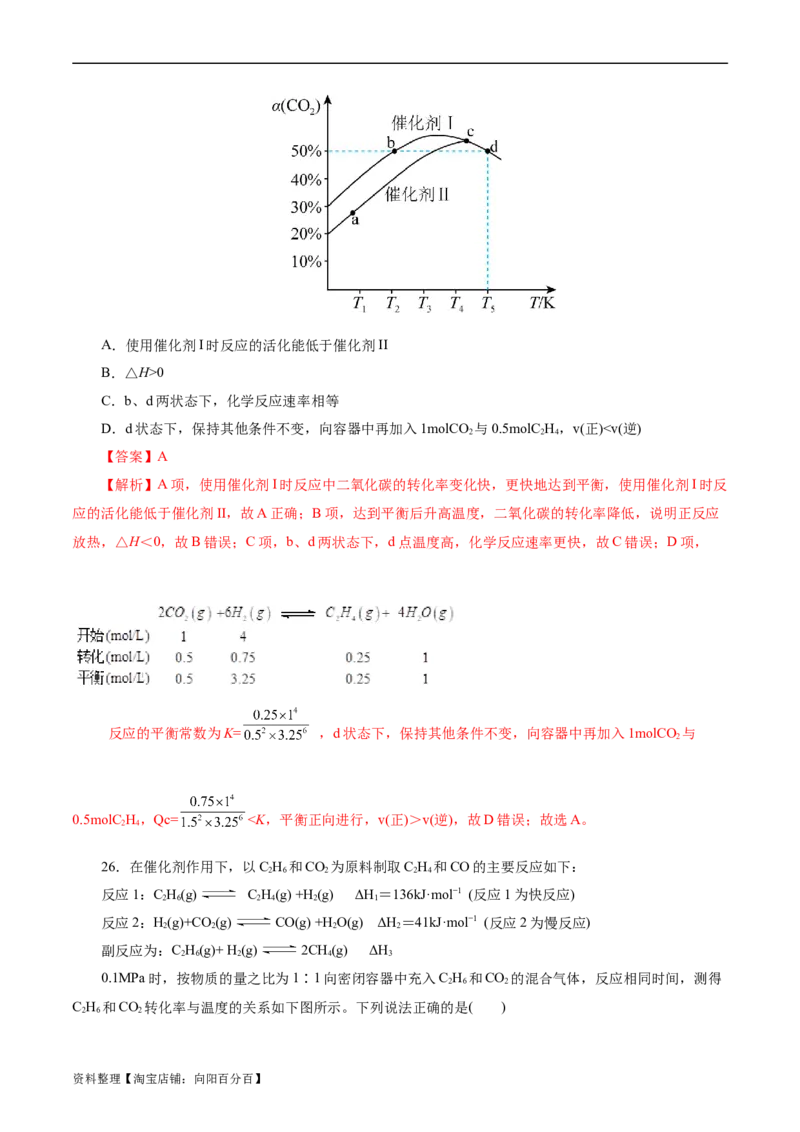
A.实线a代表n(H O)随时间变化的曲线
2
资料整理【淘宝店铺:向阳百分百】B.tmin时,v (SO )0
C.b、d两状态下,化学反应速率相等
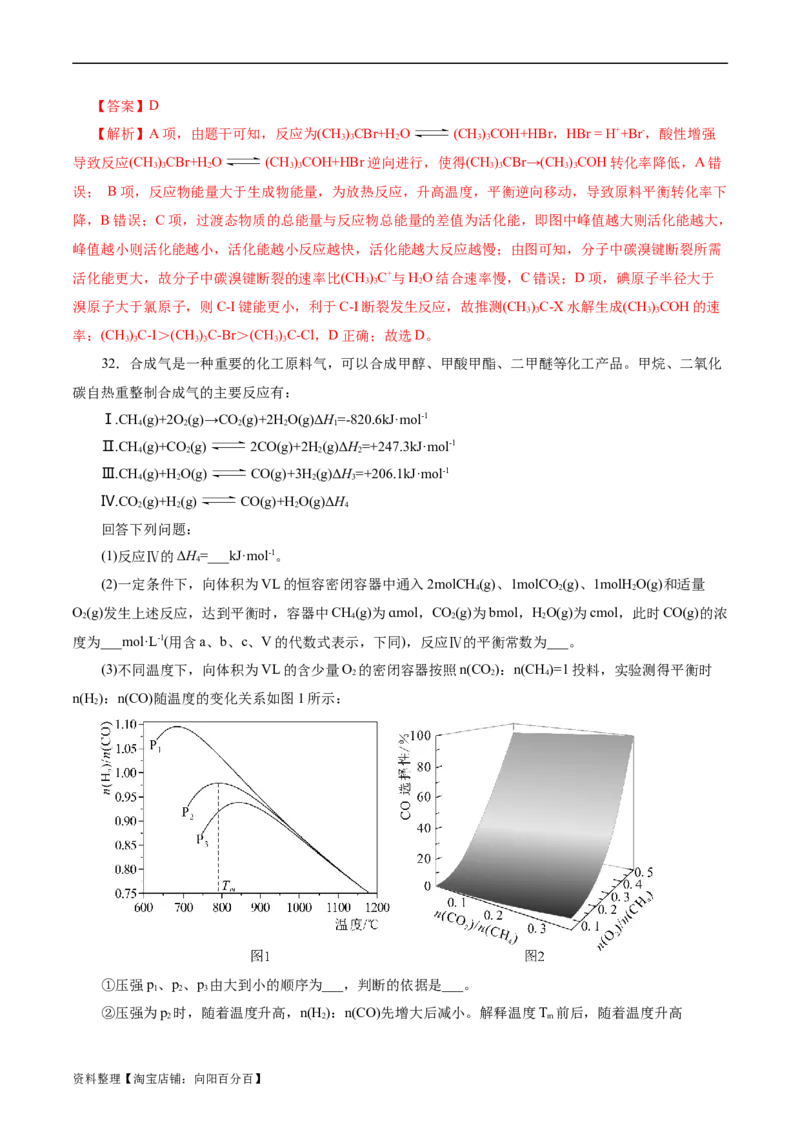
D.d状态下,保持其他条件不变,向容器中再加入1molCO 与0.5molC H,v(正)P >P 反应Ⅱ、Ⅲ是气体分子数目增大的反应,减小压强平衡正向移动,n(H )增加的程度大
3 2 1 2
于n(CO)
②升高温度平衡Ⅱ、Ⅲ、Ⅳ均正向移动,TT 后,对反应Ⅳ的促进作用更大,n(CO)增加的更多
2 m
③AC
【解析】(1)根据盖斯定律,反应Ⅳ=Ⅱ-Ⅲ,则ΔH=ΔH-ΔH=+247.3kJ·mol-1-
4 2 3
206.1kJ·mol-1=+41.2kJ·mol-1;(2)通入2molCH (g)、1molCO (g)、1molH O(g)和适量O(g),达到平衡时,容
4 2 2 2
器中CH(g)为ɑmol,CO(g)为bmol,HO(g)为cmol,设H(g)的物质的量为x,CO(g)的物质的量为y,由
4 2 2 2
C、H原子守恒有:{ ,解得x=5-2a-c,y=3-a-b,即n(H )=( 5-2a-
2
c)mol,n(CO)=( 3-a-b)mol,此时c(CO)= = mol·L-1;
则K= = ;(3)①由反应可知,反应Ⅱ、Ⅲ是气体分子数目增大的反应,减小
压强平衡正向移动,n(H )增加的程度大于n(CO),则压强p、p、p 由大到小的顺序为P>P >P ,故答案为:
2 1 2 3 3 2 1
P>P >P ;反应Ⅱ、Ⅲ是气体分子数目增大的反应,减小压强平衡正向移动,n(H )增加的程度大于
3 2 1 2
n(CO); ②由图1可知,压强为p 时,随着温度升高,n(H ):n(CO)先增大后减小,原因是反应Ⅱ、Ⅲ、
2 2
Ⅳ均为吸热反应,升高温度平衡Ⅱ、Ⅲ、Ⅳ均正向移动,TT 后,对反应Ⅳ的促进作用更大,n(CO)增加的更多,故答案为:升高温度
2 m
资料整理【淘宝店铺:向阳百分百】平衡Ⅱ、Ⅲ、Ⅳ均正向移动,TT 后,对反应Ⅳ的促进作用更大,n(CO)增加的更多;③A项,根据图2,提高n(O ):n(CH)比例,可
m 2 4
提高CO的选择性,故A符合题意;B项,根据图2,降低n(CO):n(CH)比例,不能提高CO的选择性,
2 4
故B不符合题意;C项,根据图1,升高温度、增大压强时n(H ):n(CO)比例减小,即CO的选择性提高,
2
故C符合题意;D项,根据C项分析,低温、低压时CO的选择性降低,故D不符合题意;故选AC。
33.异丁烯为重要的化工原料,工业上可采用叔丁醇(TBA)气相脱水法制备高纯异丁烯产品,主要涉
及以下反应:
反应1(主反应):(CH)C-OH(g) →(CH )C=CH (g)+HO(g)
3 3 3 2 2 2
反应2(副反应):2(CH)C=CH (g)→(CH )C=CH-C(CH )(g)
3 2 2 3 2 3 3
(1)标准摩尔生成焓是指由稳态单质生成1 mol该化合物的焓变,几种物质的标准生成焓如表,求反应
1的ΔH =_______ kJ·mol-l。
组分 HO (CH)C-OH (CH)C=CH
2 3 3 3 2 2
焓变kJ·mol-l -241.83 -339.21 -17.1
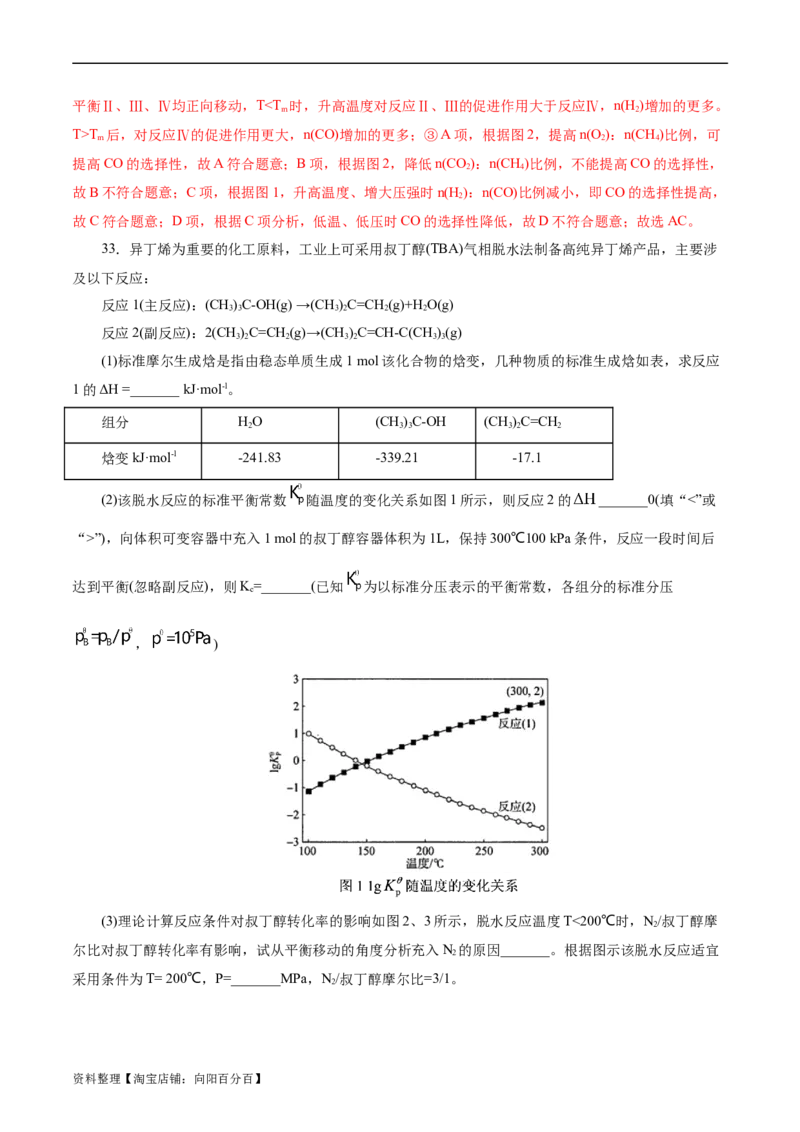
(2)该脱水反应的标准平衡常数 随温度的变化关系如图1所示,则反应2的 _______0(填“<”或
“>”),向体积可变容器中充入1 mol的叔丁醇容器体积为1L,保持300℃100 kPa条件,反应一段时间后
达到平衡(忽略副反应),则K=_______(已知 为以标准分压表示的平衡常数,各组分的标准分压
c
, )
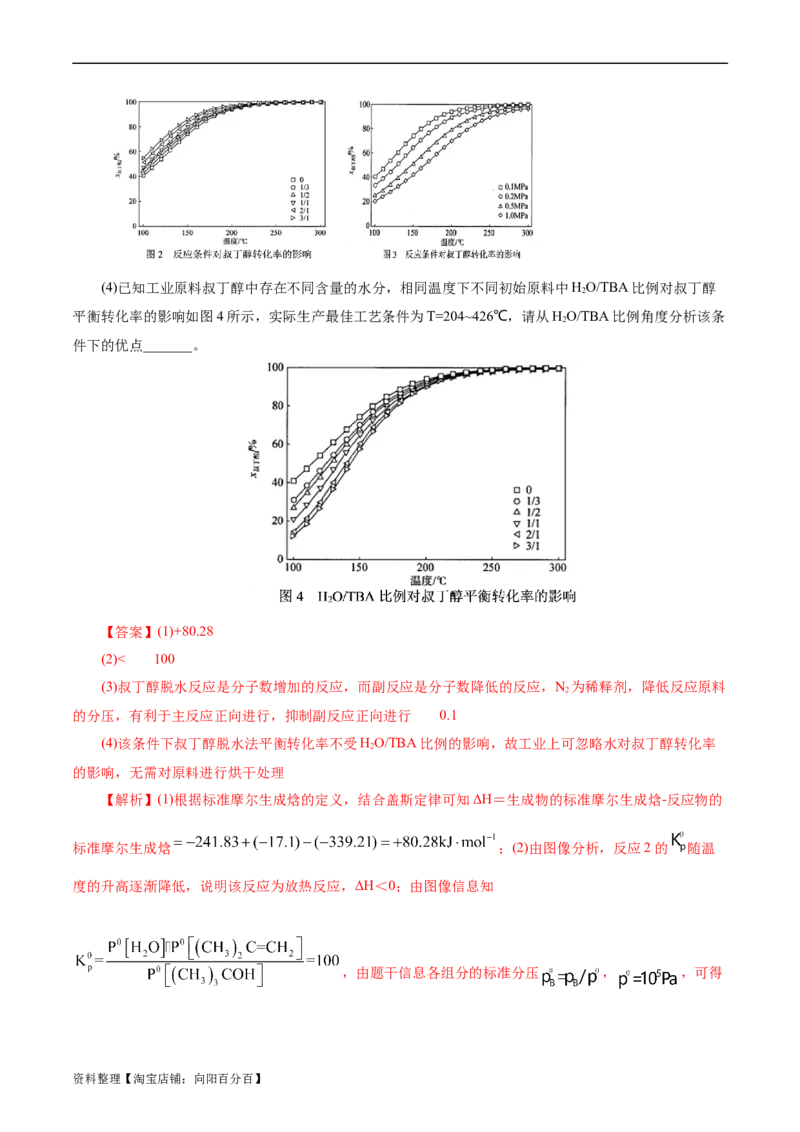
(3)理论计算反应条件对叔丁醇转化率的影响如图2、3所示,脱水反应温度T<200℃时,N/叔丁醇摩
2
尔比对叔丁醇转化率有影响,试从平衡移动的角度分析充入N 的原因_______。根据图示该脱水反应适宜
2
采用条件为T= 200℃,P=_______MPa,N/叔丁醇摩尔比=3/1。
2
资料整理【淘宝店铺:向阳百分百】(4)已知工业原料叔丁醇中存在不同含量的水分,相同温度下不同初始原料中HO/TBA比例对叔丁醇
2
平衡转化率的影响如图4所示,实际生产最佳工艺条件为T=204~426℃,请从HO/TBA比例角度分析该条
2
件下的优点_______。
【答案】(1)+80.28
(2)< 100
(3)叔丁醇脱水反应是分子数增加的反应,而副反应是分子数降低的反应,N 为稀释剂,降低反应原料
2
的分压,有利于主反应正向进行,抑制副反应正向进行 0.1
(4)该条件下叔丁醇脱水法平衡转化率不受HO/TBA比例的影响,故工业上可忽略水对叔丁醇转化率
2
的影响,无需对原料进行烘干处理
【解析】(1)根据标准摩尔生成焓的定义,结合盖斯定律可知ΔH=生成物的标准摩尔生成焓-反应物的
标准摩尔生成焓 ;(2)由图像分析,反应2的 随温
度的升高逐渐降低,说明该反应为放热反应,ΔH<0;由图像信息知
,由题干信息各组分的标准分压 , ,可得
资料整理【淘宝店铺:向阳百分百】, ,列三段式:
平衡时总物质的量为(1+x)mol,体系反应前气体总物质的量为1 mol,体积为1L,根据PV=nRT,恒压
体系,平衡时体系的体积为(1+x)L,各组分的浓度及物质的量分数分别为 ,
, , ,
, ,则 。
(3)脱水反应温度T<2000C时,N/叔丁醇摩尔比对叔丁醇转化率有影响,叔丁醇脱水反应是分子数增加的
2
反应,而副反应是分子数降低的反应,N 为稀释剂,降低反应的反应原料的分压,减小压强有利于促进主
2
反应和抑制副反应进行。由图像2、3可知叔丁醇转化率随温度升高逐渐增大,随压强增大而减小,随
N/叔丁醇摩尔比值增大而增大,故该脱水反应适宜采用条件为T=2000C, ,N/叔丁醇摩尔比
2 2
=3/1。(4)由图像4可知在T<2000C,叔丁醇平衡转化率随着HO/TBA比例的增加有一定程度的降低,即
2
反应时需要除去原料中包含的水,T>2000C,HO对叔丁醇平衡转化率影响可以忽略不计,该条件下叔丁
2
醇脱水法平衡转化率不受HO/TBA比例的影响,故工业上可忽略水对叔丁醇转化率的影响,无需对原料进
2
行烘干处理。
34.控制CO 的排放是防止温室效应等不良气候现象产生的有效途径。
2
(1)高炉炼铁会排放大量的CO 和烟尘,必须进行严格的控制。
2
已知:①3CO(g)+Fe O(s) 2Fe(s)+3CO (g) H=+a kJ/mol
2 3 2
②3C(石墨,s)+Fe
2
O
3
(s)=2Fe(s)+3CO(g) H=+48△9.0 kJ/mol
③C(石墨,s)+CO
2
(g)=2CO(g) H=+172.5△ kJ/mol
则a=____。若在恒温恒容密闭容△器中发生反应①,当达到平衡后,充入CO
2
,则达到新平衡后CO的
体积分数____(填“增大”、“减小”或“不变”,下同),其转化率_____。
(2)炼铁时需要用石灰石除去铁矿石中的脉石,该过程中涉及反应: CaCO(s) CaO(g)+CO(g)
3
ΔH>0。若在恒温恒容的密闭容器中进行上述反应达到平衡状态,在t 时刻向平衡体系中充入1 mol CO ,
1 2
t 时刻反应重新达到平衡,画出t 时刻后的正逆反应速率随时间变化的图像_____。
2 1
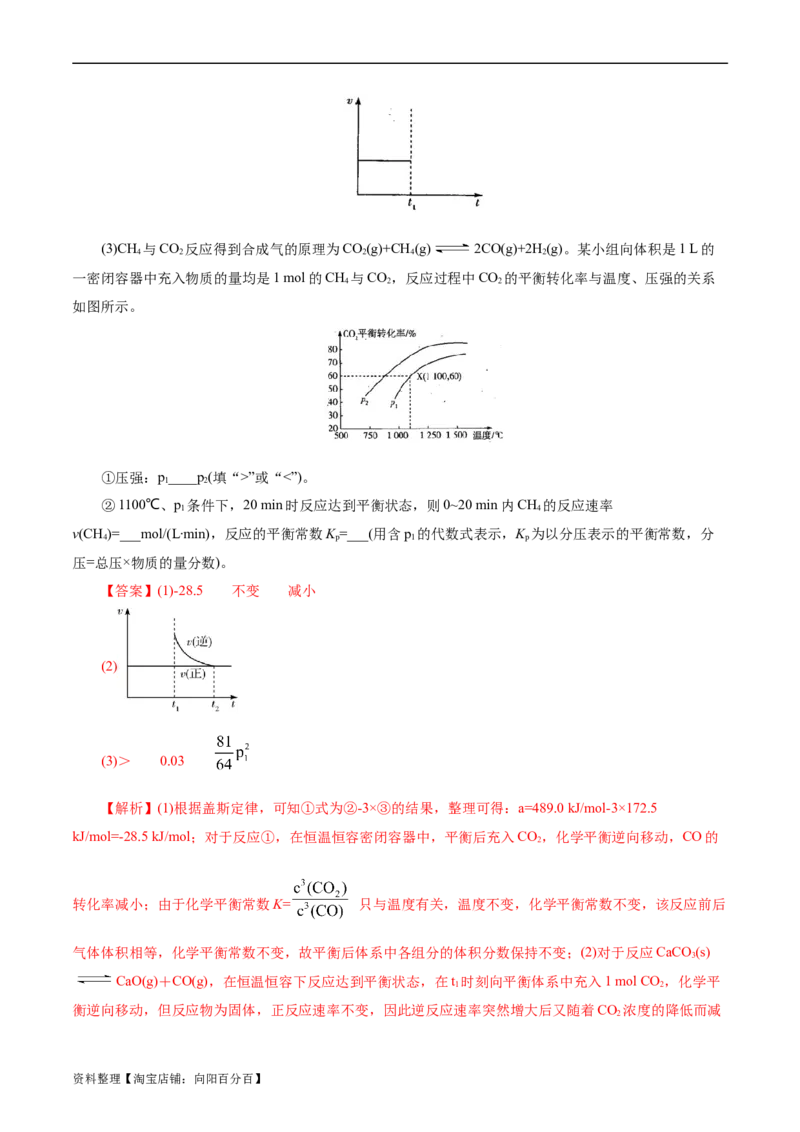
资料整理【淘宝店铺:向阳百分百】(3)CH 与CO 反应得到合成气的原理为CO(g)+CH (g) 2CO(g)+2H(g)。某小组向体积是1 L的
4 2 2 4 2
一密闭容器中充入物质的量均是1 mol的CH 与CO,反应过程中CO 的平衡转化率与温度、压强的关系
4 2 2
如图所示。
①压强:p____p(填“>”或“<”)。
1 2
②1100℃、p 条件下,20 min时反应达到平衡状态,则0~20 min内CH 的反应速率
1 4
v(CH)=___mol/(L∙min),反应的平衡常数K =___(用含p 的代数式表示,K 为以分压表示的平衡常数,分
4 p 1 p
压=总压×物质的量分数)。
【答案】(1)-28.5 不变 减小
(2)
(3)> 0.03
【解析】(1)根据盖斯定律,可知①式为②-3×③的结果,整理可得:a=489.0 kJ/mol-3×172.5
kJ/mol=-28.5 kJ/mol;对于反应①,在恒温恒容密闭容器中,平衡后充入CO,化学平衡逆向移动,CO的
2
转化率减小;由于化学平衡常数K= 只与温度有关,温度不变,化学平衡常数不变,该反应前后
气体体积相等,化学平衡常数不变,故平衡后体系中各组分的体积分数保持不变;(2)对于反应CaCO (s)
3
CaO(g)+CO(g),在恒温恒容下反应达到平衡状态,在t 时刻向平衡体系中充入1 mol CO ,化学平
1 2
衡逆向移动,但反应物为固体,正反应速率不变,因此逆反应速率突然增大后又随着CO 浓度的降低而减
2
资料整理【淘宝店铺:向阳百分百】小直至不变。用图象表示为: ;(3)①对于反应CO(g)+CH (g) 2CO(g)+2H(g),
2 4 2
在温度不变时,减小压强,化学平衡向气体体积增大的正反应方向移动,使CO 的转化率增大,根据图象
2
可知CO 的转化率:p>p,说明压强p >p ;②在温度为1100℃、压强为p 条件下,20 min时反应达
2 2 1 1 2 1
到平衡状态时,CO 的转化率为60%,即平衡时△n(CO)=1 mol×60%=0.6 mol,由于容器的容积是1 L,则
2 2
v(CO)= =0.03 mol·L-1·min-1,由于同一反应用不同物质表示反应速率时,速率比等于方程式
2
中相应物质的化学计量数的比,所以v(CH)= v(CO)=0.03 mol/(L·min );反应中CO、CH 是按1:1关系
4 2 2 4
反应的,开始时加入的物质的量都是1 mol,则反应达到平衡时,n(CH)= n(CO)=0.4 mol,n(CO)=
4 2
n(H )=2×0.6mol= 1.2 mol,n(总)=0.4 mol+0.4 mol+1.2 mol+1.2 mol=3.2 mol,则用压强分数表示是化学平衡
2
常数表示为 。
35.研究的利用对实现碳中和具有重要的意义。已知:
I. CO(g)+3H(g) CHOH(g)+H O(g) H=-49.5kJ·mol-1
2 2 3 2 1
II. CO (g)+H(g) CO(g)+HO(g) H=+41.2kJ·mol-1
2 2 2 △1
回答下列问题:
△
(1) CO(g)+2H (g) CHOH(g)+H O(g) H_______kJmol-1
2 3 2
(2)一定条件下,某恒容密闭容器中按n(H )/ n(CO)= a (a≥3) 投料,催化作用下同时发生反应I和II。
2 △ 2
反应体系中 CO(g)、CO(g)的浓度随时间变化情况如图所示。
2
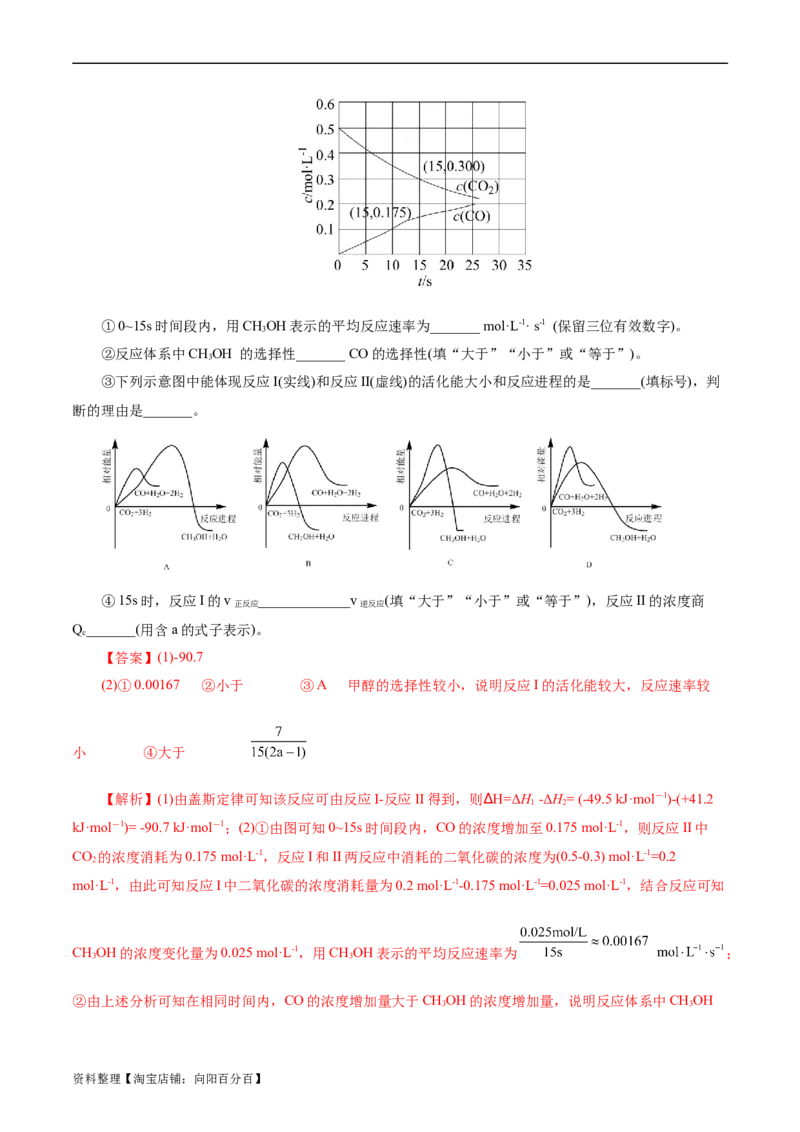
资料整理【淘宝店铺:向阳百分百】①0~15s时间段内,用CHOH表示的平均反应速率为_______ mol·L-1· s-1 (保留三位有效数字)。
3
②反应体系中CHOH 的选择性_______ CO的选择性(填“大于”“小于”或“等于”)。
3
③下列示意图中能体现反应I(实线)和反应II(虚线)的活化能大小和反应进程的是_______(填标号),判
断的理由是_______。
④15s时,反应I的v _____________v (填“大于”“小于”或“等于”),反应II的浓度商
正反应 逆反应
Q_______(用含a的式子表示)。
c
【答案】(1)-90.7
(2)①0.00167 ②小于 ③A 甲醇的选择性较小,说明反应I的活化能较大,反应速率较
小 ④大于
【解析】(1)由盖斯定律可知该反应可由反应I-反应II得到,则∆H=ΔH -ΔH= (-49.5 kJ·mol-1)-(+41.2
1 2
kJ·mol-1)= -90.7 kJ·mol-1;(2)①由图可知0~15s时间段内,CO的浓度增加至0.175 mol·L-1,则反应II中
CO 的浓度消耗为0.175 mol·L-1,反应I和II两反应中消耗的二氧化碳的浓度为(0.5-0.3) mol·L-1=0.2
2
mol·L-1,由此可知反应I中二氧化碳的浓度消耗量为0.2 mol·L-1-0.175 mol·L-1=0.025 mol·L-1,结合反应可知
CHOH的浓度变化量为0.025 mol·L-1,用CHOH表示的平均反应速率为 ;
3 3
②由上述分析可知在相同时间内,CO的浓度增加量大于CHOH的浓度增加量,说明反应体系中CHOH
3 3
资料整理【淘宝店铺:向阳百分百】的选择性小于CO的选择性;③由上述分析可知反应对甲醇的选择性小于CO,说明生成甲醇的反应较生成
CO的反应要慢,而反应的活化能越低反应速率越快,活化能越高反应速率越慢,则反应I的活化能大于反
应II,符合的图为A;④15s时,反应正向进行,正反应速率大于逆反应速率;由图可知起始时二氧化碳
的浓度为0.5mol/L,又n(H )/ n(CO)= a,则氢气的起始浓度为0.5amol/L,15s时二氧化碳的浓度为
2 2
0.300mol/L,CO的浓度0.175 mol·L-1,则反应II中消耗氢气的浓度为0.175 mol·L-1,该反应生成的水的浓
度为0.175 mol·L-1;CHOH的浓度变化量为0.025 mol·L-1,则反应I中消耗氢气的浓度为0.075 mol·L-1,生
3
成水的浓度为:0.025 mol·L-1,则此时容器中水的总浓度0.200 mol·L-1,氢气的浓度为(0.5a-0.175-0.075)
mol·L-1=(0.5a-0.175-0.075) mol·L-1=(0.5a-0.250) mol·L-1,反应II的浓度商 Q=
c
。
36.氮氧化物气体是危害最大、最难处理的大气污染物之一。控制氮氧化物废气排放的技术措施主要
分两大类:一类是源头控制;另一类是尾部控制,即烟气脱硝。烟气脱硝的方法有以下几种,回答相关问
题:
I.氨气催化还原氮氧化物
(1)已知:N(g)+3H(g) 2NH (g) H=-94.4kJ·mol-1
2 2 3 1
2NO(g) N
2
(g)+O
2
(g) H
2
=-180kJ△·mol-1
HO(l) HO(g) H=+44kJ·mol-1
2 2 3 △
且氢气的燃烧热为285.8kJ·mol-1,请写出4NH (g)+6NO(g) 5N(g)+6HO(g) H=____。
△ 3 2 2
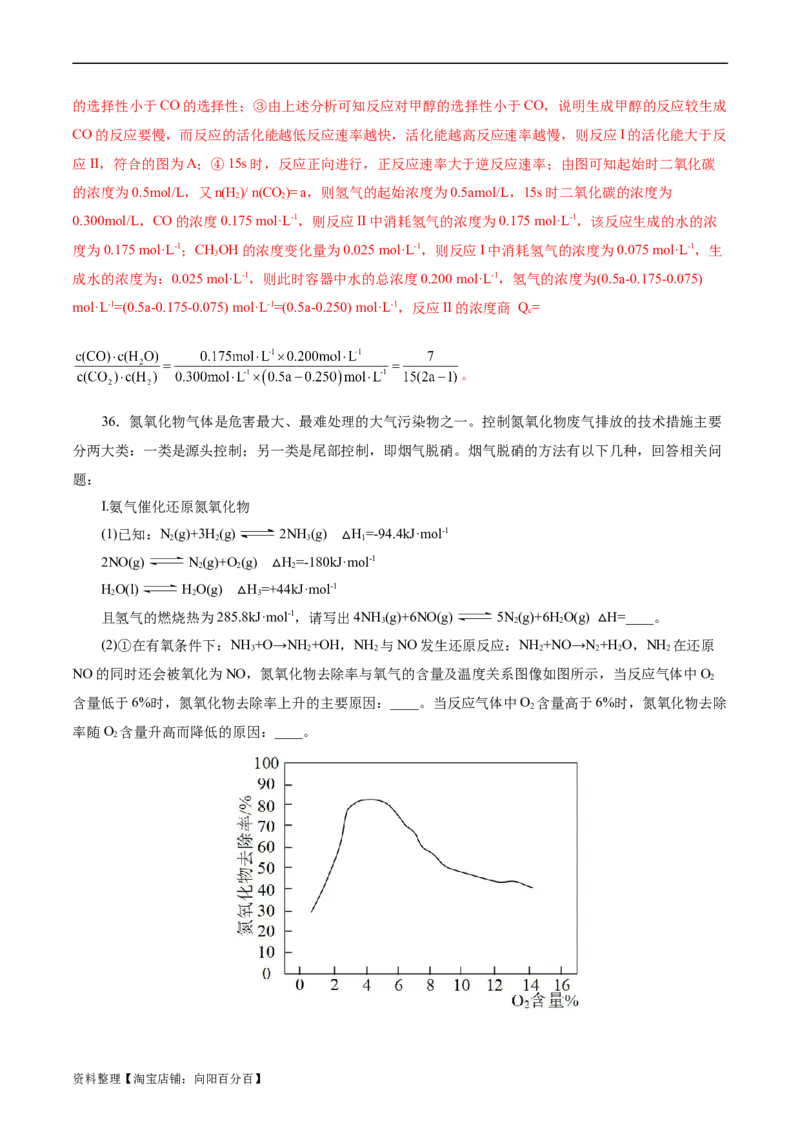
(2)①在有氧条件下:NH
3
+O→NH
2
+OH,NH
2
与NO发生还原反应:NH
2
+NO→N 2△+H
2
O,NH
2
在还原
NO的同时还会被氧化为NO,氮氧化物去除率与氧气的含量及温度关系图像如图所示,当反应气体中O
2
含量低于6%时,氮氧化物去除率上升的主要原因:____。当反应气体中O 含量高于6%时,氮氧化物去除
2
率随O 含量升高而降低的原因:____。
2
资料整理【淘宝店铺:向阳百分百】②氮氧化物去除率随着氨氮比 及温度的变化图像如图所示,应选择最佳的氨氮比为:____、
氨还原氮氧化物的最佳温度:____。
II.氢气还原氮氧化物
(3)①在催化剂表面H 还原NO的基元反应及活化能E(kJ·mol-1)如图所示。
2 a
写出氢气还原NO的总反应化学方程式:____;基元反应慢反应决定总反应速率,决定NO被还原成
N 速率的是基元反应____(填相应序号)。
2
②若对总反应初始速率与NO、H 的初始浓度的关系为v=kcx(H )cy(NO),k为速率常数,只受温度影
2 2
响。在某温度时测得的相关数据如表所示。
H 的初始压强P(H )=53.3kPa NO的初始压强P(NO)=53.3kPa
2 0 2 0
P(NO)/kPa v/(kPa•s-1) P(H )/kPa v/(kPa•s-1)
0 0 2
47.8 20.0 38.4 21.3
资料整理【淘宝店铺:向阳百分百】