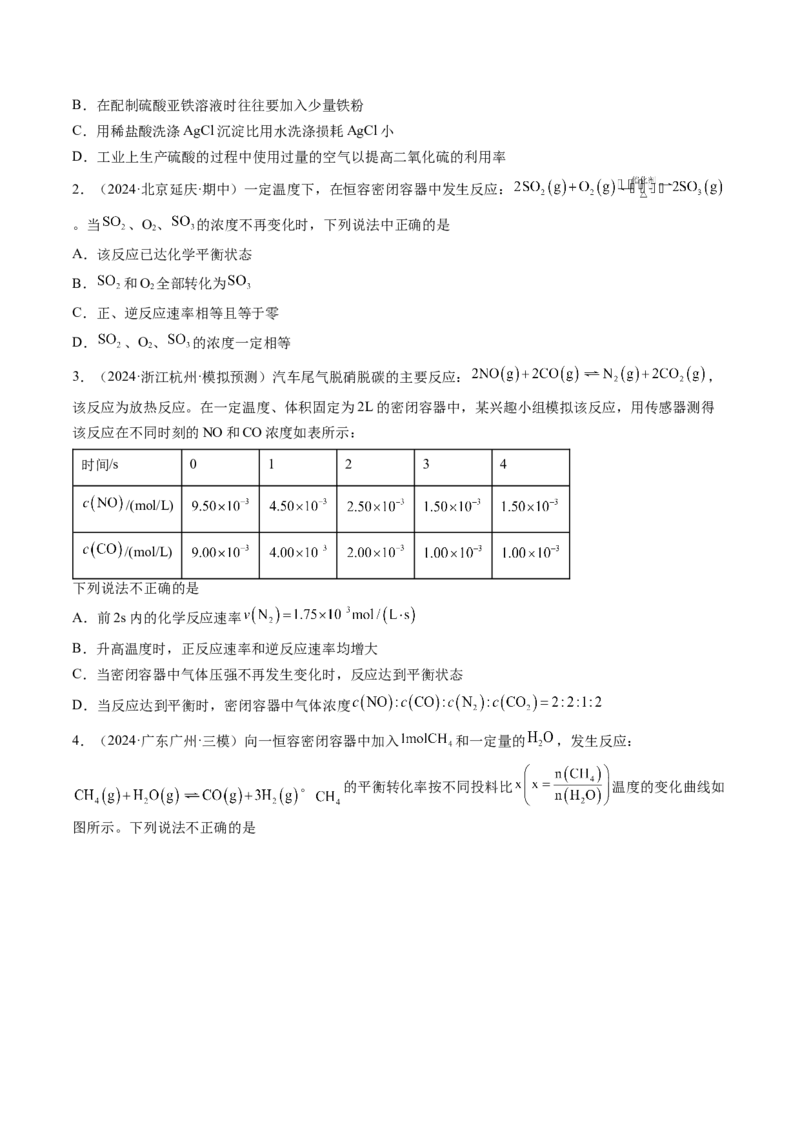文档内容
考点 26 化学平衡状态、化学平衡的移动
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
.............................................................................................................................................2
考法01 化学平衡状态...............................................................................................................................2
考法02 化学平衡移动...............................................................................................................................6
.............................................................................................................................................8
1.高考真题考点分布
考点内容 考点分布
化学平衡移动 2024辽宁卷,3分;2024山东卷,3分;2024江苏卷,3分;2024浙江卷,3分;
2024湖南卷,3分;2023北京卷,3分;2023湖南卷,3分;2023山东卷,3分;
2022天津卷,3分;2022重庆卷,3分;2022江苏卷,3分;2022浙江卷,3分;
2022北京卷,3分;2022辽宁卷,3分;2022湖南卷,3分;
化学平衡状态 2022湖北卷13题,3分;
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,化学平衡状态的特征及化学平衡的移动及其影响因素仍是高考命题
的热点。
【备考策略】【命题预测】
预计2025年高考会以新的情境载体考查勒夏特列原理的理解,通过实验、判断、图象、计算等形式对化学
平衡移动综合考查,题目难度一般适中。
考法01 化学平衡状态
1.可逆反应
(1)概念
在同一条件下,既可以向 进行,同时又能向 进行的化学反应。
(2)特点
① 性;② 性(正、逆反应是在同一条件下,同时进行);③ 性。
2.化学平衡状态
(1)概念
一定条件下的 中,当正反应速率和逆反应速率 时,反应物和生成物的浓度均保持
,即体系的组成不随时间而改变的状态。
(2)建立
(3)特征3.判断平衡状态的两种方法
(1)“正逆相等”:v =v ≠0
正 逆
①同种物质:同一物质的生成速率等于消耗速率。
②不同物质:必须标明是“异向”的反应速率关系。如aA+bB cC+dD,=时,反应达平衡状态。
(2)“变量不变”:如果一个量是随反应进行而改变的,当其不变时为平衡状态;一个随反应进行保持不变
的量,不能作为判断是否平衡的依据。
【易错提醒】规避判断化学平衡状态的两个易错点
(1)化学平衡状态判断“三关注”
①关注反应条件,是恒温恒容、恒温恒压,还是绝热恒容容器。
②关注反应特点,是等体积反应,还是非等体积反应。
③关注特殊情况,是否有固体参加或生成,或固体的分解反应。
(2)不能作为化学平衡状态“标志”的四种情况
①反应组分的物质的量之比等于化学方程式中相应物质的化学计量数之比。
②恒温恒容下的体积不变的反应,体系的压强或总物质的量不再随时间而变化,如 2HI(g) H(g)+
2
I(g)。
2
③全是气体参加的体积不变的反应,体系的平均相对分子质量不再随时间而变化,如 2HI(g) H(g)+
2
I(g)。
2
④全是气体参加的反应,恒容条件下体系的密度保持不变。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
1.在化学平衡建立过程中,v 一定大于v ( )
正 逆
2.恒温恒容下进行的可逆反应:2SO (g)+O(g) 2SO (g),当SO 的生成速率与SO 的消耗速率相等时,
2 2 3 3 2
反应达到平衡状态( )
3.任何可逆反应都有一定限度,达到了化学平衡状态即达到了该反应的限度( )
4.化学反应达到限度时,正、逆反应速率相等( )
5.化学反应达到平衡后,反应物和生成物的浓度或百分含量相等( )
6.在一定条件下,向密闭容器中充入1 mol N 和3 mol H 充分反应,生成2 mol NH ( )
2 2 3
7.向含有3 mol H 的容器中通入足量N,充分反应后会生成2 mol NH 。( )
2 2 3
8.一定条件下反应N+3H 2NH 达到平衡时,3v (H )=2v (NH )。( )
2 2 3 正 2 逆 3
9.对于NO (g)+SO (g) SO (g)+NO(g)反应,当每消耗1 mol SO 的同时生成1 mol NO 时,说明反应达
2 2 3 3 2
到平衡状态。( )
考向01 考查可逆反应
【例1】(2024·河北衡水·期中)向平衡体系 中,通入一定量由18O组成的氧
气,经过一段时间后,18O存在于A.只存在于多余O 中 B.只存在于生成的SO 中
2 3
C.存在于O、SO 及SO 中 D.只存在于O 和SO 中
2 2 3 2 3
考向02 考查平衡状态的判断
【例2】(2024·吉林四平·二模)下列描述的化学反应状态,不一定是平衡状态的是( )
A.H(g)+Br (g) 2HBr(g),恒温、恒容下,反应体系中气体的颜色保持不变
2 2
B.2NO (g) NO(g),恒温、恒容下,反应体系中气体的压强保持不变
2 2 4
C.CaCO (s) CO(g)+CaO(s),恒温、恒容下,反应体系中气体的密度保持不变
3 2
D.N(g)+3H(g) 2NH (g),反应体系中H 与N 的物质的量之比保持3∶1
2 2 3 2 2
【思维建模】判断化学平衡状态的两种方法
(1)动态标志:v =v ≠0
正 逆
①同种物质:同一物质的生成速率等于消耗速率。
②不同物质:必须标明是“异向”的反应速率关系。如aA+bB cC+dD,=时,反应达到平衡状态。
(2)“变量→不变”标志
一定条件下,当可逆反应进行时,某“物理量”应当伴随变化,当该“物理量”不再变化时,该反应达到
限度,即化学平衡状态。
【对点1】(2024·浙江衢州·模拟)下列反应属于可逆反应的是
① ②
③ ④
A.①③ B.②④ C.① D.②③
【对点2】(2024·河南许昌·模拟)一定温度下,向一体积不变的密闭容器中加入一定量的SO 和O,发生
2 2
反应:2SO (g)+O(g) 2SO (g) ΔH=-196.6 kJ·mol-1。
2 2 3
下列有关该反应的叙述正确的是( )
A.达到平衡状态时,正、逆反应速率相等
B.达到平衡状态时,SO 和O 的浓度都为0
2 2
C.若起始时加入2 mol SO 和1 mol O ,则达平衡时放出的热量为196.6 kJ
2 2
D.若反应达到平衡状态后,2 min时生成a mol SO ,则4 min时生成2a mol SO
3 3
考法02 化学平衡移动
1.化学平衡移动
(1)原因:反应条件改变引起v ≠v 。
正 逆
(2)化学平衡移动方向与化学反应速率的关系
①v
正
>v
逆
时,平衡向 方向移动;
②v
正
<v
逆
时,平衡向 方向移动。
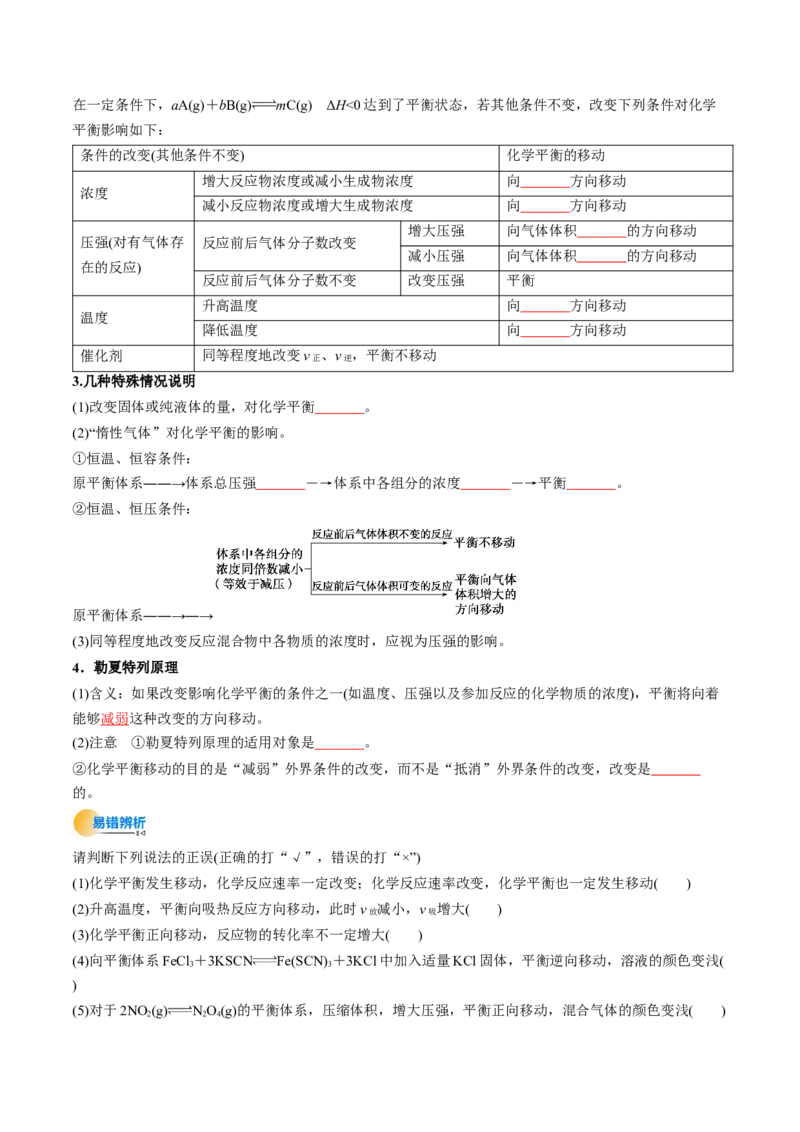
2.影响因素在一定条件下,aA(g)+bB(g) mC(g) ΔH<0达到了平衡状态,若其他条件不变,改变下列条件对化学
平衡影响如下:
条件的改变(其他条件不变) 化学平衡的移动
增大反应物浓度或减小生成物浓度 向 方向移动
浓度
减小反应物浓度或增大生成物浓度 向 方向移动
增大压强 向气体体积 的方向移动
压强(对有气体存 反应前后气体分子数改变
减小压强 向气体体积 的方向移动
在的反应)
反应前后气体分子数不变 改变压强 平衡
升高温度 向 方向移动
温度
降低温度 向 方向移动
催化剂 同等程度地改变v 、v ,平衡不移动
正 逆
3.几种特殊情况说明
(1)改变固体或纯液体的量,对化学平衡 。
(2)“惰性气体”对化学平衡的影响。
①恒温、恒容条件:
原平衡体系――→体系总压强 ―→体系中各组分的浓度 ―→平衡 。
②恒温、恒压条件:
原平衡体系――→―→
(3)同等程度地改变反应混合物中各物质的浓度时,应视为压强的影响。
4.勒夏特列原理
(1)含义:如果改变影响化学平衡的条件之一(如温度、压强以及参加反应的化学物质的浓度),平衡将向着
能够减弱这种改变的方向移动。
(2)注意 ①勒夏特列原理的适用对象是 。
②化学平衡移动的目的是“减弱”外界条件的改变,而不是“抵消”外界条件的改变,改变是
的。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)化学平衡发生移动,化学反应速率一定改变;化学反应速率改变,化学平衡也一定发生移动( )
(2)升高温度,平衡向吸热反应方向移动,此时v 减小,v 增大( )
放 吸
(3)化学平衡正向移动,反应物的转化率不一定增大( )
(4)向平衡体系FeCl +3KSCN Fe(SCN) +3KCl中加入适量KCl固体,平衡逆向移动,溶液的颜色变浅(
3 3
)
(5)对于2NO (g) NO(g)的平衡体系,压缩体积,增大压强,平衡正向移动,混合气体的颜色变浅( )
2 2 4(6)反应达到平衡状态时,其他条件不变,分离出固体生成物,v 减小。( )
正
(7)对于反应:3SiCl (g)+2N(g)+6H(g) Si N(s)+12HCl(g) ΔH<0,其他条件不变,增大Si N 物质
4 2 2 3 4 3 4
的量,平衡向左移动。( )
(8)对于反应:2SO (g)+O(g) 2SO (g) ΔH<0,降低温度,正反应速率减小程度比逆反应速率减小程
2 2 3
度大。( )
(9)化学平衡正向移动,反应物的转化率一定增大。( )
考向01 考查外界条件对化学平衡的影响
【例1】(2024·江苏盐城·一模)某温度下,在一恒容密闭容器中进行如下两个反应并达到平衡:
①2X(g)+Y(g) Z(s)+ 2Q(g) ΔH<0
1
②M(g)+N(g) R(g)+Q(g) ΔH>0
2
下列叙述错误的是( )
A.加入适量Z,①和②平衡均不移动
B.通入稀有气体Ar,①平衡正向移动
C.降温时无法判断Q浓度的增减
D.通入Y,则N的浓度增大
【思维建模】惰性气体(稀有气体、不参与反应的气体)与平衡移动的关系
(1)恒温、恒容条件
原平衡体系――→体系总压强增大→体系中各组分的浓度不变→平衡不移动。
(2)恒温、恒压条件
原平衡体系――→容器容积增大,各反应气体的分压减小―→体系中各组分的浓度同倍数减小(等效于减
压)
考向02 考查化学平衡移动方向、转化率的分析判断
【例2】(2024·湖南岳阳·二模)在一定温度下的密闭容器中发生反应:xA(g)+yB(g)zC(g),平衡时测
得A的浓度为0.50 mol·L-1。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓
度为0.30 mol·L-1。下列有关判断正确的是( )
A.x+y0
B.加入一定量Z,达新平衡后m(Y)减小
C.加入等物质的量的Y和Z,达新平衡后c(Z)增大
D.加入一定量氩气,平衡不移动
【对点2】(2024·辽宁丹东·模拟)将等物质的量的N、H 充入某密闭容器中,在一定条件下,发生如下
2 2
反应并达到平衡:N(g)+3H(g) 2NH (g) ΔH<0。当改变某个条件并维持新条件直至新的平衡时,下
2 2 3
表中关于新平衡与原平衡的比较正确的是( )
选项 改变条件 新平衡与原平衡比较
A 增大压强 N 的浓度一定变小
2
B 升高温度 N 的转化率变小
2
C 充入一定量H H 的转化率不变,N 的转化率变大
2 2 2
D 使用适当催化剂 NH 的体积分数增大
3
【对点3】(2024·北京·三模)下列事实不能用化学平衡移动原理解释的是
A.锌片与稀 反应过程中,加入少量 固体,促进 的产生
B.密闭烧瓶内的 和 的混合气体,受热后颜色加深
C.水垢中含有 ,可先用 溶液浸泡处理,再用盐酸溶解
D. 的醋酸溶液加水稀释100倍,
1.(2023·广东深圳·模拟预测)下列事实中,不能用化学平衡移动原理解释的是
A.棕色的 体系加压后,颜色先变深后逐渐变浅B.在配制硫酸亚铁溶液时往往要加入少量铁粉
C.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
2.(2024·北京延庆·期中)一定温度下,在恒容密闭容器中发生反应:
。当 、O、 的浓度不再变化时,下列说法中正确的是
2
A.该反应已达化学平衡状态
B. 和O 全部转化为
2
C.正、逆反应速率相等且等于零
D. 、O、 的浓度一定相等
2
3.(2024·浙江杭州·模拟预测)汽车尾气脱硝脱碳的主要反应: ,
该反应为放热反应。在一定温度、体积固定为2L的密闭容器中,某兴趣小组模拟该反应,用传感器测得
该反应在不同时刻的NO和CO浓度如表所示:
时间/s 0 1 2 3 4
/(mol/L)
/(mol/L)
下列说法不正确的是
A.前2s内的化学反应速率
B.升高温度时,正反应速率和逆反应速率均增大
C.当密闭容器中气体压强不再发生变化时,反应达到平衡状态
D.当反应达到平衡时,密闭容器中气体浓度
4.(2024·广东广州·三模)向一恒容密闭容器中加入 和一定量的 ,发生反应:
。 的平衡转化率按不同投料比 温度的变化曲线如
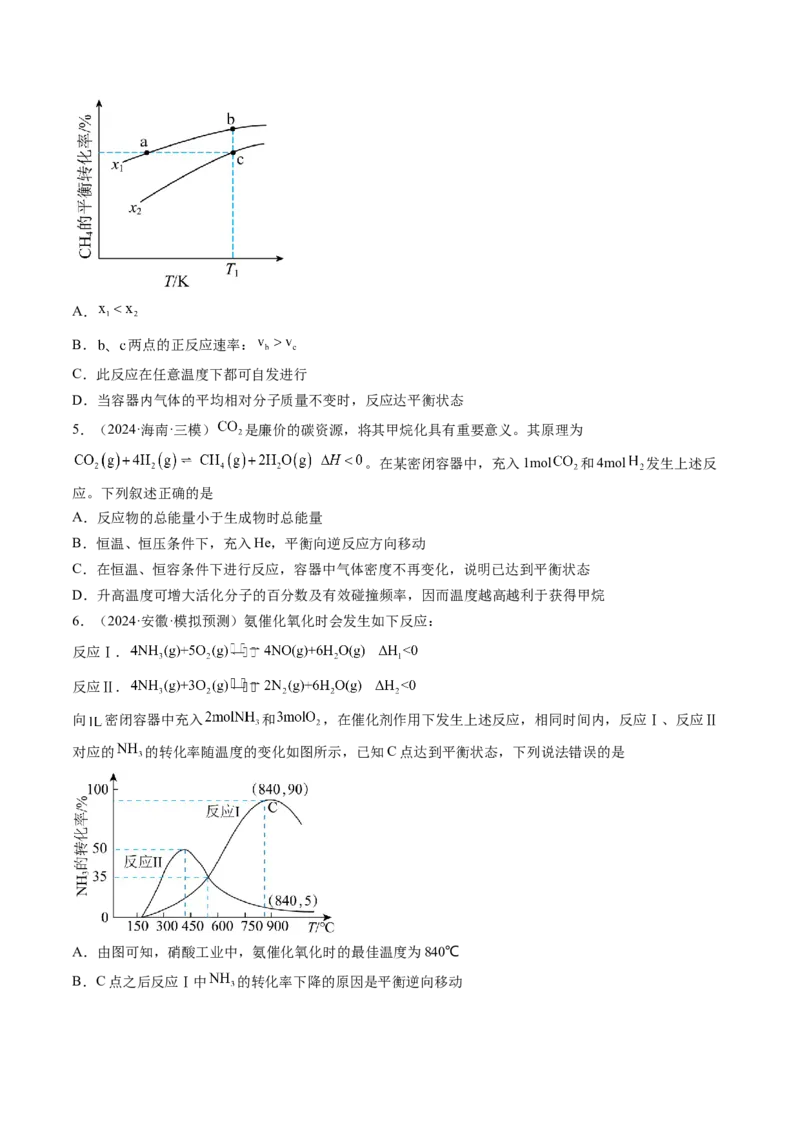
图所示。下列说法不正确的是A.
B. 两点的正反应速率:
C.此反应在任意温度下都可自发进行
D.当容器内气体的平均相对分子质量不变时,反应达平衡状态
5.(2024·海南·三模) 是廉价的碳资源,将其甲烷化具有重要意义。其原理为
。在某密闭容器中,充入1mol 和4mol 发生上述反
应。下列叙述正确的是
A.反应物的总能量小于生成物时总能量
B.恒温、恒压条件下,充入He,平衡向逆反应方向移动
C.在恒温、恒容条件下进行反应,容器中气体密度不再变化,说明已达到平衡状态
D.升高温度可增大活化分子的百分数及有效碰撞频率,因而温度越高越利于获得甲烷
6.(2024·安徽·模拟预测)氨催化氧化时会发生如下反应:
反应Ⅰ.
反应Ⅱ.
向 密闭容器中充入 和 ,在催化剂作用下发生上述反应,相同时间内,反应Ⅰ、反应Ⅱ
对应的 的转化率随温度的变化如图所示,已知C点达到平衡状态,下列说法错误的是
A.由图可知,硝酸工业中,氨催化氧化时的最佳温度为840℃
B.C点之后反应Ⅰ中 的转化率下降的原因是平衡逆向移动C.混合体系中 保持不变说明反应Ⅱ达到平衡状态
D.C点对应温度下,反应Ⅰ的平衡常数
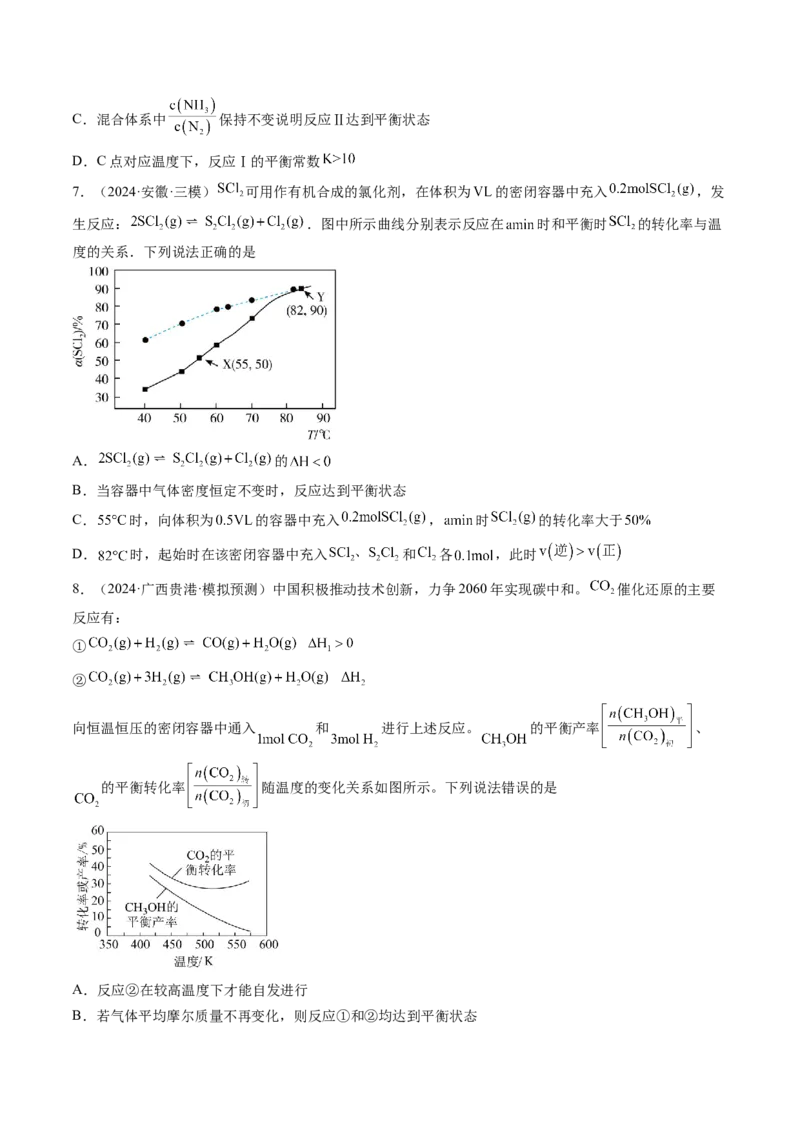
7.(2024·安徽·三模) 可用作有机合成的氯化剂,在体积为 的密闭容器中充入 ,发
生反应: .图中所示曲线分别表示反应在 时和平衡时 的转化率与温
度的关系.下列说法正确的是
A. 的
B.当容器中气体密度恒定不变时,反应达到平衡状态
C. 时,向体积为 的容器中充入 , 时 的转化率大于
D. 时,起始时在该密闭容器中充入 和 各 ,此时
8.(2024·广西贵港·模拟预测)中国积极推动技术创新,力争2060年实现碳中和。 催化还原的主要
反应有:
①
②
向恒温恒压的密闭容器中通入 和 进行上述反应。 的平衡产率 、
的平衡转化率 随温度的变化关系如图所示。下列说法错误的是
A.反应②在较高温度下才能自发进行
B.若气体平均摩尔质量不再变化,则反应①和②均达到平衡状态C.任意温度下的平衡转化率:
D.平衡时 随温度升高先减小后增大
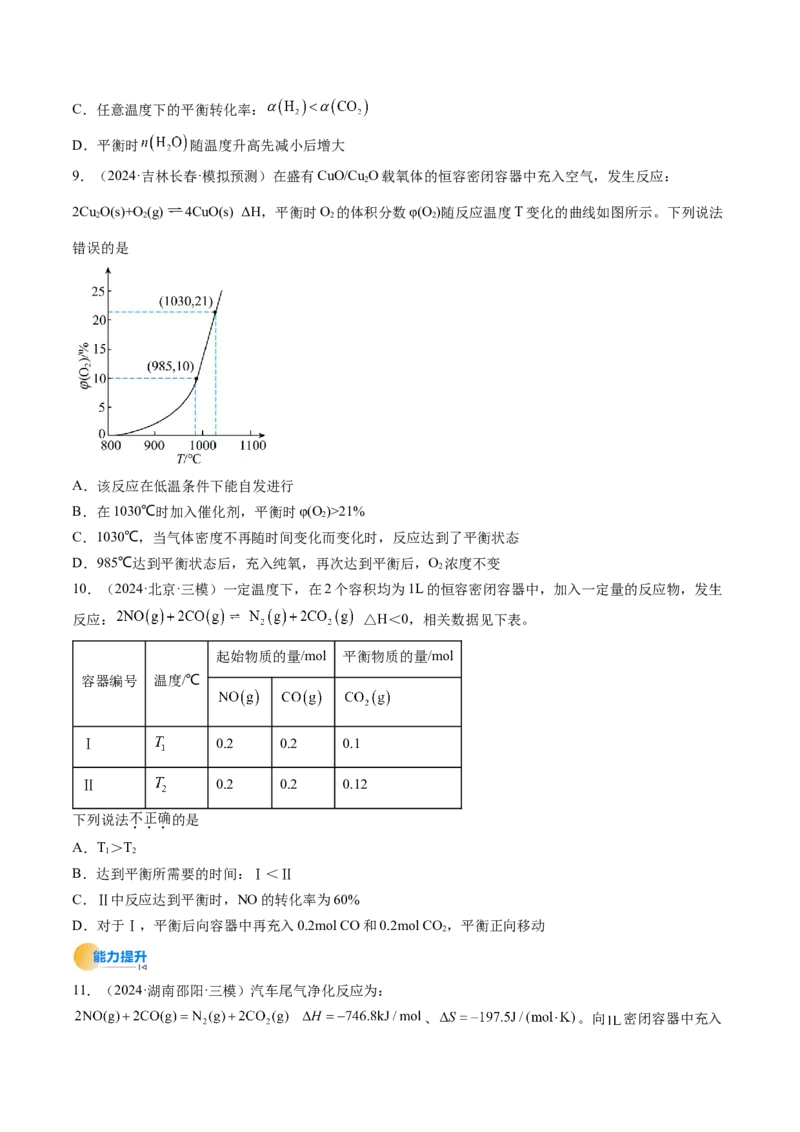
9.(2024·吉林长春·模拟预测)在盛有CuO/Cu O载氧体的恒容密闭容器中充入空气,发生反应:
2
2Cu O(s)+O (g) 4CuO(s) ΔH,平衡时O 的体积分数φ(O)随反应温度T变化的曲线如图所示。下列说法
2 2 2 2
错误的是
A.该反应在低温条件下能自发进行
B.在1030℃时加入催化剂,平衡时φ(O)>21%
2
C.1030℃,当气体密度不再随时间变化而变化时,反应达到了平衡状态
D.985℃达到平衡状态后,充入纯氧,再次达到平衡后,O 浓度不变
2
10.(2024·北京·三模)一定温度下,在2个容积均为1L的恒容密闭容器中,加入一定量的反应物,发生
反应: △H<0,相关数据见下表。
起始物质的量/mol 平衡物质的量/mol
容器编号 温度/℃
Ⅰ 0.2 0.2 0.1
Ⅱ 0.2 0.2 0.12
下列说法不正确的是
A.T>T
1 2
B.达到平衡所需要的时间:Ⅰ<Ⅱ
C.Ⅱ中反应达到平衡时,NO的转化率为60%
D.对于Ⅰ,平衡后向容器中再充入0.2mol CO和0.2mol CO ,平衡正向移动
2
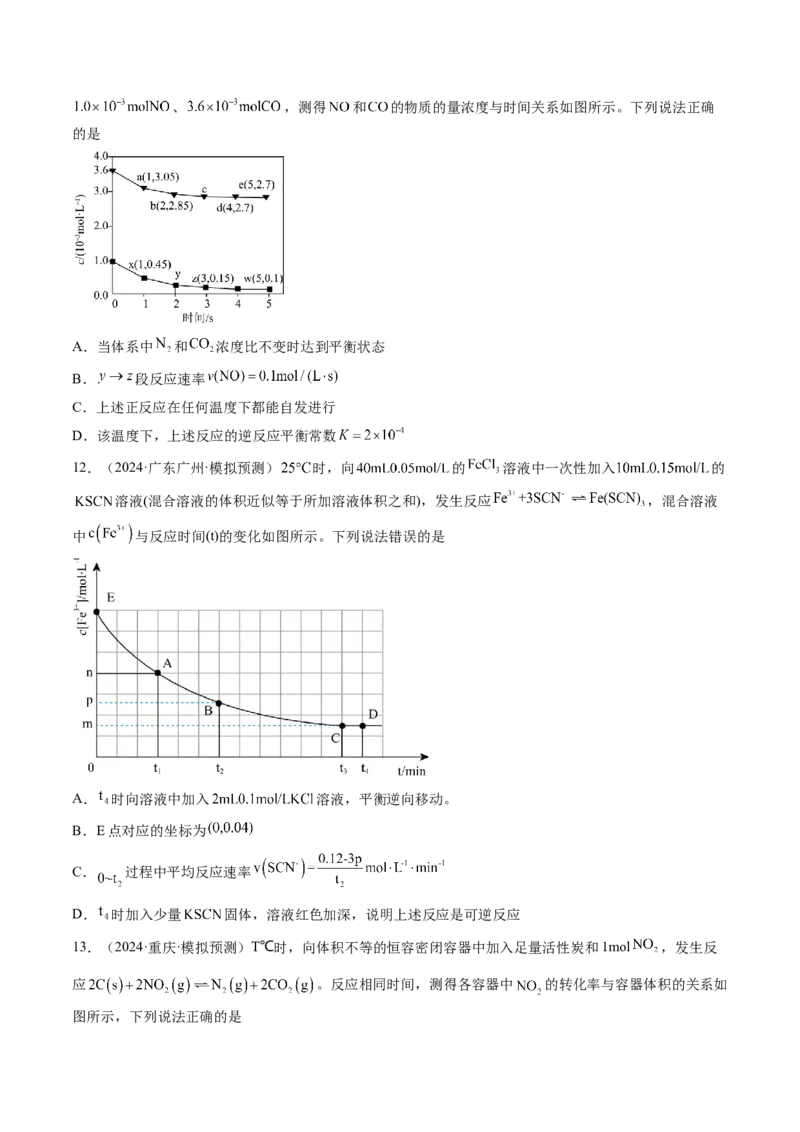
11.(2024·湖南邵阳·三模)汽车尾气净化反应为:
、 。向 密闭容器中充入、 ,测得 和 的物质的量浓度与时间关系如图所示。下列说法正确
的是
A.当体系中 和 浓度比不变时达到平衡状态
B. 段反应速率
C.上述正反应在任何温度下都能自发进行
D.该温度下,上述反应的逆反应平衡常数
12.(2024·广东广州·模拟预测) 时,向 的 溶液中一次性加入 的
溶液(混合溶液的体积近似等于所加溶液体积之和),发生反应 ,混合溶液
中 与反应时间(t)的变化如图所示。下列说法错误的是
A. 时向溶液中加入 溶液,平衡逆向移动。
B.E点对应的坐标为
C. 过程中平均反应速率
D. 时加入少量 固体,溶液红色加深,说明上述反应是可逆反应
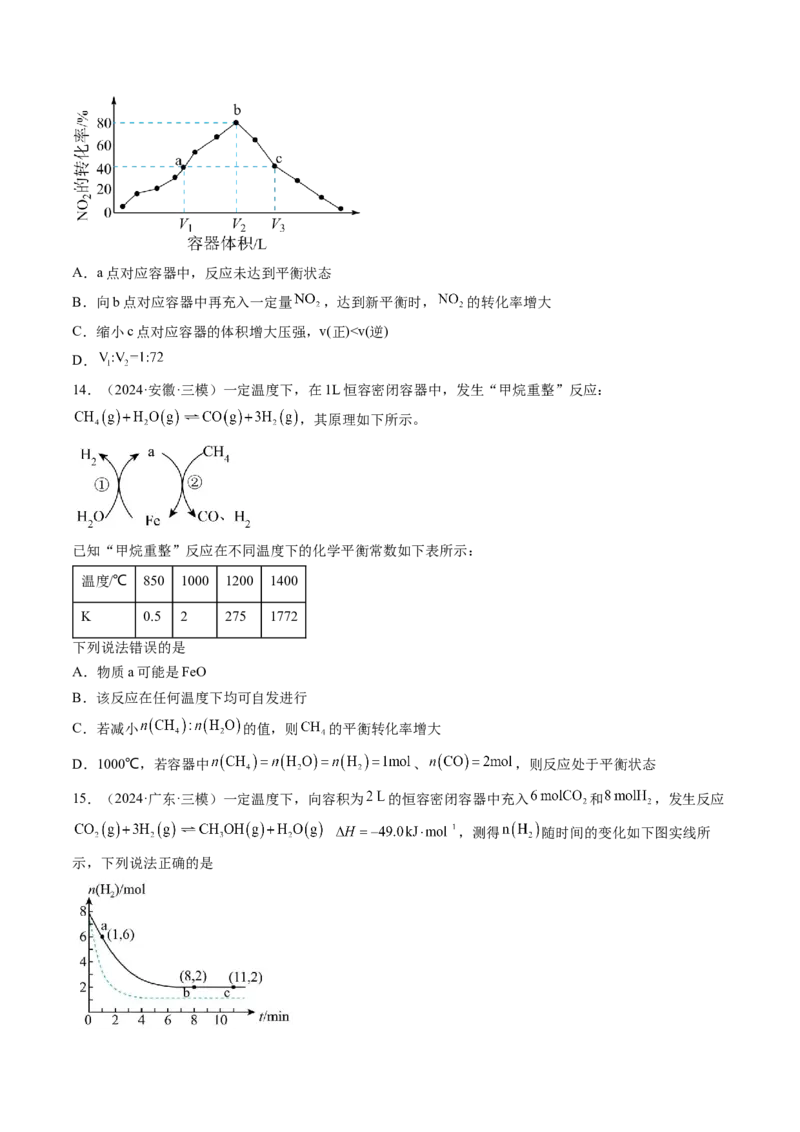
13.(2024·重庆·模拟预测)T℃时,向体积不等的恒容密闭容器中加入足量活性炭和1mol ,发生反
应 。反应相同时间,测得各容器中 的转化率与容器体积的关系如
图所示,下列说法正确的是A.a点对应容器中,反应未达到平衡状态
B.向b点对应容器中再充入一定量 ,达到新平衡时, 的转化率增大
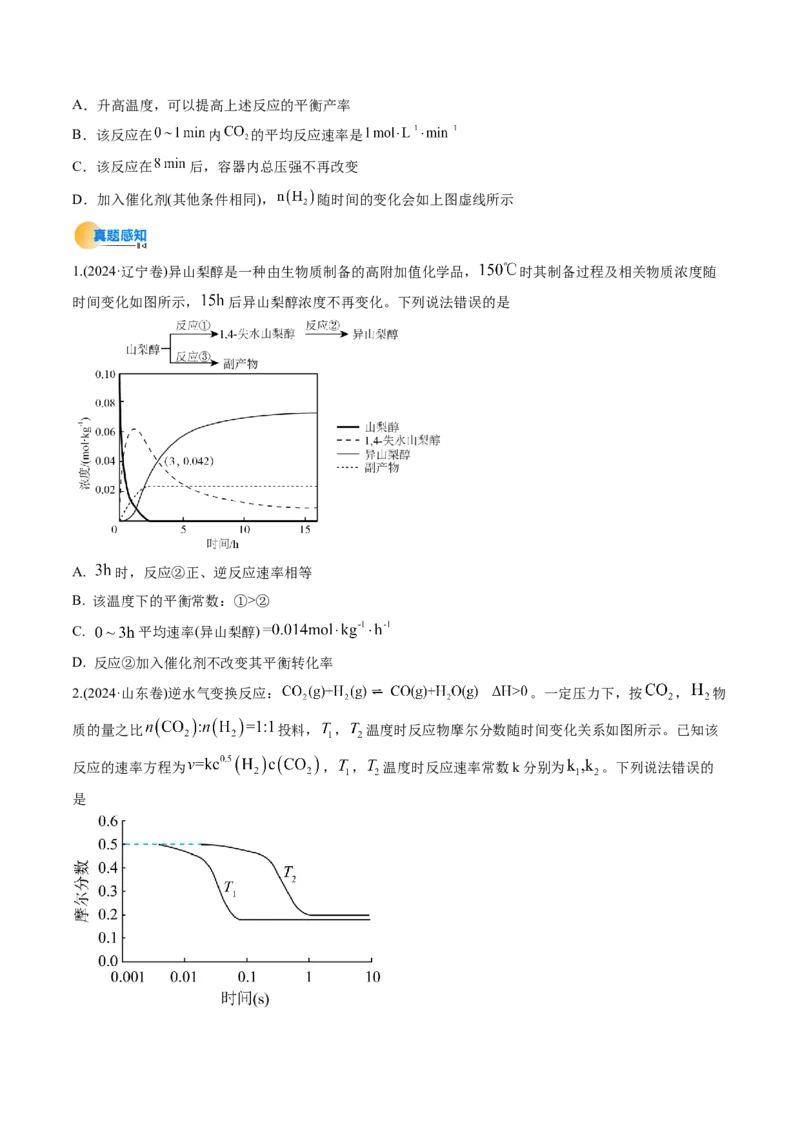
C.缩小c点对应容器的体积增大压强,v(正)②
C. 平均速率(异山梨醇)
D. 反应②加入催化剂不改变其平衡转化率
2.(2024·山东卷)逆水气变换反应: 。一定压力下,按 , 物
质的量之比 投料, , 温度时反应物摩尔分数随时间变化关系如图所示。已知该
反应的速率方程为 , , 温度时反应速率常数k分别为 。下列说法错误的
是A.
B. 温度下达平衡时反应速率的比值:
C. 温度不变,仅改变体系初始压力,反应物摩尔分数随时间的变化曲线不变
D. 温度下,改变初始投料比例,可使平衡时各组分摩尔分数与 温度时相同
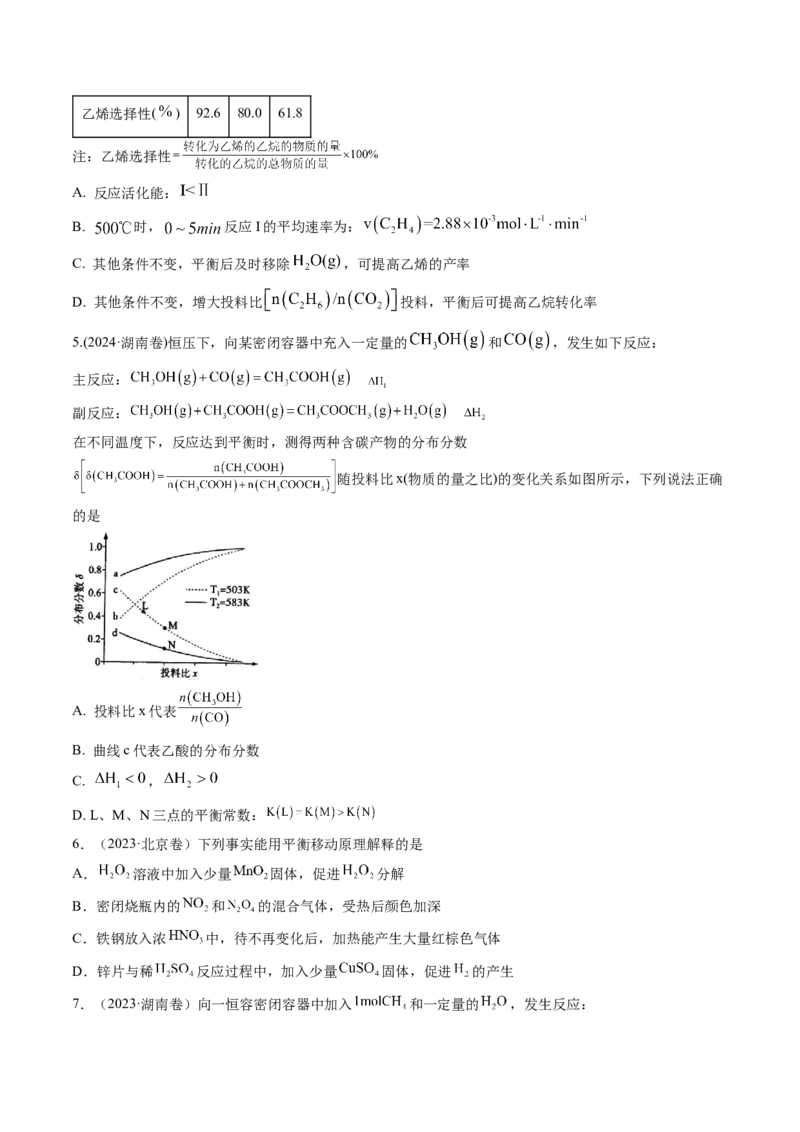
3.(2024·江苏卷)二氧化碳加氢制甲醇的过程中的主要反应(忽略其他副反应)为:
①
②
、 下,将一定比例 、 混合气匀速通过装有催化剂的绝热反应管。装置及L、L、
1 2
L…位点处(相邻位点距离相同)的气体温度、CO和 的体积分数如图所示。下列说法正确的是
3
A. L 处与L 处反应①的平衡常数K相等
4 5
B. 反应②的焓变
C. L 处的 的体积分数大于L 处
6 5
D. 混合气从起始到通过L 处,CO的生成速率小于 的生成速率
1
4.(2024·浙江卷6月)二氧化碳氧化乙烷制备乙烯,主要发生如下两个反应:
I.
II.
向容积为 的密闭容器中投入 和 ,不同温度下,测得 时(反应均未平衡)的
相关数据见下表,下列说法不正确的是
温度( ) 400 500 600
乙烷转化率( ) 2.2 9.0 17.8乙烯选择性( ) 92.6 80.0 61.8
注:乙烯选择性
A. 反应活化能:
B. 时, 反应I的平均速率为:
C. 其他条件不变,平衡后及时移除 ,可提高乙烯的产率
D. 其他条件不变,增大投料比 投料,平衡后可提高乙烷转化率
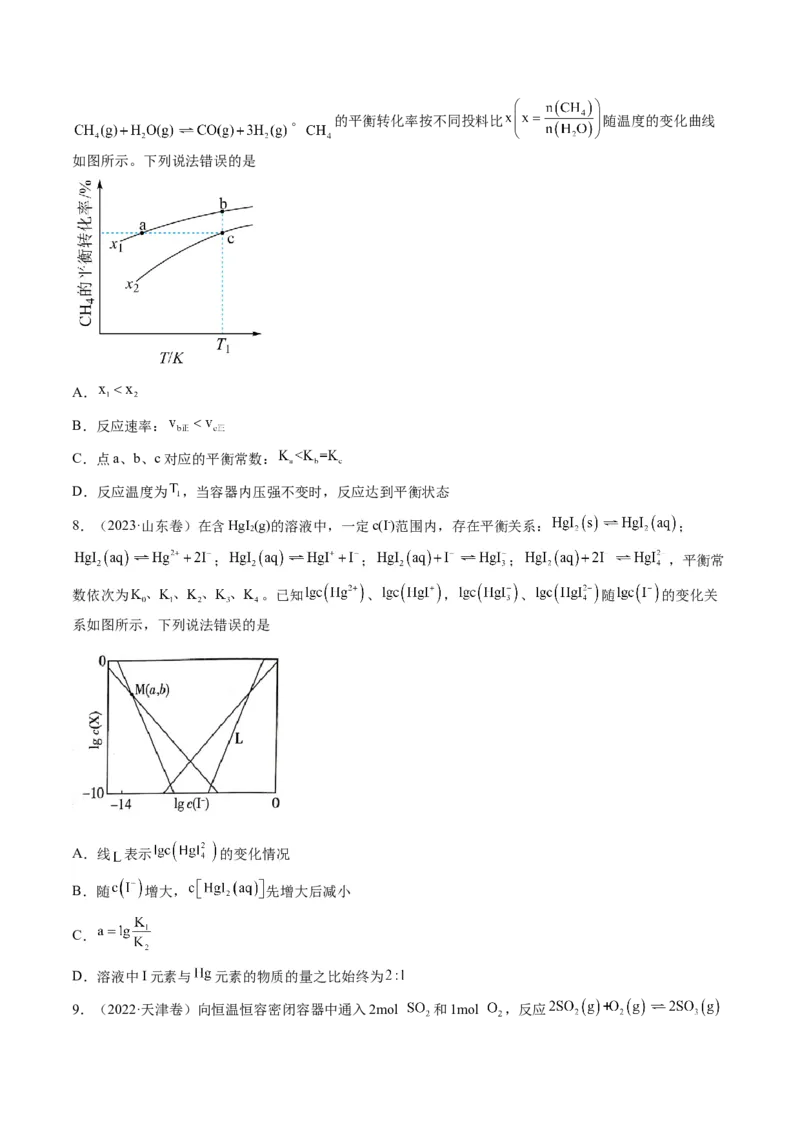
5.(2024·湖南卷)恒压下,向某密闭容器中充入一定量的 和 ,发生如下反应:
主反应:
副反应:
在不同温度下,反应达到平衡时,测得两种含碳产物的分布分数
随投料比x(物质的量之比)的变化关系如图所示,下列说法正确
的是
A. 投料比x代表
B. 曲线c代表乙酸的分布分数
C. ,
D. L、M、N三点的平衡常数:
6.(2023·北京卷)下列事实能用平衡移动原理解释的是
A. 溶液中加入少量 固体,促进 分解
B.密闭烧瓶内的 和 的混合气体,受热后颜色加深
C.铁钢放入浓 中,待不再变化后,加热能产生大量红棕色气体
D.锌片与稀 反应过程中,加入少量 固体,促进 的产生
7.(2023·湖南卷)向一恒容密闭容器中加入 和一定量的 ,发生反应:。 的平衡转化率按不同投料比 随温度的变化曲线
如图所示。下列说法错误的是
A.
B.反应速率:
C.点a、b、c对应的平衡常数:
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态
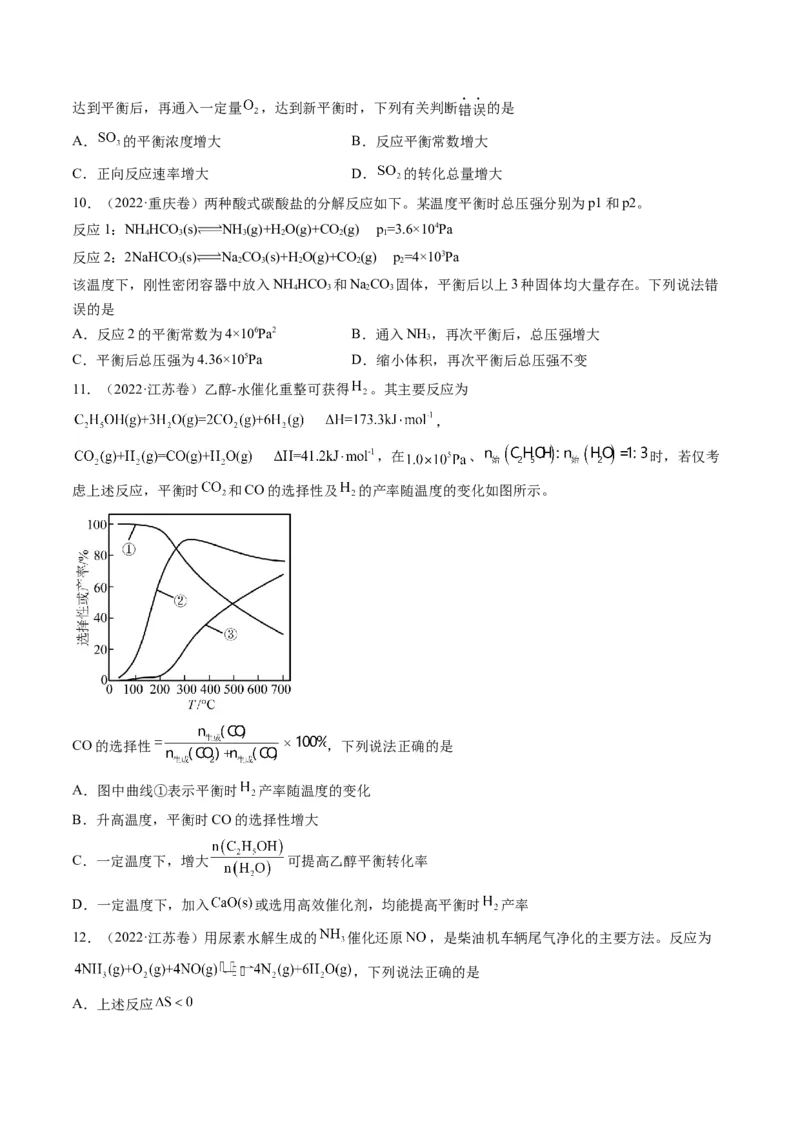
8.(2023·山东卷)在含HgI (g)的溶液中,一定c(I-)范围内,存在平衡关系: ;
2
; ; ; ,平衡常
数依次为 。已知 、 , 、 随 的变化关
系如图所示,下列说法错误的是
A.线 表示 的变化情况
B.随 增大, 先增大后减小
C.
D.溶液中I元素与 元素的物质的量之比始终为
9.(2022·天津卷)向恒温恒容密闭容器中通入2mol 和1mol ,反应达到平衡后,再通入一定量 ,达到新平衡时,下列有关判断错误的是
A. 的平衡浓度增大 B.反应平衡常数增大
C.正向反应速率增大 D. 的转化总量增大
10.(2022·重庆卷)两种酸式碳酸盐的分解反应如下。某温度平衡时总压强分别为p1和p2。
反应1:NH HCO (s) NH (g)+HO(g)+CO(g) p=3.6×104Pa
4 3 3 2 2 1
反应2:2NaHCO (s) NaCO(s)+HO(g)+CO(g) p=4×103Pa
3 2 3 2 2 2
该温度下,刚性密闭容器中放入NH HCO 和NaCO 固体,平衡后以上3种固体均大量存在。下列说法错
4 3 2 3
误的是
A.反应2的平衡常数为4×106Pa2 B.通入NH ,再次平衡后,总压强增大
3
C.平衡后总压强为4.36×105Pa D.缩小体积,再次平衡后总压强不变
11.(2022·江苏卷)乙醇-水催化重整可获得 。其主要反应为
,
,在 、 时,若仅考
虑上述反应,平衡时 和CO的选择性及 的产率随温度的变化如图所示。
CO的选择性 ,下列说法正确的是
A.图中曲线①表示平衡时 产率随温度的变化
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率
12.(2022·江苏卷)用尿素水解生成的 催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
,下列说法正确的是
A.上述反应B.上述反应平衡常数
C.上述反应中消耗 ,转移电子的数目为
D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小
13.(2022·浙江卷)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下
列说法不正确的是
A.实验①, ,
B.实验②, 时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
14.(2022·北京卷)某 多孔材料孔径大小和形状恰好将 “固定”,能高选择性吸附 。废
气中的 被吸附后,经处理能全部转化为 。原理示意图如下。
已知:
下列说法不正确的是
A.温度升高时不利于 吸附
B.多孔材料“固定” ,促进 平衡正向移动
C.转化为 的反应是
D.每获得 时,转移电子的数目为
15.(2022·辽宁卷)某温度下,在 恒容密闭容器中 发生反应2X(s) Y(g)+2Z(g),有关数据
如下:时间段/ 产物Z的平均生成速率/
0~2 0.20
0~4 0.15
0~6 0.10
下列说法错误的是
A. 时,Z的浓度大于
B. 时,加入 ,此时
C. 时,Y的体积分数约为33.3%
D. 时,X的物质的量为
16.(2022·湖南卷)向体积均为1L的两恒容容器中分别充入 和 发生反应:
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所
示。下列说法正确的是
A. B.气体的总物质的量:
C.a点平衡常数: D.反应速率:
17.(2022·广东卷)恒容密闭容器中, 在不同温度下达平衡时,
各组分的物质的量(n)如图所示。下列说法正确的是
A.该反应的
B.a为 随温度的变化曲线C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入 ,H 的平衡转化率增大
2
18.(2022·江苏卷)乙醇-水催化重整可获得 。其主要反应为
,
,在 、 时,若仅考
虑上述反应,平衡时 和CO的选择性及 的产率随温度的变化如图所示。
CO的选择性 ,下列说法正确的是
A.图中曲线①表示平衡时 产率随温度的变化
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率
19.(2022·海南卷)某温度下,反应CH=CH (g)+HO(g) CHCHOH(g)在密闭容器中达到平衡,下列
2 2 2 3 2
说法正确的是
A.增大压强, ,平衡常数增大
B.加入催化剂,平衡时 的浓度增大
C.恒容下,充入一定量的 ,平衡向正反应方向移动
D.恒容下,充入一定量的 , 的平衡转化率增大
20.(2022·浙江卷)AB型强电解质在水中的溶解(可视作特殊的化学反应)表示为AB(s)=An+(aq)+Bn-(aq),
其焓变和熵变分别为ΔH和ΔS。对于不同组成的AB型强电解质,下列说法正确的是
A.ΔH和ΔS均大于零
B.ΔH和ΔS均小于零
C.ΔH可能大于零或小于零,ΔS大于零
D.ΔH和ΔS均可能大于零或小于零