文档内容
考点 31 盐类的水解
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
.............................................................................................................................................2
考法01 盐类的水解及其规律...................................................................................................................2
考法02 盐类水解的影响因素及应用.......................................................................................................5
考法03 溶液中粒子浓度大小比较...........................................................................................................9
...........................................................................................................................................12
1.高考真题考点分布
考点内容 考点分布
2024·贵州卷,3分;2024·北京卷,3分;2024·湖北卷,3分;2023·天津卷,3
分;
盐类水解及其应用
2023·江苏卷,3分;2023·北京卷,3分;2022浙江卷,2分;2022浙江,2分;
2022海南卷,4分;2021广东卷,2分;2021北京卷,3分;
2024·江苏卷,3分;2024·湖南卷,3分;2024·山东卷,3分;2024·安徽卷,3
分;
离子浓度大小比较 2023·福建卷,3分;2023·重庆卷,3分;2023·天津卷,3分;2022重庆卷1,3
分;
202天津卷,3分;
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,水解方程式的书写、影响水解平衡的因素、水解在生产生活中的应
用、离子浓度大小的比较仍是高考命题的热点。
【备考策略】【命题预测】
预计2025年高考会以新的情境载体考查有关影响水解平衡的因素、电荷守恒、元素守恒、离子浓度大小的
比较知识,题目难度一般较大。
考法01 盐类的水解及其规律
1.盐类水解的实质
盐电离→→生成弱电解质→破坏了水的电离平衡→水的电离程度增大→c(H+)≠c(OH-)→溶液呈碱性或酸
性。
2.盐类水解的条件
(1)盐溶于水;
(2)盐在组成上必须具有弱酸根阴离子或弱碱阳离子。
3.盐类水解规律
有弱才水解,无弱不水解;越弱越水解,都弱都水解;谁强显谁性,同强显中性。
4.盐类水解方程式的书写
(1)一般要求
如NH Cl的水解离子方程式为NH+HO NH ·H O+H+。
4 2 3 2
(2)多元弱酸盐水解反应分步进行,以第一步为主,一般只写第一步水解方程式。如NaCO 的水解离子方
2 3
程式为CO+HO HCO+OH-。
2
(3)多元弱碱盐水解反应,水解离子方程式一步写完。如FeCl 的水解离子方程式为Fe3++3HO Fe(OH)
3 2 3
+3H+。
【易错提醒】
阴、阳离子相互促进且进行彻底的水解反应,如NaS溶液与AlCl 溶液混合反应的水解离子方程式为3S2-
2 3
+2Al3++6HO===3H S↑+2Al(OH) ↓。相互促进水解时,由于反应彻底,故生成物中出现的不溶于水的
2 2 3沉淀或气体均要注明状态,即写上“↓”或“↑”符号,中间用“===”连接。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)溶液呈中性的盐一定是强酸、强碱生成的盐。( )
(2)酸式盐溶液可能呈酸性,也可能呈碱性。( )
(3)某盐溶液呈酸性,该盐一定发生了水解反应。( )
(4)同温度、同浓度的NaCO 和CHCOONa溶液相比,CHCOONa溶液的pH大。( )
2 3 3 3
(5)常温下,pH=11的CHCOONa溶液与pH=3的CHCOOH溶液,水的电离程度相同。( )
3 3
(6)向NaAlO 溶液中滴加NaHCO 溶液,有沉淀和气体生成。( )
2 3
(7)酸式盐溶液一定呈酸性( )
(8)某盐溶液呈中性,则该盐一定是强酸、强碱盐( )
(9)同浓度的NaCO 溶液和CHCOONa溶液相比,前者pH大;同浓度的NaCO 溶液和NaHCO 溶液相比,
2 3 3 2 3 3
后者pH小( )
(10)常温下,pH=10的CHCOONa溶液与pH=4的NH Cl溶液中水的电离程度相同( )
3 4
【答案】(1)× (2)√ (3)× (4)× (5)× (6)× (7)× (8)× (9)√ (10)√
考向01 考查水解离子方程式
【例1】(2024·江苏镇江·一模)下列物质在常温时发生水解,对应的离子方程式正确的是( )
A.Na CO:CO+2HO HCO+2OH-
2 3 2 2 3
B.CuSO :Cu2++2HO===Cu(OH) +2H+
4 2 2
C.NaAlO :AlO+2HO Al(OH) +OH-
2 2 3
D.NaF:F-+HO===HF+OH-
2
【答案】C
【解析】A项,应为CO+HO HCO+OH-、HCO+HO HCO +OH-;B项,应为Cu2++2HO
2 2 2 3 2
Cu(OH) +2H+;D项,应为F-+HO HF+OH-。
2 2
【思维建模】书写水解相互促进且进行到底反应方程式
以FeCl 溶液与NaCO 溶液混合为例。
3 2 3
第一步:写出发生反应的两种离子及对应的产物。不溶性物质加“↓”,易分解的物质写分解产物。
Fe3++CO——Fe(OH) ↓+CO↑
3 2
第二步:配平电荷。
2Fe3++3CO——2Fe(OH) ↓+3CO↑
3 2
第三步:确定水的位置。因产物Fe(OH) 中含有H,反应物中无H,故HO为反应物。
3 2
2Fe3++3CO+HO——2Fe(OH) ↓+3CO↑
2 3 2
第四步:根据质量守恒定律配平。
2Fe3++3CO+3HO===2Fe(OH) ↓+3CO↑
2 3 2考向02 考查盐类水解规律
【例2】(2024·河南濮阳·质检)根据表中信息,判断0.10 mol·L-1的下列各物质的溶液pH最大的是( )
酸 电离常数(常温下)
CHCOOH K=1.75×10-5
3 a
HCO K =4.5×10-7,K =4.7×10-11
2 3 a1 a2
HS K =1.1×10-7,K =1.3×10-13
2 a1 a2
A.CHCOONa B.Na CO
3 2 3
C.NaHCO D.Na S
3 2
【答案】D
【解析】 根据表格中的酸的电离常数可知,酸性的强弱顺序为CHCOOH> H CO> H S>HCO> HS-,根据
3 2 3 2
越弱越水解的规律可知,水解能力强弱顺序为S2->CO>HS->HCO>CH COO-,故选项中0.10 mol·L-1的各
3
溶液pH最大的是NaS。
2
【思维建模】盐类水解程度大小比较的规律
1.组成盐的弱碱阳离子水解使溶液显酸性,组成盐的弱酸根离子水解使溶液显碱性。
2.盐对应的酸(或碱)越弱,水解程度越大,溶液碱性(或酸性)越强。
3.相同条件下的水解程度:
(1)正盐>相应的酸式盐,如NaCO>NaHCO ;
2 3 3
(2)水解相互促进的盐>单独水解的盐>水解相互抑制的盐。
【对点1】(2024·黑龙江伊春·模拟)下列电离或水解方程式正确的是( )
A.NaSO 的水解:SO 2-+2HO HSO +2OH-
2 3 3 2 2 3
B.NaHCO 的电离:NaHCO Na++H++CO2-
3 3 3
C.KHS溶液中HS-的电离:HS-+HO HO++S2-
2 3
D.NaClO溶液与FeCl 溶液混合:2ClO-+Fe2++2HO===2HClO+Fe(OH) ↓
2 2 2
【答案】C
【解析】NaSO 水解的离子方程式为SO 2-+HO HSO -+OH-,故A错误;NaHCO 的电离方程式为
2 3 3 2 3 3
NaHCO ===Na++HCO -,故B错误;KHS溶液中HS-的电离方程式为HS-+HO HO++S2-,故C正
3 3 2 3
确;NaClO溶液与FeCl 溶液混合发生氧化还原反应及双水解反应,故D错误。
2
【对点2】(2024·安徽合肥·模拟)已知在常温下测得浓度均为0.1 mol·L-1的下列6种溶液的pH如表所
示:
溶质 CHCOONa NaHCO NaCO NaClO NaCN C HONa
3 3 2 3 6 5
pH 8.8 9.7 11.6 10.3 11.1 11.3
下列反应不能成立的是( )
A.CO+HO+2NaClO===Na CO+2HClO
2 2 2 3
B.CO+HO+NaClO===NaHCO+HClO
2 2 3C.CO+HO+C HONa===NaHCO+C HOH
2 2 6 5 3 6 5
D.CHCOOH+NaCN===CH COONa+HCN
3 3
【答案】A
【解析】利用盐类水解规律“越弱越水解”,并结合题给信息可判断出对应酸的酸性强弱关系是
CHCOOH>H CO>HClO>HCN>C HOH>HCO - , 利 用 “ 强 酸 制 弱 酸 ” 进 行 判 断 。 酸 性
3 2 3 6 5 3
HCO>HClO>HCO -,因此 CO +HO+2NaClO===NaHCO +2HClO,A 项不成立,B 项成立;酸性
2 3 3 2 2 3
HCO>C HOH>HCO -,C项成立;酸性CHCOOH>HCN,D项成立。
2 3 6 5 3 3
考法02 盐类水解的影响因素及应用
1.内因——越弱越水解
形成盐的酸或碱越弱,其盐就越易水解。如同一条件下水解程度:NaCO>NaSO ,NaCO>NaHCO 。
2 3 2 3 2 3 3
2.外因
因素及其变化 水解平衡 水解程度 水解产生离子的浓度
温度 升高 右移 增大 增大
增大 右移 减小 增大
浓度
减小 (即稀释) 右移 增大 减小
外加 酸 弱碱阳离子水解程度减小
酸碱 碱 弱酸阴离子水解程度减小
以Fe3++3HO Fe(OH) +3H+为例
2 3
条件 移动方向 H+数 pH 现象
升温 向右 增多 减小 颜色变深
通HCl 向左 增多 减小 颜色变浅
加HO 向右 增多 增大 颜色变浅
2
加NaHCO 向右 减小 增大 生成红褐色沉淀,放出气体
3
【易错提醒】酸式盐一般既存在水解,又存在电离。如果酸式盐的电离程度大于其水解程度,溶液显酸性,
如NaHSO 溶液;如果酸式盐的水解程度大于其电离程度,则溶液显碱性,如NaHCO 溶液。
3 3
3.水解的应用
(1)判断溶液的酸碱性
NaCO 溶液呈碱性的原因: CO + H O HCO + OH - (用离子方程式表示)。
2 3 2
(2)判断盐溶液中粒子的种类及浓度的大小
如NaCO 溶液中存在的粒子有Na+ 、CO 、HCO、HCO 、OH-、H+、HO,且c(Na+)>2c(CO),c(OH
2 3 2 3 2
-)>c(H+)。
(3)判断离子能否共存
若阴、阳离子发生水解相互促进的反应,水解程度较大而不能大量共存,有的甚至水解完全。常见的水解
相互促进的反应进行完全的有Al3+、Fe3+与CO、HCO、AlO等。
(4)配制、保存某些盐溶液
如配制 FeCl 溶液时,为防止出现 Fe(OH) 沉淀,常加几滴盐酸来抑制 FeCl 的水解;在实验室盛放
3 3 3NaCO、CHCOONa、NaS等溶液的试剂瓶不能用磨口玻璃塞,应用橡胶塞。
2 3 3 2
(5)判断盐溶液蒸干灼烧时所得的产物
如AlCl 、FeCl 溶液蒸干后得到 Al(OH) 、 Fe(OH ) ,灼烧后得到 Al O 、 F e O ,CuSO 溶液蒸干后得到
3 3 3 3 2 3 2 3 4
CuSO 固体。
4
(6)解释生活中的现象或事实
如明矾净水、热纯碱溶液除油污、草木灰不能与铵盐混用、泡沫灭火器原理等。
(7)物质的提纯(水解除杂)
如MgCl 溶液中混有少量Fe3+杂质时,因Fe3+水解的程度比Mg2+的水解程度大,可加入MgO 或Mg(OH)
2 2
等,导致Fe3+的水解平衡向右移动,生成Fe(OH) 沉淀而除去。
3
4.水解常数与电离平衡常数
(1)水解常数的概念
在一定温度下,能水解的盐(强碱弱酸盐、强酸弱碱盐或弱酸弱碱盐)在水溶液中达到水解平衡时,生成的
弱酸(或弱碱)浓度和氢氧根离子(或氢离子)浓度之积与溶液中未水解的弱酸根阴离子(或弱碱的阳离子)浓度
之比是一个常数,该常数就叫水解平衡常数。
(2)水解常数(K )与电离常数的定量关系
h
①强碱弱酸盐如CHCOONa溶液:CHCOO-+HO CHCOOH+OH-
3 3 2 3
K =
h
=
==
即K =。
h
②强酸弱碱盐如NH Cl溶液:NH+HO NH ·H O+H+
4 2 3 2
K =
h
=
==
即K =。
h
【结论归纳】
①K·K =K 或K ·K =K 。
a h w b h w
②Na CO 的水解常数K =。
2 3 h
③NaHCO 的水解常数K =。
3 h
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)水解平衡右移,盐离子的水解程度可能增大,也可能减小( )
(2)稀溶液中,盐的浓度越小,水解程度越大,其溶液酸性(或碱性)也越强( )
(3)关于FeCl 溶液,加水稀释时,的值减小( )
3
(4)通入适量的HCl气体,使FeCl 溶液中,增大( )
3
【答案】(1)√ (2)× (3)√ (4) ×考向01 考查盐类水解及其影响因素
【例1】(2024·吉林辽源·一模)一定条件下,CHCOONa溶液存在水解平衡:CHCOO-+HO
3 3 2
CHCOOH+OH-,下列说法正确的是( )
3
A.加入少量NaOH固体,c(CHCOO-)增大
3
B.加入少量FeCl 固体,c(CHCOO-)增大
3 3
C.稀释溶液,溶液的pH增大
D.加入适量醋酸得到的酸性混合溶液中:c(Na+)>c(CHCOO-)>c(H+)>c(OH-)
3
【答案】A
【解析】加入少量NaOH固体,会增大溶液中OH-的浓度,使平衡向左移动,c(CHCOO-)增大,故A项
3
正确;加入少量FeCl 固体,FeCl 水解显酸性,CHCOONa水解显碱性,在同一溶液中相互促进水解,
3 3 3
c(CHCOO-)减小,故B项不正确;稀释溶液,c(OH-)减小,溶液的pH减小,故C项不正确;若c(Na+)>
3
c(CHCOO-)>c(H+)>c(OH-),则有c(Na+)+c(H+)>c(OH-)+c(CHCOO-),不符合电荷守恒原理,故D
3 3
项不正确。
考向02 考查盐类水解的应用
【例2】(2024·福建厦门·质检)下列物质的水溶液在空气中小心加热蒸干至质量不再减少为止,能得到较
纯净的原溶质的是( )
①CuSO ②FeSO ③KCO ④Ca(HCO ) ⑤NH HCO ⑥KMnO ⑦FeCl
4 4 2 3 3 2 4 3 4 3
A.全部都可以 B.仅①②③
C.仅①③⑥ D.仅①③
【答案】D
【解析】FeSO 溶液加热过程中生成Fe(OH) 和HSO ,又由于Fe(OH) 会被氧化生成Fe(OH) ,故蒸干后
4 2 2 4 2 3
得到Fe (SO ) 和Fe(OH) 的混合物;Ca(HCO ) 受热会分解生成CaCO ;NH HCO 受热分解生成NH 、
2 4 3 3 3 2 3 4 3 3
HO、CO;KMnO 受热分解生成KMnO 和MnO ;FeCl 受热促进水解生成Fe(OH) 和盐酸,而盐酸挥发
2 2 4 2 4 2 3 3
进一步促进其水解,最终水解彻底,受热分解得到的固体物质是Fe O。
2 3
【思维建模】盐溶液蒸干灼烧时所得产物的判断
(1)盐溶液水解生成难挥发性酸时,蒸干后一般得原物质,如CuSO (aq)――→CuSO (s);
4 4
盐溶液水解生成易挥发性酸时,蒸干灼烧后一般得对应的氧化物,如
AlCl (aq)――→Al(OH) ――→Al O。
3 3 2 3
(2)酸根离子易水解的强碱盐,如NaCO 溶液等蒸干后可得到原物质。
2 3
(3)考虑盐受热时是否分解。
(4)还原性盐在蒸干时会被O 氧化,如NaSO (aq)――→NaSO (s)。
2 2 3 2 4
考向03 考查水解平衡常数及其应用
【例3】(2024·江西宜春·质检)已知常温下,NaCO 溶液的水解常数K =2×10-4,则当溶液中
2 3 h
c(HCO)∶c(CO)=2∶1时,试求该溶液的pH=____________。
【答案】10【解析】K ==2×10-4,又c(HCO)∶c(CO)=2∶1,则c(OH-)=10-4 mol·L-1,结合常温下K =1.0×10-14,
h W
可得c(H+)=10-10 mol·L-1,则pH=10。
【对点1】(2024·江西鹰潭·模拟)在一定条件下,NaS溶液中存在水解平衡:S2-+HO HS-+OH
2 2
-。下列说法正确的是( )
A.稀释溶液,水解平衡常数增大
B.加入CuSO 固体,HS-浓度减小
4
C.升高温度,减小
D.加入NaOH固体,溶液pH减小
【答案】B
【解析】水解常数只与温度有关,A错误;Cu2++S2-===CuS↓,平衡左移,HS-浓度减小,B正确;水解
为吸热反应,升高温度平衡右移,因而增大,C错误;加入NaOH固体,溶液pH增大,D错误。
【对点2】(2024·广东韶关·模拟)下列有关问题与盐类的水解有关的是( )
①NH Cl与ZnCl 溶液可作焊接金属中的除锈剂
4 2
②草木灰与铵态氮肥不能混合施用
③实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
④加热蒸干CuCl 溶液得到Cu(OH) 固体
2 2
A.仅①②③ B.仅②③④
C.仅①④ D.①②③④
【答案】D
【解析】①NH Cl与ZnCl 溶液水解均显酸性,可以除去金属表面的锈;②草木灰的主要成分为碳酸钾,
4 2
水解显碱性,而铵态氮肥水解显酸性,因而不能混合施用;③碳酸钠溶液水解显碱性,而磨口玻璃塞中的
二氧化硅会与碱反应生成硅酸钠,将瓶塞与瓶口黏合在一块儿而打不开,因此实验室盛放碳酸钠的试剂瓶
应用橡胶塞;④CuCl 溶液中存在水解平衡:CuCl +2HO Cu(OH) +2HCl,加热时,HCl挥发使平衡
2 2 2 2
不断右移,最终得到Cu(OH) 固体。
2
【对点3】(2024·山东泰安·模拟)常温下,用NaOH溶液吸收SO 得到pH=9的NaSO 溶液,吸收过程
2 2 3
中水的电离平衡____________(填“向左”“向右”或“不”)移动。试计算所得溶液中=____________。
(常温下HSO 的电离常数K =1.0×10-2,K =6.0×10-8)
2 3 a1 a2
【答案】向右 60
【解析】NaOH电离出的OH-抑制水的电离,NaSO 电离出的SO水解促进水的电离。SO+HO HSO
2 3 2
+OH-的水解常数K ===,所以==60。
h
考法03 溶液中粒子浓度大小比较
一、熟悉两大理论
1.电离理论
(1)弱电解质的电离是微弱的,电离产生的微粒都非常少,同时还要考虑水的电离,如氨水溶液中:
NH ·H O、NH、OH-浓度的大小关系是c(NH ·H O)>c(OH-)>c(NH)。
3 2 3 2(2)多元弱酸的电离是分步进行的,其主要是第一级电离(第一步电离程度远大于第二步电离)。如在HS溶
2
液中:HS、HS-、S2-、H+的浓度大小关系是c(H S)>c(H+)>c(HS-)>c(S2-)。
2 2
2.水解理论
(1)弱电解质离子的水解损失是微量的(相互促进的水解除外),但由于水的电离,故水解后酸性溶液中c(H+)
或碱性溶液中c(OH-)总是大于水解产生的弱电解质的浓度。如NH Cl溶液中:NH、Cl-、NH ·H O、H+的
4 3 2
浓度大小关系是c(Cl-)>c(NH)>c(H+)>c(NH ·H O)。
3 2
(2)多元弱酸酸根离子的水解是分步进行的,其主要是第一步水解,如在NaCO 溶液中:CO、HCO、
2 3
HCO 的浓度大小关系应是c(CO)>c(HCO)>c(H CO)。
2 3 2 3
二、把握两种守恒
1.电荷守恒规律
电解质溶液中,无论存在多少种离子,溶液都是呈电中性,即阴离子所带负电荷总数一定等于阳离子所带
正电荷总数。如NaHCO 溶液中存在着Na+、H+、HCO、CO、OH-,存在如下关系:c(Na+)+c(H
3
+)===c(HCO)+c(OH-)+2c(CO)。
2.元素质量守恒规律
电解质溶液中,由于某些离子能够水解,离子种类增多,但元素质量是守恒的。如KS溶液中S2-、HS-都
2
能水解,故S元素以S2-、HS-、HS三种形式存在,它们之间有如下守恒关系:c(K+)=2c(S2-)+2c(HS-)
2
+2c(H S)。
2
考向01 考查单一溶液中粒子浓度的关系
【例1】(2024·广东梅州·一模)室温下,下列指定溶液中粒子的浓度关系正确的是( )
A.0.1 mol ·L-1(NH )SO 溶液:c(SO)>c(NH)>c(H+)>c(OH-)
4 2 4
B.0.1 mol ·L-1NaCO 溶液:c(OH-)=c(H+)+c(HCO)+c(H CO)
2 3 2 3
C.0.1 mol ·L-1明矾溶液:c(SO)>c(K+)>c(Al3+)>c(H+)>c(OH-)
D.0.1 mol ·L-1的NaHCO 溶液:c(Na+)=c(HCO)+c(H CO)+2c(CO)
3 2 3
【答案】C
【解析】0.1 mol ·L-1(NH )SO 溶液中铵根离子水解,溶液显酸性,但水解程度不大,则c(NH)>c(SO)>
4 2 4
c(H+)>c(OH-),A错误;根据质子守恒,应是c(OH-)=c(H+)+c(HCO)+2c(H CO),B错误;明矾溶液
2 3
中Al3+发生水解,C正确;由元素质量守恒知,c(CO)不应乘以2,D错误。
【思维建模】比较电解质溶液中粒子浓度相对大小的解题思路考向02 考查混合溶液中粒子浓度关系
【例2】(2024·四川绵阳·质检)25 ℃时,在10 mL浓度均为0.1 mol ·L-1 的NaOH和NH ·H O混合溶液
3 2
中滴加0.1 mol ·L-1的盐酸。下列有关溶液中粒子浓度关系正确的是( )
A.未加盐酸时:c(OH-)>c(Na+)=c(NH ·H O)
3 2
B.加入10 mL盐酸时:c(NH)+c(H+)=c(OH-)
C.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
D.加入20 mL盐酸时:c(Cl-)=c(NH)+c(Na+)
【答案】B
【解析】A项,NH ·H O是弱电解质,能部分电离,溶液中c(Na+)>c(NH ·H O);B项,当加入10 mL盐酸
3 2 3 2
时,恰好将NaOH中和完,溶液中c(Na+)=c(Cl-),根据电荷守恒:c(Na+)+c(NH)+c(H+)=c(Cl-)+c(OH
-)可知,c(NH)+c(H+)=c(OH-);C项,溶液pH=7时,溶液中c(H+)=c(OH-),根据电荷守恒可知c(Na
+)+c(NH)=c(Cl-);D项,加入20 mL盐酸时,恰好将NaOH和NH ·H O中和完,根据元素质量守恒有
3 2
c(Na+)+c(NH)+c(NH ·H O)=c(Cl-)。
3 2
【思维建模】构建思维模型
【对点1】(2024·陕西咸阳·模拟)常温下,浓度均为0.1 mol·L-1的下列溶液中,粒子的物质的量浓度关系正确的是( )
A.氨水中,c(NH)=c(OH-)=0.1 mol·L-1
B.NHCl溶液中,c(NH)>c(Cl-)
4
C.Na SO 溶液中,c(Na+)>c(SO)>c(OH-)=c(H+)
2 4
D.Na SO 溶液中,c(Na+)=2c(SO)+c(HSO)+c(H SO )
2 3 2 3
【答案】C
【解析】氨水为弱碱溶液,只能部分电离出OH-,结合电荷守恒:c(NH)+c(H+)=c(OH-),可得c(NH)<
c(OH-)<0.1 mol·L-1,A错误;NH Cl溶液中,NH部分水解、Cl-浓度不变,则溶液中:c(NH)<c(Cl-),
4
B错误;NaSO 溶液显中性:c(OH-)=c(H+),结合电荷守恒可得:c(Na+)=2c(SO),溶液中离子浓度大小
2 4
为c(Na+)>c(SO)>c(OH-)=c(H+),C正确;根据NaSO 溶液中的元素质量守恒可得:c(Na+)=2c(SO)+
2 3
2c(HSO)+2c(H SO ),D错误。
2 3
【对点2】(2024·安徽滁州·模拟)一定温度下,下列溶液的离子浓度关系式正确的是( )
A.pH=5的HS溶液中,c(H+)=c(HS-)=1×10-5 mol ·L-1
2
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的HC O 溶液与pH=12的NaOH溶液以任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC O)
2 2 4 2
D.pH相同的①CHCOONa,②NaHCO ,③NaClO三种溶液的c(Na+):①>②>③
3 3
【答案】D
【解析】A项,pH=5的HS溶液中,H+的浓度为1×10-5 mol ·L-1,但是HS-的浓度会小于H+的浓度,
2
H+来自HS的第一步电离、HS-的电离和水的电离,故H+的浓度大于HS-的浓度,故不正确;B项,弱
2
碱不完全电离,弱碱稀释10倍时,pH减小不到一个单位,a<b+1,故不正确;C项,草酸是弱酸,氢氧
化钠是强碱,无论怎样混合得到的溶液都符合电荷守恒,而该等式中缺少草酸根,不符合电荷守恒,故不
正确;D项,因为酸性:醋酸>碳酸>次氯酸,根据越弱越水解的原则,pH相同的三种钠盐,浓度的大小
关系为醋酸钠>碳酸氢钠>次氯酸钠,则钠离子的浓度为①>②>③,故正确。
1.(2024·广东佛山·学业考试)下列物质溶于水,因水解而呈碱性的是
A. B. C. D.
【答案】A
【解析】A.KS是强碱弱酸盐,溶于水电离出的硫离子水解呈碱性,故A符合题意;
2
B.NH 与水反应生成一水合氨电离而呈碱性,故B不符合题意;
3
C. 是强酸弱碱盐,Cu2+水解呈酸性,故C不符合题意;
D. 是强酸酸式盐,电离出氢离子呈酸性,故D不符合题意;答案选A。
2.(2024·广东东莞·期末)下列溶液中离子能大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
【答案】D
【解析】A.在溶液中, 、 会发生反应,生成 等,再与Ba2+反应生成BaCO 沉淀,不能大量
3
共存,A不符合题意;
B.在溶液中, 能与 反应生成HClO,能将 氧化,不能大量共存,B不符合题意;
C.在溶液中, 与 能发生双水解反应,不能大量共存,C不符合题意;
D.在溶液中, 、 、 、 不能发生反应,可大量共存,D符合题意;
故选D。
3.(2024·湖北襄阳·期中)下列反应的离子方程式正确的是
A.向次氯酸钠溶液中通入足量二氧化硫:ClO-+SO+H O=HClO+HSO
2 2
B.偏铝酸钠溶液和碳酸氢钠溶液反应:AlO +H O+HCO =Al(OH) ↓+CO
2 3
C.HSO 溶液中滴入氯化钙溶液:SO +Ca2+=CaSO ↓
2 3 3
D.向硫酸亚铁溶液中通硫化氢气体:HS+Fe2+=FeS↓+2H+
2
【答案】B
【解析】A.向次氯酸钠溶液中通入足量二氧化硫,发生氧化还原反应,
,A错误;
B.偏铝酸根和碳酸氢根发生双水解,B正确;
C.根据强酸制弱酸原理,HSO 溶液中滴入氯化钙溶液不反应,C错误;
2 3
D.硫酸亚铁溶液中通入HS气体,该反应不发生,无法获得氯化亚铁,D错误;
2
故答案为:B。
4.(2024·安徽合肥·期末)在日常生产生活中,经常涉及化学反应原理,下列过程或现象与盐类水解无关
的是
A.加热氯化铁溶液,颜色变深
B. 与 溶液可用作焊接金属时的除锈剂
C.氯化钙溶液中滴加甲基橙,溶液显黄色
D.实验室中盛放 溶液的试剂瓶不能用磨口玻璃塞
【答案】C
【解析】A.氯化铁为强酸弱碱盐,加热能促进Fe3+的水解平衡正向移动,生成氢氧化铁胶体,溶液的颜
色加深,故A不符合题意;
B.NH Cl与ZnCl 都是强酸弱碱盐,水解呈酸性,产生的HCl可以作为除锈剂,与盐类水解有关,故B不
4 2符合题意;
C.氯化钙是强酸强碱盐,氯化钙溶液是中性的,滴加甲基橙,溶液显黄色,与盐类水解无关,故C符合
题意;
D.NaCO 是强碱弱酸盐,水解后呈碱性,玻璃中的成分SiO 在碱性溶液中反应生成硅酸钠,容易使瓶塞
2 3 2
粘住瓶口,与盐类水解有关,故D不符合题意;
故选C。
5.(2024·吉林延边·期中)下列问题与盐的水解有关的有几项
①NH Cl与ZnCl 溶液可作焊接金属时的、除锈剂;
4 2
②NaHCO 与Al (SO ) 两种溶液可作泡沫灭火剂;
3 2 4 3
③草木灰(主要成分KCO)与铵态氮肥不能混合施用;
2 3
④实验室中盛放NaCO 溶液的试剂瓶不能用磨口玻璃塞;
2 3
⑤加热蒸干CuCl 溶液并灼烧,可以得到CuO固体;
2
⑥要除去FeCl 溶液中混有的Fe2+,可通入氧化剂Cl;
3 2
⑦热纯碱溶液洗涤油污的能力比冷纯碱溶液强;
⑧误将钡盐[ BaCl 、Ba(NO )]当作食盐食用后,常用0.5%的NaSO 溶液解毒;
2 3 2 2 4
⑨石灰岩(喀斯特地貌)溶洞的形成;
⑩BaCO 不能作“钡餐”,而BaSO 可以。
3 4
A.4 B.5 C.6 D.7
【答案】C
【解析】①NH Cl与ZnCl 溶液都是强酸弱碱盐,水解使溶液显弱酸性,因此可作焊接金属时的、除锈
4 2
剂,与盐的水解有关,①符合题意;
②NaHCO 是强碱弱酸盐,水解使溶液显碱性;Al (SO ) 是强酸弱碱盐,水解使溶液显酸性,当两种溶液
3 2 4 3
混合时,水解反应相互促进,会发生反应产生Al(OH) 沉淀、CO 气体,它们不支持燃烧,能够隔绝空
3 2
气,因此可作泡沫灭火剂,与盐的水解反应有关,②符合题意;
③草木灰(主要成分KCO)水解使溶液显碱性,当其与铵态氮肥混合会发生反应产生NH 逸出,导致肥效
2 3 3
降低,因此二者不能混合施用,与盐的水解反应有关,③符合题意;
④Na CO 溶液水解显碱性,能够与玻璃中的SiO 发生反应,产生的物质NaSiO 会将试剂瓶与玻璃塞粘在
2 3 2 2 3
一起,因此实验室中盛放NaCO 溶液的试剂瓶不能用磨口玻璃塞,与盐的水解反应有关,④符合题意;
2 3
⑤CuCl 是强酸弱碱盐,在溶液中CuCl 发生水解反应产生Cu(OH) 、HCl,加热溶液,水解产生的HCl挥
2 2 2
发逸出,当蒸干CuCl 溶液时并灼烧,产生固体Cu(OH) 分解产生CuO,因此最终可以得到CuO固体,与
2 2
盐的水解反应有关,⑤符合题意;
⑥Fe2+具有还原性,与Cl 会发生反应产生FeCl ,达到除杂目的,故要除去FeCl 溶液中混有的Fe2+,可通
2 3 3
入氧化剂Cl,与盐的水解反应无关,⑥不符合题意;
2
⑦碱性溶液能够与油脂发生反应产生可溶性物质,因而可去除油污;纯碱是碳酸钠,属于强碱弱酸盐,水
解使溶液显碱性,盐水解反应是吸热反应,升高温度,盐水解程度增大,盐溶液碱性增强,因而热纯碱溶
液洗涤油污的能力比冷纯碱溶液强,与盐的水解反应有关,⑦符合题意;
⑧误将钡盐[ BaCl 、Ba(NO )]当作食盐食用后,常用0.5%的NaSO 溶液解毒,是由于它们会发生复分解
2 3 2 2 4反应产生既不溶于水,也不溶于酸的BaSO 沉淀,与盐的水解反应无关,⑧不符合题意;
4
⑨石灰岩(喀斯特地貌)溶洞的形成是由于CaCO 与溶于水的CO、HO发生反应产生可溶性Ca(HCO ) 随流
3 2 2 3 2
水被冲走形成溶洞,与盐的水解反应无关,⑨不符合题意;
⑩BaCO 不能作“钡餐”,而BaSO 可以,是由于BaCO 不溶于水,但能够溶于盐酸,而BaSO 既不溶于
3 4 3 4
水,也不溶于酸,因此BaCO 不能作“钡餐”,而BaSO 可以,与盐的水解反应无关,⑩不符合题意;
3 4
综上所述可知:物质应用与盐的水解反应有关的是①②③④⑤⑦,共6项,故合理选项是C。
6.(2024·广东·二模)安息香酸(HR)是最简单的一元芳香酸,其钠盐(用NaR表示)的水溶液呈碱性。已知
常温下, 。下列说法正确的是
A.常温下, HR水溶液的
B.向NaR水溶液中加水稀释,溶液的pH升高
C.NaR水溶液中,
D.常温下,NaR溶液的碱性比同浓度的 溶液弱
【答案】D
【解析】A.由题意,HR是有机酸,是弱酸,不完全电离,常温下,0.001mol⋅L-1 HR水溶液的pH>3,A
错误;
B.NaR水溶液中由于R-水解显碱性,加水稀释水解程度变大,但是碱性变弱,溶液的pH减小,B错误;
C.NaR水溶液中的质子守恒为c(HR)+c(H+)=c(OH-),C错误;
D.由已知,K (HR)>K (H CO),HR酸性比碳酸强,根据越弱越水解,同浓度的NaHCO 溶液水解程度
a a1 2 3 3
大,碱性强,故NaR溶液的碱性弱,D正确;
本题选D。
7.(2024·贵州毕节·期末)在0.1mol/L 溶液中各种微粒浓度关系错误的是
A.
B. mol/L
C.
D.
【答案】A
【解析】A.根据电荷守恒,c(Na+)+c(H+)=2c( )+c( )+c(OH-),故A错误;
B.根据物料守恒,c(Na+)=2{c(CO )+c(HCO )+c(H CO)},则
2 3
,故B正确;
C.碳酸钠水解后呈现碱性,因此 ,故C正确;
D.根据质子守恒,c(OH-)=c(H+)+c(HCO )+2c(H CO),故D正确;
2 3故答案A。
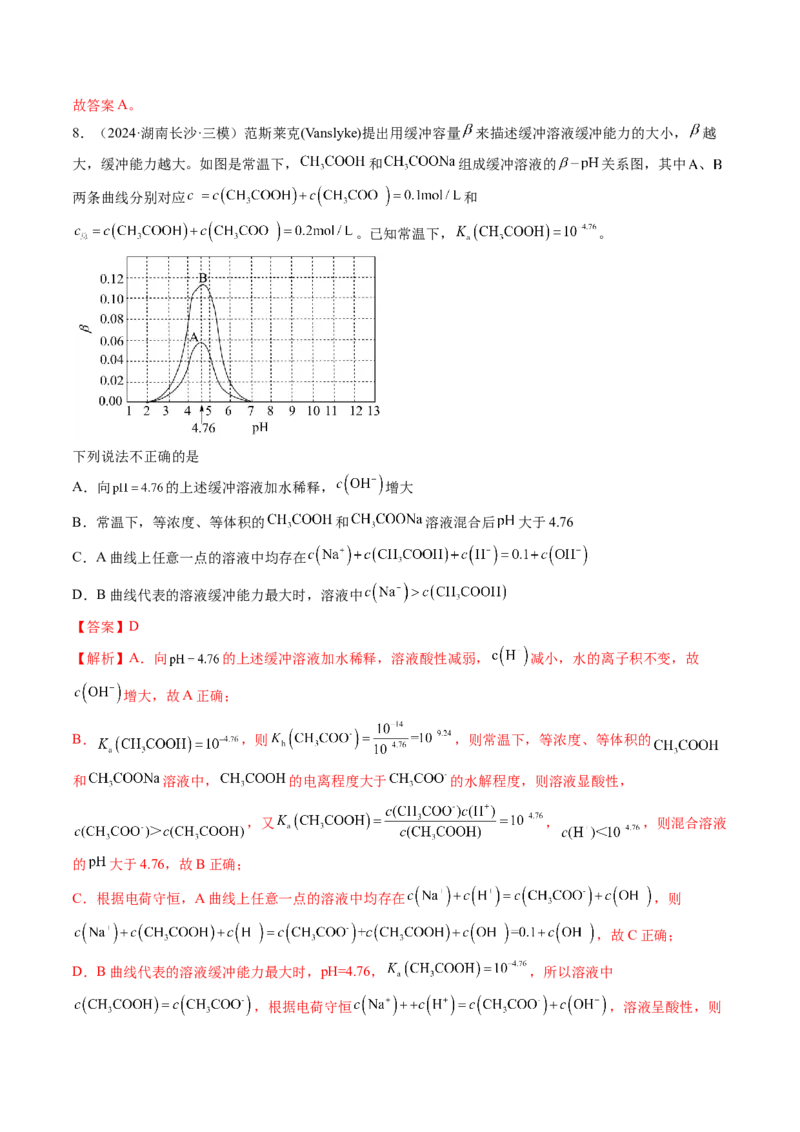
8.(2024·湖南长沙·三模)范斯莱克(Vanslyke)提出用缓冲容量 来描述缓冲溶液缓冲能力的大小, 越
大,缓冲能力越大。如图是常温下, 和 组成缓冲溶液的 关系图,其中
两条曲线分别对应 和
。已知常温下, 。
下列说法不正确的是
A.向 的上述缓冲溶液加水稀释, 增大
B.常温下,等浓度、等体积的 和 溶液混合后 大于4.76
C.A曲线上任意一点的溶液中均存在
D.B曲线代表的溶液缓冲能力最大时,溶液中
【答案】D
【解析】A.向 的上述缓冲溶液加水稀释,溶液酸性减弱, 减小,水的离子积不变,故
增大,故A正确;
B. ,则 ,则常温下,等浓度、等体积的
和 溶液中, 的电离程度大于 的水解程度,则溶液显酸性,
,又 , ,则混合溶液
的 大于4.76,故B正确;
C.根据电荷守恒,A曲线上任意一点的溶液中均存在 ,则
,故C正确;
D.B曲线代表的溶液缓冲能力最大时,pH=4.76, ,所以溶液中
,根据电荷守恒 ,溶液呈酸性,则,所以 ,故D错误;
故选D。
9.(2024·广东梅州·一模)乙氨酸( )是一种两性有机物,可与盐酸反应生成盐酸盐(
)。已知 水溶液呈酸性,下列叙述正确的是
A. 水溶液的pH=3
B. 水溶液加水稀释,pH升高
C. 在水中的电离方程式为:
D. 水溶液中:
【答案】B
【解析】A.HOOCCH NH Cl为强酸弱碱盐,电离出的 会发生水解,弱碱离子的水解较为
2 3
微弱,因此0.001mol/L溶液的pH>3,故A错误;
B.稀释溶液时, 水解程度将增大,根据勒夏特列原理可知溶液中将氢离子浓度减小,溶
液pH升高,故B正确;
C.HOOCCH NH Cl为强酸弱碱盐,在水中电离方程式为HOOCCH NH Cl= +Cl-,故C错
2 3 2 3
误;
D.根据电荷守恒可知,溶液中c(OH−)+c(Cl−)=c( )+c(H+),根据物料守恒,有c(Cl−)=c(
)+c(HOOCCH NH ),都与选项中等式不对应,故D错误;
2 2
故答案为B。
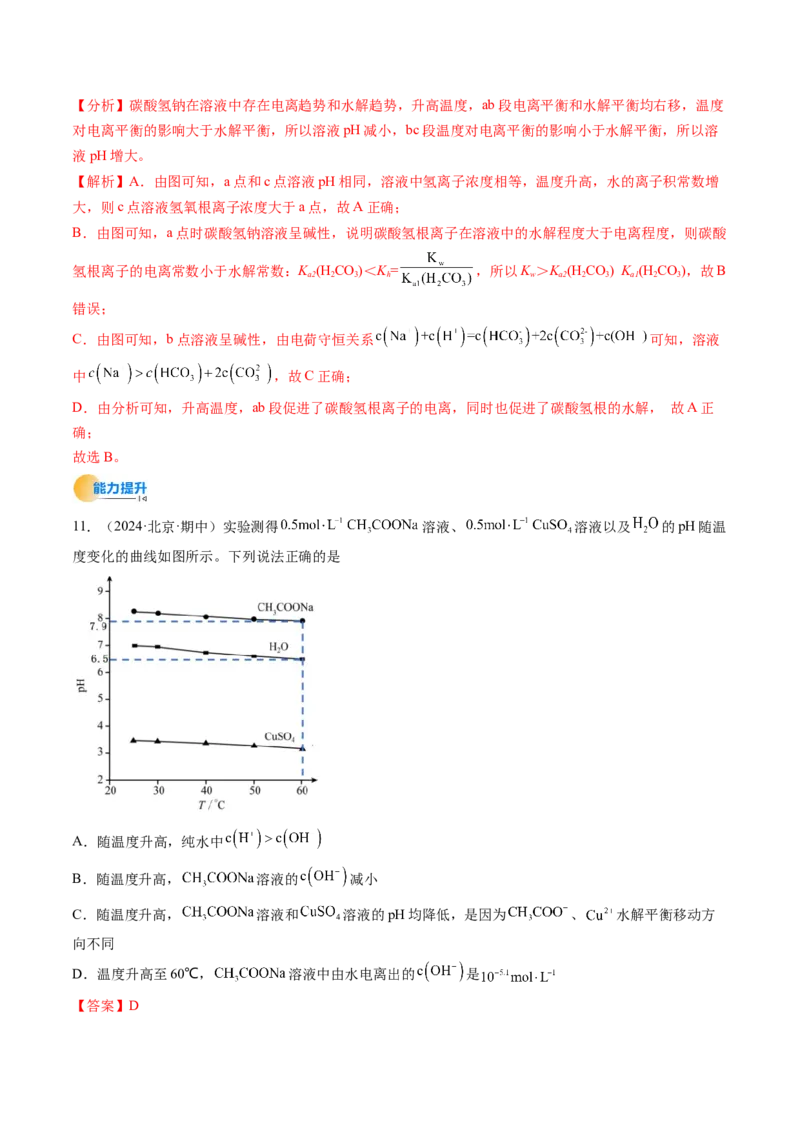
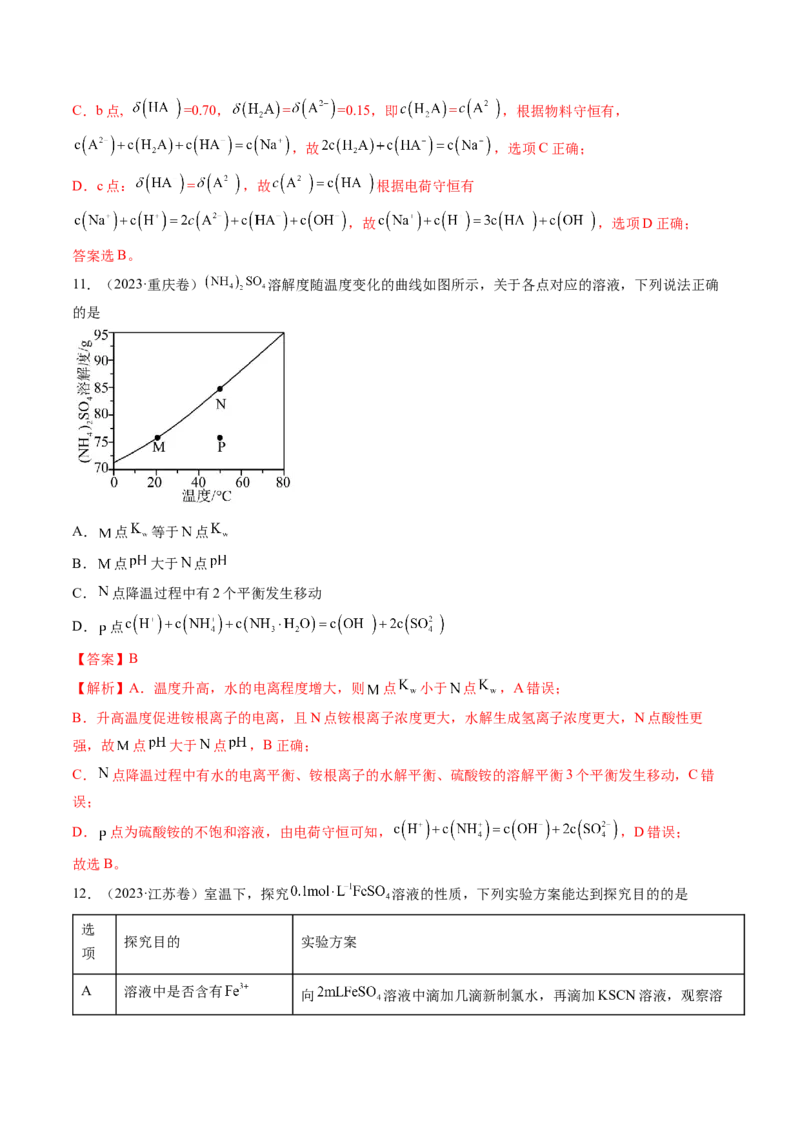
10.(2024·山东青岛·期中)如图为某实验测得 溶液在升温过程中(不考虑水挥发)的pH
变化曲线,下列说法错误的是
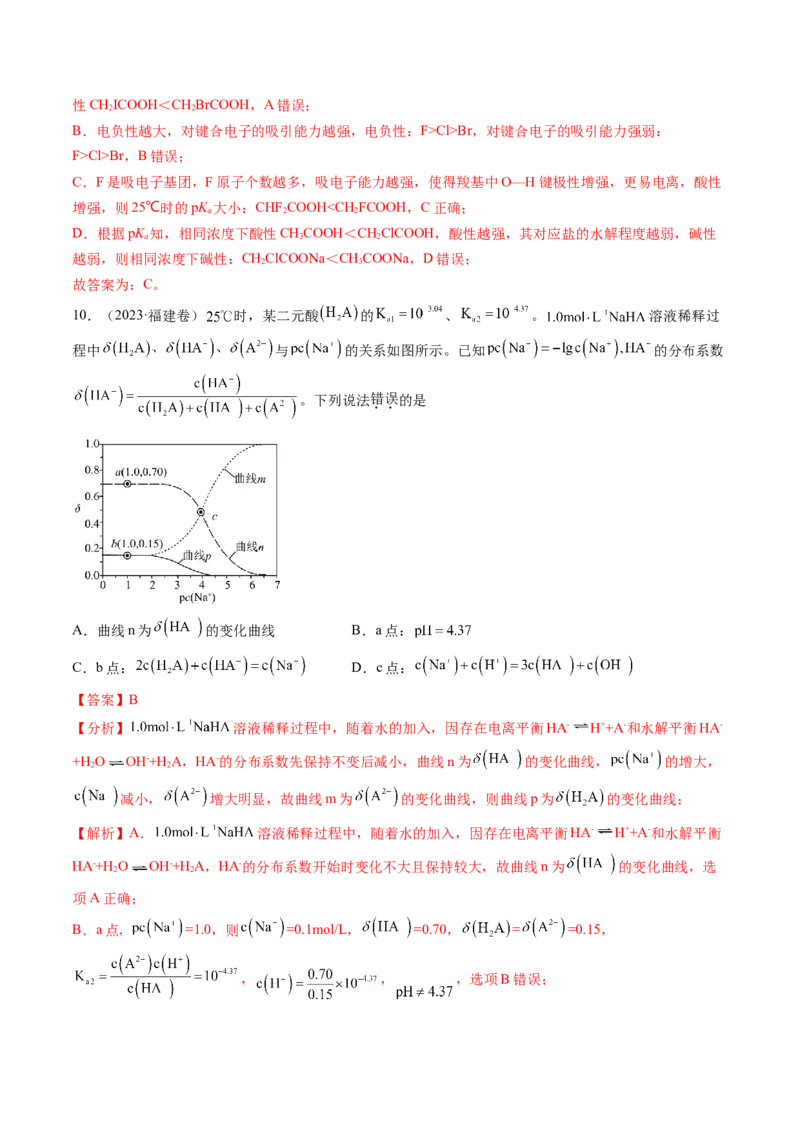
A.溶液的 :a点Cl>Br,对键合电子的吸引能力强弱:
F>Cl>Br,B错误;
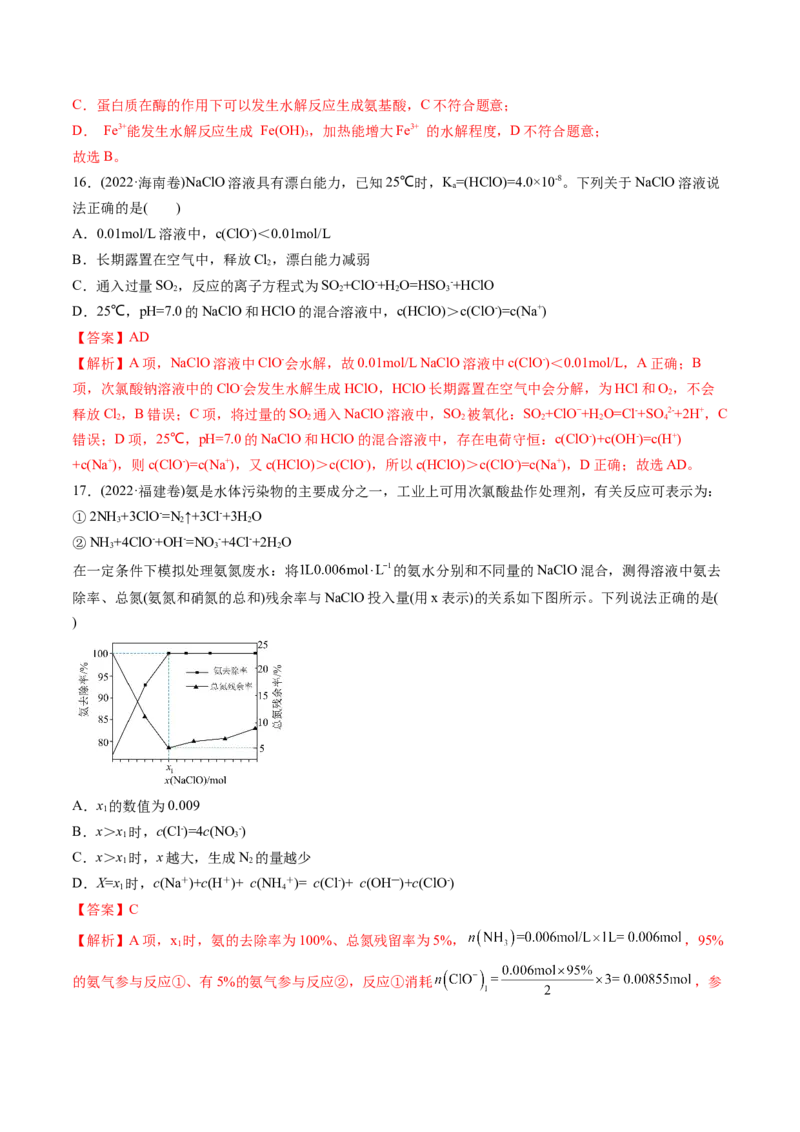
C.F是吸电子基团,F原子个数越多,吸电子能力越强,使得羧基中O—H键极性增强,更易电离,酸性
增强,则25℃时的pK 大小:CHF COOHx 时,反应①也生成氯离子,所以c(Cl-)>4c(NO -),B错误;C项,x>x 时,x越大,氨总去
1 3 1
除率不变,氮残余率增大,说明生成的硝酸根离子越多,生成N 的量越少,C正确;D项,x=x 时,氨的
2 1
去除率为100%,溶液中没有NH +和ClO-,含有Na+、H+、NO -、Cl-和OH-,根据电荷守恒得c(Na+)+c(H
4 3
+)= c(Cl-)+ c(OH―)+c(NO -),D错误;故选C。
3
18.(2022·浙江卷) 时,向 浓度均为0.1mol·L-1的盐酸和醋酸的混合溶液中逐滴加入0.1mol·L-1的
NaOH溶液(醋酸的K=1.8×10-5;用0.1mol·L-1的NaOH溶液滴定20mL等浓度的盐酸,滴定终点的 突
a
跃范围4.3~9.7)。下列说法不正确的是( )
A.恰好中和时,溶液呈碱性
B.滴加NaOH溶液至pH=4.3的过程中,发生反应的离子方程式为:H++OH-=H O
2
C.滴定过程中,c(Cl-)=c(CH COO-)+c(CH COOH)
3 3
D. 时,c(Na+)>c(Cl-)>c(CHCOO-)>c(CHCOOH)
3 3
【答案】B
【解析】A项,恰好中和时,生成氯化钠溶液和醋酸钠溶液,其中醋酸根离子会水解,溶液显碱性,A正
确;B项,滴加NaOH溶液至pH=4.3的过程中,若只发生反应的离子方程式:H++OH-=H O,则滴加
2
NaOH溶液的体积为20mL,则根据电离常数,0.1mol·L-1的醋酸中,c(H+)≈c(CH COO-)=
3
= = >1.0×10-4.3,故用氢氧化钠滴定的过程中,醋酸也参加了反应,则离子
方程式为:H++OH-=H O和CHCOOH+OH-=CH COO-+H O,B错误;C项,滴定前盐酸和醋酸的浓度相
2 3 3 2
同,故滴定过程中,根据物料守恒可知:c(Cl-)=c(CH COO-)+c(CH COOH),C正确;D项,向20mL浓度
3 3
均为0.1mol·L-1的盐酸和醋酸的混合溶液中逐滴加入0.1mol·L-1的NaOH溶液,当盐酸的体积为20ml时,
溶液为氯化钠和醋酸的混合溶液,显酸性,需要再滴加适量的氢氧化钠,当加入的NaOH溶液的体积为
30mL时,溶液为NaCl和等浓度的CHCOONa、CHCOOH,根据Ka=1.8×10-5>Kh= 可知,
3 3
此时溶液仍然呈酸性,需继续滴加NaOH溶液,故有c(Na+)>c(Cl-)>c(CHCOO-)>c(CHCOOH),D正
3 3
确;故选B。
19.(2022·浙江卷) 时,苯酚(C HOH)的K=1.0×10-10,下列说法正确的是( )
6 5 a
A.相同温度下,等 的C HONa和CHCOONa溶液中,c (C HO-)>c(CHCOO-)
6 5 3 6 5 3
B.将浓度均为0.1mol·L-1的C HONa和NaOH溶液加热,两种溶液的 均变大
6 5
C. 时,C HOH溶液与NaOH溶液混合,测得 ,则此时溶液中c (C HO-)= c (C HOH)
6 5 6 5 6 5
D. 时,0.1mol·L-1的C HOH溶液中加少量C HONa固体,水的电离程度变小
6 5 6 5
【答案】C
【解析】A项,醋酸的酸性大于苯酚,则醋酸根离子的水解程度较小,则相同温度下,等pH的C HONa
6 5
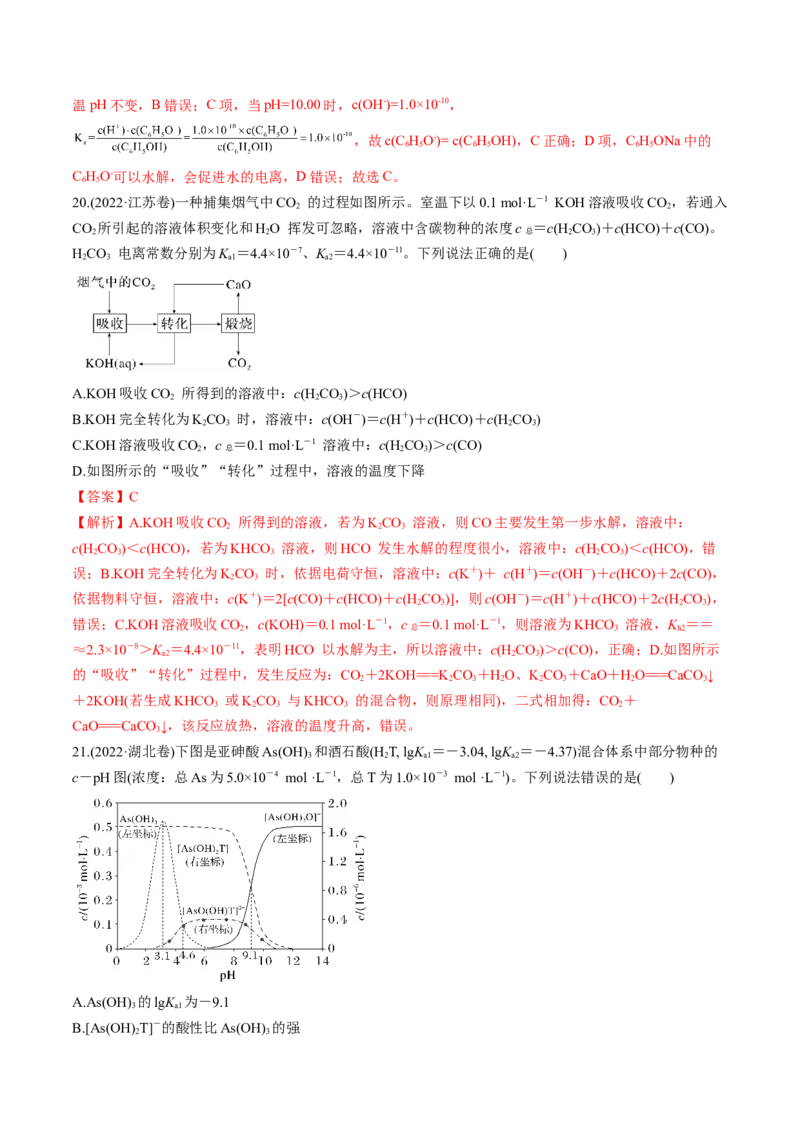
和CHCOONa溶液中c(C HO-)K ,所以[As(OH) T]-的酸性比As(OH) 的强,B
3 3 a1 a a1 2 3
正确;C.由图可知As(OH) 的浓度为左坐标,浓度的数量级为10-3 mol/L,[As(OH) T]-的浓度为右坐标,
3 2
浓度的数量级为10-6 mol/L,所以pH=3.1时,As(OH) 的浓度比[As(OH) T]-的高,C正确;D.由题给条
3 2
件可知,酒石酸(H T lgK =-3.04 lgK =-4.37),As(OH) 的lgK 为-9.1,即酒石酸的第一步电离常数远
2 a1 a2 3 a1
大于亚砷酸的第一步电离常数,所以酒石酸的酸性远强于As(OH) ,另外总As的浓度也小于总T的浓度,
3
所以当pH=7.0时,溶液中浓度最高的物种不是As(OH) ,D错误。
3
22.(2022·湖南卷)为探究FeCl 的性质,进行了如下实验(FeCl 和NaSO 溶液浓度均为0.1 mol·L-1)。
3 3 2 3
实验 操作与现象
① 在5 mL水中滴加2滴FeCl 溶液,呈棕黄色;煮沸,溶液变红褐色
3
在5 mL FeCl 溶液中滴加2滴NaSO 溶液,变红褐色;再滴加K[Fe(CN) ]溶液,
3 2 3 3 6
②
产生蓝色沉淀
在5 mL Na SO 溶液中滴加2滴FeCl 溶液,变红褐色;将上述混合液分成两份,一
2 3 3
③
份滴加K[Fe(CN) ]溶液,无蓝色沉淀生成;另一份煮沸,产生红褐色沉淀
3 6
依据上述实验现象,结论不合理的是( )
A.实验①说明加热促进Fe3+水解反应
B.实验②说明Fe3+既发生了水解反应,又发生了还原反应
C.实验③说明Fe3+发生了水解反应,但没有发生还原反应
D.整个实验说明SO对Fe3+的水解反应无影响,但对还原反应有影响
【答案】D
【解析】铁离子的水解反应为吸热反应,加热煮沸可促进水解平衡正向移动,使水解程度加深,生成较多
的氢氧化铁,从而使溶液显红褐色,故A正确;在5 mL FeCl 溶液中滴加2滴同浓度的NaSO 溶液,根据
3 2 3
现象分析可知,Fe3+既发生了水解反应,生成红褐色的氢氧化铁,又被亚硫酸根离子还原,生成亚铁离子,
加入铁氰化钾溶液后,生成蓝色沉淀,故B正确;实验③中在5 mL Na SO 溶液中滴加2滴同浓度的
2 3
FeCl 溶液,根据现象分析可知,仍发生铁离子的水解反应,但未发生铁离子的还原反应,即水解反应比氧
3
化还原反应的速率快,故C正确;结合三组实验,说明铁离子与亚硫酸根离子混合时,铁离子的水解反应
占主导作用,比氧化还原反应的速率快,因实验证据不足,不能说明亚硫酸根离子对铁离子的水解作用无
影响,事实上,亚硫酸根离子水解显碱性,可促进铁离子的水解反应,故D错误。