文档内容
解密 02 物质的量
一、选择题
1.(2021·通榆县第一中学校高三月考)下列说法中正确的是( )
A.摩尔是物质质量的单位,用“mol”表示 B.标准状况下,物质的摩尔体积约为22.4mol/L
C.阿伏伽德罗常数的真实值为6.02×1023 D.物质的摩尔质量常用单位是“g/mol”
2.(2021·甘肃武威市武威十八中高三月考)“物质的量”是国际单位制中的一个基本物理量,下列有关
说法正确的是( )
A.2gH 含有1mol氢分子 B.2mol氧气的摩尔质量为64g·mol-1
2
C.1mol任何物质都含有6.02×1023个分子 D.质量相等的CO和CO,物质的量之比为2∶3
2
3.(2021·衡水中学高三月考)全氮阴离子盐是一种新型超高能含能材料,全氮阴离子化学式为N ,某
种全氮阴离子盐结构如图。下列有关说法正确的是( )
A.该全氮阴离子盐属于有机物 B.N-的摩尔质量为71g/mol
5
C.每个 N-含有26个电子 D.该全氮阴离子盐既含共价键又含离子键
5
4.(2021·南开中学高三月考)下列选项中的物质所含指定原子数目一定相等的是( )
A.温度和压强不同,相同质量的一氧化二氮和二氧化碳两种气体的总原子数
B.等温等压下,相同体积的乙烯和乙炔、乙烷的混合气体的总原子数
C.等温等压下,相同体积的氧气和臭氧两种气体中的氧原子数
D.相同物质的量、不同体积的氨气和甲烷两种气体中的氢原子数
5.NO,俗称笑气,是一种无色有甜味气体,在室温下稳定,有轻微麻醉作用,并能致人发笑。下列
2
叙述中正确的是( )
A.笑气的摩尔质量为44 g B.6.02×1023个笑气分子的质量为44 g
C.1 mol笑气的质量为44 g/mol D.4.4 g笑气含有N 个NO分子
A 2
6.假设把12C的相对原子质量定为24,且以0.024kg 12C所含的原子数为阿伏加德罗常数值,下列数
6
值肯定不变的是( )
A.气体摩尔体积(标准状况) B.标准状况下,16g O 所占的体积
2
C.O 的式量 D.一定条件下,跟2g H 相化合的O 的物质的量
2 2 2
7.(2021·周口市中英文学校高三月考)在标准状况下, mg气体A与ng气体B的分子数相同。则与此
有关的下列说法中不正确的是( )
A.气体A与气体B的摩尔质量之比为m:n
B.同温同压下,气体A与气体B的密度之比为n:m
C.质量相同的气体A与气体B的分子数之比为n:m
D.相同状况下,同体积的气体A与气体B的质量之比为m:n
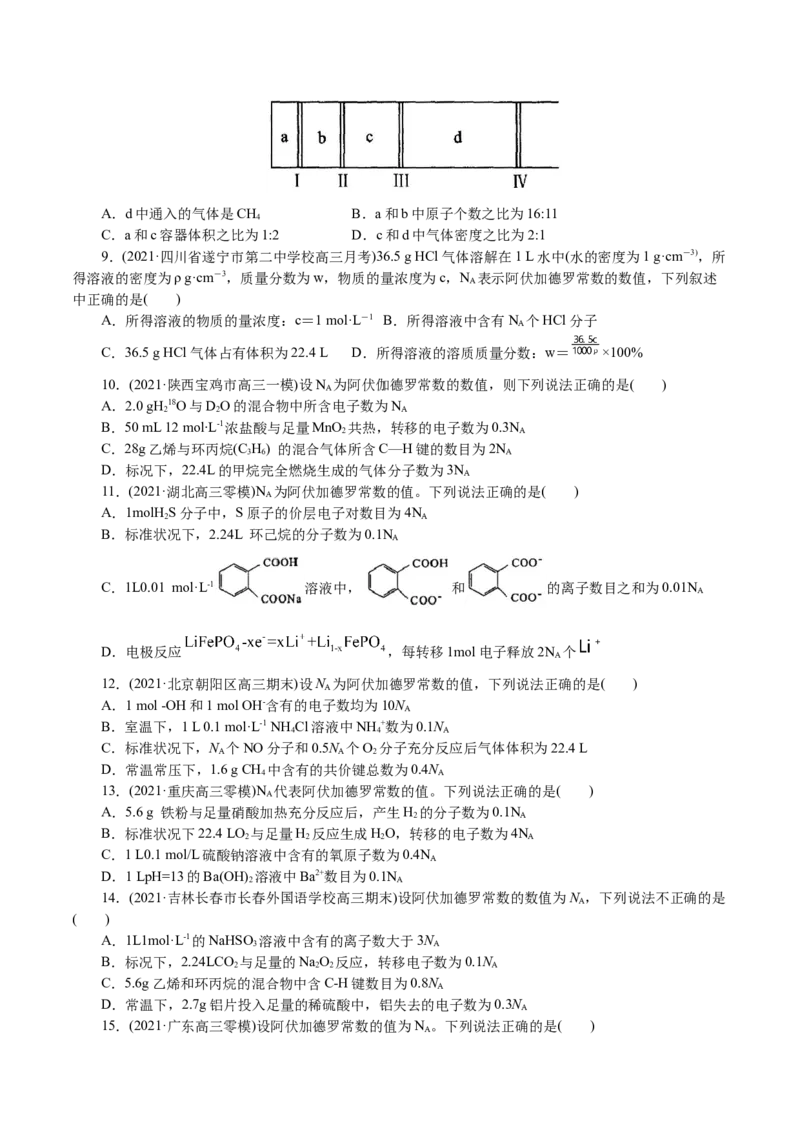
8.(2021·重庆复旦中学高三月考)某温度下,向图中所示a、b、c、d中通入等质量的CH、CO、O、
4 2 2
SO 四种气体中的一种(已知密封隔板Ⅰ、Ⅱ、Ⅲ、Ⅳ可自由滑动,且与容器内壁摩擦不计)。下列说法中错
2
误的是( )A.d中通入的气体是CH B.a和b中原子个数之比为16:11
4
C.a和c容器体积之比为1:2 D.c和d中气体密度之比为2:1
9.(2021·四川省遂宁市第二中学校高三月考)36.5 g HCl气体溶解在1 L水中(水的密度为1 g·cm-3),所
得溶液的密度为ρ g·cm-3,质量分数为w,物质的量浓度为c,N 表示阿伏加德罗常数的数值,下列叙述
A
中正确的是( )
A.所得溶液的物质的量浓度:c=1 mol·L-1 B.所得溶液中含有N 个HCl分子
A
C.36.5 g HCl气体占有体积为22.4 L D.所得溶液的溶质质量分数:w= ×100%
10.(2021·陕西宝鸡市高三一模)设N 为阿伏伽德罗常数的数值,则下列说法正确的是( )
A
A.2.0 gH18O与DO的混合物中所含电子数为N
2 2 A
B.50 mL 12 mol∙L-1浓盐酸与足量MnO 共热,转移的电子数为0.3N
2 A
C.28g乙烯与环丙烷(C H) 的混合气体所含C—H键的数目为2N
3 6 A
D.标况下,22.4L的甲烷完全燃烧生成的气体分子数为3N
A
11.(2021·湖北高三零模)N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.1molH S分子中,S原子的价层电子对数目为4N
2 A
B.标准状况下,2.24L 环己烷的分子数为0.1N
A
C.1L0.01 mol·L-1 溶液中, 和 的离子数目之和为0.01N
A
D.电极反应 ,每转移1mol电子释放2N 个
A
12.(2021·北京朝阳区高三期末)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1 mol -OH和1 mol OH-含有的电子数均为10N
A
B.室温下,1 L 0.1 mol·L-1 NH Cl溶液中NH +数为0.1N
4 4 A
C.标准状况下,N 个NO分子和0.5N 个O 分子充分反应后气体体积为22.4 L
A A 2
D.常温常压下,1.6 g CH 中含有的共价键总数为0.4N
4 A
13.(2021·重庆高三零模)N 代表阿伏加德罗常数的值。下列说法正确的是( )
A
A.5.6 g 铁粉与足量硝酸加热充分反应后,产生H 的分子数为0.1N
2 A
B.标准状况下22.4 LO 与足量H 反应生成HO,转移的电子数为4N
2 2 2 A
C.1 L0.1 mol/L硫酸钠溶液中含有的氧原子数为0.4N
A
D.1 LpH=13的Ba(OH) 溶液中Ba2+数目为0.1N
2 A
14.(2021·吉林长春市长春外国语学校高三期末)设阿伏加德罗常数的数值为N ,下列说法不正确的是
A
( )
A.1L1mol·L-1的NaHSO 溶液中含有的离子数大于3N
3 A
B.标况下,2.24LCO 与足量的NaO 反应,转移电子数为0.1N
2 2 2 A
C.5.6g乙烯和环丙烷的混合物中含C-H键数目为0.8N
A
D.常温下,2.7g铝片投入足量的稀硫酸中,铝失去的电子数为0.3N
A
15.(2021·广东高三零模)设阿伏加德罗常数的值为N 。下列说法正确的是( )
AA.1 mol Cl 和Fe充分反应,转移电子数为3 N
2 A
B.标准状况下,1.12L 苯含有C-H键的个数为3 N
A
C.22 g CO 和足量NaO 反应,产生的气体的分子数为0.25 N
2 2 2 A
D.0.5 mol乙酸乙酯在酸性条件下水解,生成乙醇的分子数为1.0 N
A
16.(2021·北京通州区高三期末)N 为阿伏加德罗常数的值,下列说法不正确的是( )
A
A.44g CO 含氧原子数为2N
2 A
B.17g羟基(-OH)所含电子总数为9N
A
C.1mol/L CuCl 溶液中含Cl-数目为2N
2 A
D.标准状况下,22.4L氖气含有的电子数为10N
A
17.(2021·陕西渭南市高三一模)用N 代表阿伏加德罗常数的值,下列说法正确的是( )
A
A.所含共价键数目均为0.4N 的白磷( )和甲烷的物质的量相等
A
B.向FeI 溶液中通入适量Cl,当有1mol Fe2+被氧化时,反应转移的电子数为3N
2 2 A
C.通入了1 mol Cl 的新制氯水中,HClO、Cl-、ClO-粒子数目之和为2N
2 A
D.常温下,向1L 0.1 mol·L-1醋酸钠溶液中加入醋酸至中性,则溶液中CHCOO-的数目为0.1N
3 A
18.(2021·长春市第二十九中学高三期末)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.36 g由35Cl和37Cl组成的氯气中所含质子数一定为17N
A
B.一定条件下,6.4 g铜与过量的硫粉反应,转移电子数目为0.2N
A
C.常温常压下,水蒸气通过过氧化钠使其增重4 g时,反应中转移的电子数为2N
A
D.0.4 mol NH 与0.6 mol O 在加热及催化剂条件下充分反应,得到NO的分子数为0.4N
3 2 A
19.(2021·广东汕头市高三期末)疫情期间,消毒剂如氯仿、84消毒液、双氧水等起到重要作用。设
N 为阿伏伽德罗常数的值,下列有关说法正确的是( )
A
A.标准状况下,11.2L氯仿(CHCl )含有C-Cl数目为1.5N
3 A
B.1L 1mol/L NaClO溶液中含有ClO- 数目为N
A
C.常温下,1mol Cl 与NaOH溶液反应制漂白液时,转移电子数目为N
2 A
D.17g H O 中含有过氧键数目为N
2 2 A
20.(2021·湖南长沙市长郡中学高三月考)设N 为阿伏加德罗常数的值,下列有关叙述不正确的是(
A
)
A.0.1mol的11B中,含有0.6N 个中子
A
B.0℃、101kPa下,0.1mol乙炔和甲醛(HCHO)的混合物中含有 键的数目为0.2N
A
C.将1mol Cl 通入足量水中,所得溶液中Cl、HClO、Cl-、ClO-三种微粒数目之和为2N
2 2 A
D.常温下,1L0.50 mol·L-1NH Cl溶液与2L0.25 mol·L-1NH Cl溶液所含NH +的物质的量后者小
4 4 4
21.(2021·兴宁市第一中学高三期末)设N 为阿伏加德罗常数的值。下列说法错误的是 ( )
A
A.标准状况下,2.24LC1 完全溶于水,所得溶液中含氯微粒总数为0.2N
2 A
B.常温常压下,0.5mol氨基(-NH )含有的电子数为4.5N
2 A
C.64g铜与一定浓度的硝酸完全反应时,转移的电子数为2N
A
D.标准状况下,22.4L由O 与N 组成的混合气体含有的原子数目为2N
2 2 A
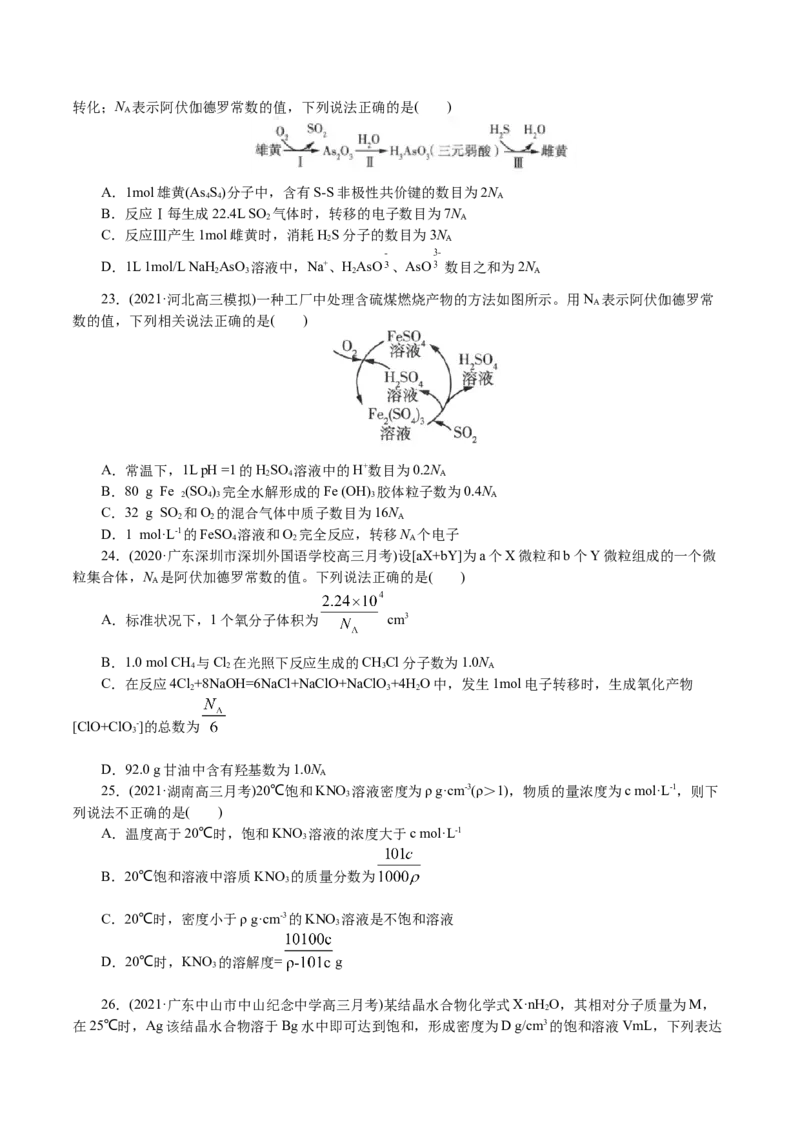
22.(2021·河北高三模拟)雄黄(As S, )与雌黄(As S)在古代均曾入药。二者可发生如图
4 4 2 3转化;N 表示阿伏伽德罗常数的值,下列说法正确的是( )
A
A.1mol雄黄(As S)分子中,含有S-S非极性共价键的数目为2N
4 4 A
B.反应Ⅰ每生成22.4L SO 气体时,转移的电子数目为7N
2 A
C.反应Ⅲ产生1mol雌黄时,消耗HS分子的数目为3N
2 A
D.1L 1mol/L NaH AsO 溶液中,Na+、HAsO 、AsO 数目之和为2N
2 3 2 A
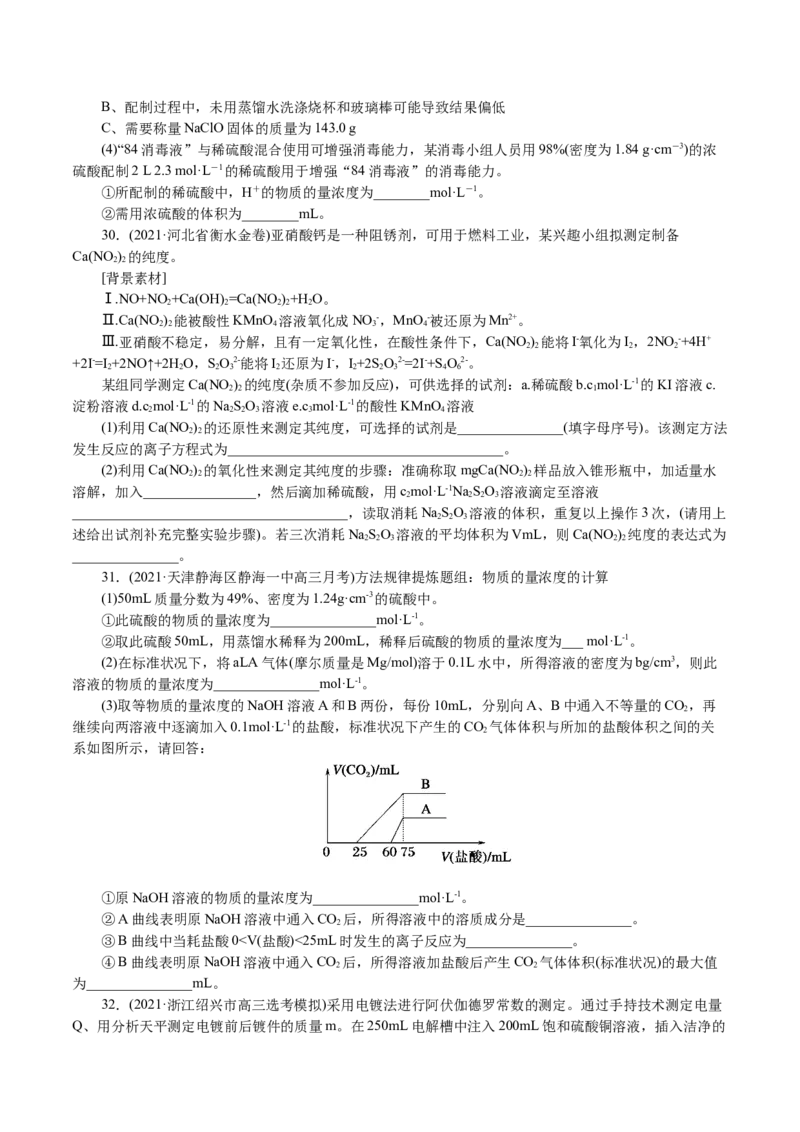
23.(2021·河北高三模拟)一种工厂中处理含硫煤燃烧产物的方法如图所示。用N 表示阿伏伽德罗常
A
数的值,下列相关说法正确的是( )
A.常温下,1L pH =1的HSO 溶液中的H+数目为0.2N
2 4 A
B.80 g Fe (SO ) 完全水解形成的Fe (OH) 胶体粒子数为0.4N
2 4 3 3 A
C.32 g SO 和O 的混合气体中质子数目为16N
2 2 A
D.1 mol·L-1的FeSO 溶液和O 完全反应,转移N 个电子
4 2 A
24.(2020·广东深圳市深圳外国语学校高三月考)设[aX+bY]为a个X微粒和b个Y微粒组成的一个微
粒集合体,N 是阿伏加德罗常数的值。下列说法正确的是( )
A
A.标准状况下,1个氧分子体积为 cm3
B.1.0 mol CH 与Cl 在光照下反应生成的CHCl分子数为1.0N
4 2 3 A
C.在反应4Cl+8NaOH=6NaCl+NaClO+NaClO +4H O中,发生1mol电子转移时,生成氧化产物
2 3 2
[ClO+ClO -]的总数为
3
D.92.0 g甘油中含有羟基数为1.0N
A
25.(2021·湖南高三月考)20℃饱和KNO 溶液密度为ρ g·cm-3(ρ>1),物质的量浓度为c mol·L-1,则下
3
列说法不正确的是( )
A.温度高于20℃时,饱和KNO 溶液的浓度大于c mol·L-1
3
B.20℃饱和溶液中溶质KNO 的质量分数为
3
C.20℃时,密度小于ρ g·cm-3的KNO 溶液是不饱和溶液
3
D.20℃时,KNO 的溶解度= g
3
26.(2021·广东中山市中山纪念中学高三月考)某结晶水合物化学式X·nH O,其相对分子质量为M,
2
在25℃时,Ag该结晶水合物溶于Bg水中即可达到饱和,形成密度为D g/cm3的饱和溶液VmL,下列表达式中不正确的是( )
A.该饱和溶液的质量分数为
B.溶质X在25℃时的溶解度为 克
C.该饱和溶液的密度为
D.该饱和溶液的物质的量浓度为 mol/L
二、非选择题
27.化学计量在化学中占有重要地位,回答下列问题:
(1)0.3 mol NH 分子中所含原子数与________个HO分子中所含原子数相等。
3 2
(2)含0.4 mol Al3+的Al (SO ) 中所含的SO的物质的量是________。
2 4 3
(3)16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为__________。
(4)在一定温度和压强下,1体积气体X 跟3体积气体Y 化合生成2体积气态化合物,则该化合物的化
2 2
学式是____________。
28.用N 表示阿伏加德罗常数的数值,按要求完成下列填空。
A
(1)1 mol O 中含有____________个氧气分子,含有________个氧原子。
2
(2)0.5 mol H O中含有________个水分子,含有________个原子。
2
(3)6 mol NO 和_____mol NO 所含原子数相等,与 1 mol CO 所含电子数相等的 H 的物质的量是
2 2 2
_____mol,6 mol H O与___mol NH 所含氢原子数相等,1 mol HCl与____mol CH 所含电子数相等。
2 3 4
(4)1个CO 分子含有_______个电子,1 mol CO 含有______mol e-,_____个e-。
2 2
(5)1个HO分子含有______个原子,2 mol H O含有_______mol e-,______个e-。
2 2
(6)1.204×1024个水分子的物质的量是_____;1 mol H SO 中氧原子数为________。
2 4
(7)某硫酸钠溶液中含有3.01×1022个Na+,则该溶液中SO 的物质的量是______,Na+的物质的量是
______。
(8)1 mol NaCl中氯离子数为________,离子总数为________。
29.(2021·石嘴山市第三中学高三月考)已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”
通常稀释100倍(体积之比)后使用。请回答下列问题:
(1)该“84消毒液”的物质的量浓度约为________mol·L-1。(保留小数点后一位)
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=________mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒
液。下列说法正确的是________(填字母)。
A、容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制B、配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
C、需要称量NaClO固体的质量为143.0 g
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓
硫酸配制2 L 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为________mol·L-1。
②需用浓硫酸的体积为________mL。
30.(2021·河北省衡水金卷)亚硝酸钙是一种阻锈剂,可用于燃料工业,某兴趣小组拟测定制备
Ca(NO ) 的纯度。
2 2
[背景素材]
Ⅰ.NO+NO +Ca(OH) =Ca(NO)+H O。
2 2 2 2 2
Ⅱ.Ca(NO ) 能被酸性KMnO 溶液氧化成NO -,MnO -被还原为Mn2+。
2 2 4 3 4
Ⅲ.亚硝酸不稳定,易分解,且有一定氧化性,在酸性条件下,Ca(NO ) 能将I-氧化为I,2NO -+4H+
2 2 2 2
+2I-=I +2NO↑+2HO,SO2-能将I 还原为I-,I+2S O2-=2I-+S O2-。
2 2 2 3 2 2 2 3 4 6
某组同学测定Ca(NO ) 的纯度(杂质不参加反应),可供选择的试剂:a.稀硫酸b.cmol·L-1的KI溶液c.
2 2 1
淀粉溶液d.cmol·L-1的NaSO 溶液e.cmol·L-1的酸性KMnO 溶液
2 2 2 3 3 4
(1)利用Ca(NO ) 的还原性来测定其纯度,可选择的试剂是_______________(填字母序号)。该测定方法
2 2
发生反应的离子方程式为_______________________________________。
(2)利用Ca(NO ) 的氧化性来测定其纯度的步骤:准确称取mgCa(NO) 样品放入锥形瓶中,加适量水
2 2 2 2
溶解,加入________________,然后滴加稀硫酸,用cmol·L-1NaSO 溶液滴定至溶液
2 2 2 3
_______________________________________,读取消耗NaSO 溶液的体积,重复以上操作3次,(请用上
2 2 3
述给出试剂补充完整实验步骤)。若三次消耗NaSO 溶液的平均体积为VmL,则Ca(NO ) 纯度的表达式为
2 2 3 2 2
_______________。
31.(2021·天津静海区静海一中高三月考)方法规律提炼题组:物质的量浓度的计算
(1)50mL质量分数为49%、密度为1.24g·cm-3的硫酸中。
①此硫酸的物质的量浓度为_______________mol·L-1。
②取此硫酸50mL,用蒸馏水稀释为200mL,稀释后硫酸的物质的量浓度为___ mol·L-1。
(2)在标准状况下,将aLA气体(摩尔质量是Mg/mol)溶于0.1L水中,所得溶液的密度为bg/cm3,则此
溶液的物质的量浓度为_______________mol·L-1。
(3)取等物质的量浓度的NaOH溶液A和B两份,每份10mL,分别向A、B中通入不等量的CO,再
2
继续向两溶液中逐滴加入0.1mol·L-1的盐酸,标准状况下产生的CO 气体体积与所加的盐酸体积之间的关
2
系如图所示,请回答:
①原NaOH溶液的物质的量浓度为_______________mol·L-1。
②A曲线表明原NaOH溶液中通入CO 后,所得溶液中的溶质成分是_______________。
2
③B曲线中当耗盐酸0