文档内容
解密 07 非金属及其化合物
一、选择题
1.(2021·启东高三联考)2020年9月,我国作出对于全球减排具有里程碑意义的承诺:2060年实现碳
中和。碳中和是指直接或间接产生的温室气体排放总量,通过植树造林、节能减排、碳捕集与封存等形式,
抵消自身产生的二氧化碳排放量,实现二氧化碳“零排放”。下列有关说法正确的是( )
A.CO 是导致温室效应和酸雨的主要气体
2
B.煤的液化、气化主要是为了减少CO 的排放
2
C.CO 催化加氢合成低碳烯烃属于化合反应
2
D.CO 分子间有间隔,故可将其压缩液化后封存
2
【答案】D
【解析】A项,二氧化硫是导致酸雨的气体,而不是二氧化碳,故A错误;B项,煤的液化、气化是
不能减少CO 的排放的,如煤气化的生成物即煤气主要成分是一氧化碳,燃烧依然生成二氧化碳,且生成
2
二氧化碳分子数目相同,故B错误;C项,CO 催化加氢合成低碳烯烃的同时还有HO生成,不属于化合
2 2
反应,故C错误;D项,二氧化碳分子之间有间隔,在受压时间隔变小,故可将其压缩液化后封存,故D
正确。故选D。
2.(2021·安徽省”皖南八校“高三联考)下列关于非金属及其化合物的说法错误的是( )
A.液氮汽化时要吸收大量的热,可用作制冷剂
B.向氯水中加入碳酸氢钠粉末,有气泡产生,说明氯水中含有H+
C.用二氧化硫漂白过的草帽辫日久又变成黄色
D.铜分别与足量的浓硝酸和稀硝酸充分反应,消耗的还原剂与氧化剂的物质的量之比相同
【答案】D
【解析】A项,液氮汽化时要吸收大量的热,可用作制冷剂,A正确;B项,向氯水中加入碳酸氢钠
粉末,有气泡产生,说明氯水中含有H+,B正确;C项,二氧化硫 的漂白性不稳定,故二氧化硫漂白过的
草帽辫日久又变成黄色,C正确;D项,Cu与浓硝酸反应的还原产物为二氧化氮,而与稀硝酸反应的还原
产物为NO,还原产物的价态不同,故消耗的还原剂与氧化剂的物质的量之比不同,D错误;故选D。
3.(2021·潍坊市统考高三化学质量检测)硫元素最常见和最稳定的一种同素异形体是黄色的正交α-型,
1912年E.Beckmann由硫在碘中的冰点降低法测得它含有S 分子。1891年,M.R.Engel用浓盐酸和硫代硫
8
酸盐的饱和溶液在0℃下作用首次制得了一种菱形的 -硫,后来证明含有S 分子。下列说法正确的是(
6
)
A.S 和S 分子都是由S原子组成,所以它们是一种物质
6 8
B.S 和S 分子分别与铁粉反应,所得产物不同
6 8
C.S 和S 分子分别与过量的氧气反应可以得到SO
6 8 3
D.等质量的S 和S 分子分别与足量的KOH反应,消耗KOH的物质的量相同
6 8
【答案】D
【解析】A项,S 和S 分子都是由S原子组成,它们是不同的物质,互为同素异形体,故A错误;B
6 8
项,S 和S 是硫元素的不同单质,化学性质相似,因此它们分别与铁粉反应,所得产物相同,故B错误;
6 8
C项,不管氧气过量还是少量,S 和S 分子分别与氧气反应可以得到SO ,故C错误;D项,等质量的S
6 8 2 6
和S 分子,其硫原子的物质的量相同,因此它们分别与足量的 KOH反应,消耗KOH的物质的量相同,故
8
D正确。故选D。
4.(2021·吉林省德惠市实验中学、前郭五中等九校高三联考)下列有关硫元素及其化合物的说法或描
述正确的是( )A.硫黄矿制备硫酸经历两步:SO /点燃,SO HSO
2 3 2 4
B.酸雨与土壤中的金属氧化物反应后,硫元素以单质的形式进入土壤中
C.在燃煤中加入石灰石可减少SO 排放,发生的反应为2CaCO +2SO +O 2CO+2CaSO
2 3 2 2 2 4
D.土壤中的闪锌矿(ZnS)遇到硫酸铜溶液转化为铜蓝(CuS),说明CuS很稳定,不具有还原性
【答案】C
【解析】A项,用硫黄制硫酸时,第一步只能将硫氧化成 SO ,故A错误;B项,酸雨与土壤中的金
2
属氧化物反应后,硫元素以SO 2-的形式进入土壤中,故B错误;C项,在燃煤中加入石灰石,高温下石灰
4
石分解生成CaO,可与SO 以及氧气反应生成硫酸钙,故C正确;D项,土壤中的闪锌矿(ZnS)遇到硫酸铜
2
溶液转化为铜蓝(CuS),说明CuS的溶解度比ZnS的小,与CuS很稳定不具有还原性无关,故D错误;故
选C。
5.(2021·湖南怀化市期末)下列关于氯及其化合物的叙述正确的是( )
A.氯气的性质很活泼,它与氢气混合后立即发生爆炸
B.实验室制取氯气时,尾气常用氢氧化钠溶液吸收
C.氯气与氢氧化钠溶液反应能制漂白液,其有效成分为NaClO
3
D.某氯水中加入硝酸银溶液生成白色沉淀,说明该氯水一定不含Cl
2
【答案】B
【解析】A项,氯气的性质很活泼,它与氢气混合后,在光照条件下能发生爆炸,故A错误;B项,
氢氧化钠和氯气反应生成氯化钠、次氯酸钠和水,实验室制取氯气时,尾气常用氢氧化钠溶液吸收,故B
正确;C项,漂白液的有效成分为NaClO,故C错误;D项,某氯水中加入硝酸银溶液生成白色沉淀,说
明该氯水一定含有Cl-,不能确定是否含有Cl,故D错误;故选B。
2
6.下列关于非金属及其化合物的说法错误的是( )
A.液氮汽化时要吸收大量的热,可用作制冷剂
B.向氯水中加入碳酸氢钠粉末,有气泡产生,说明氯水中含有H+
C.用二氧化硫漂白过的草帽辫日久又变成黄色
D.铜分别与足量的浓硝酸和稀硝酸充分反应,消耗的还原剂与氧化剂的物质的量之比相同
【答案】D
【解析】A项,液氮汽化时要吸收大量的热,可用作制冷剂,A正确;B项,向氯水中加入碳酸氢钠
粉末,有气泡产生,说明氯水中含有H+,B正确;C项,二氧化硫 的漂白性不稳定,故二氧化硫漂白过的
草帽辫日久又变成黄色,C正确;D项,Cu与浓硝酸反应的还原产物为二氧化氮,而与稀硝酸反应的还原
产物为NO,还原产物的价态不同,故消耗的还原剂与氧化剂的物质的量之比不同,D错误;故选D。
7.化学工业在经济发展中的作用举足轻重。下列有关工业生产的叙述中正确的是( )
A.硫酸生产中常采用高压条件提高SO 的转化率
2
B.合成氨中及时分离氨气可提高反应速率
C.硫酸生产中可用水直接吸收SO 生成硫酸
3
D. 纯碱厂最好建在合成氨厂附近
【答案】D
【解析】A项,生成硫酸时采用常压条件,常压条件二氧化硫的转化率已经很大,高压转化率增大不
多,但是提高了生成成本,故A错误;B项,及时分离出生成物可使平衡右移,反应物浓度降低,反应速
率减小,故B错误;C项,在吸收塔中,直接用水吸收SO ,易形成酸雾,降低SO 吸收效率,应用98.3%
3 3
硫酸吸收SO ,故C错误;D项,纯碱生成中需要大量氨气来形成氨盐水更好的吸收二氧化碳,纯碱厂最
3
好建在合成氨厂附近可降低运输成本,故D正确;故选D。8.下列现象或事实可用同一原理解释的是( )
A.浓硫酸和浓盐酸长期暴露在空气中浓度降低 B.氯水和活性炭使红墨水褪色
C.铁片和铝片置于冷的浓硫酸中均无明显现象 D.二氧化硫和过氧化钠使品红褪色
【答案】C
【解析】A项,浓硫酸具有吸水性,浓度降低是因溶剂增多,而浓盐酸易挥发浓度减小是因溶质减少,
原因不同,A错误;B项,氯水中HClO具有强氧化性使红墨水褪色,而活性炭具有吸附性使红墨水褪色,
原理不同,B错误;C项,铁片和铝片置于冷的浓硫酸中均无明显现象,均是因为发生了钝化,原理相同,
C正确;D项,过氧化钠具有强氧化性,能使品红褪色,二氧化硫能使品红溶液褪色,发生的是非氧化还
原反应,原理不相同,D错误。故选C。
9.(2021·浙江高三月考)NCl 为黄色油状液体,可用于漂白,也用于柠檬等水果的熏蒸处理,其相关
3
性质的说法不正确的是( )
A.缓慢与水发生反应:NCl +2H O=HNO +3HCl
3 2 2
B.具有强氧化性,能与HCl气体反应生成Cl
2
C.很不稳定,受热或受震动时发生猛烈爆炸而分解:2NCl N↑+ Cl ↑
3 2 2
D.遇碱迅速分解得到一种碱性气体和能杀灭新冠病毒的消毒液
【答案】A
【解析】A项,在NCl 中,N显-3价,Cl显+1价,缓慢与水发生反应:NCl +3H O=NH +3HClO,
3 3 2 3
HClO还可将NH 氧化为N,A不正确;B项,NCl 中Cl显+1价,HCl中Cl显-1价,NCl 与HCl中Cl元
3 2 3 3
素发生归中反应,生成Cl 和NH ,若HCl过量,则生成NH Cl,B正确;C项,NCl 很不稳定,对光、热、
2 3 4 3
有机化合物都十分敏感,甚至震动时都会发生猛烈爆炸,从而生成N 和Cl,C正确;D项,NCl 遇碱会
2 2 3
发生迅速分解,生成NH 和NaClO,NaClO可作杀灭新冠病毒的消毒液,D正确;故选A。
3
10.(2021·浙江选考模拟)已知:100%硫酸吸收SO 可生成焦硫酸(分子式为HSO 或HSO ·SO );焦
3 2 2 7 2 4 3
硫酸水溶液发生如下电离:HSO(aq)=H+(aq)+ HS O- (aq),HS O- (aq) H+(aq)+ SO (aq)
2 2 7 2 7 2 7 2 72-
K =2.7×10-2。下列说法不正确的是( )
2
A.焦硫酸具有强氧化性
B.NaSO 水溶液显中性
2 2 7
C.98%的HSO 可以表示为SO • HO
2 4 3 2
D.焦硫酸与水反应的化学方程式:HSO+H O=2HSO
2 2 7 2 2 4
【答案】B
【解析】A项,由浓硫酸中+6价硫具有强氧化性可知,焦硫酸中+6价硫也具有强氧化性,A正确;B
项,NaSO 可写成NaSO ·SO ,溶于水后SO 和水反应生成硫酸,溶液显酸性,B错误;C项,假设浓硫
2 2 7 2 4 3 3
酸的质量为100 g,则HSO 的质量为100 g×98%=98 g,HO的质量为100 g-98 g=2 g,则HSO 的物质的
2 4 2 2 4
量为 =1 mol,HO的物质的量为 = mol,故98%的HSO 可表示为HSO • HO,如
2 2 4 2 4 2
果把HSO 表示为SO ·HO,则98%的浓硫酸也可表示为SO • HO,C正确;D项,焦硫酸与水反应可
2 4 3 2 3 2
表示为HSO ·SO +H O=2HSO ,D正确。
2 4 3 2 2 4
11.(2021·江苏扬州市期末)2020年7月31日上午,北斗三号全球卫星导航系统正式开通。下列说法
正确的是( )
A.控制系统的芯片是硅晶体,硅晶体用作半导体材料是因为其原子的最外层电子数多
B.火箭推进剂发生的化学反应为2NH + N O = 3N + 4H O,其中氢元素被氧化
2 4 2 4 2 2
C.火箭发射时会产生大量红色的烟雾, 该现象与反应产生的NO 有关
xD.火箭头部的一层特殊材料能起到保护作用,是由于其在熔化时能放出大量的热
【答案】C
【解析】A项,硅晶体用作半导体材料是因其具有单向导电性,与最外层电子数多少无关,故A错误;
B项,由反应可知中的N由-2价转变成0价,作还原剂,N元素被氧化物,中的N化合价由+4价转变成0
价,作氧化剂,N元素被还原,H的化合价反应前后保持不变,故B错误;C项,火箭燃料为偏二甲肼和
四氧化二氮,其中四氧化二氮进入空气后立刻会分解为红棕色的二氧化氮,红色烟雾是火箭刚点火时没有
被燃尽,扩散到空中的棕红色二氧化氮,故C正确;D项,熔化过程吸收大量的热,从而起到给火箭降温
保护设备的作用,故D错误;故选C。
12.(2021·广东中山市期末)在无机非金属材料中,硅一直扮演着主要的角色.请你利用元素周期律的
相关知识,预测硅及其化合物的性质.下列说法不正确的是( )
A.晶体硅的导电性介于导体和绝缘体之间,是良好的半导体材料
B.SiO 是酸性氧化物,可以与NaOH反应:SiO+2NaOH=Na SiO+H O
2 2 2 3 2
C. NaSiO 可溶于水,在水溶液中电离方程式为:NaSiO=2Na++SiO 2-
2 3 2 3 3
D.由反应NaSiO+2HCl=2NaCl+H SiO↓,可以证明HSiO 是一种弱酸
2 3 2 3 2 3
【答案】D
【解析】A项,晶体硅是灰黑色有金属光泽、硬而脆的固体,导电性介于导体和绝缘体之间,是良好
的半导体材料,A说法正确;B项,SiO 是酸性氧化物,可以与NaOH反应生成盐和水:
2
SiO+2NaOH=Na SiO+H O,B说法正确;C项,NaSiO 为强电解质,可溶于水,在水溶液中完全电离,
2 2 3 2 2 3
电离方程式:NaSiO=2Na++SiO 2-,C说法正确;D项,由反应NaSiO+2HCl=2NaCl+H SiO↓,HSiO 为
2 3 3 2 3 2 3 2 3
沉淀,生成的沉淀不一定为弱电解质,则不能证明HSiO 是一种弱酸,D说法错误;故选D。
2 3
13.(2021·四川资阳市高三一模)“过犹不及”深刻诠释了化学反应的定量关系。下列反应进行到指定程
度,继续增加画线物质的量,不会使反应发生变化的是(忽略气体溶解及与水的反应) ( )
A.在Ca(HCO ) 溶液中滴加Ca(OH) 溶液至HCO -完全反应
3 2 2 3
B.将Cl 通入FeBr 溶液至Fe2+完全氧化
2 2
C.将NH 通入CuSO 溶液至Cu2+完全沉淀
3 4
D.在KAl(SO ) 溶液中滴加Ba(OH) 溶液至沉淀物质的量最大
4 2 2
【答案】A
【解析】A项,Ca(HCO ) 溶液中滴加Ca(OH) 溶液至HCO -完全反应,反应的离子方程式为Ca2++
3 2 2 3
HCO -+OH-=CaCO ↓+H O,继续滴加Ca(OH) 溶液不再发生其他反应,即原反应不会发生变化,A符合题
3 3 2 2
意;B项,由于Fe2+的还原性比Br-强,将Cl 通入FeBr 溶液先与Fe2+反应:Cl+2Fe2+=2Cl-+2Fe3+,Fe2+完全
2 2 2
氧化后如果继续通入Cl,溶液中的Br-就会被氧化:Cl+2Br-=2Cl-+Br ,即原反应发生了变化,B不符题意;
2 2 2
C项,将NH 通入CuSO 溶液至Cu2+完全沉淀,发生反应2NH +2H O+Cu2+=Cu(OH) ↓+2NH +,若继续通入
3 4 3 2 2 4
NH ,会发生络合反应Cu(OH) +4NH=[Cu(NH)](OH) ,沉淀溶解,即原反应发生了变化,C不符题意;D
3 2 3 3 4 2
项,在KAl(SO ) 溶液中滴加Ba(OH) 溶液至沉淀物质的量最大,发生反应为2Al3++3SO 2-+3Ba2++6OH-
4 2 2 4
=2Al(OH) ↓+3BaSO ↓,若继续滴加Ba(OH) 溶液,溶液中会发生反应SO 2-+2Al(OH) +Ba2++2OH-=2 AlO-
3 4 2 4 3 2
+BaSO ↓+4H O,即原反应发生了变化,D不符题意;故选A。
4 2
14.(2021·湖南省常德芷兰实验学校月考)已知 NH CuSO 与足量的10mol·L-1硫酸混合微热,产生下列
4 3
现象:①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色。据此判断下列说法正确的是
( )
A.反应中硫酸作氧化剂 B.NH CuSO 中氮元素被氧化
4 3
C.刺激性气味的气体是氨气 D.1mol NH CuSO 完全反应转移0.5 mol电子
4 3
【答案】D
【解析】根据实验现象分析,红色金属为Cu,溶液呈现蓝色,说明溶液中含有Cu2+,因为加入足量
的硫酸,所以刺激性气味的气体应是SO ,据此分析,反应的化学方程式为2NH CuSO +2HSO =Cu+
2 4 3 2 4CuSO +2SO ↑+2HO+(NH )SO 。A项,根据上述分析,只有Cu元素的化合价发生变化,从+1价变成
4 2 2 4 2 4
了产物中的0价和+2价即硫酸的组成元素没有发生变化,所以硫酸既不是氧化剂又不是还原剂,只表现酸
性,故A错误;B项,NH CuSO 中氮元素的化合价没有变化,故B错误;C项,根据上述分析,刺激性
4 3
气味的气体为SO ,不是氨气,故C错误;D项,亚铜自身发生氧化还原反应,从反应的化学方程式
2
2NH CuSO +2HSO =Cu+CuSO +2SO ↑+2HO+(NH )SO 可知2molNH CuSO 完全反应转移电子物质
4 3 2 4 4 2 2 4 2 4 4 3
的量为1mol,故1molNH CuSO 完全反应转移电子物质的量为0.5mol,故D正确;故选D。
4 3
15.(2020·安徽省濉溪县高三联考)利用自然资源制备相关化学物质,下列化学工艺不可行的是( )
A.提取食盐后母液 含Br 的液体 粗溴 纯溴
2
B.石英砂 粗硅 粗四氯化硅 高纯硅
C.FeS SO HSO HSO
2 2 2 3 2 4
D.铝土矿 Na[Al(OH)]溶液 Al(OH) Al O 铝
4 3 2 3
【答案】C
【解析】A项,提取食盐后的母液中提取单质溴的过程,要知道母液中是溴离子,需要先用Cl 氧化,
2
此工艺可行的,故A正确;B项,由石英砂先制粗硅,再用H 还原SiCl 得到Si,是工业上制高纯硅的流
2 4
程,工艺可行的,故B正确;C项,应首先进行二氧化硫的催化氧化,然后用98.3%的硫酸吸收,此工艺
不可行,故C错误;D项,工业上用铝土矿制铝的过程,每一步所加试剂必须过量,此工艺可行的,故D
正确;故选C。
16.(2020·安徽省2020年江南十校综合素质测试)ClO 是一种极易溶于水且几乎不与冷水反应的黄绿
2
色气体(沸点11℃),实验室制备纯净ClO 溶液的装置如图所示:
2
已知下列反应:NaClO+HCl→NaCl+ClO +Cl+H O;NaClO+HCl→NaCl+ClO +H O;
3 2 2 2 2 2 2
NaClO+Cl→NaCl+ClO (均未配平)。下列说法正确的是( )
2 2 2
A.a中通入的N 可用CO 或SO 代替 B.b中NaClO 可用饱和食盐水代替
2 2 2 2
C.c中广口瓶最好放在冰水浴中冷却 D.d中吸收尾气后只生成一种溶质
【答案】C
【解析】A项,a中通入的N 的目的是氮气性质稳定且不影响实验,可将a中产生的ClO 和Cl 吹出
2 2 2
并进入后续装置,继续实验,二氧化硫具有还原性,可将ClO 、NaClO 等物质还原,故A错误;B项,b
2 3
中NaClO 的作用是吸收ClO 中混有的氯气和氯化氢杂质气体,用饱和食盐水可吸收氯化氢,但不能吸收
2 2
氯气,故B错误;C项,ClO 是一种极易溶于水且几乎不与冷水反应的黄绿色气体,故c中广口瓶最好放
2
在冰水浴中冷却,有利于吸收ClO ,故C正确;D项,d中氢氧化钠和ClO 发生歧化反应生成NaCl和
2 2
NaClO,产物至少两种,故D错误;故选C。
3
17.(2020·长沙七校联考)实验室探究SO 与Fe(NO ) 溶液反应的原理,装置如下图,实验中Y装置产
2 3 3
生白色沉淀。下列说法不正确的是( )A.滴加浓硫酸之前应进行的操作是打开弹簧夹,通入一段时间N
2
B.Y中产生的白色沉淀是BaSO 或BaSO
4 3
C.产生白色沉淀的原因可能是在酸性条件下SO 与NO - 反应生成了SO 2-
2 3 4
D.若将Fe(NO ) 换成FeCl ,Y中也能产生白色沉淀,说明Fe3+也能将SO 氧化
3 3 3 2
【答案】B
【解析】A项,通入一段时间N ,是为了排除空气中O 的干扰,故A正确;B项,由于NO -在酸性
2 2 3
条件下具有强氧化性,能将SO 2 -氧化为SO 2 -,所以Y中产生的白色沉淀是BaSO ,故B不正确;同理,
3 4 4
C项,正确;D项,若将Fe(NO ) 换成FeCl ,Y中也能产生白色沉淀,且沉淀为BaSO ,说明Fe3+也能将
3 3 3 4
SO 氧化,D正确;故选B。
2
18.下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项 陈述Ⅰ 陈述Ⅱ 判断
向浓盐酸中加入浓硫酸 浓盐酸易挥发,浓硫酸与水作用放出大
A Ⅰ对,Ⅱ对;有
可制备氯化氢气体 量的热
由于Cu具有还原性,浓HNO 具有氧
3
B Cu能与浓HNO 反应 化性,在任何条件下生成的气体一定是 Ⅰ对,Ⅱ错;无
3
NO
2
硫单质在纯氧中燃烧有
C 部分二氧化硫被氧化为SO Ⅰ对,Ⅱ对;无
少量SO 生成 3
3
硝酸铵和碱石灰共热用
D 铵盐与碱能发生复分解反应 Ⅰ对,Ⅱ对;有
于实验室制备NH
3
【答案】A
【解析】A项,浓硫酸具有吸水性,溶于水放出大量的热,又因为浓盐酸易挥发,所以向浓盐酸中加
入浓硫酸可制备氯化氢气体,A正确;B项,铜与稀硝酸反应生成NO,B错误;C项,硫单质在纯氧中燃
烧只能生成SO ,C错误;D项,硝酸铵受热易发生爆炸,实验室一般用氯化铵与熟石灰共热制备氨气,D
2
错误。
19.(2020·湖南省金太阳高三联考)下列实验操作、现象和结论均正确的是( )
选项 实验操作和现象 结论
向NaBr溶液中分别 滴入少量氯水和苯,振荡、静置,溶液上层
A Br-的还原性强于Cl-
呈橙红色
相同条件下,分别 向20mL0.1mol/LKMnO 溶液
4
和20mL0.5mol/LKMnO 溶液中滴加相同浓度和体积的草酸溶液 浓度对反应速率的影响:浓
B 4
(过量),0.5mol/LKMnO 溶液紫色褪去的时间更短(生成的Mn2+对 度越大,反应速率越快
4
该反应无影响)
C 向淀粉碘化钾溶液中通入过量氯气,溶液由无色变 为蓝色,后蓝 氯气具有强氧化性和漂白性色褪去
室温下,用pH试纸测得0.1mol/LNa SO 溶液的pH约为10, HSO -结合H+的能力比SO 2-
D 2 3 3 3
0.1mol/LNaHSO 溶液的pH约为5 的强
3
【答案】A
【解析】A项,NaBr溶液中滴入氯水,发生反应2Br-+Cl =Br +2Cl-,由此得出还原性Br->Cl-,A正
2 2
确;B项,要通过溶液紫色褪去的时间长短比较反应速率快慢,应该让酸性高锰酸钾的体积和浓度均相同,
改变草酸的浓度,B错误;C项,淀粉碘化钾溶液中通入过量氯气,溶液先变蓝后褪色,氯气只表现氧化
性,氯气没有漂白性,C错误;D项,0.1mol/LNa SO 溶液的pH大,碱性强,则结合H+的能力强,D错误;
2 3
故选A。
20.根据下列实验和现象,所得实验结论正确的是( )
选项 实验 现象 实验结论
原溶液中含有 SO 2-、
向某溶液中先滴加适量稀硝酸,再滴加少 4
A 出现白色沉淀 SO 2-、HSO -中的一种
量BaCl 溶液 3 3
2 或几种
在管口观察到
B 向装有Fe(NO ) 溶液的试管中加入稀硫酸 HNO 分解成了NO
3 2 红棕色气体 3 2
左边棉球变为
C 橙色,右边棉 氧化性:Cl>Br >I
2 2 2
球变为蓝色
D SO 和SO 混合气体通入Ba(NO ) 溶液 出现白色沉淀 得到的沉淀只有BaSO
2 3 3 2 4
【答案】D
【解析】A项,加入的硝酸能把SO 2-、HSO -氧化为SO 2-,再加入BaCl 都能生成白色沉淀BaSO,所
3 3 4 2 4
以溶液含有SO 2-、SO 2-、HSO -中的一种或几种,但是若溶液中含有Ag+,也能与BaCl 反应生成白色沉淀,
4 3 3 2
A不正确;B项,加入的硫酸与NO -构成硝酸,能氧化Fe2+,而NO -被还原为NO,NO遇空气生成红棕色
3 3
的NO ,故硝酸分解生成NO 的结论是不正确;C项,含有NaBr的棉球显橙色,说明Cl 的氧化性强于
2 2 2
Br ,因溴易挥发,与Cl 一起与含有KI淀粉的棉球作用而呈蓝色,无法确定是哪种物质把I-氧化为I ,故
2 2 2
结论不正确;D项,SO 溶于水生成硫酸,电离出的H+与NO -构成的硝酸把SO 氧化为SO 2-,所以白色沉
3 3 2 4
淀只有BaSO,故D的结论是正确的。
4
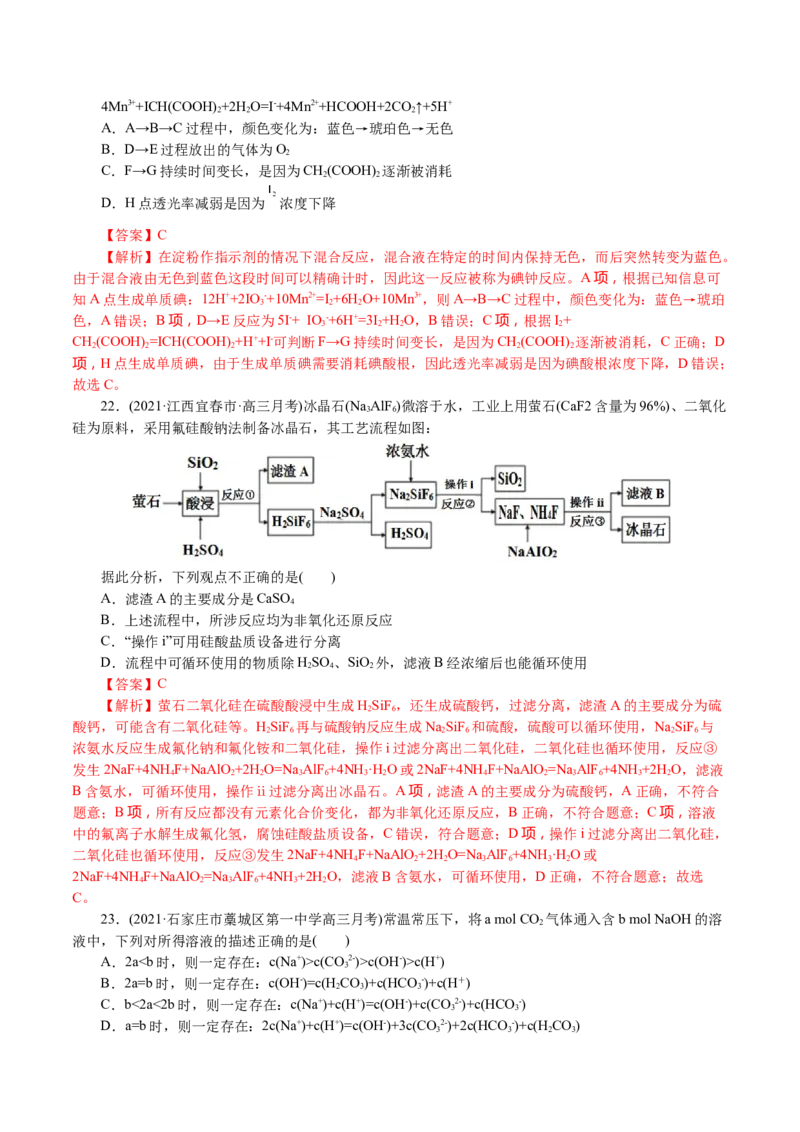
21.(2021·福建厦门市期末)将KIO 、HSO 、HO、MnSO 、CH(COOH) 及可溶性淀粉(指示剂)混合
3 2 4 2 2 4 2 2
进行碘钟实验,通过光线传感器绘制出碘钟振荡反应曲线如下图。下列说法正确的是( )
已知:碘钟周期性振荡的反应如下,除I 与Mn3+外,其他物质在此溶液中为无色或浅色。12H++2IO -
2 3
+10Mn2+=I +6H O+10Mn3+(琥珀色)
2 2
IO -+3H O=I-+3O ↑+3H O
3 2 2 2 2
5I-+ IO -+6H+=3I +H O
3 2 2
I+ CH(COOH) =ICH(COOH)+H++I-
2 2 2 24Mn3++ICH(COOH) +2H O=I-+4Mn2++HCOOH+2CO ↑+5H+
2 2 2
A.A→B→C过程中,颜色变化为:蓝色→琥珀色→无色
B.D→E过程放出的气体为O
2
C.F→G持续时间变长,是因为CH(COOH) 逐渐被消耗
2 2
D.H点透光率减弱是因为 浓度下降
【答案】C
【解析】在淀粉作指示剂的情况下混合反应,混合液在特定的时间内保持无色,而后突然转变为蓝色。
由于混合液由无色到蓝色这段时间可以精确计时,因此这一反应被称为碘钟反应。A项,根据已知信息可
知A点生成单质碘:12H++2IO -+10Mn2+=I +6H O+10Mn3+,则A→B→C过程中,颜色变化为:蓝色→琥珀
3 2 2
色,A错误;B项,D→E反应为5I-+ IO -+6H+=3I +H O,B错误;C项,根据I+
3 2 2 2
CH(COOH) =ICH(COOH)+H++I-可判断F→G持续时间变长,是因为CH(COOH) 逐渐被消耗,C正确;D
2 2 2 2 2
项,H点生成单质碘,由于生成单质碘需要消耗碘酸根,因此透光率减弱是因为碘酸根浓度下降,D错误;
故选C。
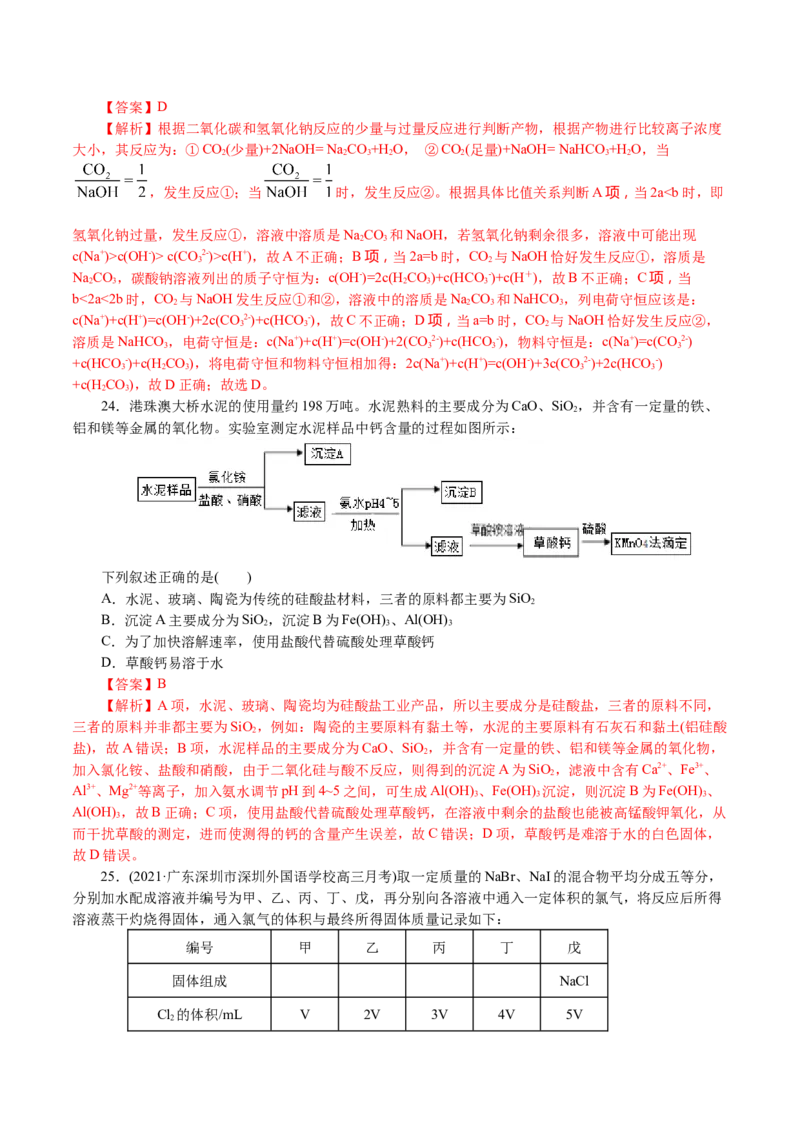
22.(2021·江西宜春市·高三月考)冰晶石(Na AlF)微溶于水,工业上用萤石(CaF2含量为96%)、二氧化
3 6
硅为原料,采用氟硅酸钠法制备冰晶石,其工艺流程如图:
据此分析,下列观点不正确的是( )
A.滤渣A的主要成分是CaSO
4
B.上述流程中,所涉反应均为非氧化还原反应
C.“操作i”可用硅酸盐质设备进行分离
D.流程中可循环使用的物质除HSO 、SiO 外,滤液B经浓缩后也能循环使用
2 4 2
【答案】C
【解析】萤石二氧化硅在硫酸酸浸中生成HSiF,还生成硫酸钙,过滤分离,滤渣A的主要成分为硫
2 6
酸钙,可能含有二氧化硅等。HSiF 再与硫酸钠反应生成NaSiF 和硫酸,硫酸可以循环使用,NaSiF 与
2 6 2 6 2 6
浓氨水反应生成氟化钠和氟化铵和二氧化硅,操作i过滤分离出二氧化硅,二氧化硅也循环使用,反应③
发生2NaF+4NH F+NaAlO+2H O=Na AlF+4NH·HO或2NaF+4NH F+NaAlO=Na AlF+4NH+2H O,滤液
4 2 2 3 6 3 2 4 2 3 6 3 2
B含氨水,可循环使用,操作ⅱ过滤分离出冰晶石。A项,滤渣A的主要成分为硫酸钙,A正确,不符合
题意;B项,所有反应都没有元素化合价变化,都为非氧化还原反应,B正确,不符合题意;C项,溶液
中的氟离子水解生成氟化氢,腐蚀硅酸盐质设备,C错误,符合题意;D项,操作i过滤分离出二氧化硅,
二氧化硅也循环使用,反应③发生2NaF+4NH F+NaAlO+2H O=Na AlF+4NH·HO或
4 2 2 3 6 3 2
2NaF+4NH F+NaAlO=Na AlF+4NH+2H O,滤液B含氨水,可循环使用,D正确,不符合题意;故选
4 2 3 6 3 2
C。
23.(2021·石家庄市藁城区第一中学高三月考)常温常压下,将a mol CO 气体通入含b mol NaOH的溶
2
液中,下列对所得溶液的描述正确的是( )
A.2ac(CO 2-)>c(OH-)>c(H+)
3
B.2a=b时,则一定存在:c(OH-)=c(H CO)+c(HCO-)+c(H+)
2 3 3
C.b<2a<2b时,则一定存在:c(Na+)+c(H+)=c(OH-)+c(CO 2-)+c(HCO-)
3 3
D.a=b时,则一定存在:2c(Na+)+c(H+)=c(OH-)+3c(CO 2-)+2c(HCO-)+c(H CO)
3 3 2 3【答案】D
【解析】根据二氧化碳和氢氧化钠反应的少量与过量反应进行判断产物,根据产物进行比较离子浓度
大小,其反应为:①CO(少量)+2NaOH= Na CO+H O, ②CO(足量)+NaOH= NaHCO +H O,当
2 2 3 2 2 3 2
,发生反应①;当 时,发生反应②。根据具体比值关系判断A项,当2ac(OH-)> c(CO2-)>c(H+),故A不正确;B项,当2a=b时,CO 与NaOH恰好发生反应①,溶质是
3 2
NaCO,碳酸钠溶液列出的质子守恒为:c(OH-)=2c(H CO)+c(HCO-)+c(H+),故B不正确;C项,当
2 3 2 3 3
b<2a<2b时,CO 与NaOH发生反应①和②,溶液中的溶质是NaCO 和NaHCO ,列电荷守恒应该是:
2 2 3 3
c(Na+)+c(H+)=c(OH-)+2c(CO 2-)+c(HCO-),故C不正确;D项,当a=b时,CO 与NaOH恰好发生反应②,
3 3 2
溶质是NaHCO ,电荷守恒是:c(Na+)+c(H+)=c(OH-)+2(CO 2-)+c(HCO-),物料守恒是:c(Na+)=c(CO 2-)
3 3 3 3
+c(HCO-)+c(H CO),将电荷守恒和物料守恒相加得:2c(Na+)+c(H+)=c(OH-)+3c(CO 2-)+2c(HCO-)
3 2 3 3 3
+c(H CO),故D正确;故选D。
2 3
24.港珠澳大桥水泥的使用量约198万吨。水泥熟料的主要成分为CaO、SiO,并含有一定量的铁、
2
铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
下列叙述正确的是( )
A.水泥、玻璃、陶瓷为传统的硅酸盐材料,三者的原料都主要为SiO
2
B.沉淀A主要成分为SiO,沉淀B为Fe(OH) 、Al(OH)
2 3 3
C.为了加快溶解速率,使用盐酸代替硫酸处理草酸钙
D.草酸钙易溶于水
【答案】B
【解析】A项,水泥、玻璃、陶瓷均为硅酸盐工业产品,所以主要成分是硅酸盐,三者的原料不同,
三者的原料并非都主要为SiO,例如:陶瓷的主要原料有黏土等,水泥的主要原料有石灰石和黏土(铝硅酸
2
盐),故A错误;B项,水泥样品的主要成分为CaO、SiO,并含有一定量的铁、铝和镁等金属的氧化物,
2
加入氯化铵、盐酸和硝酸,由于二氧化硅与酸不反应,则得到的沉淀A为SiO,滤液中含有Ca2+、Fe3+、
2
Al3+、Mg2+等离子,加入氨水调节pH到4~5之间,可生成Al(OH) 、Fe(OH) 沉淀,则沉淀B为Fe(OH) 、
3 3 3
Al(OH) ,故B正确;C项,使用盐酸代替硫酸处理草酸钙,在溶液中剩余的盐酸也能被高锰酸钾氧化,从
3
而干扰草酸的测定,进而使测得的钙的含量产生误差,故C错误;D项,草酸钙是难溶于水的白色固体,
故D错误。
25.(2021·广东深圳市深圳外国语学校高三月考)取一定质量的NaBr、NaI的混合物平均分成五等分,
分别加水配成溶液并编号为甲、乙、丙、丁、戊,再分别向各溶液中通入一定体积的氯气,将反应后所得
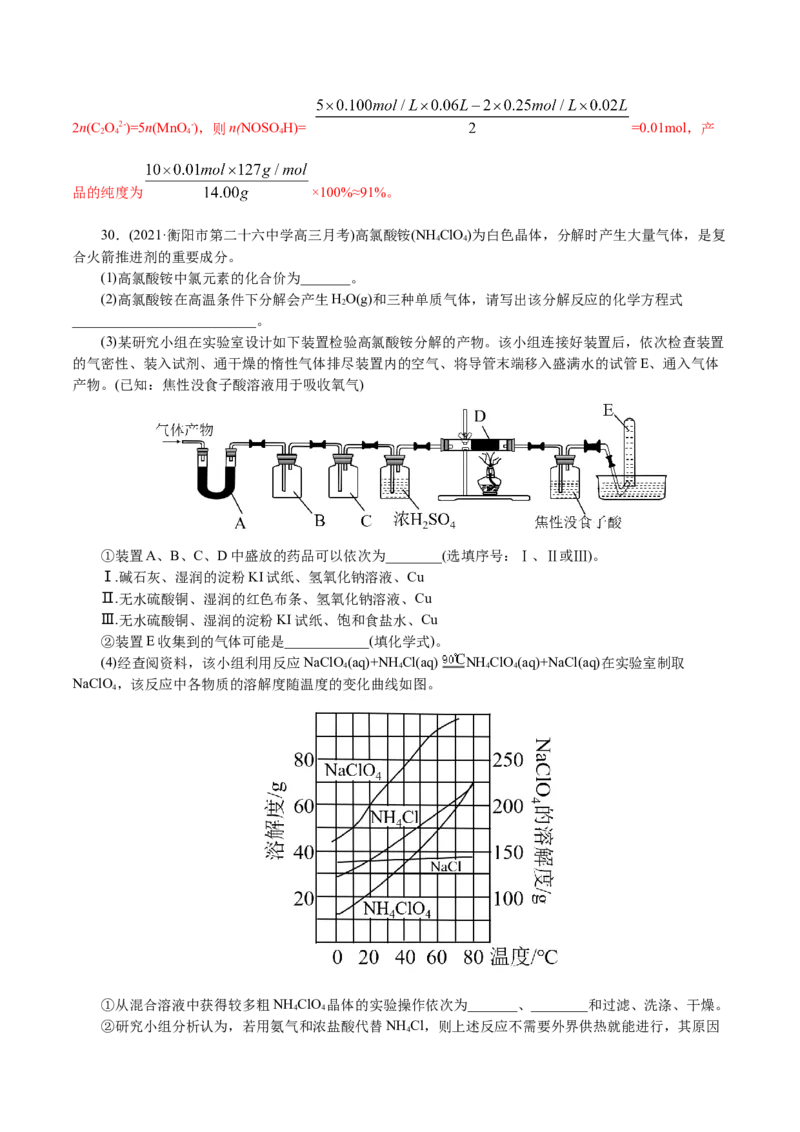
溶液蒸干灼烧得固体,通入氯气的体积与最终所得固体质量记录如下:
编号 甲 乙 丙 丁 戊
固体组成 NaCl
Cl 的体积/mL V 2V 3V 4V 5V
2固体质量/g 54.62 43.64 35.48 30.14 29.25
下列实验结论正确的是( )
A.甲溶液中发生的反应是Cl+2Br-=2Cl-+Br
2 2
B.乙中固体组成为NaBr、NaCl
C.标准状况下Cl 的体积V为2688mL
2
D.原混合物中NaBr的物质的量为1mol
【答案】D
【解析】向NaBr、NaI的混合溶液中通入Cl,需考虑置换反应发生的先后,因还原性I->Br->Cl-,
2
故先有2NaI+Cl =2NaCl+I …①,反应完后再有2NaBr+Cl =2NaCl+Br …②;戊中固体NaCl质量29.25g,
2 2 2 2
根据钠离子守恒可知NaBr、NaI的物质的量之和等于NaCl的物质的量,为 =0.5mol。A项,根
据Na元素守恒可知固体甲的物质的量为0.5mol,则其平均摩尔质量为 =109.24g/mol,NaCl的摩尔
质量为58.5g/mol,NaBr的摩尔质量为103g/mol,NaI的摩尔质量为150g/mol,所以固体甲为NaI、NaBr、
NaCl,则溶液中碘离子还未被完全氧化,所以甲溶液中不可能发生Cl+2Br-=2Cl-+Br ,故A错误;B项,
2 2
乙丙对比,固体的质量减少了43.64g-35.48=8.16g,丙丁对比,固体的质量减少了35.48g-30.14g=5.34g,且
丁到戊固体的质量还在减少,说明丁中NaBr还未完全反应;若乙中不含NaI,由于通入的氯气的变化量相
同,则乙丙减少的和丙丁减少都应是VL氯气能够反应的NaBr与生成的NaCl的差值,但实际上并不
相等,说明乙中含有NaI,固体组成应为NaI、NaBr、NaCl,故B错误;C项,甲、乙固体组成均为为
NaI、NaBr、NaCl,所以甲和乙对比固体减少的质量就是VL氯气反应的NaI和NaCl的质量的差值,所以
n(NaI)= =0.12mol,则VL氯气的物质的量为0.06mol,所以体积为0.06mol22.4L/
mol=1.344L=1344mL,故C错误;D项,固体甲与通入氯气前相比减少的质量为VL氯气反应的NaI和
NaCl的质量的差值,即54.62g-43.64g=10.98g,所以通氯气前的总质量为54.62g+10.98g=65.6g,令原溶液
中NaI的物质的量为x,NaBr的物质的量为y,则 ,解得
x=0.3mol,y=0.2mol,由于原混合物五等分,则原来混合物中溴化钠的物质的量=0.2mol×5=1mol,故D正
确;故选D。
二、非选择题
26.(2021·山东潍坊市质检)硫及其化合物在生产生活中用途广泛,用化学反应原理研究它们的性质和
用途有重要意义。回答下列问题:
(1)亚硫酰氯(SOCl )是一种液态化合物,沸点为77℃。向盛有10 mL水的锥形瓶中小心滴加8~10滴
2
SOCl ,观察到剧烈反应,液面上有白雾生成,并有刺激性气味气体逸出。轻轻振荡锥形瓶,白雾消失后,
2
向溶液中滴加AgNO 溶液,有不溶于稀硝酸的白色沉淀生成。
3
①SOCl 与水反应的化学方程式为___________。
2
②蒸干AlCl 溶液不能得到无水AlCl ,将SOCl 与AlCl ·6H O混合加热,可得到无水AlCl ,试解释原
3 3 2 3 2 3
因:___________。
(2)利用反应2HS+SO =3S↓+2HO可将石油气中的HS转化为S。研究小组同学在实验室中进行如下
2 2 2 2
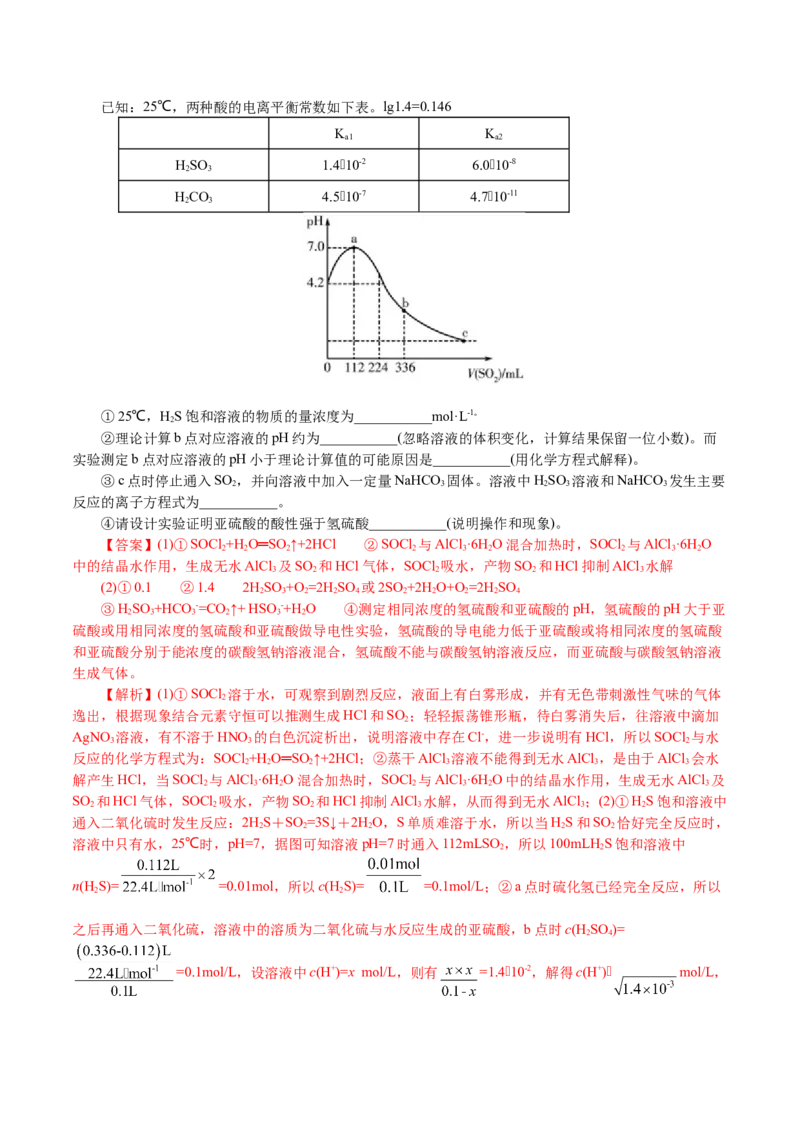
实验:25℃,向100 mL H S饱和溶液中缓缓通入SO 气体(气体体积换算成标准状况),测得溶液pH与通
2 2
入SO 的体积关系如图所示。
2已知:25℃,两种酸的电离平衡常数如下表。lg1.4=0.146
K K
a1 a2
HSO 1.410-2 6.010-8
2 3
HCO 4.510-7 4.710-11
2 3
①25℃,HS饱和溶液的物质的量浓度为___________mol·L-1。
2
②理论计算b点对应溶液的pH约为___________(忽略溶液的体积变化,计算结果保留一位小数)。而
实验测定b点对应溶液的pH小于理论计算值的可能原因是___________(用化学方程式解释)。
③c点时停止通入SO ,并向溶液中加入一定量NaHCO 固体。溶液中HSO 溶液和NaHCO 发生主要
2 3 2 3 3
反应的离子方程式为___________。
④请设计实验证明亚硫酸的酸性强于氢硫酸___________(说明操作和现象)。
【答案】(1)①SOCl +H O═SO↑+2HCl ②SOCl 与AlCl ·6H O混合加热时,SOCl 与AlCl ·6H O
2 2 2 2 3 2 2 3 2
中的结晶水作用,生成无水AlCl 及SO 和HCl气体,SOCl 吸水,产物SO 和HCl抑制AlCl 水解
3 2 2 2 3
(2)①0.1 ②1.4 2HSO +O =2H SO 或2SO +2H O+O=2H SO
2 3 2 2 4 2 2 2 2 4
③HSO +HCO-=CO ↑+ HSO -+H O ④测定相同浓度的氢硫酸和亚硫酸的pH,氢硫酸的pH大于亚
2 3 3 2 3 2
硫酸或用相同浓度的氢硫酸和亚硫酸做导电性实验,氢硫酸的导电能力低于亚硫酸或将相同浓度的氢硫酸
和亚硫酸分别于能浓度的碳酸氢钠溶液混合,氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸与碳酸氢钠溶液
生成气体。
【解析】(1)①SOCl 溶于水,可观察到剧烈反应,液面上有白雾形成,并有无色带刺激性气味的气体
2
逸出,根据现象结合元素守恒可以推测生成HCl和SO ;轻轻振荡锥形瓶,待白雾消失后,往溶液中滴加
2
AgNO 溶液,有不溶于HNO 的白色沉淀析出,说明溶液中存在Cl-,进一步说明有HCl,所以SOCl 与水
3 3 2
反应的化学方程式为:SOCl +H O═SO↑+2HCl;②蒸干AlCl 溶液不能得到无水AlCl ,是由于AlCl 会水
2 2 2 3 3 3
解产生HCl,当SOCl 与AlCl ·6H O混合加热时,SOCl 与AlCl ·6H O中的结晶水作用,生成无水AlCl 及
2 3 2 2 3 2 3
SO 和HCl气体,SOCl 吸水,产物SO 和HCl抑制AlCl 水解,从而得到无水AlCl ;(2)①HS饱和溶液中
2 2 2 3 3 2
通入二氧化硫时发生反应:2HS+SO =3S↓+2HO,S单质难溶于水,所以当HS和SO 恰好完全反应时,
2 2 2 2 2
溶液中只有水,25℃时,pH=7,据图可知溶液pH=7时通入112mLSO ,所以100mLH S饱和溶液中
2 2
n(H S)= =0.01mol,所以c(H S)= =0.1mol/L;②a点时硫化氢已经完全反应,所以
2 2
之后再通入二氧化硫,溶液中的溶质为二氧化硫与水反应生成的亚硫酸,b点时c(H SO )=
2 4
=0.1mol/L,设溶液中c(H+)=x mol/L,则有 =1.410-2,解得c(H+) mol/L,所以pH=-lg =1.4;由于亚硫酸具有较强还原性易被空气中的氧气氧化生成生成硫酸,使溶液的
酸性变强,相应的化学方程式为2HSO +O =2H SO 或2SO +2H O+O=2H SO ;根据表格中的数据可知酸
2 3 2 2 4 2 2 2 2 4
性:HSO > H CO> HSO -,所以离子反应方程式为HSO +HCO-=CO ↑+ HSO -+H O;④酸性越强同浓度
2 3 2 3 3 2 3 3 2 3 2
的溶液pH越小,所以可以测定相同浓度的氢硫酸和亚硫酸的pH,氢硫酸的pH大于亚硫酸;酸性越强电
离程度越大,同浓度的溶液导电性越强,用相同浓度的氢硫酸和亚硫酸做导电性实验,氢硫酸的导电能力
低于亚硫酸;强酸可以和弱酸盐反应生成强酸盐和弱酸,所以可以将相同浓度的氢硫酸和亚硫酸分别于能
浓度的碳酸氢钠溶液混合,氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸与碳酸氢钠溶液生成气体。
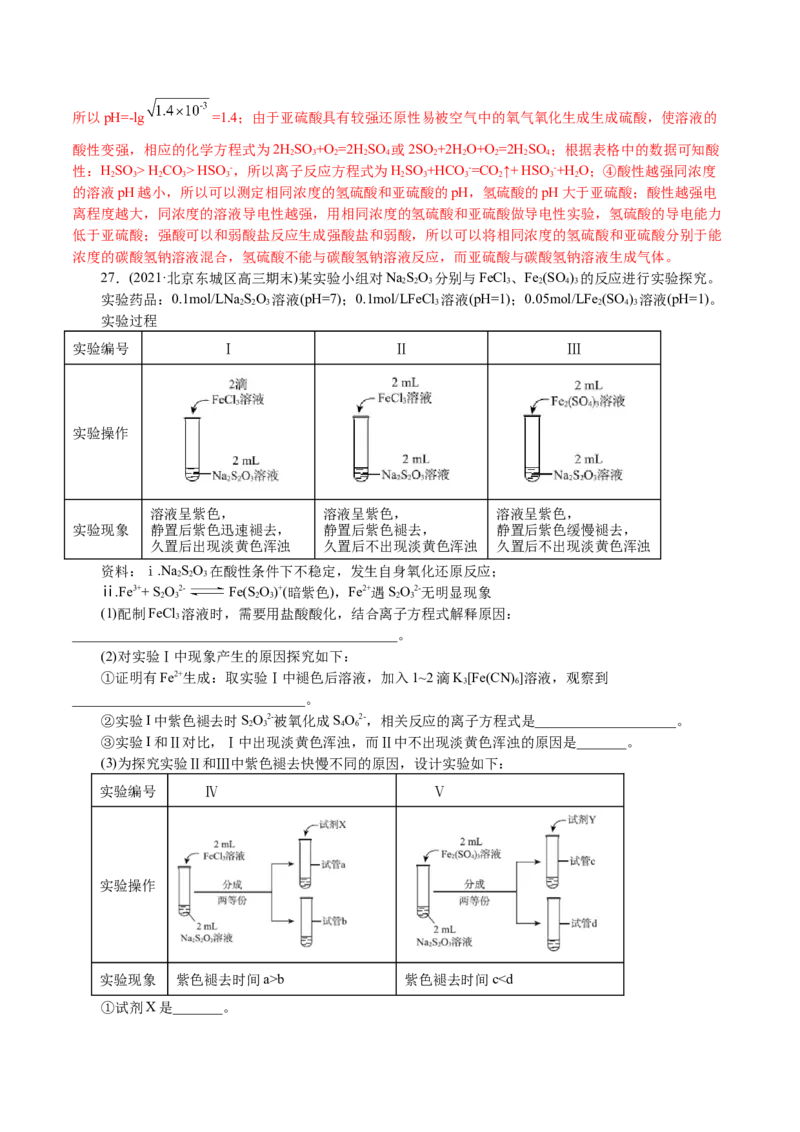
27.(2021·北京东城区高三期末)某实验小组对NaSO 分别与FeCl 、Fe (SO ) 的反应进行实验探究。
2 2 3 3 2 4 3
实验药品:0.1mol/LNa SO 溶液(pH=7);0.1mol/LFeCl 溶液(pH=1);0.05mol/LFe (SO ) 溶液(pH=1)。
2 2 3 3 2 4 3
实验过程
实验编号 Ⅰ Ⅱ Ⅲ
实验操作
溶液呈紫色, 溶液呈紫色, 溶液呈紫色,
实验现象 静置后紫色迅速褪去, 静置后紫色褪去, 静置后紫色缓慢褪去,
久置后出现淡黄色浑浊 久置后不出现淡黄色浑浊 久置后不出现淡黄色浑浊
资料:ⅰ.Na SO 在酸性条件下不稳定,发生自身氧化还原反应;
2 2 3
ⅱ.Fe3++ S O2- Fe(S O)+(暗紫色),Fe2+遇SO2-无明显现象
2 3 2 3 2 3
(1)配制FeCl 溶液时,需要用盐酸酸化,结合离子方程式解释原因:
3
______________________________________________。
(2)对实验Ⅰ中现象产生的原因探究如下:
①证明有Fe2+生成:取实验Ⅰ中褪色后溶液,加入1~2滴K[Fe(CN) ]溶液,观察到
3 6
_________________________________。
②实验I中紫色褪去时SO2-被氧化成SO2-,相关反应的离子方程式是____________________。
2 3 4 6
③实验I和Ⅱ对比,Ⅰ中出现淡黄色浑浊,而Ⅱ中不出现淡黄色浑浊的原因是_______。
(3)为探究实验Ⅱ和Ⅲ中紫色褪去快慢不同的原因,设计实验如下:
实验编号 Ⅳ Ⅴ
实验操作
实验现象 紫色褪去时间a>b 紫色褪去时间cb,说明硫
酸根离子能减慢反应速率,褪色时间较长;实验Ⅴ中探究氯离子对速率的影响,向试管c中加入氯化钠固
体,紫色褪去时间c