文档内容
解密 12 化学工艺流程
一、单选题
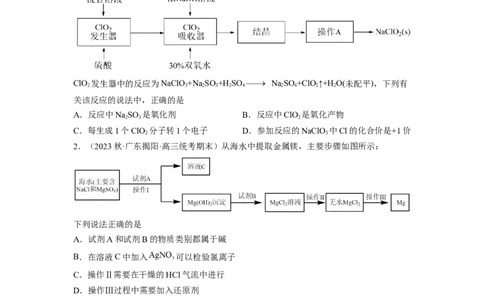
1.(2021秋·广东清远·高一连州市连州中学校考期中)ClO 和亚氯酸钠(NaClO)都是广泛
2 2
使用的漂白剂、消毒剂。高浓度ClO 气体易发生爆炸,在生产、使用时需要用其他气体进
2
行稀释。某工厂生产ClO 和NaClO 的工艺流程如下:
2 2
ClO 发生器中的反应为NaClO+Na SO +H SO Na SO +ClO ↑+H O(未配平),下列有
2 3 2 3 2 4 2 4 2 2
关该反应的说法中,正确的是
A.反应中NaSO 是氧化剂 B.反应中ClO 是氧化产物
2 3 2
C.每生成1个ClO 分子转1个电子 D.参加反应的NaClO 中Cl的化合价是+1价
2 3
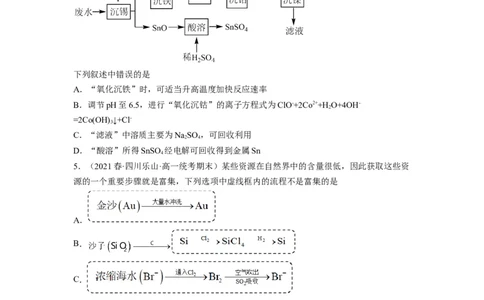
2.(2023秋·广东揭阳·高三统考期末)从海水中提取金属镁,主要步骤如图所示:
下列说法正确的是
A.试剂A和试剂B的物质类别都属于碱
B.在溶液C中加入 可以检验氯离子
C.操作Ⅱ需要在干燥的HCl气流中进行
D.操作Ⅲ过程中需要加入还原剂
3.(山东省潍坊市2023届高三下学期一模考试化学试题)由含硒废料(主要含S、Se、
、CuO、ZnO、 等)在实验室中制取硒的流程如图:
下列说法错误的是
A.“分离”时得到含硫煤油的方法是分液B.“酸溶”操作的目的是除去废料中的金属氧化物
C.“浸取”后的分离操作所用玻璃仪器为烧杯、漏斗、玻璃棒
D.“酸化”时发生反应的离子方程式:
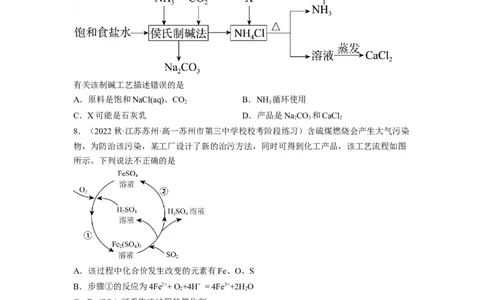
4.(2023春·山东·高三校联考开学考试)某电镀厂废水的pH为0.45,主要含有Sn2+、
Ni2+和SO ,还含有少量的Fe2+和Co2+,处理该废水的一种工艺流程如图所示:
下列叙述中错误的是
A.“氧化沉铁”时,可适当升高温度加快反应速率
B.调节pH至6.5,进行“氧化沉钴”的离子方程式为ClO-+2Co2++H O+4OH-
2
=2Co(OH) ↓+Cl-
3
C.“滤液”中溶质主要为NaSO ,可回收利用
2 4
D.“酸溶”所得SnSO 经电解可回收得到金属Sn
4
5.(2021春·四川乐山·高一统考期末)某些资源在自然界中的含量很低,因此获取这些资
源的一个重要步骤就是富集,下列选项中虚线框内的流程不是富集的是
A.
B.
C.
D.
6.(2021秋·河南信阳·高三河南宋基信阳实验中学校考阶段练习)下列从海洋中获取物质
的方案不合理的是( )
A.粗盐 饱和食盐水 Cl 漂白粉
2B.苦卤 Br (aq) HBr(aq) 粗Br
2 2
C.除去粗盐中杂质(Mg2+、SO 、Ca2+),加入的药品顺序:NaOH溶液→BaCl 溶液
2
→NaCO 溶液→过滤后加盐酸
2 3
D.海水 Mg(OH) MgCl 溶液 Mg
2 2
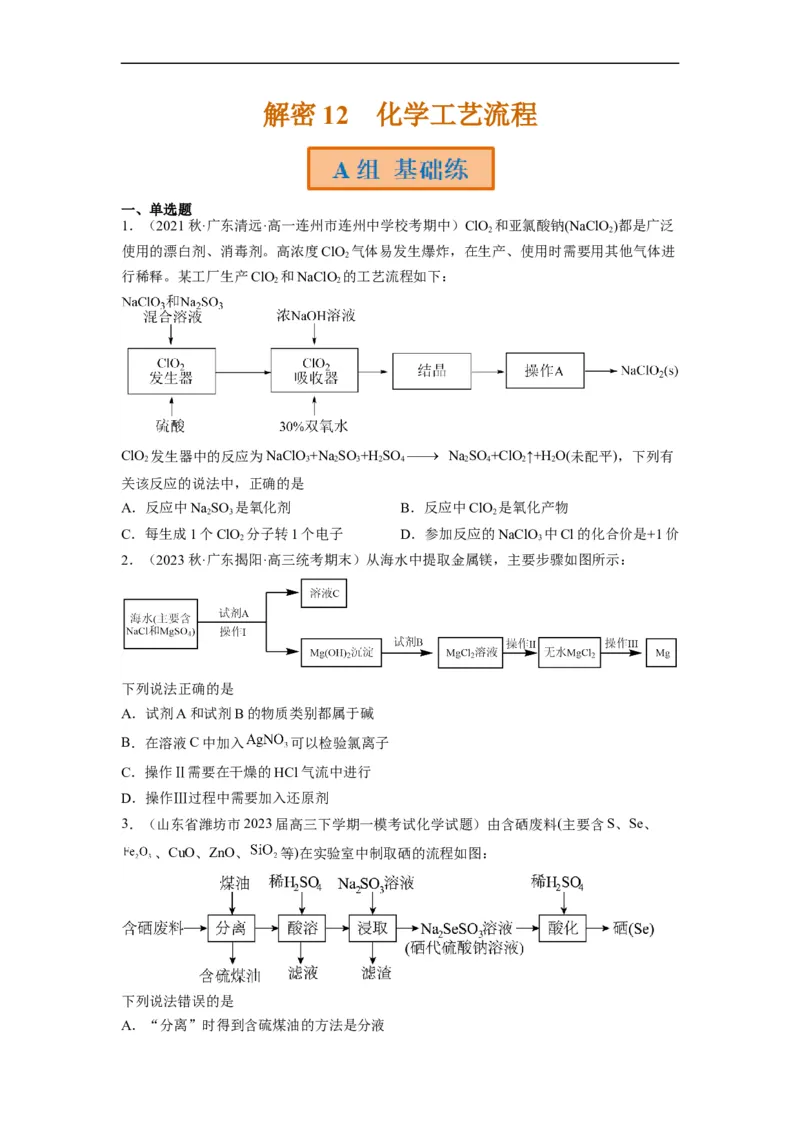
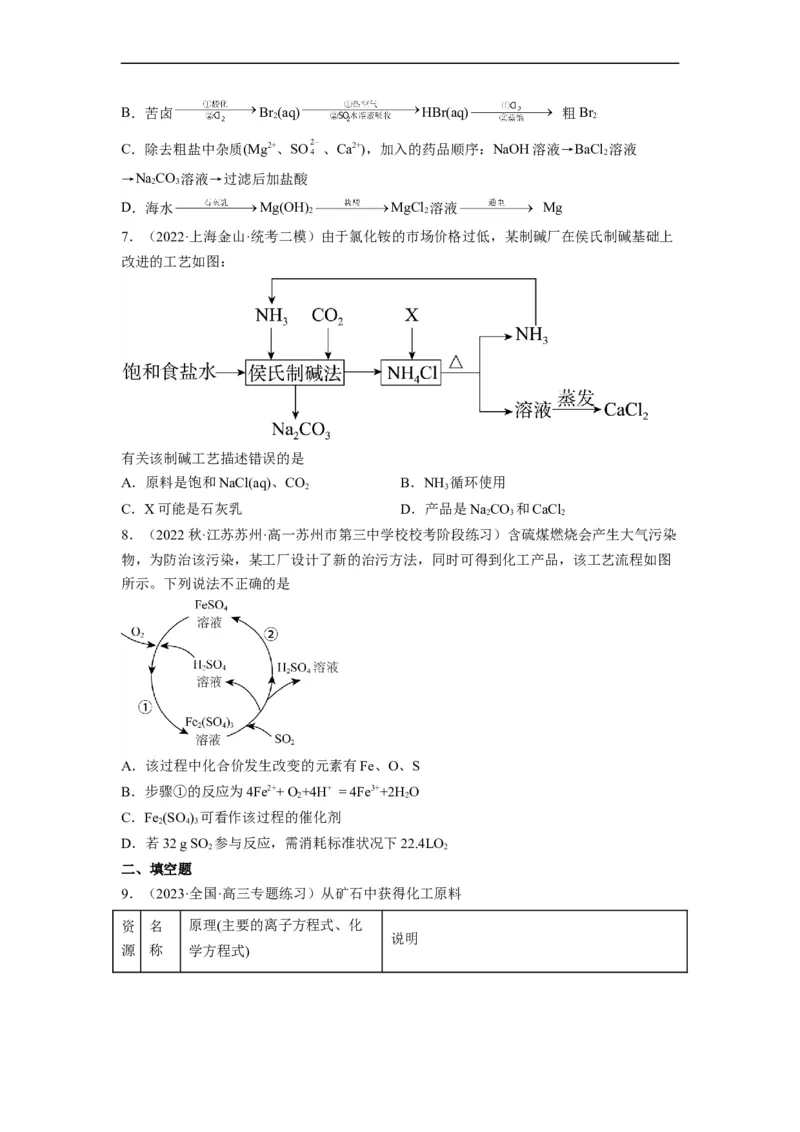
7.(2022·上海金山·统考二模)由于氯化铵的市场价格过低,某制碱厂在侯氏制碱基础上
改进的工艺如图:
有关该制碱工艺描述错误的是
A.原料是饱和NaCl(aq)、CO B.NH 循环使用
2 3
C.X可能是石灰乳 D.产品是NaCO 和CaCl
2 3 2
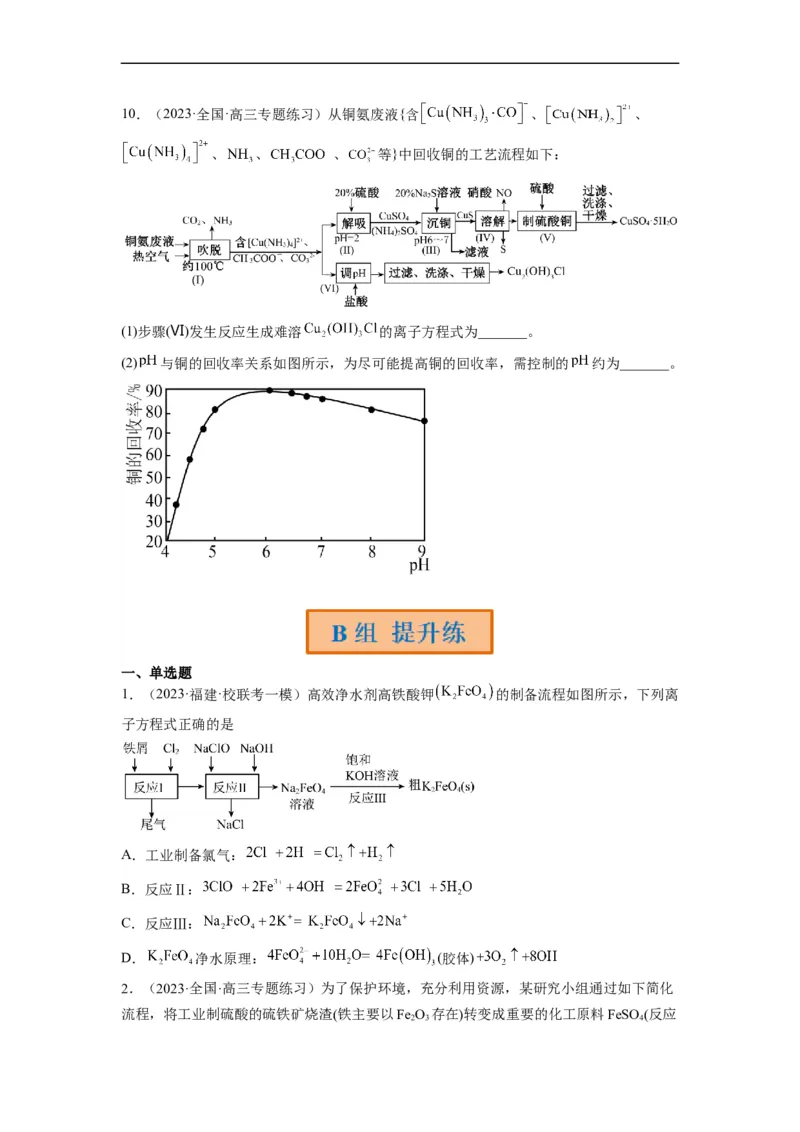
8.(2022秋·江苏苏州·高一苏州市第三中学校校考阶段练习)含硫煤燃烧会产生大气污染
物,为防治该污染,某工厂设计了新的治污方法,同时可得到化工产品,该工艺流程如图
所示。下列说法不正确的是
A.该过程中化合价发生改变的元素有Fe、O、S
B.步骤①的反应为4Fe2++ O +4H+ = 4Fe3++2H O
2 2
C.Fe (SO ) 可看作该过程的催化剂
2 4 3
D.若32 g SO 参与反应,需消耗标准状况下22.4LO
2 2
二、填空题
9.(2023·全国·高三专题练习)从矿石中获得化工原料
资 名 原理(主要的离子方程式、化
说明
源 称 学方程式)1.
工
(沸腾炉)
业
制 (接触
三步反应都是_______;为了充分利用,进入
硫
室)
接触室的气体要净化、预热;用98%_______
酸
(吸收塔)
吸收 ,得到发烟硫酸,再稀释
2.
铝
的
冶 一
炼
系列的变化是为了得到纯净的
矿
产 3.
粗
粗硅提纯:
硅
,氧化产物不是
的
_______,是_______
提
纯
4.
硅
酸
盐
制玻璃的原料是_______、_______、
工
_______,玻璃的主要成分是_______、
业
_______、_______
—
—
玻
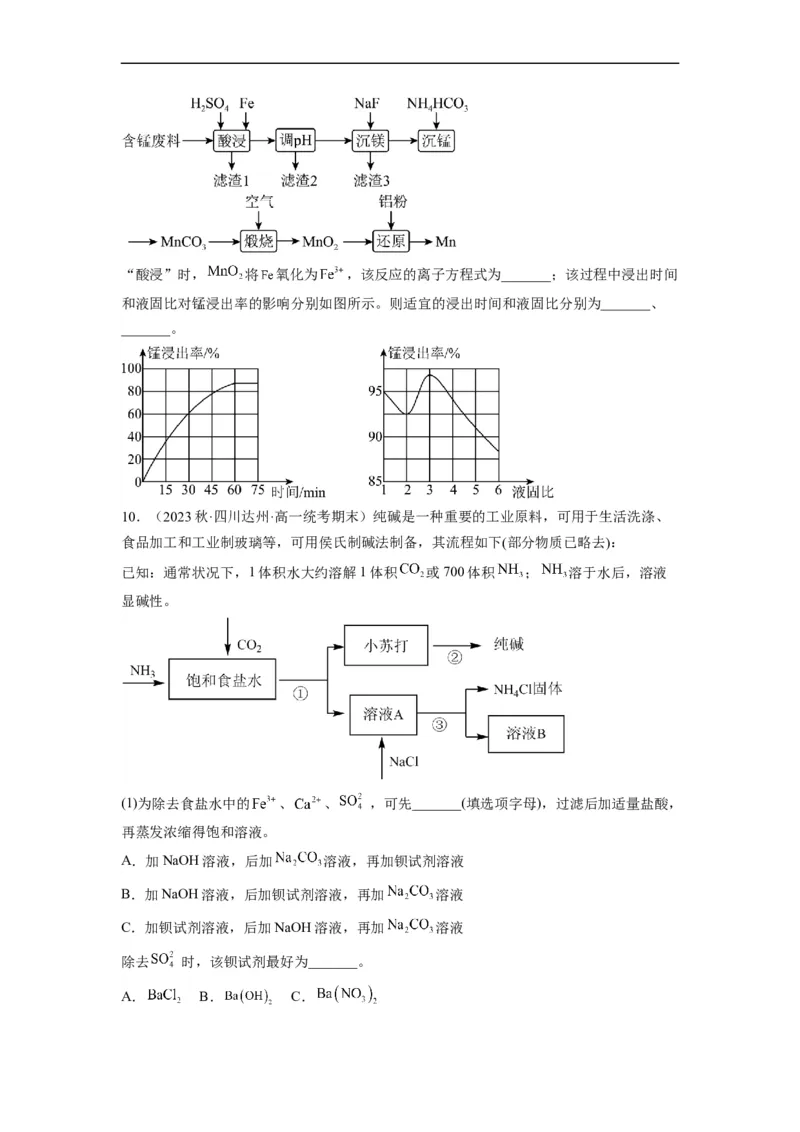
璃10.(2023·全国·高三专题练习)从铜氨废液{含 、 、
、 、 、 等}中回收铜的工艺流程如下:
(1)步骤(Ⅵ)发生反应生成难溶 的离子方程式为_______。
(2) 与铜的回收率关系如图所示,为尽可能提高铜的回收率,需控制的 约为_______。
一、单选题
1.(2023·福建·校联考一模)高效净水剂高铁酸钾 的制备流程如图所示,下列离
子方程式正确的是
A.工业制备氯气:
B.反应Ⅱ:
C.反应Ⅲ:
D. 净水原理: (胶体)
2.(2023·全国·高三专题练习)为了保护环境,充分利用资源,某研究小组通过如下简化
流程,将工业制硫酸的硫铁矿烧渣(铁主要以Fe O 存在)转变成重要的化工原料FeSO (反应
2 3 4条件略)。
活化硫铁矿还原Fe3+的主要反应为FeS+7Fe (SO )+8H O=15FeSO +8H SO ,不考虑其他反
2 2 4 3 2 4 2 4
应,下列叙述不正确的是
A.第Ⅰ步HSO 与Fe O 反应的离子方程式是Fe O+6H+=2Fe3++3H O
2 4 2 3 2 3 2
B.检验第Ⅱ步中Fe3+是否完全还原,应选择KMnO 溶液或K[Fe(CN) ]溶液
4 3 6
C.在第Ⅳ步通入空气引起溶液pH降低的原因是Fe2+被氧化为Fe3+,Fe3+水解产生H+
D.反应FeS+7Fe (SO )+8H O=15FeSO +8H SO 中1molFeS 反应转移14mol电子
2 2 4 3 2 4 2 4 2
3.(2023·全国·高三专题练习)与氮同主族,在中性及碱性环境下常以 的形式存
在,铋及其化合物广泛应用于电子、医药等领域。以辉铋矿(主要成分为 ,含少量
等杂质)为原料,采用湿法冶金工艺制备精铋的工艺流程如图所示,下列说法错误的
是
A.“浸出”产生S的主要离子反应为
B.“浸出”时盐酸可以还原杂质
C.“浸出”“置换”“再生”“电解精炼”中均有氧化还原反应发生
D.“再生液”不能加入“浸出”操作中循环利用
4.(2023·湖南株洲·高三湖南省茶陵县第一中学校考阶段练习)从某含有 、 、
的工业废液中回收铜并制备氯化铁晶体的流程如下:则下列说法错误的是
A.试剂a是铁、试剂b是盐酸
B.试剂c是氯气,相应的反应为
C.操作Ⅰ、操作Ⅱ所用仪器相同,均要用到烧杯、分液漏斗、玻璃棒
D.加入过量试剂c之后,溶液W依然能使少量酸性 溶液褪色
5.(2023秋·天津北辰·高三天津市第四十七中学校考期末)元素铬(Cr)的几种化合物存在
下列转化关系:
已知:2CrO +2H+ Cr O +HO。KCrO 溶液绿色,KCrO 溶液黄色, KCr O 溶液
2 2 2 2 4 2 2 7
橙红色。下列判断错误的是
A.反应①表明Cr O 可能有两性氧化物的性质 B.反应②利用了HO 的氧化性
2 3 2 2
C.反应③中溶液颜色变化是由化学平衡移动引起的 D.基态Cr原子的电子排布式是
[Ar]3d44s2
6.(2022春·重庆沙坪坝·高三重庆八中校考阶段练习)铅属于三大重金属污染物之一,是
一种严重危害人体健康的重金属元素。工业中常对铅蓄电池中的铅膏(含PbSO 和PbO 等)
4 2
进行处理后回收金属铅,工艺流程如图所示:
下列说法正确的是
A.铅蓄电池放电时可将化学能100%转化为电能
B.电解时,电极材料均为铅棒
C.向废铅膏中加入(NH )CO 和HO 后,溶液温度不宜过高
4 2 3 2 2
D.BF 的电子式为
7.(2021秋·江苏南通·高三校考阶段练习)以红土镍矿(主要成分为NiS,还反应少量CaS和 )为原料制备 的流程如下 :
已知:①“煅烧”得到 、CaO和 ;②“酸浸”时,有 和 产生。
下列关于说法错误的是
A.“煅烧”时,为加快反应速率,可以将红土镍矿粉碎
B.“沉钙”后所得滤液中,主要存在的离子有: 、 、
C.“还原”时,反应的离子方程式为:
D.该流程中, 是可以循环使用的物质
8.(2022秋·山东济南·高三济南市历城第二中学校考期末)将废旧锌锰电池进行回收处理
以实现资源的再生利用,初步处理后的废料中含 、 、 及 等,用
该废料制备 和 的一种工艺流程如下:(已知: 的金属活动性强于 , 在
酸性条件下比较稳定, 大于5.5时易被氧化)
下列说法错误的是
A.“还原焙烧”时 元素被还原,有气体产物生成
B.滤渣1、滤渣2的主要成分分别为炭黑、氢氧化铁
C.“净化”时通入的 可用 来代替, 的作用是调节溶液的 大于5.5以便
于除去杂质离子
D.“电解”时的阳极反应式为
二、填空题
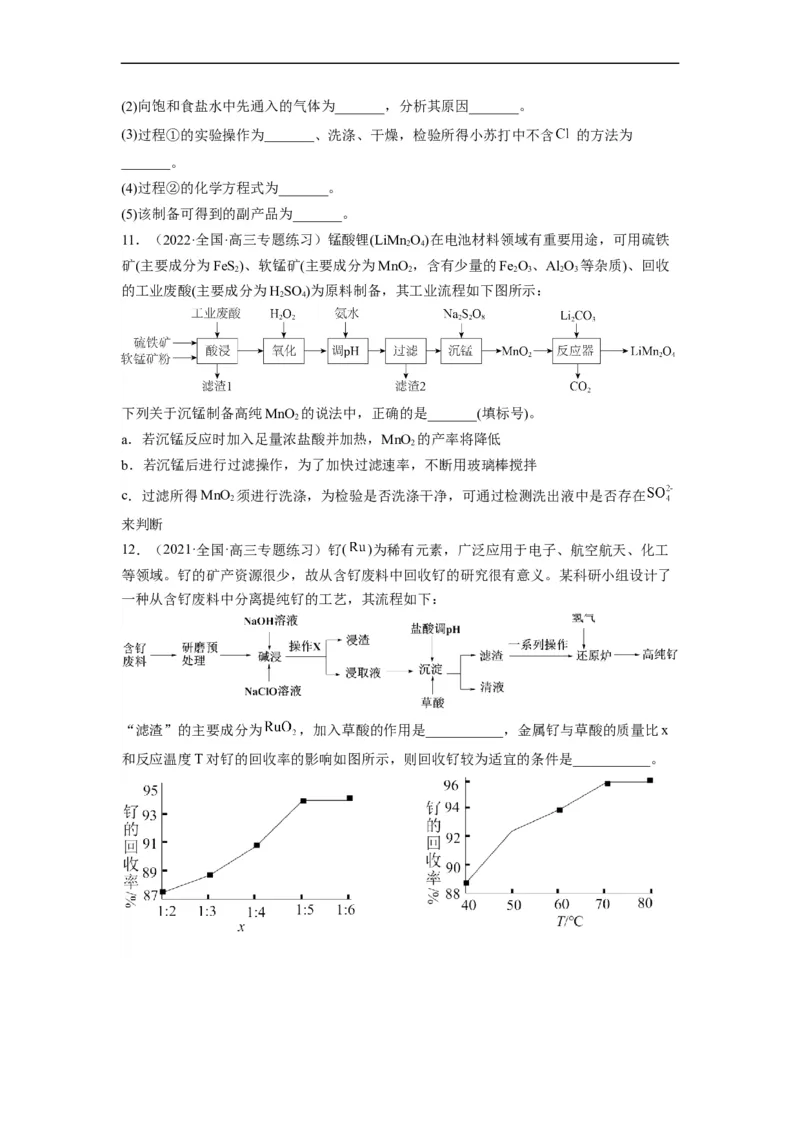
9.(2023·全国·高三专题练习)实验室用含锰废料(主要成分为 ,还含有少量
)为原料制备 的工艺流程如下:“酸浸”时, 将 氧化为 ,该反应的离子方程式为_______;该过程中浸出时间
和液固比对锰浸出率的影响分别如图所示。则适宜的浸出时间和液固比分别为_______、
_______。
10.(2023秋·四川达州·高一统考期末)纯碱是一种重要的工业原料,可用于生活洗涤、
食品加工和工业制玻璃等,可用侯氏制碱法制备,其流程如下(部分物质已略去):
已知:通常状况下,1体积水大约溶解1体积 或700体积 ; 溶于水后,溶液
显碱性。
(1)为除去食盐水中的 、 、 ,可先_______(填选项字母),过滤后加适量盐酸,
再蒸发浓缩得饱和溶液。
A.加NaOH溶液,后加 溶液,再加钡试剂溶液
B.加NaOH溶液,后加钡试剂溶液,再加 溶液
C.加钡试剂溶液,后加NaOH溶液,再加 溶液
除去 时,该钡试剂最好为_______。
A. B. C.(2)向饱和食盐水中先通入的气体为_______,分析其原因_______。
(3)过程①的实验操作为_______、洗涤、干燥,检验所得小苏打中不含 的方法为
_______。
(4)过程②的化学方程式为_______。
(5)该制备可得到的副产品为_______。
11.(2022·全国·高三专题练习)锰酸锂(LiMn O)在电池材料领域有重要用途,可用硫铁
2 4
矿(主要成分为FeS)、软锰矿(主要成分为MnO ,含有少量的Fe O、Al O 等杂质)、回收
2 2 2 3 2 3
的工业废酸(主要成分为HSO )为原料制备,其工业流程如下图所示:
2 4
下列关于沉锰制备高纯MnO 的说法中,正确的是_______(填标号)。
2
a.若沉锰反应时加入足量浓盐酸并加热,MnO 的产率将降低
2
b.若沉锰后进行过滤操作,为了加快过滤速率,不断用玻璃棒搅拌
c.过滤所得MnO 须进行洗涤,为检验是否洗涤干净,可通过检测洗出液中是否存在
2
来判断
12.(2021·全国·高三专题练习)钌( )为稀有元素,广泛应用于电子、航空航天、化工
等领域。钌的矿产资源很少,故从含钌废料中回收钌的研究很有意义。某科研小组设计了
一种从含钌废料中分离提纯钌的工艺,其流程如下:
“滤渣”的主要成分为 ,加入草酸的作用是___________,金属钌与草酸的质量比x
和反应温度T对钌的回收率的影响如图所示,则回收钌较为适宜的条件是___________。