文档内容
2022—2023学年度上学期期末考试高三试题 4.4-萜烯醇的结构如图所示,下列说法错误的是( )
A.分子式为CHO
10 18 HC
化 学 3 CH 3
B.能与氯化铁溶液反应显紫色
CH
C.分子中含有1个手性碳原子 OH 3
命题人:丹东二中 王婷婷 审题人:丹东二中 栾逸尘
D.能发生氧化反应、消去反应、加成反应和取代反应
考试时间:75分钟 满分:100分
5.下列反应的离子方程式书写正确的是( )
可能用到的相对原子质量:H-1 Li-7 C-12 O-16 Na-23 Al-27 S-32 A.向Ca(ClO) 2 溶液中通入少量CO 2 :ClO-+CO 2 +H 2 O=HCO 3 -+HClO
Cl-35.5 Fe-56 Cu-64 Ce-140 B.惰性电极电解MgCl溶液:2Cl-+2HO=电=解==H↑+Cl↑+2OH-
2 2 2 2
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一个选项符合要求)
C.FeI溶液中加入足量的Br:2Fe2++4I-+3Br=2Fe3++2I+6Br-
2 2 2 2
1“.神舟”飞天、“嫦娥”奔月、“天问”探火、“羲和”探日,勇攀科技高峰,逐梦航天强国,化学功
D.NHCl溶于DO中:NH++DO�NH?DO+H+
4 2 4 2 3 2
不可没。以下相关说法正确的是( )
6.路易斯碱是指能作为电子对给予体的原子、分子、离子或原子团。NH、HO、CO、CHOH、
3 2 2 3
A.神舟十三号返回舱上使用的酚醛空心微球外层为酚醛树脂,酚醛树脂属于有机高分子
OH-均为常见的路易斯碱。下列说法正确的是( )
材料
A.CO、HO都是由极性键形成的非极性分子
2 2
B.嫦娥五号在地月往返旅程中搭载了存储抗疫歌曲等内容的芯片,芯片主要成分为SiC
B.NH的键角大于HO的键角
3 2
C.天问一号热控材料纳米气凝胶的胶粒直径小于1nm
C.CHOH中的C、HO中的O杂化方式不同
3 2
D.羲和号卫星反射镜使用了高技术陶瓷材料,高技术陶瓷属于传统无机非金属材料
D.CHOH的沸点高于甲醛沸点的原因是由于范德华力大
3
2.下列化学用语错误的是( )
7.利用下列实验装置完成相应实验,能达到实验目的是( )
A B C D
A.CHCl的电子式:∶Cl∶C∶Cl∶
2 2
溴、苯的混合液
分水器
进水
浓硫酸
乙醇、 乙醇、 酒精
水 碎 铁 乙酸、
瓷 片 出水 丝 A 溶 gN 液 O3 浓 碎 硫 瓷 酸 片 碎瓷片 N 溶 a 浓 O 液 H 溴水
加热器
验证苯和液溴发生取 利用分水器提高乙酸
分离乙醇和水 验证酒精脱水生成乙烯
代反应 乙酯的产率
8.物质类别和元素价态是学习元素及其化合物
含N 含S
物质 物质
性质的重要认识视角。下图是硫和氮元素部分“价 D E
W 含氧酸
类”二维关系图。下列相关说法错误的是( )
Z Y 氧化物
C F
A.图中A和C可以反应生成B X
单质
B
B.可以实现R→Y→Z→W的转化
R氢化物
A
C.A的水溶液为酸性,R的水溶液为碱性,可以
+5+4 +2 0 -3 -2 0 +4 +6
说明N的非金属性比S强
N的化合价 S的化合价
D.C可以使品红溶液褪色,R可以使无色酚酞溶液变红
高三化学-1 高三化学-2
∶
∶
∶
∶
∶
∶
H
H
H
B.甲醛分子中π键的电子云轮廓图: O C
H
C.HO的VSEPR模型:
2
D.HO的空间填充模型:
2 2
3.设N为阿伏加德罗常数的值,下列叙述错误的是( )
A
A.30gCHCOOH和HCHO的混合物中含有的碳原子数目为N
3 A
B.由乙烯制备1mol一氯乙烷需要氯气的分子数为N
A
C.0.3molCl与足量铁粉反应,转移的电子数为0.6N
2 A
D.64g环状S( )分子中含有2N个S-S键
8 A9.下列实验操作和实验现象所对应的实验结论均正确的是( )
A.V的价层电子排布图为:
选项 实验操作 实验现象 实验结论
B.该反应消除了NO的污染,总反应方程式为:4NH+6NO=催=化==剂==5N+6HO
把分别盛有NaCl溶液和Fe(OH) 3 胶 观察到Fe(OH) 3 胶体中有 丁达尔效应是胶体 3 2 2
A 体的两烧杯置于暗处,均用红色激 一条光亮的通路,NaCl溶 C.V5+-OH、V4+-OH在该反应过程中均作催化剂
和溶液的本质区别
光笔照射烧杯中的液体 液无明显现象
D.每消除掉1molNO,整个反应过程转移2mol电子
向10mL0.1mol/LAgNO溶液中先滴
3 先产生白色沉淀,后产生 Ksp(AgI)Y>W
B.缩小c点对应容器的体积增大压强,v(正)Y>Z Y Z 1 2
D.向b点对应容器中再充入一定量NO,达到新平衡
D.R、Y、W只能组成一种三元化合物 2
12.氨催化还原法可用于消除某些污染气体。据文献报道,某种污染气体的消除反应历程如 时,NO 2 的转化率减小
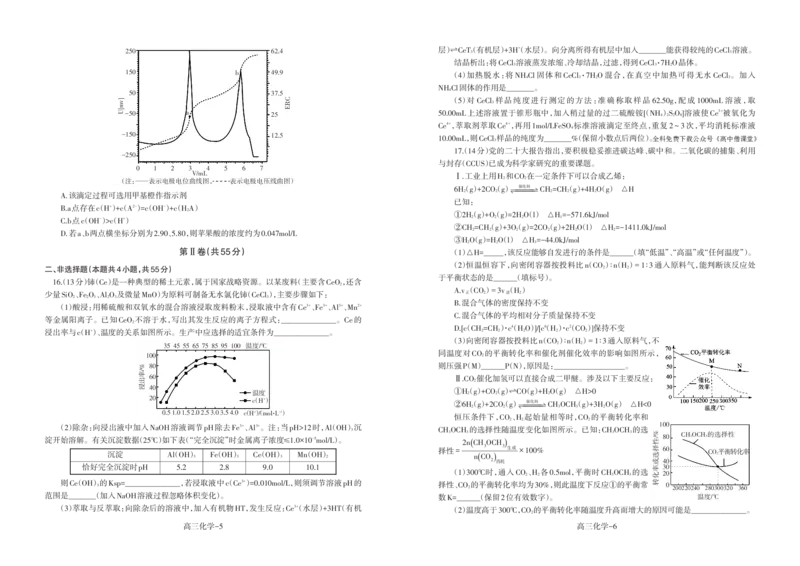
图所示,下列叙述正确的是( ) 15.电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方
NH 法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位(ERC)也产生了突跃,进而确
3
V5+-O-…NH+
4 V5+=O O
HO
定滴定终点的位置。苹果酸( ,用HA表示)是应用广泛的植物酸味剂,现利用
V5+-O-…NH 3 +…HO-V4+ H 2 O OH 2
V5+-OH NO O OH
电位滴定法向5.60mL苹果酸溶液滴加0.18mol/LNaOH溶液以测定苹果酸溶液的浓度,滴定曲
V5+-O-…NH 3 +-N=O…HO-V4+ O 2
线如图所示。下列说法正确的是( )
V5+-O-…NH+-N=O V4+-OH
3
N+HO
2 2
高三化学-3 高三化学-4250
150 b
50
-50 a
-150
-250
]vm[U
62.4
49.9
37.5
25
12.5
CRE
0 1 2 3 4 5 6 7
V/mL
(注:——表示电极电位曲线图, 表示电极电压线曲图)
A.该滴定过程可选用甲基橙作指示剂
B.a点存在c(H+)+c(A2-)=c(OH-)+c(HA)
2
C.b点c(OH-)>c(H+)
D.若a、b两点横坐标分别为2.90、5.80,则苹果酸的浓度约为0.047mol/L
第Ⅱ卷(共55分)
二、非选择题(本题共4小题,共55分)
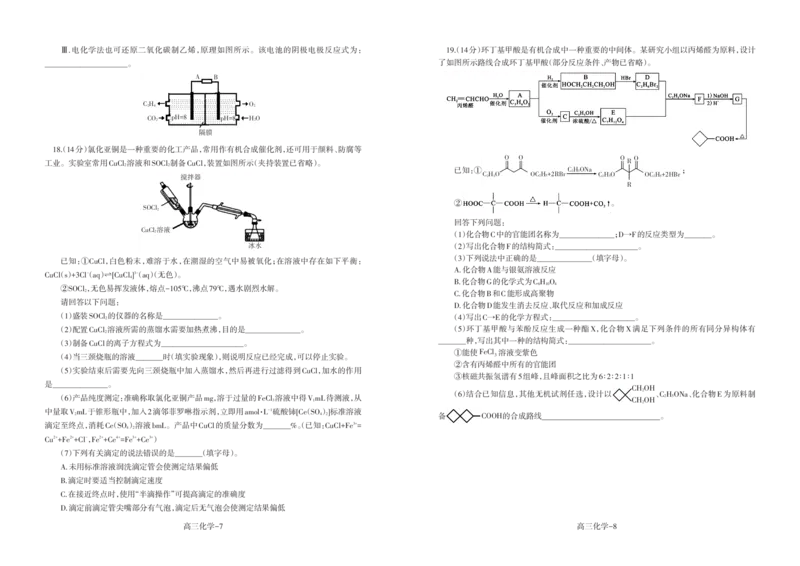
16(.13分)铈(Ce)是一种典型的稀土元素,属于国家战略资源。以某废料(主要含CeO,还含
2
少量SiO、FeO、AlO及微量MnO)为原料可制备无水氯化铈(CeCl),主要步骤如下:
2 2 3 2 3 3
(1)酸浸:用稀硫酸和双氧水的混合溶液浸取废料粉末,浸取液中含有Ce3+、Fe3+、Al3+、Mn2+
等金属阳离子。已知CeO不溶于水,写出其发生反应的离子方程式:______________。Ce的
2
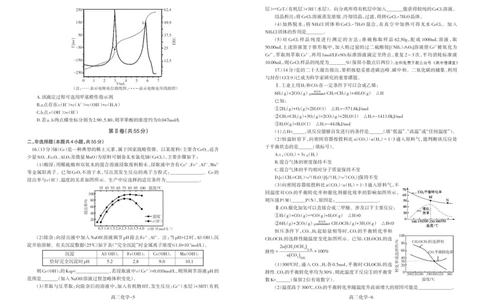
浸出率与c(H+)、温度的关系如图所示。生产中应选择的适宜条件为______________。
35455565758595100温度/℃
0.51.01.52.02.53.03.54.0c(H+)(/mol?L-1)
%/率出浸
层)�CeT(有机层)+3H(+水层)。向分离所得有机层中加入_______能获得较纯的CeCl溶液。 3 3
结晶析出:将CeCl溶液蒸发浓缩、冷却结晶,过滤,得到CeCl?7HO晶体。
3 3 2
(4)加热脱水:将NHCl固体和CeCl?7HO混合,在真空中加热可得无水CeCl。加入
4 3 2 3
NHCl固体的作用是_______。
4
(5)对CeCl样品纯度进行测定的方法:准确称取样品62.50g,配成1000mL溶液,取
3
50.00mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵([NH)SO]溶液使Ce3+被氧化为 4 22 8
Ce4+,萃取剂萃取Ce4+,再用1mol/LFeSO标准溶液滴定至终点,重复2~3次,平均消耗标准液
4
10.00mL,则CeCl样品的纯度为_______%(保留小数点后两位)。
3
17(.14分)党的二十大报告指出,要积极稳妥推进碳达峰、碳中和。二氧化碳的捕集、利用
与封存(CCUS)已成为科学家研究的重要课题。
Ⅰ.工业上用H和CO在一定条件下可以合成乙烯:
2 2
6H( 2 g)+2CO( 2 g) 催 化 剂 CH 2 =CH( 2 g)+4H 2 O(g) △H
已知:
①2H(g)+O(g)=2HO(l) △H=-571.6kJ/mol
2 2 2 1
②CH=CH(g)+3O(g)=2CO(g)+2HO(l) △H=-1411.0kJ/mol
2 2 2 2 2 2
③HO(g)=HO(l) △H=-44.0kJ/mol
2 2 3
(1)△H=_____,该反应能够自发进行的条件是______(填“低温”、“高温”或“任何温度”)。
(2)恒温恒容下,向密闭容器按投料比n(CO)∶n(H)=1∶3通入原料气,能判断该反应处
2 2
于平衡状态的是______(填标号)。
A.v(CO)=3v(H)
正 2 逆 2
B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变
D.[c(CH=CH)?c(4HO)]/[c(6H)?c(2CO)]保持不变
2 2 2 2 2
(3)向密闭容器按投料比n(CO)∶n(H)=1∶3通入原料气,不
2 2
同温度对CO的平衡转化率和催化剂催化效率的影响如图所示,
100 2
80 则压强P(M)______P(N),原因是:__________________。
60 Ⅱ.CO催化加氢可以直接合成二甲醚。涉及以下主要反应:
2
40
温度 ①H( 2 g)+CO( 2 g)�CO(g)+H 2 O(g) △H>0
20 c(H+)
②6H( 2 g)+2CO( 2 g) 催 化 剂 CH 3 OCH( 3 g)+3H 2 O(g) △H<0
恒压条件下,CO、H起始量相等时,CO的平衡转化率和
2 2 2
(2)除杂:向浸出液中加入NaOH溶液调节pH除去Fe3+、Al3+。注:当pH>12时,A(lOH) 3 沉 CH 3 OCH 3 的选择性随温度变化如图所示。已知:CH 3 OCH 3 的选 淀开始溶解。有关沉淀数据(25℃)如下表(“完全沉淀”时金属离子浓度≤1.0?10-5mol/L)。 2n(CHOCH)
择性=
3 3生成
?100%
沉淀 A(lOH)
3
Fe(OH)
3
Ce(OH)
3
Mn(OH)
2
n(CO)
2消耗
恰好完全沉淀时pH 5.2 2.8 9.0 10.1
(1)300℃时,通入CO、H各0.5mol,平衡时CHOCH的选 2 2 3 3
则Ce(OH) 3 的Ksp=______________,若浸取液中c(Ce3+)=0.010mol/L,则须调节溶液pH的 择性、CO 2 的平衡转化率均为30%,则此温度下反应①的平衡常
范围是_______(加入NaOH溶液过程忽略体积变化)。 数K=______(保留2位有效数字)。
(3)萃取与反萃取:向除杂后的溶液中,加入有机物HT,发生反应:Ce3(+ 水层)+3HT(有机 (2)温度高于300℃,CO的平衡转化率随温度升高而增大的原因可能是______________。
2
%/性择选或率化转
100
80 CH 3 OCH 3 的选择性
60 CO平衡转化率
2
40
30
20
0 200220240 280300320 360
温度/℃
高三化学-5 高三化学-6Ⅲ.电化学法也可还原二氧化碳制乙烯,原理如图所示。该电池的阴极电极反应式为: 19(.14分)环丁基甲酸是有机合成中一种重要的中间体。某研究小组以丙烯醛为原料,设计
_____________________。 了如图所示路线合成环丁基甲酸(部分反应条件、产物已省略)。
A B
CH O
2 4 2
CO pH=8 pH=8 HO
2 2
隔膜
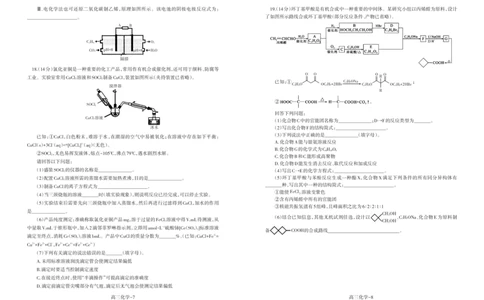
18(.14分)氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料、防腐等
O O O O
工业。实验室常用CuCl溶液和SOCl制备CuCl,装置如图所示(夹持装置已省略)。 R
2 2
已知:① CHONa ;
CHO OCH+2RBr2 5 CHO OCH+2HBr
搅拌器 2 5 2 5 2 5 2 5
R
② 。
SOCl
2
回答下列问题:
CuCl溶液
2 (1)化合物C中的官能团名称为______________;D→F的反应类型为_______。
冰水 (2)写出化合物F的结构简式:_____________________。
(3)下列说法中正确的是______________(填字母)。
已知:①CuCl,白色粉末,难溶于水,在潮湿的空气中易被氧化;在溶液中存在如下平衡:
A.化合物A能与银氨溶液反应
CuC(ls)+3Cl(-aq)�[CuCl]3(-aq)(无色)。
4
B.化合物G的化学式为CHO
6 10 4
②SOCl,无色易挥发液体,熔点-105℃,沸点79℃,遇水剧烈水解。
2 C.化合物B和C能形成高聚物
请回答以下问题:
D.化合物D能发生消去反应、取代反应和加成反应
(1)盛装SOCl的仪器的名称是______________。 (4)写出C→E的化学方程式:_____________________。
2
(2)配置CuCl溶液所需的蒸馏水需要加热煮沸,目的是______________。 (5)环丁基甲酸与苯酚反应生成一种酯X,化合物X满足下列条件的所有同分异构体有
2
_______种,写出其中一种的结构简式:_____________________。
(3)制备CuCl的离子方程式为_____________________。
①能使FeCl溶液变紫色
(4)当三颈烧瓶的溶液_______时(填实验现象),则说明反应已经完成,可以停止实验。 3
②含有丙烯醛中所有的官能团
(5)实验结束后需要先向三颈烧瓶中加入蒸馏水,然后再进行过滤得到CuCl,加水的作用
③核磁共振氢谱有5组峰,且峰面积之比为6∶2∶2∶1∶1
是______________。
CHOH
2
(6)结合已知信息,其他无机试剂任选,设计以 、CHONa、化合物E为原料制
(6)产品纯度测定:准确称取氯化亚铜产品mg,溶于过量的FeCl 3 溶液中得V 1 mL待测液,从 CH 2 OH 2 5
中量取VmL于锥形瓶中,加入2滴邻菲罗啉指示剂,立即用amol?L-1硫酸铈[Ce(SO)]标准溶液
2 42 备 COOH的合成路线 。
滴定至终点,消耗Ce(SO)溶液bmL。产品中CuCl的质量分数为_______%。(已知:CuCl+Fe3+=
42
Cu2++Fe2++Cl-,Fe2++Ce4+=Fe3++Ce3+)
(7)下列有关滴定的说法错误的是_______(填字母)。
A.未用标准溶液润洗滴定管会使测定结果偏低
B.滴定时要适当控制滴定速度
C.在接近终点时,使用“半滴操作”可提高滴定的准确度
D.滴定前滴定管尖嘴部分有气泡,滴定后无气泡会使测定结果偏低
高三化学-7 高三化学-8