文档内容
2017年贵州省安顺市中考化学试卷
一、选择题(共6小题,每小题3分,满分18分)
1.(3分)宣纸是中国文房四宝之一,其制作工艺被列入我国首批非物质文化遗产
名录.下列关于宣纸的传统制作工序中主要发生化学变化的是( )
A.挑选原料 B.加碱蒸煮
C.竹帘捞纸 D.剪裁纸张
2.(3分)下列符号中,既表示一个原子,又表示一种元素,还能表示一种物质的
是( )
A.He B.N C.H D.2O
2 2
3.(3分)在化学反应前后,物质所含元素化合价发生变化的反应属于氧化还原反
应.氧化还原反应与四种基本反应类型间的关系如图所示,下列举例中错误的是
( )
第1页(共23页)A.例1:C+O CO
2 2
B.例2:2H O 2H ↑+O ↑
2 2 2
C.例3:Mg(OH) +2HCl═MgCl +2H O
2 2 2
D.例4:Cu+2AgNO ═2Ag+Cu(NO )
3 3 2
4.(3分)安顺生产茶叶,茶叶中含锌、硒、茶氨酸(化学式为C H O N )等多种成
7 14 3 2
分,茶树适宜在pH为5﹣6的土壤中生长.下列说法不正确的是( )
A.茶氨酸由碳、氢、氧、氮四种元素组成
B.茶树不宜在碱性土壤中生长
C.一个茶氨酸分子中含有3个氧原子
D.茶叶中的锌、硒指单质,茶氨酸属于有机物
5.(3分)在溶液中能大量共存且呈无色的离子组是( )
A.Na+、Fe3+、NO ﹣、Cl﹣B.Ba2+、NH +、SO 2﹣、OH﹣
3 4 4
C.Ag+、H+、Cl﹣、NO ﹣ D.H+、Na+、NO ﹣、SO 2﹣
3 3 4
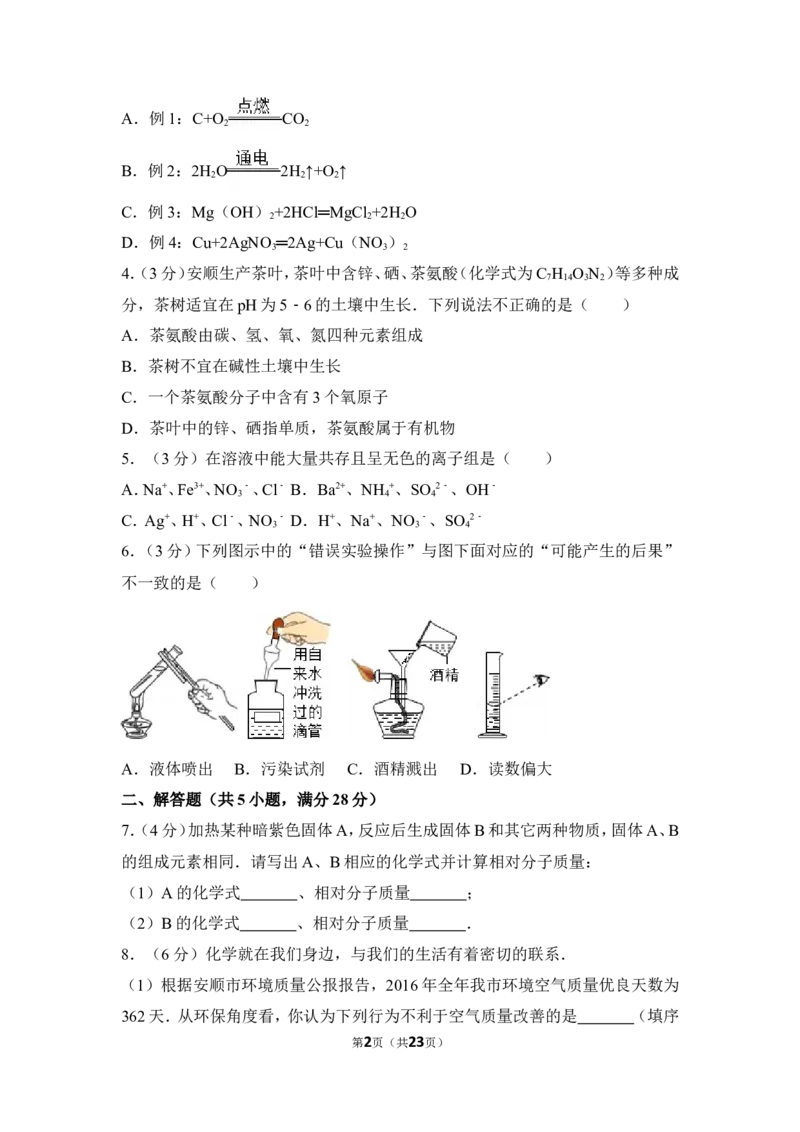
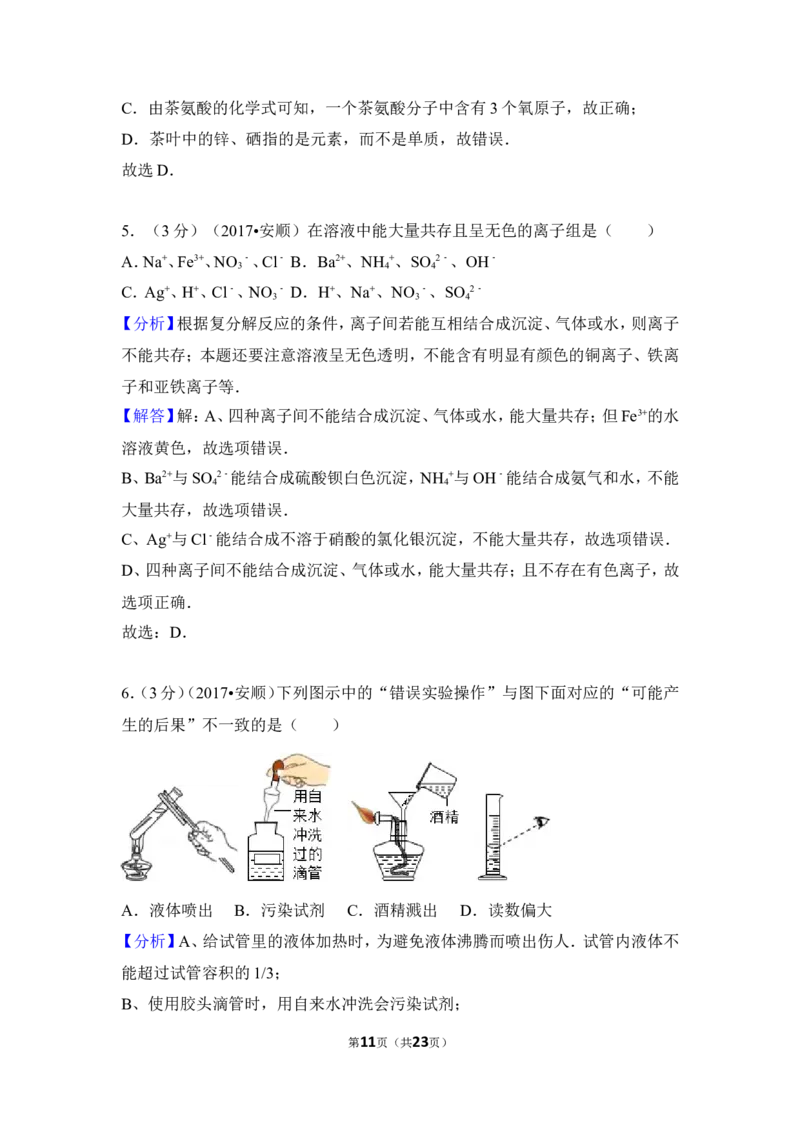
6.(3分)下列图示中的“错误实验操作”与图下面对应的“可能产生的后果”
不一致的是( )
A.液体喷出 B.污染试剂 C.酒精溅出 D.读数偏大
二、解答题(共5小题,满分28分)
7.(4分)加热某种暗紫色固体A,反应后生成固体B和其它两种物质,固体A、B
的组成元素相同.请写出A、B相应的化学式并计算相对分子质量:
(1)A的化学式 、相对分子质量 ;
(2)B的化学式 、相对分子质量 .
8.(6分)化学就在我们身边,与我们的生活有着密切的联系.
(1)根据安顺市环境质量公报报告,2016年全年我市环境空气质量优良天数为
362天.从环保角度看,你认为下列行为不利于空气质量改善的是 (填序
第2页(共23页)号).
①居民燃煤取暖 ②退耕还林 ③燃放烟花爆竹 ④焚烧秸秆
(2)某同学洗衣服,手抓洗衣粉放到水中时,有发热的感觉,说明洗衣粉溶于水
(填“放出”或“吸收”)热量.
(3)汽车车体钢铁涂上各种颜色的油漆除了美观外,最主要的目的是 .
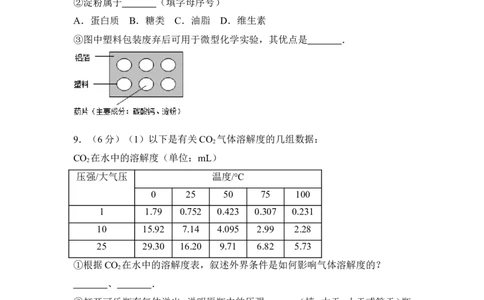
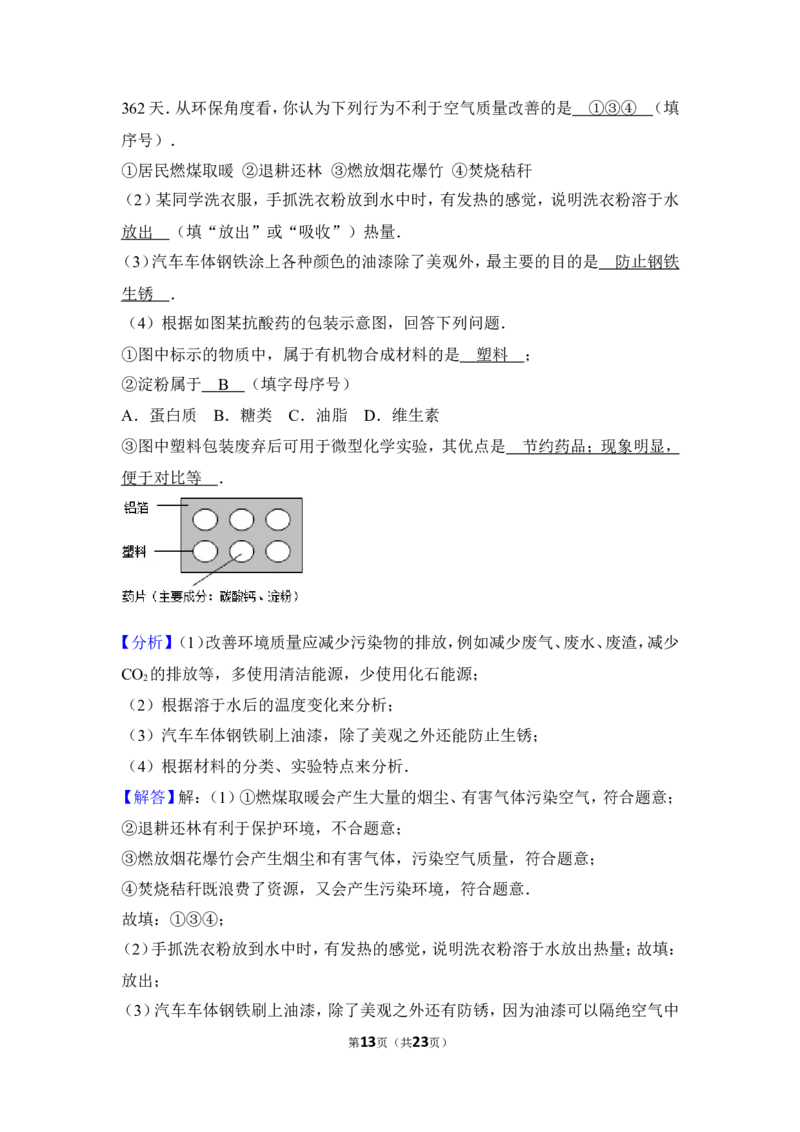
(4)根据如图某抗酸药的包装示意图,回答下列问题.
①图中标示的物质中,属于有机物合成材料的是 ;
②淀粉属于 (填字母序号)
A.蛋白质 B.糖类 C.油脂 D.维生素
③图中塑料包装废弃后可用于微型化学实验,其优点是 .
9.(6分)(1)以下是有关CO 气体溶解度的几组数据:
2
CO 在水中的溶解度(单位:mL)
2
压强/大气压 温度/℃
0 25 50 75 100
1 1.79 0.752 0.423 0.307 0.231
10 15.92 7.14 4.095 2.99 2.28
25 29.30 16.20 9.71 6.82 5.73
①根据CO 在水中的溶解度表,叙述外界条件是如何影响气体溶解度的?
2
、 .
②打开可乐瓶有气体溢出,说明原瓶中的压强 (填:大于、小于或等于)瓶
外大气压强.
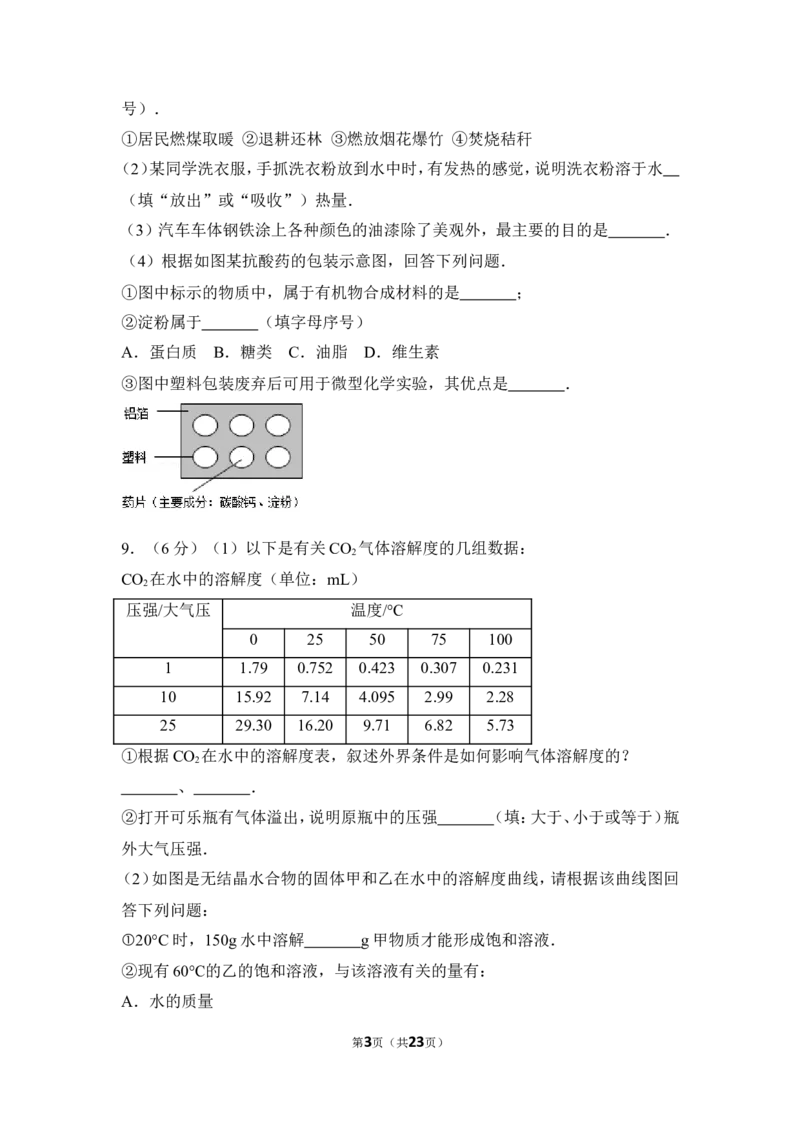
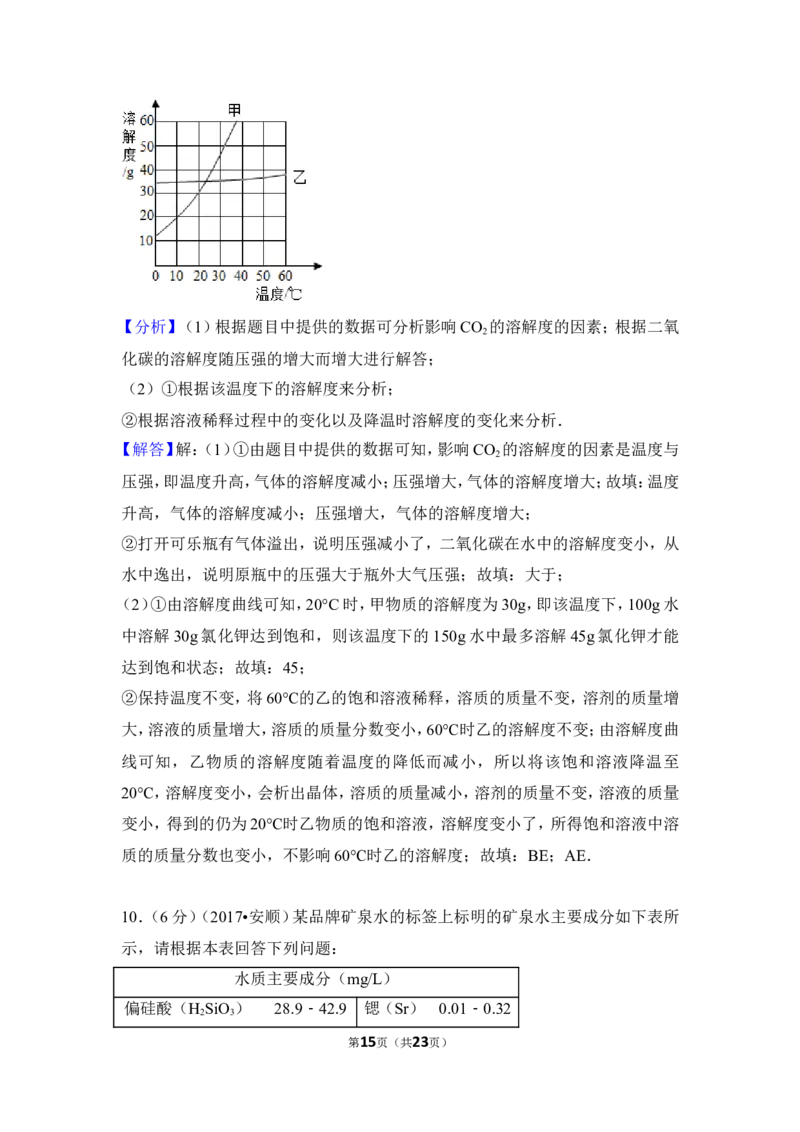
(2)如图是无结晶水合物的固体甲和乙在水中的溶解度曲线,请根据该曲线图回
答下列问题:
①20°C时,150g水中溶解 g甲物质才能形成饱和溶液.
②现有60℃的乙的饱和溶液,与该溶液有关的量有:
A.水的质量
第3页(共23页)B.溶液中溶质的质量
C.溶液的质量
D.乙的质量分数
E.60℃时乙的溶解度
保持温度不变,将该饱和溶液稀释,不变的量是 (填序号,下同);如果将
该饱和溶液降温至20℃,不变的量是 .
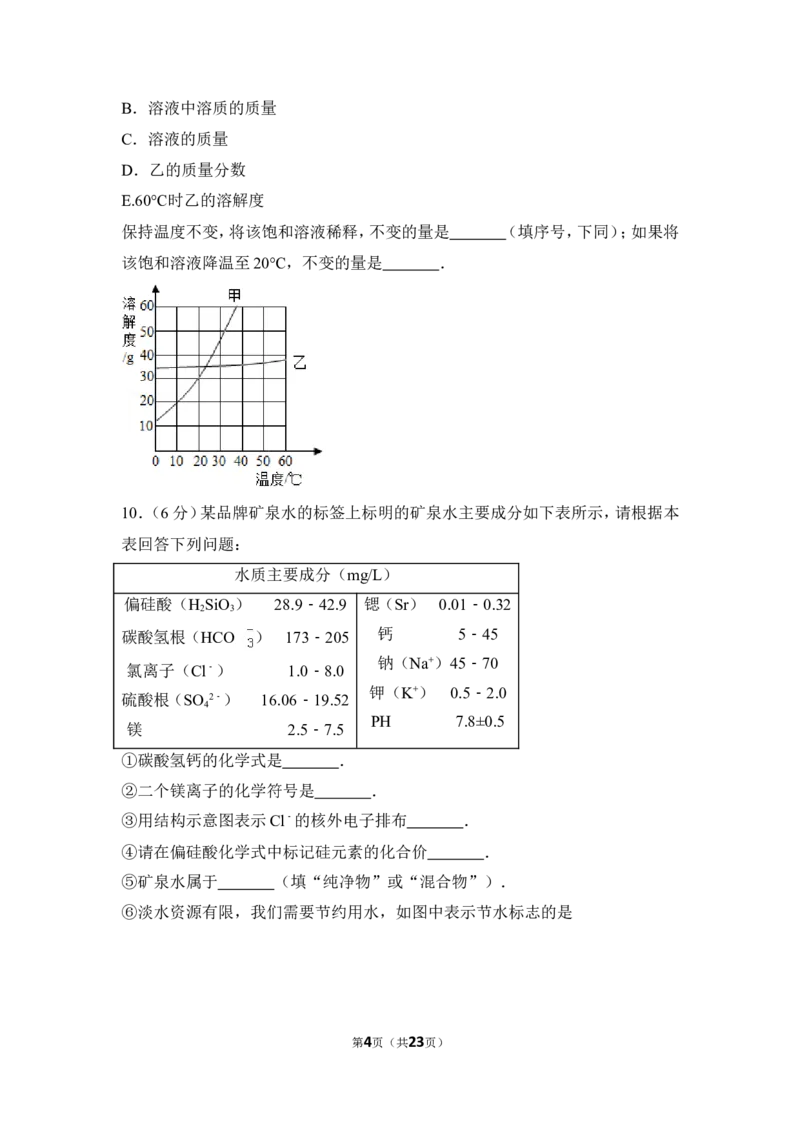
10.(6分)某品牌矿泉水的标签上标明的矿泉水主要成分如下表所示,请根据本
表回答下列问题:
水质主要成分(mg/L)
偏硅酸(H SiO ) 28.9﹣42.9 锶(Sr) 0.01﹣0.32
2 3
碳酸氢根(HCO ) 173﹣205 钙 5﹣45
钠(Na+)45﹣70
氯离子(Cl﹣) 1.0﹣8.0
钾(K+) 0.5﹣2.0
硫酸根(SO 2﹣) 16.06﹣19.52
4
PH 7.8±0.5
镁 2.5﹣7.5
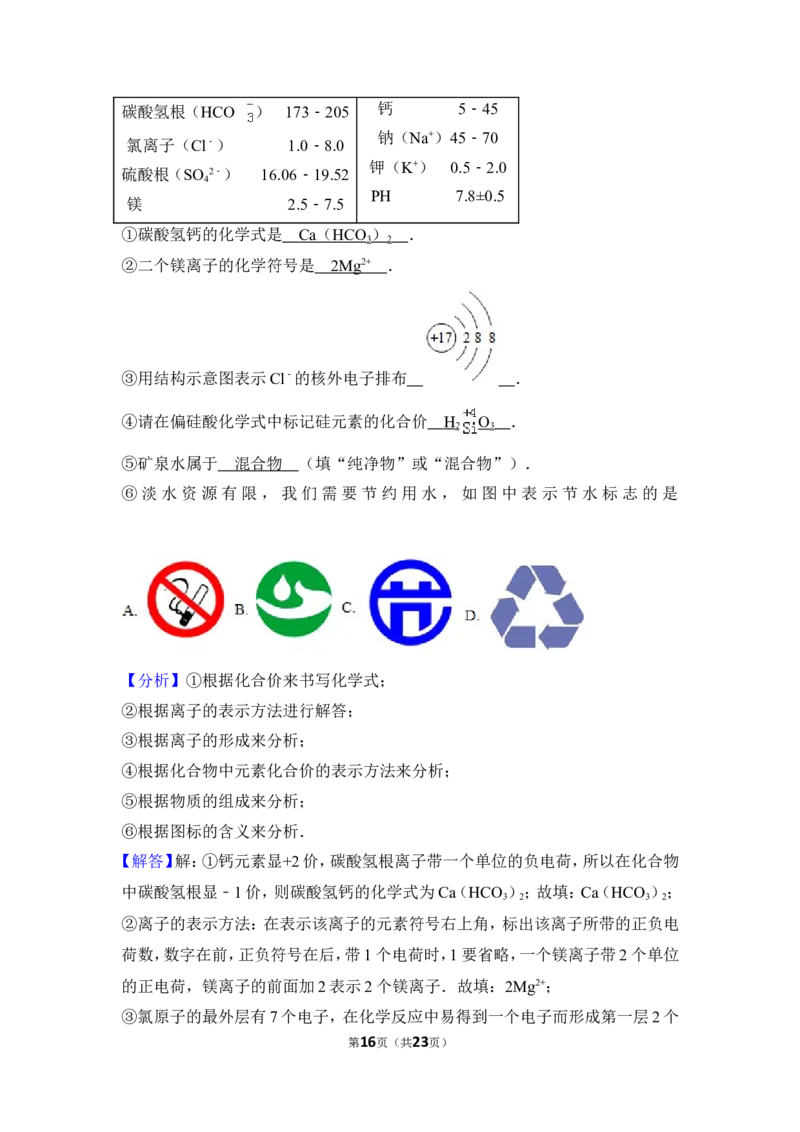
①碳酸氢钙的化学式是 .
②二个镁离子的化学符号是 .
③用结构示意图表示Cl﹣的核外电子排布 .
④请在偏硅酸化学式中标记硅元素的化合价 .
⑤矿泉水属于 (填“纯净物”或“混合物”).
⑥淡水资源有限,我们需要节约用水,如图中表示节水标志的是
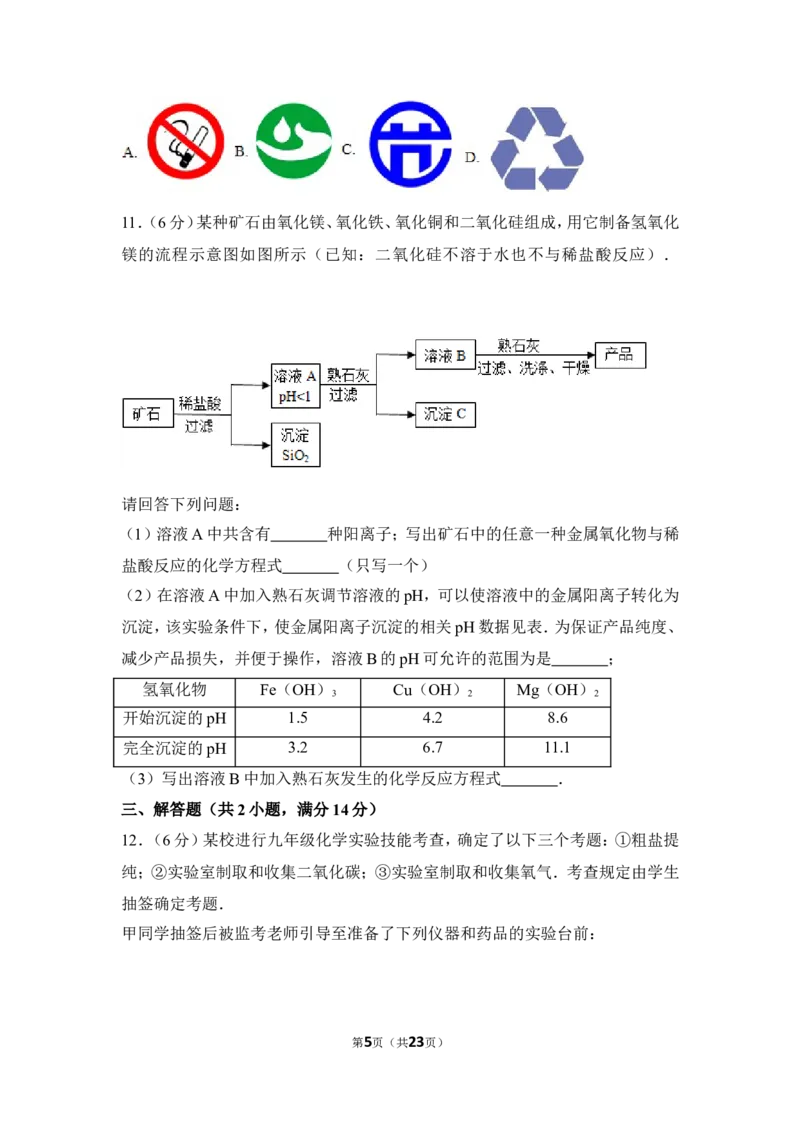
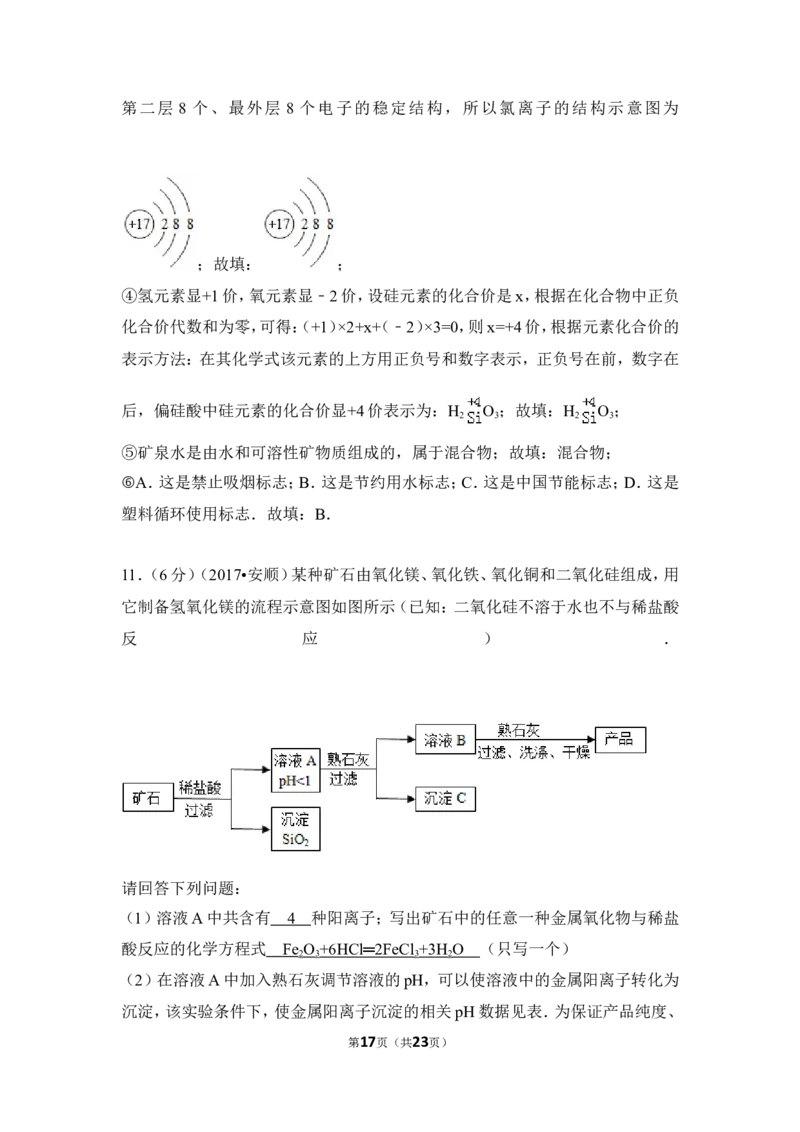
第4页(共23页)11.(6分)某种矿石由氧化镁、氧化铁、氧化铜和二氧化硅组成,用它制备氢氧化
镁的流程示意图如图所示(已知:二氧化硅不溶于水也不与稀盐酸反应).
请回答下列问题:
(1)溶液A中共含有 种阳离子;写出矿石中的任意一种金属氧化物与稀
盐酸反应的化学方程式 (只写一个)
(2)在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为
沉淀,该实验条件下,使金属阳离子沉淀的相关pH数据见表.为保证产品纯度、
减少产品损失,并便于操作,溶液B的pH可允许的范围为是 ;
氢氧化物 Fe(OH) Cu(OH) Mg(OH)
3 2 2
开始沉淀的pH 1.5 4.2 8.6
完全沉淀的pH 3.2 6.7 11.1
(3)写出溶液B中加入熟石灰发生的化学反应方程式 .
三、解答题(共2小题,满分14分)
12.(6分)某校进行九年级化学实验技能考查,确定了以下三个考题:①粗盐提
纯;②实验室制取和收集二氧化碳;③实验室制取和收集氧气.考查规定由学生
抽签确定考题.
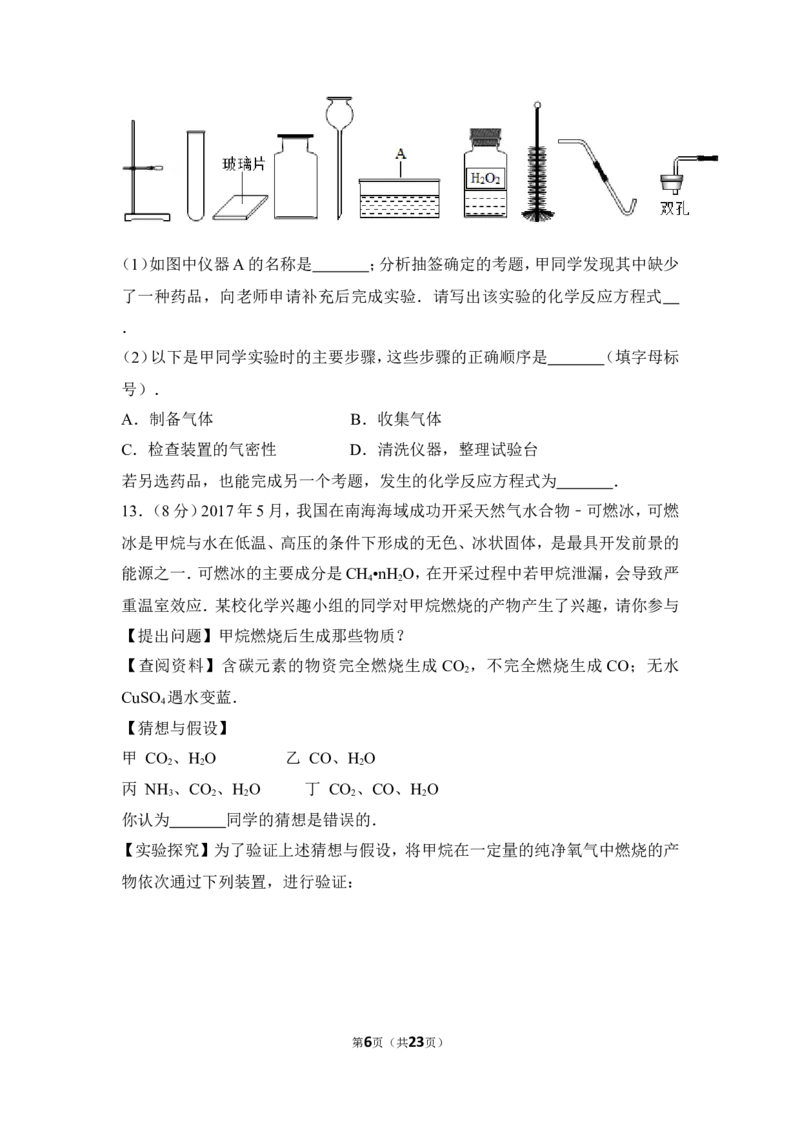
甲同学抽签后被监考老师引导至准备了下列仪器和药品的实验台前:
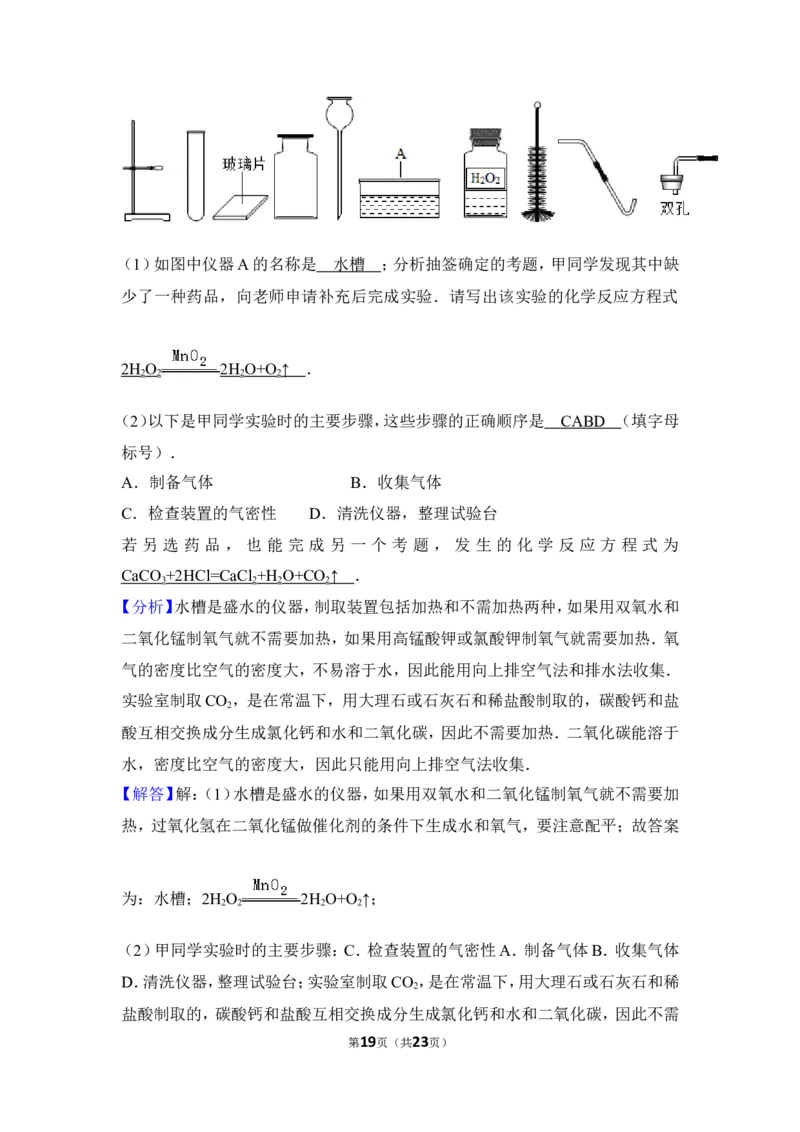
第5页(共23页)(1)如图中仪器A的名称是 ;分析抽签确定的考题,甲同学发现其中缺少
了一种药品,向老师申请补充后完成实验.请写出该实验的化学反应方程式
.
(2)以下是甲同学实验时的主要步骤,这些步骤的正确顺序是 (填字母标
号).
A.制备气体 B.收集气体
C.检查装置的气密性 D.清洗仪器,整理试验台
若另选药品,也能完成另一个考题,发生的化学反应方程式为 .
13.(8分)2017年5月,我国在南海海域成功开采天然气水合物﹣可燃冰,可燃
冰是甲烷与水在低温、高压的条件下形成的无色、冰状固体,是最具开发前景的
能源之一.可燃冰的主要成分是CH •nH O,在开采过程中若甲烷泄漏,会导致严
4 2
重温室效应.某校化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与
【提出问题】甲烷燃烧后生成那些物质?
【查阅资料】含碳元素的物资完全燃烧生成 CO ,不完全燃烧生成 CO;无水
2
CuSO 遇水变蓝.
4
【猜想与假设】
甲 CO 、H O 乙 CO、H O
2 2 2
丙 NH 、CO 、H O 丁 CO 、CO、H O
3 2 2 2 2
你认为 同学的猜想是错误的.
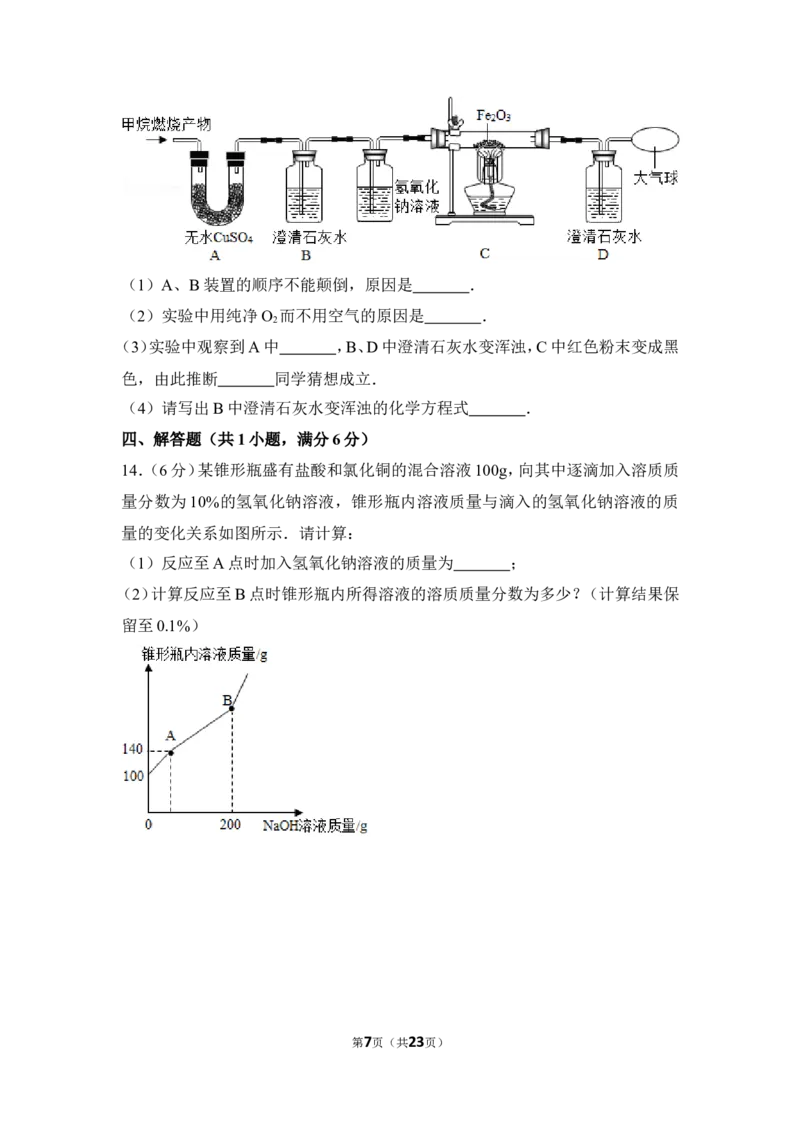
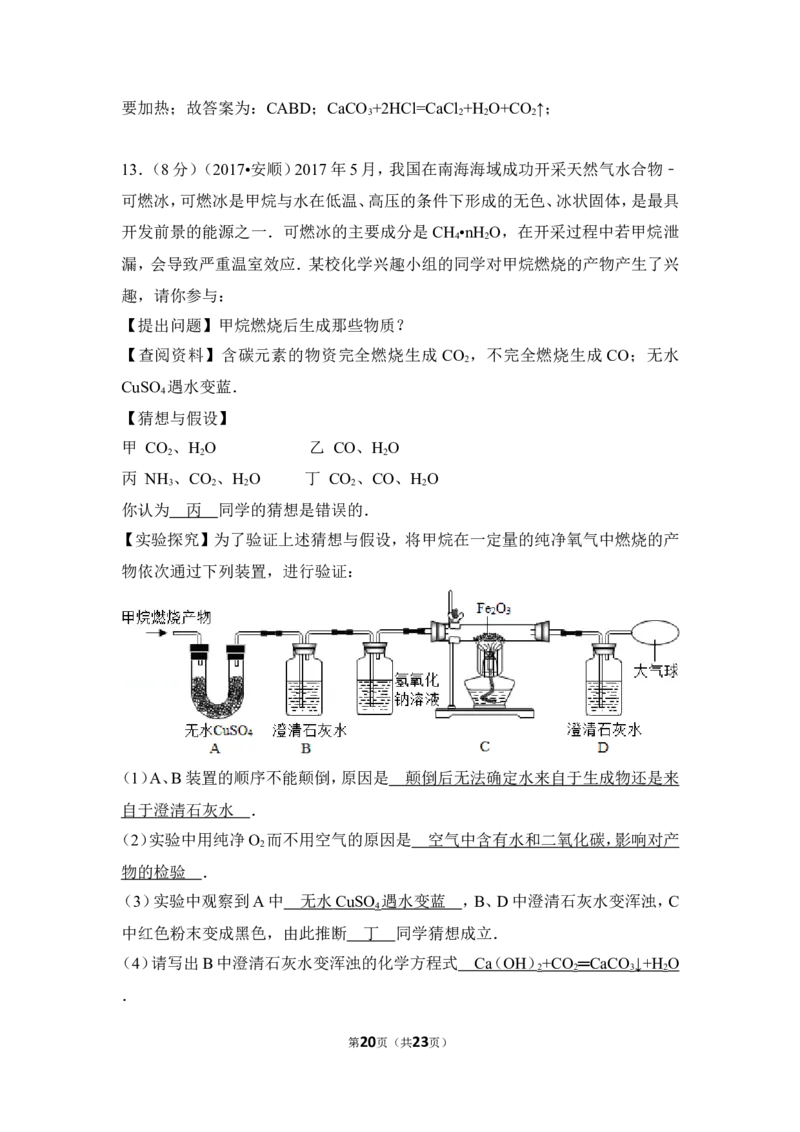
【实验探究】为了验证上述猜想与假设,将甲烷在一定量的纯净氧气中燃烧的产
物依次通过下列装置,进行验证:
第6页(共23页)(1)A、B装置的顺序不能颠倒,原因是 .
(2)实验中用纯净O 而不用空气的原因是 .
2
(3)实验中观察到A中 ,B、D中澄清石灰水变浑浊,C中红色粉末变成黑
色,由此推断 同学猜想成立.
(4)请写出B中澄清石灰水变浑浊的化学方程式 .
四、解答题(共1小题,满分6分)
14.(6分)某锥形瓶盛有盐酸和氯化铜的混合溶液100g,向其中逐滴加入溶质质
量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量与滴入的氢氧化钠溶液的质
量的变化关系如图所示.请计算:
(1)反应至A点时加入氢氧化钠溶液的质量为 ;
(2)计算反应至B点时锥形瓶内所得溶液的溶质质量分数为多少?(计算结果保
留至0.1%)
第7页(共23页)2017 年贵州省安顺市中考化学试卷
参考答案与试题解析
一、选择题(共6小题,每小题3分,满分18分)
1.(3分)(2017•安顺)宣纸是中国文房四宝之一,其制作工艺被列入我国首批非
物质文化遗产名录.下列关于宣纸的传统制作工序中主要发生化学变化的是(
)
A.挑选原料 B.加碱蒸煮
C.竹帘捞纸 D.剪裁纸张
【分析】有新物质生成的变化叫化学变化,没有新物质生成的变化叫物理变化.化
学变化的特征是:有新物质生成.判断物理变化和化学变化的依据是:是否有新
物质生成.
【解答】解:A、挑选原料中的砍伐木柴,没有新物质生成,属于物理变化,故选项
错误;
B、加碱蒸煮生成新物质,属于化学变化,故选项正确;
C、竹帘捞纸的过程中没有新物质生成,属于物理变化,故选项错误;
D、剪裁纸张的过程中没有新物质生成,属于物理变化,故选项错误;
第8页(共23页)故选B.
2.(3分)(2017•安顺)下列符号中,既表示一个原子,又表示一种元素,还能表示
一种物质的是( )
A.He B.N C.H D.2O
2 2
【分析】根据元素符号的含义进行分析解答,金属、固体非金属、稀有气体都是由
原子直接构成的,故它们的元素符号,既能表示一个原子,又能表示一种元素,还
能表示一种物质.
【解答】解:元素符号能表示一种元素,还能表示该元素的一个原子;化学式能表
示一种物质;当元素符号又是化学式时,就同时具备了上述三层意义.
A.He属于稀有气体元素,可表示氦元素,表示一个氦原子,还能表示氦气这一纯
净物,故选项符合题意.
B.该符号是氮气的化学式,不是元素符号,故选项不符合题意.
C.H属于非金属元素,可表示氢元素,表示一个氢原子,但不能表示一种物质,故
选项不符合题意.
D.该符号只能表示2个氧分子,故选项不符合题意.
故选A.
3.(3分)(2017•安顺)在化学反应前后,物质所含元素化合价发生变化的反应属
于氧化还原反应.氧化还原反应与四种基本反应类型间的关系如图所示,下列举
例中错误的是( )
A.例1:C+O CO
2 2
B.例2:2H O 2H ↑+O ↑
2 2 2
C.例3:Mg(OH) +2HCl═MgCl +2H O
2 2 2
第9页(共23页)D.例4:Cu+2AgNO ═2Ag+Cu(NO )
3 3 2
【分析】复分解反应中各种元素化合价都没有升降,所以复分解反应都不是氧化
还原反应.置换反应中元素化合价一定有升降,所以置换反应都是氧化还原反应
化合反应和分解反应中有的是氧化还原反应,有的不是氧化还原反应.
【解答】解:A、C+O CO 中,碳氧两种元素的化合价都发生了变化,是氧化
2 2
还原反应.
B、2H O 2H ↑+O ↑中,氢氧两种元素的化合价都发生了变化,是氧化还原
2 2 2
反应.
C、Mg(OH)+2HCl═MgCl +2H O为复分解反应,各种元素的化合价都没有发生
2 2 2
变化,不是氧化还原反应.
D、Cu+2AgNO ═2Ag+Cu(NO )中,银铜两种元素的化合价都发生了变化,是氧
3 3 2
化还原反应.
故选C.
4.(3分)(2017•安顺)安顺生产茶叶,茶叶中含锌、硒、茶氨酸(化学式为
C H O N )等多种成分,茶树适宜在pH为5﹣6的土壤中生长.下列说法不正确
7 14 3 2
的是( )
A.茶氨酸由碳、氢、氧、氮四种元素组成
B.茶树不宜在碱性土壤中生长
C.一个茶氨酸分子中含有3个氧原子
D.茶叶中的锌、硒指单质,茶氨酸属于有机物
【分析】A.根据化学式的意义来分析;
B.根据茶树适宜生长的pH来分析;
C.根据分子结构来分析;
D.根据物质的组成来分析.
【解答】解:A.由茶氨酸的化学式可知,茶氨酸是由碳、氢、氧、氮四种元素组成,
故正确;
B.茶树适宜在pH为5﹣6的土壤中生长,即适宜在偏酸性土壤中生长,不宜在碱
性土壤中生长,故正确;
第10页(共23页)C.由茶氨酸的化学式可知,一个茶氨酸分子中含有3个氧原子,故正确;
D.茶叶中的锌、硒指的是元素,而不是单质,故错误.
故选D.
5.(3分)(2017•安顺)在溶液中能大量共存且呈无色的离子组是( )
A.Na+、Fe3+、NO ﹣、Cl﹣B.Ba2+、NH +、SO 2﹣、OH﹣
3 4 4
C.Ag+、H+、Cl﹣、NO ﹣ D.H+、Na+、NO ﹣、SO 2﹣
3 3 4
【分析】根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子
不能共存;本题还要注意溶液呈无色透明,不能含有明显有颜色的铜离子、铁离
子和亚铁离子等.
【解答】解:A、四种离子间不能结合成沉淀、气体或水,能大量共存;但Fe3+的水
溶液黄色,故选项错误.
B、Ba2+与SO 2﹣能结合成硫酸钡白色沉淀,NH +与OH﹣能结合成氨气和水,不能
4 4
大量共存,故选项错误.
C、Ag+与Cl﹣能结合成不溶于硝酸的氯化银沉淀,不能大量共存,故选项错误.
D、四种离子间不能结合成沉淀、气体或水,能大量共存;且不存在有色离子,故
选项正确.
故选:D.
6.(3分)(2017•安顺)下列图示中的“错误实验操作”与图下面对应的“可能产
生的后果”不一致的是( )
A.液体喷出 B.污染试剂 C.酒精溅出 D.读数偏大
【分析】A、给试管里的液体加热时,为避免液体沸腾而喷出伤人.试管内液体不
能超过试管容积的1/3;
B、使用胶头滴管时,用自来水冲洗会污染试剂;
第11页(共23页)C、根据酒精灯使用的注意事项进行分析;
D、用量筒量液读数时,视线应与量筒内液体凹液面的最低处保持水平,视线偏高
(俯视),会导致读数偏大.
【解答】解:A、给试管里的液体加热时,试管内液体超过试管容积的1/3,会导致
液体沸腾喷出伤人,故A正确;
B、使用胶头滴管时,用自来水冲洗,会使滴管沾有自来水,自来水中含有一些可
溶性杂质,所以能污染试剂,故B正确;
C、使用酒精灯时,绝对禁止向燃着的酒精灯内添加酒精,防止发生火灾,故C错
误;
D、用量筒量液读数时,视线偏高(俯视)会导致读数偏大;故D正确;
故选C.
二、解答题(共5小题,满分28分)
7.(4分)(2017•安顺)加热某种暗紫色固体A,反应后生成固体B和其它两种物
质,固体A、B的组成元素相同.请写出A、B相应的化学式并计算相对分子质量:
(1)A的化学式 KMnO 、相对分子质量 15 8 ;
4
(2)B的化学式 K MnO 、相对分子质量 19 7 .
2 4
【分析】根据加热某种暗紫色固体A,反应后生成固体B和其它两种物质,固体
A、B的组成元素相同,所以A是高锰酸钾,高锰酸钾在加热的条件下生成锰酸钾、
二氧化锰和氧气,所以B是锰酸钾,然后将推出的物质进行验证即可.
【解答】解:加热某种暗紫色固体A,反应后生成固体B和其它两种物质,固体A、
B的组成元素相同,所以A是高锰酸钾,高锰酸钾在加热的条件下生成锰酸钾、
二氧化锰和氧气,所以B是锰酸钾,经过验证,推导正确,所以
(1)A是KMnO ,相对分子质量为:39+55+16×4=158;
4
(2)B是K MnO ,相对分子质量为:39×2+55+16×4=197.
2 4
故答案为:(1)KMnO ,39+55+16×4=158;
4
(2)K MnO ,39×2+55+16×4=197.
2 4
8.(6分)(2017•安顺)化学就在我们身边,与我们的生活有着密切的联系.
(1)根据安顺市环境质量公报报告,2016年全年我市环境空气质量优良天数为
第12页(共23页)362天.从环保角度看,你认为下列行为不利于空气质量改善的是 ①③④ (填
序号).
①居民燃煤取暖 ②退耕还林 ③燃放烟花爆竹 ④焚烧秸秆
(2)某同学洗衣服,手抓洗衣粉放到水中时,有发热的感觉,说明洗衣粉溶于水
放出 (填“放出”或“吸收”)热量.
(3)汽车车体钢铁涂上各种颜色的油漆除了美观外,最主要的目的是 防止钢铁
生锈 .
(4)根据如图某抗酸药的包装示意图,回答下列问题.
①图中标示的物质中,属于有机物合成材料的是 塑料 ;
②淀粉属于 B (填字母序号)
A.蛋白质 B.糖类 C.油脂 D.维生素
③图中塑料包装废弃后可用于微型化学实验,其优点是 节约药品;现象明显,
便于对比等 .
【分析】(1)改善环境质量应减少污染物的排放,例如减少废气、废水、废渣,减少
CO 的排放等,多使用清洁能源,少使用化石能源;
2
(2)根据溶于水后的温度变化来分析;
(3)汽车车体钢铁刷上油漆,除了美观之外还能防止生锈;
(4)根据材料的分类、实验特点来分析.
【解答】解:(1)①燃煤取暖会产生大量的烟尘、有害气体污染空气,符合题意;
②退耕还林有利于保护环境,不合题意;
③燃放烟花爆竹会产生烟尘和有害气体,污染空气质量,符合题意;
④焚烧秸秆既浪费了资源,又会产生污染环境,符合题意.
故填:①③④;
(2)手抓洗衣粉放到水中时,有发热的感觉,说明洗衣粉溶于水放出热量;故填:
放出;
(3)汽车车体钢铁刷上油漆,除了美观之外还有防锈,因为油漆可以隔绝空气中
第13页(共23页)的氧气和水,防止与铁反应而生锈;故填:防止钢铁生锈;
(4)①有机合成材料包括塑料、合成橡胶和合成纤维,故填:塑料;
②淀粉是一种糖类物质;故填:糖类;
③塑料包装废弃后可用于微型实验,其优点是节约药品;现象明显,便于对比等,
故答案为:节约药品;现象明显,便于对比等.
9.(6分)(2017•安顺)(1)以下是有关CO 气体溶解度的几组数据:
2
CO 在水中的溶解度(单位:mL)
2
压强/大气压 温度/℃
0 25 50 75 100
1 1.79 0.752 0.423 0.307 0.231
10 15.92 7.14 4.095 2.99 2.28
25 29.30 16.20 9.71 6.82 5.73
①根据CO 在水中的溶解度表,叙述外界条件是如何影响气体溶解度的?
2
温度升高,气体的溶解度减小 、 压强增大,气体的溶解度增大 .
②打开可乐瓶有气体溢出,说明原瓶中的压强 大于 (填:大于、小于或等于)
瓶外大气压强.
(2)如图是无结晶水合物的固体甲和乙在水中的溶解度曲线,请根据该曲线图回
答下列问题:
①20°C时,150g水中溶解 4 5 g甲物质才能形成饱和溶液.
②现有60℃的乙的饱和溶液,与该溶液有关的量有:
A.水的质量
B.溶液中溶质的质量
C.溶液的质量
D.乙的质量分数
E.60℃时乙的溶解度
保持温度不变,将该饱和溶液稀释,不变的量是 BE (填序号,下同);如果将
该饱和溶液降温至20℃,不变的量是 AE .
第14页(共23页)【分析】(1)根据题目中提供的数据可分析影响CO 的溶解度的因素;根据二氧
2
化碳的溶解度随压强的增大而增大进行解答;
(2)①根据该温度下的溶解度来分析;
②根据溶液稀释过程中的变化以及降温时溶解度的变化来分析.
【解答】解:(1)①由题目中提供的数据可知,影响CO 的溶解度的因素是温度与
2
压强,即温度升高,气体的溶解度减小;压强增大,气体的溶解度增大;故填:温度
升高,气体的溶解度减小;压强增大,气体的溶解度增大;
②打开可乐瓶有气体溢出,说明压强减小了,二氧化碳在水中的溶解度变小,从
水中逸出,说明原瓶中的压强大于瓶外大气压强;故填:大于;
(2)①由溶解度曲线可知,20°C时,甲物质的溶解度为30g,即该温度下,100g水
中溶解30g氯化钾达到饱和,则该温度下的150g水中最多溶解45g氯化钾才能
达到饱和状态;故填:45;
②保持温度不变,将60℃的乙的饱和溶液稀释,溶质的质量不变,溶剂的质量增
大,溶液的质量增大,溶质的质量分数变小,60℃时乙的溶解度不变;由溶解度曲
线可知,乙物质的溶解度随着温度的降低而减小,所以将该饱和溶液降温至
20℃,溶解度变小,会析出晶体,溶质的质量减小,溶剂的质量不变,溶液的质量
变小,得到的仍为20℃时乙物质的饱和溶液,溶解度变小了,所得饱和溶液中溶
质的质量分数也变小,不影响60℃时乙的溶解度;故填:BE;AE.
10.(6分)(2017•安顺)某品牌矿泉水的标签上标明的矿泉水主要成分如下表所
示,请根据本表回答下列问题:
水质主要成分(mg/L)
偏硅酸(H SiO ) 28.9﹣42.9 锶(Sr) 0.01﹣0.32
2 3
第15页(共23页)碳酸氢根(HCO ) 173﹣205 钙 5﹣45
钠(Na+)45﹣70
氯离子(Cl﹣) 1.0﹣8.0
钾(K+) 0.5﹣2.0
硫酸根(SO 2﹣) 16.06﹣19.52
4
PH 7.8±0.5
镁 2.5﹣7.5
①碳酸氢钙的化学式是 C a ( HCO ) .
3 2
②二个镁离子的化学符号是 2M g 2 + .
③用结构示意图表示Cl﹣的核外电子排布 .
④请在偏硅酸化学式中标记硅元素的化合价 H O .
2 3
⑤矿泉水属于 混合物 (填“纯净物”或“混合物”).
⑥淡水资源有限,我们需要节约用水,如图中表示节水标志的是
【分析】①根据化合价来书写化学式;
②根据离子的表示方法进行解答;
③根据离子的形成来分析;
④根据化合物中元素化合价的表示方法来分析;
⑤根据物质的组成来分析;
⑥根据图标的含义来分析.
【解答】解:①钙元素显+2价,碳酸氢根离子带一个单位的负电荷,所以在化合物
中碳酸氢根显﹣1价,则碳酸氢钙的化学式为Ca(HCO );故填:Ca(HCO );
3 2 3 2
②离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电
荷数,数字在前,正负符号在后,带1个电荷时,1要省略,一个镁离子带2个单位
的正电荷,镁离子的前面加2表示2个镁离子.故填:2Mg2+;
③氯原子的最外层有7个电子,在化学反应中易得到一个电子而形成第一层2个
第16页(共23页)第二层 8 个、最外层 8 个电子的稳定结构,所以氯离子的结构示意图为
;故填: ;
④氢元素显+1价,氧元素显﹣2价,设硅元素的化合价是x,根据在化合物中正负
化合价代数和为零,可得:(+1)×2+x+(﹣2)×3=0,则x=+4价,根据元素化合价的
表示方法:在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在
后,偏硅酸中硅元素的化合价显+4价表示为:H O ;故填:H O ;
2 3 2 3
⑤矿泉水是由水和可溶性矿物质组成的,属于混合物;故填:混合物;
⑥A.这是禁止吸烟标志;B.这是节约用水标志;C.这是中国节能标志;D.这是
塑料循环使用标志.故填:B.
11.(6分)(2017•安顺)某种矿石由氧化镁、氧化铁、氧化铜和二氧化硅组成,用
它制备氢氧化镁的流程示意图如图所示(已知:二氧化硅不溶于水也不与稀盐酸
反 应 ) .
请回答下列问题:
(1)溶液A中共含有 4 种阳离子;写出矿石中的任意一种金属氧化物与稀盐
酸反应的化学方程式 F e O +6HCl═2FeCl +3H O (只写一个)
2 3 3 2
(2)在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为
沉淀,该实验条件下,使金属阳离子沉淀的相关pH数据见表.为保证产品纯度、
第17页(共23页)减少产品损失,并便于操作,溶液B的pH可允许的范围为是 6. 7 ~ 8. 6 ;
氢氧化物 Fe(OH) Cu(OH) Mg(OH)
3 2 2
开始沉淀的pH 1.5 4.2 8.6
完全沉淀的pH 3.2 6.7 11.1
(3)写出溶液B中加入熟石灰发生的化学反应方程式 MgC l +Ca ( OH ) ═Mg
2 2
( OH ) ↓+CaCl .
2 2
【分析】(1)稀盐酸和氧化镁反应生成氯化镁和水,和氧化铁反应生成氯化铁和
水,和氧化铜反应生成氯化铜和水;
(2)根据表中提供的信息可以判断溶液B的pH可允许的范围;
(3)氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙.
【解答】解:(1)溶液A中含有镁离子、铁离子、铜离子和氢离子等4种阳离子;
稀盐酸和氧化镁反应生成氯化镁和水,和氧化铁反应生成氯化铁和水,和氧化铜
反应生成氯化铜和水,反应的化学方程式为:
MgO+2HCl═MgCl +H O,Fe O +6HCl═2FeCl +3H O,CuO+2HCl═CuCl +H O.
2 2 2 3 3 2 2 2
故填:Fe O +6HCl═2FeCl +3H O.
2 3 3 2
(2)由表中数据可知,溶液pH在6.7时,铁离子和铜离子完全形成沉淀,而镁离
子在pH=8.6时开始产生沉淀,因此溶液B的pH可允许的范围为是6.7~8.6.
故填:6.7~8.6.
(3)溶液B中加入熟石灰时,氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙,
发生的化学反应方程式为:MgCl +Ca(OH) ═Mg(OH) ↓+CaCl .
2 2 2 2
故填:MgCl +Ca(OH) ═Mg(OH) ↓+CaCl .
2 2 2 2
三、解答题(共2小题,满分14分)
12.(6分)(2017•安顺)某校进行九年级化学实验技能考查,确定了以下三个考题
①粗盐提纯;②实验室制取和收集二氧化碳;③实验室制取和收集氧气.考查规
定由学生抽签确定考题.
甲同学抽签后被监考老师引导至准备了下列仪器和药品的实验台前:
第18页(共23页)(1)如图中仪器A的名称是 水槽 ;分析抽签确定的考题,甲同学发现其中缺
少了一种药品,向老师申请补充后完成实验.请写出该实验的化学反应方程式
2H O 2H O+O ↑ .
2 2 2 2
(2)以下是甲同学实验时的主要步骤,这些步骤的正确顺序是 CABD (填字母
标号).
A.制备气体 B.收集气体
C.检查装置的气密性 D.清洗仪器,整理试验台
若 另 选 药 品 , 也 能 完 成 另 一 个 考 题 , 发 生 的 化 学 反 应 方 程 式 为
CaCO +2HCl=CaCl +H O+CO ↑ .
3 2 2 2
【分析】水槽是盛水的仪器,制取装置包括加热和不需加热两种,如果用双氧水和
二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧
气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.
实验室制取CO ,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐
2
酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于
水,密度比空气的密度大,因此只能用向上排空气法收集.
【解答】解:(1)水槽是盛水的仪器,如果用双氧水和二氧化锰制氧气就不需要加
热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;故答案
为:水槽;2H O 2H O+O ↑;
2 2 2 2
(2)甲同学实验时的主要步骤:C.检查装置的气密性A.制备气体B.收集气体
D.清洗仪器,整理试验台;实验室制取CO ,是在常温下,用大理石或石灰石和稀
2
盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需
第19页(共23页)要加热;故答案为:CABD;CaCO +2HCl=CaCl +H O+CO ↑;
3 2 2 2
13.(8分)(2017•安顺)2017年5月,我国在南海海域成功开采天然气水合物﹣
可燃冰,可燃冰是甲烷与水在低温、高压的条件下形成的无色、冰状固体,是最具
开发前景的能源之一.可燃冰的主要成分是CH •nH O,在开采过程中若甲烷泄
4 2
漏,会导致严重温室效应.某校化学兴趣小组的同学对甲烷燃烧的产物产生了兴
趣,请你参与:
【提出问题】甲烷燃烧后生成那些物质?
【查阅资料】含碳元素的物资完全燃烧生成 CO ,不完全燃烧生成 CO;无水
2
CuSO 遇水变蓝.
4
【猜想与假设】
甲 CO 、H O 乙 CO、H O
2 2 2
丙 NH 、CO 、H O 丁 CO 、CO、H O
3 2 2 2 2
你认为 丙 同学的猜想是错误的.
【实验探究】为了验证上述猜想与假设,将甲烷在一定量的纯净氧气中燃烧的产
物依次通过下列装置,进行验证:
(1)A、B装置的顺序不能颠倒,原因是 颠倒后无法确定水来自于生成物还是来
自于澄清石灰水 .
(2)实验中用纯净O 而不用空气的原因是 空气中含有水和二氧化碳,影响对产
2
物的检验 .
(3)实验中观察到A中 无水 CuSO 遇水变蓝 ,B、D中澄清石灰水变浑浊,C
4
中红色粉末变成黑色,由此推断 丁 同学猜想成立.
(4)请写出B中澄清石灰水变浑浊的化学方程式 C a( OH ) +CO ═CaCO ↓+H O
2 2 3 2
.
第20页(共23页)【分析】(1)A、B装置的顺序不能颠倒,这是因为如果颠倒后无法确定水来自于
生成物还是来自于澄清石灰水;
(2)空气中含有水和二氧化碳;
(3)白色固体硫酸铜和水反应生成蓝色固体五水硫酸铜;
高温条件下,氧化铁和一氧化碳反应生成铁和二氧化碳;
(4)二氧化碳能使澄清的石灰水变浑浊,是因为二氧化碳和石灰水中的氢氧化钙
反 应 生 成 了 碳 酸 钙 沉 淀 和 水 , 反 应 的 化 学 方 程 式 为 : Ca ( OH )
+CO ═CaCO ↓+H O.
2 2 3 2
【解答】解:(1)A、B装置的顺序不能颠倒,原因是颠倒后无法确定水来自于生成
物还是来自于澄清石灰水.
故填:颠倒后无法确定水来自于生成物还是来自于澄清石灰水.
(2)实验中用纯净O 而不用空气的原因是空气中含有水和二氧化碳,影响对产物
2
的检验.
故填:空气中含有水和二氧化碳,影响对产物的检验.
(3)实验中观察到A中无水CuSO 遇水变蓝,B、D中澄清石灰水变浑浊,C中红
4
色粉末变成黑色,由此推断丁同学猜想成立.
故填:无水CuSO 遇水变蓝;丁.
4
(4)二氧化碳能使澄清的石灰水变浑浊,是因为二氧化碳和石灰水中的氢氧化钙
反 应 生 成 了 碳 酸 钙 沉 淀 和 水 , 反 应 的 化 学 方 程 式 为 : Ca ( OH )
+CO ═CaCO ↓+H O.
2 2 3 2
故填:Ca(OH) +CO ═CaCO ↓+H O.
2 2 3 2
四、解答题(共1小题,满分6分)
14.(6分)(2017•安顺)某锥形瓶盛有盐酸和氯化铜的混合溶液100g,向其中逐
滴加入溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量与滴入的氢氧
化钠溶液的质量的变化关系如图所示.请计算:
(1)反应至A点时加入氢氧化钠溶液的质量为 40 g ;
(2)计算反应至B点时锥形瓶内所得溶液的溶质质量分数为多少?(计算结果保
留至0.1%)
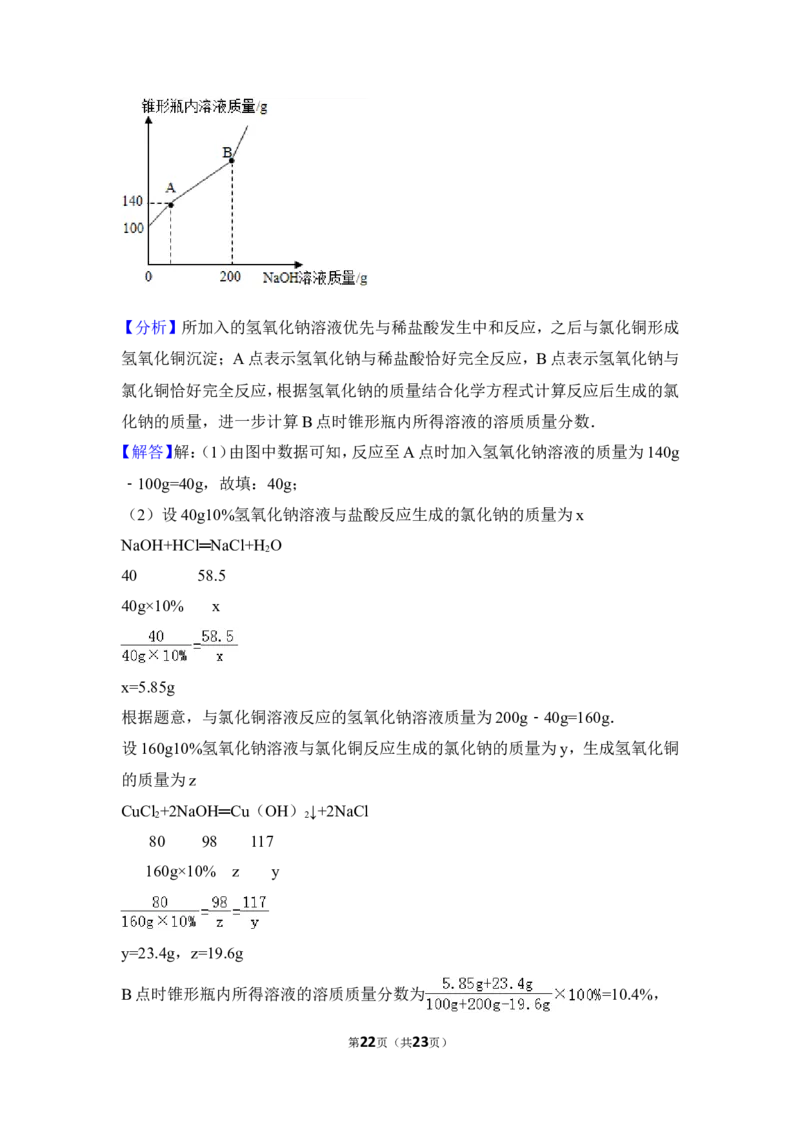
第21页(共23页)【分析】所加入的氢氧化钠溶液优先与稀盐酸发生中和反应,之后与氯化铜形成
氢氧化铜沉淀;A点表示氢氧化钠与稀盐酸恰好完全反应,B点表示氢氧化钠与
氯化铜恰好完全反应,根据氢氧化钠的质量结合化学方程式计算反应后生成的氯
化钠的质量,进一步计算B点时锥形瓶内所得溶液的溶质质量分数.
【解答】解:(1)由图中数据可知,反应至A点时加入氢氧化钠溶液的质量为140g
﹣100g=40g,故填:40g;
(2)设40g10%氢氧化钠溶液与盐酸反应生成的氯化钠的质量为x
NaOH+HCl═NaCl+H O
2
40 58.5
40g×10% x
x=5.85g
根据题意,与氯化铜溶液反应的氢氧化钠溶液质量为200g﹣40g=160g.
设160g10%氢氧化钠溶液与氯化铜反应生成的氯化钠的质量为y,生成氢氧化铜
的质量为z
CuCl +2NaOH═Cu(OH) ↓+2NaCl
2 2
80 98 117
160g×10% z y
y=23.4g,z=19.6g
B点时锥形瓶内所得溶液的溶质质量分数为 =10.4%,
第22页(共23页)答:所得溶液的溶质质量分数为10.4%.
第23页(共23页)