文档内容
2022-2023 学年度(上)六校高二期初考试
化学试题
考试时间:75分钟 满分:100分
可能用到的相对原子质量:Na:23 Cl:35.5 Fe:56 S:32 O:16 N:14 Zn:65
一、单选题(本大题共15小题,每题3分,共45分)
化学与人类的生产、生活息息相关,下列说法正确的是( )
A. 绿色化学的核心是对环境污染进行综合治理
1.
B. “温室效应”“酸雨”的形成都与氮氧化合物有关
C. 高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路”
D. 汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N 和
2
CO
2
下列反应对应的离子方程式能用“H++OH−=H O”表示的是 ( )
2
2.
A. 醋酸和氢氧化钠溶液反应 B. 氢氧化镁和盐酸反应
C.硫酸氢钠和氢氧化钾溶液的反应 D. 氢氧化钡和稀硫酸反应
若N 表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A
①标准状况下,2.24L四氯化碳含碳原子数为0.1N
3. A
aN
②标准状况下,aL氧气和氮气的混合气体含有的分子数约为 A
22.4
③1mol·L−1Mg(NO
)
溶液中含有NO−的数目为2N
3 2 3 A
④同温同压下,体积相同的氢气和氩气所含的原子数相等
⑤46gNO 和N O 混合气体中含有原子数为3N
2 2 4 A
⑥1L0.5mol·L−1Na SO 溶液中,含有的氧原子总数为2N
2 4 A
A. ②⑥ B. ②⑤ C. ②③ D. ②③⑥
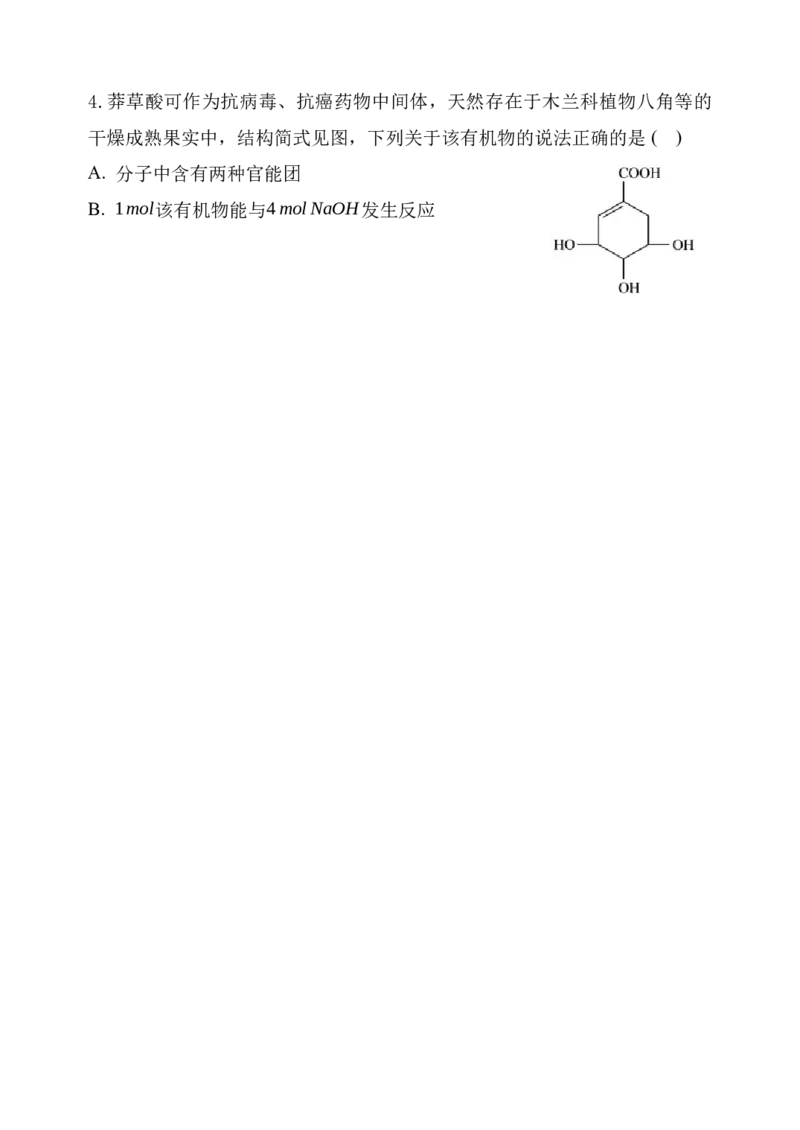
下载最新免费模拟卷,到公众号:一枚试卷君4.莽草酸可作为抗病毒、抗癌药物中间体,天然存在于木兰科植物八角等的
干燥成熟果实中,结构简式见图,下列关于该有机物的说法正确的是 ( )
A. 分子中含有两种官能团
B. 1mol该有机物能与4molNaOH发生反应C. 在水溶液中,羧基和羟基均能电离出H+
D. 该有机物能发生取代反应、加成反应、氧化反应和加聚反应
5.门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第4周期的三
种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类
硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当
准确。根据元素周期律,下列有关X性质的描述中错误的是( )
A. X单质不易与水反应 B. XO 可被碳或氢气还原为X
2
C. XCl 的沸点比SiCl 的高 D. X H 的稳定性比SiH 的高
4 4 4 4
6.下列实验操作或者结论正确的是( )
A. 配制一定物质的量浓度的溶液时,容量瓶必须洁净、干燥,使用前还要检
验是否漏水
B. 实验室配制100.0g,20%的氯化钠溶液,可取20.0g的NaCl于烧杯中,再
加入80.0mL的水,充分搅拌后即可
C. 实验室里需要480mL2.0mol·L−1的氢氧化钠溶液,配制溶液时先称量氢氧
化钠固体38.4g,然后再按照溶解、冷却、移液、定容、摇匀等步骤进行操作
D. 实验室配制500mL0.2mol·L−1的硫酸亚铁溶液,如果在称量时把砝码和硫
酸亚铁固体放反(其他操作都正确),则最终溶液浓度会偏大
7.下列关于△H的判断正确的是( )
S(s)+O (g)=SO (g)△H
2 2 1
S(g)+O (g)=SO (g)△H
2 2 2
OH− (aq)+H+ (aq)=H O(l)△H
2 3
OH− (aq)+CH COOH(aq)=CH COO− (aq)+H O(l)△H
3 3 2 4
A. △H <0,△H <0且△H <△H B. △H >△H
1 2 1 2 1 2
C. △H <0,△H >0 D. △H >△H
3 4 3 4
8.根据所给的实验装置,下列有关实验的相关叙述正确的是 ( )
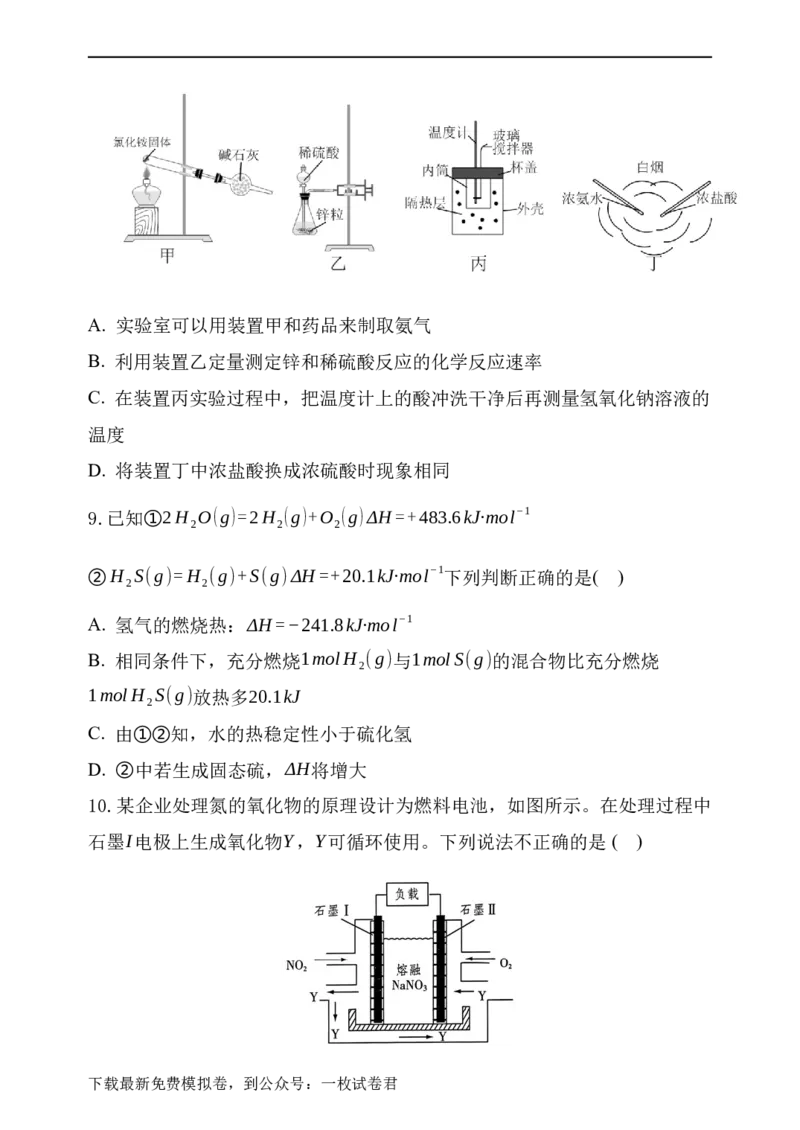
下载最新免费模拟卷,到公众号:一枚试卷君A. 实验室可以用装置甲和药品来制取氨气
B. 利用装置乙定量测定锌和稀硫酸反应的化学反应速率
C. 在装置丙实验过程中,把温度计上的酸冲洗干净后再测量氢氧化钠溶液的
温度
D. 将装置丁中浓盐酸换成浓硫酸时现象相同
9.已知①2H O(g)=2H (g)+O (g)ΔH=+483.6kJ·mol−1
2 2 2
②H S(g)=H (g)+S(g)ΔH=+20.1kJ·mol−1下列判断正确的是( )
2 2
A. 氢气的燃烧热:ΔH=−241.8kJ·mol−1
B. 相同条件下,充分燃烧1molH (g)与1molS(g)的混合物比充分燃烧
2
1molH S(g)放热多20.1kJ
2
C. 由①②知,水的热稳定性小于硫化氢
D. ②中若生成固态硫,ΔH将增大
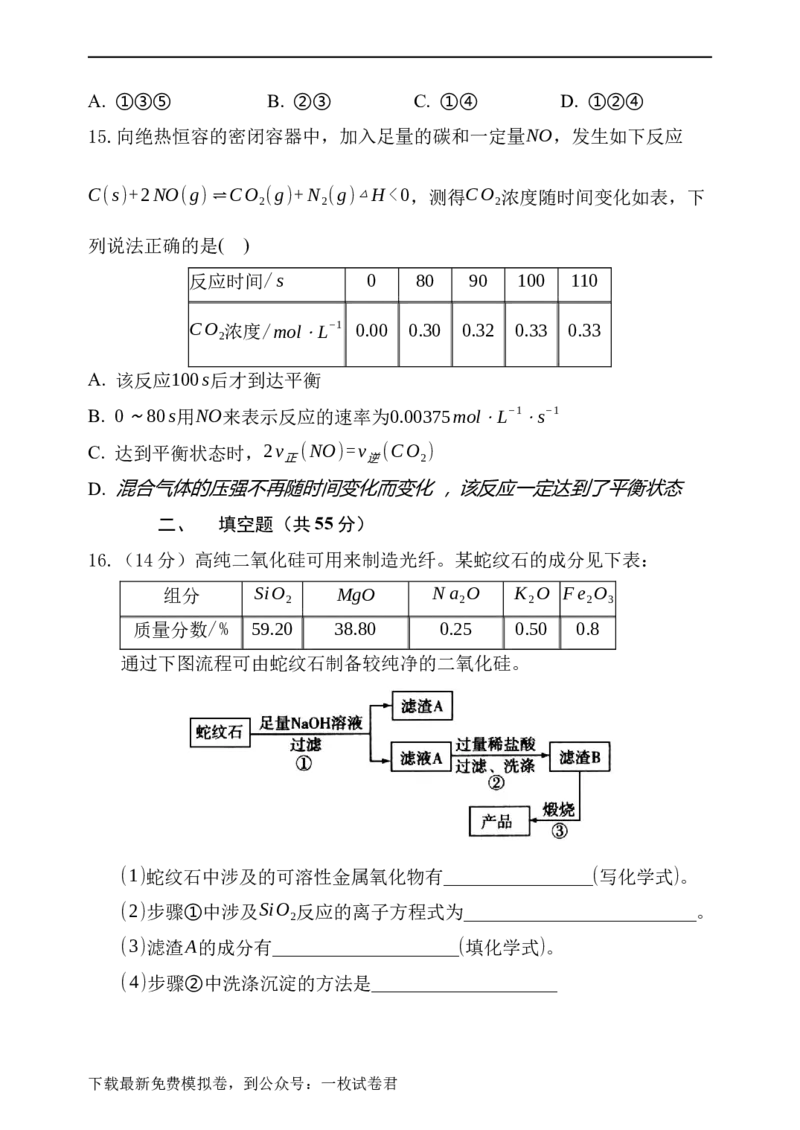
10.某企业处理氮的氧化物的原理设计为燃料电池,如图所示。在处理过程中
石墨I电极上生成氧化物Y,Y可循环使用。下列说法不正确的是 ( )
下载最新免费模拟卷,到公众号:一枚试卷君A. 该电池放电时电子流动的方向是石墨I电极→负载→石墨II电极→熔融
NaNO →石墨I电极
3
B. 石墨II附近发生的反应为O +4e−+2N O 4NO−
2 2 5 3
C. O 在石墨II附近发生还原反应,Y为N O
2 2 5
D. 相同条件下,放电过程中消耗的NO 和O 的体积比为4:1
2 2
11. N O和CO可在催化剂 (Pt O+ )表面转化为无害气体,其反应原理为:
2 2
N O(g)+CO(g) CO (g)+N (g),下列有关该反应说法正确的是 ( )
2 2 2
A. 催化剂能改变反应的ΔH
B. 通入过量CO,可使N O转化率达100%
2
C. 保持温度和容器体积不变,通入He增大压强,反应速率不变
D. 保持温度和压强不变,通入He反应速率不变
12.乳酸( )成为近年来研究热点之一。下列说法错误的是 ( )
A. 乳酸的分子式为C H O
3 6 3
B. 1mol乳酸分别与足量Na和NaHCO 反应产生的气体物质的量之比2:1
3
C. 乳酸既可以与乙醇又可以与乙酸发生酯化反应
D. 乳酸可与铁粉反应制备补铁剂
13.分子式C H O的同分异构体中,能与金属钠反应生成氢气,又能被氧化
5 12
为醛有 ( )
A. 3种 B. 4种 C. 7种 D. 8种
14.下列有关烷烃的叙述中,正确的是( )
①在烷烃分子中,所有的化学键都是单键
②烷烃中除甲烷外,很多都能使酸性KMnO 溶液的紫色褪去
4
下载最新免费模拟卷,到公众号:一枚试卷君③分子通式为C H 的烃不一定是烷烃
n 2n+2
④所有的烷烃在光照条件下都能与氯气发生取代反应
⑤光照条件下,乙烷通入溴水中,可使溴水褪色A. ①③⑤ B. ②③ C. ①④ D. ①②④
15.向绝热恒容的密闭容器中,加入足量的碳和一定量NO,发生如下反应
C(s)+2NO(g)⇌CO (g)+N (g)△H<0,测得CO 浓度随时间变化如表,下
2 2 2
列说法正确的是( )
反应时间/s 0 80 90 100 110
CO 浓度/mol⋅L−1 0.00 0.30 0.32 0.33 0.33
2
A. 该反应100s后才到达平衡
B. 0~80s用NO来表示反应的速率为0.00375mol⋅L−1 ⋅s−1
C. 达到平衡状态时,2v (NO)=v (CO )
正 逆 2
D. 混合气体的压强不再随时间变化而变化,该反应一定达到了平衡状态
二、 填空题(共55分)
16.(14分)高纯二氧化硅可用来制造光纤。某蛇纹石的成分见下表:
组分 SiO MgO Na O K O Fe O
2 2 2 2 3
质量分数/% 59.20 38.80 0.25 0.50 0.8
通过下图流程可由蛇纹石制备较纯净的二氧化硅。
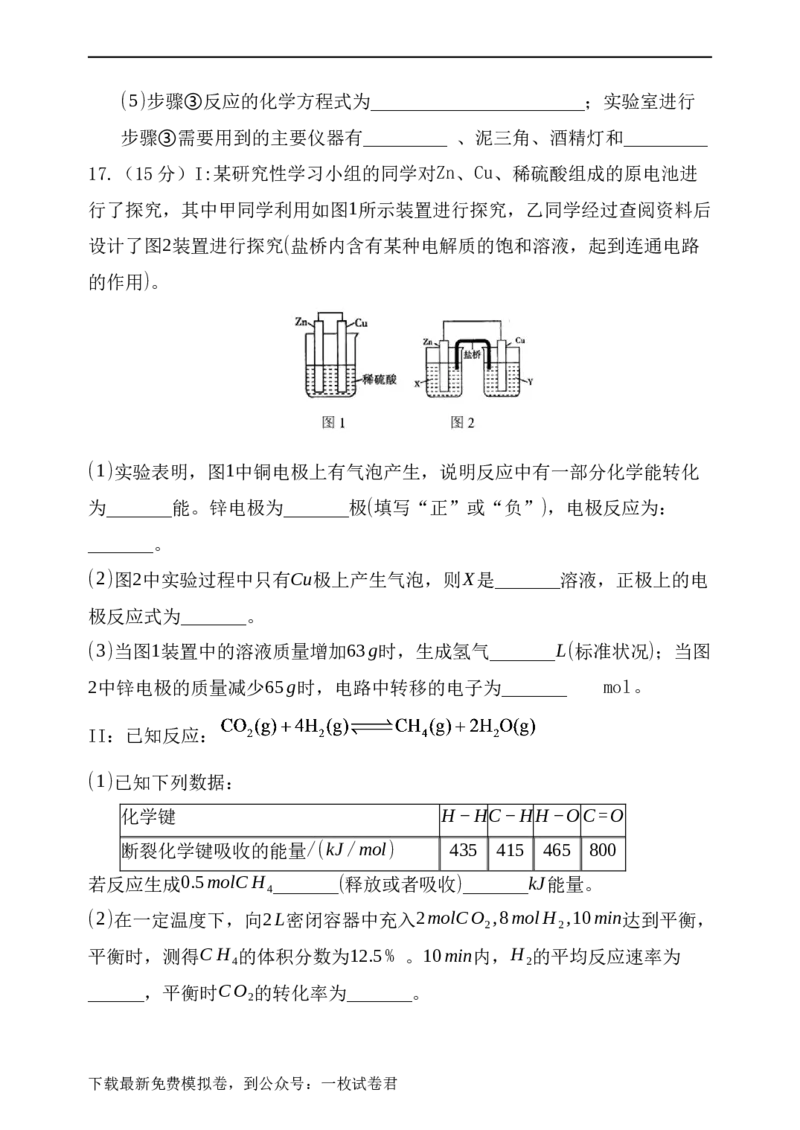
(1)蛇纹石中涉及的可溶性金属氧化物有________________(写化学式)。
(2)步骤①中涉及SiO 反应的离子方程式为_________________________。
2
(3)滤渣A的成分有____________________(填化学式)。
(4)步骤②中洗涤沉淀的方法是____________________
下载最新免费模拟卷,到公众号:一枚试卷君(5)步骤③反应的化学方程式为_______________________;实验室进行
步骤③需要用到的主要仪器有_________ 、泥三角、酒精灯和_________
17.(15分)I:某研究性学习小组的同学对Zn、Cu、稀硫酸组成的原电池进
行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后
设计了图2装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路
的作用)。
(1)实验表明,图1中铜电极上有气泡产生,说明反应中有一部分化学能转化
为_______能。锌电极为_______极(填写“正”或“负”),电极反应为:
_______。
(2)图2中实验过程中只有Cu极上产生气泡,则X是_______溶液,正极上的电
极反应式为_______。
(3)当图1装置中的溶液质量增加63g时,生成氢气_______L(标准状况);当图
2中锌电极的质量减少65g时,电路中转移的电子为_______ mol。
II:已知反应:
(1)已知下列数据:
化学键 H−HC−HH−OC=O
断裂化学键吸收的能量/(kJ/mol) 435 415 465 800
若反应生成0.5molCH _______(释放或者吸收)_______kJ能量。
4
(2)在一定温度下,向2L密闭容器中充入2molCO ,8molH ,10min达到平衡,
2 2
平衡时,测得CH 的体积分数为12.5% 。10min内,H 的平均反应速率为
4 2
______,平衡时CO 的转化率为_______。
2
下载最新免费模拟卷,到公众号:一枚试卷君18.(15分)某同学为了验证Fe3+是否能将H SO 氧化成SO2−,用
2 3 4
50mL0.1mol·L−1FeCl 溶液吸收制取SO 气体的尾气后,进行以下实验:
3 2
(1)取少量样品溶液于试管中,先滴入足量的稀盐酸,再滴入氯化钡溶液,如
果有白色沉淀生成,由此证据可证明Fe3+能够把H SO 氧化成_________。
2 3
(2)由此可写出该反应的化学方程式为_______________________,反应中的
氧化产物是________(写化学式)。
(3)该同学为了探究吸收液中其他成分(Fe3+、Fe2+、H SO )的可能组合进行
2 3
了以下探究:
①提出假设。假设1:溶液中存在Fe2+。假设2:溶液中存在Fe3+、Fe2+。
假设3:溶液中存在____________________。
②设计方案,进行实险,验证假设。请写出实验步骤以及预期现象和结论(可
不填满)。限选实验试剂和仪器:试管、滴管、0.1mol·L−1KMnO 溶液、
4
0.1mol·L−1KSCN溶液、品红稀溶液。
已知:H SO 可使品红溶液由红色变为无色。
2 3
实验步骤 预期现象和结论
步骤1:用试管取样品溶液
若出现红色,则假设2成
2∼3mL,并滴入
立,假设1、3不成立;若
________________
未出现红色,则假设2不
成立,假设1或3成立
步骤2:
___________________ ___________________
下载最新免费模拟卷,到公众号:一枚试卷君19.(11分)有机化合物A、B、C、D、E间的转化关系如下图。B气体在标
准状况下的密度为1.25g/L,E是一种有机高分子材料。❑
→
已知:2R−COOH+2CH =CH ❑
2 2¿2R−COO−CH=CH +2H O
2 2
¿
请回答:(1)写出C中官能团的名称___________。
(2)B在一定的条件下可转化为A,其反应类型为___________。
(3)由葡萄糖制A的化学方程式为___________。
(4)下列说法正确的是___________。
可用碳酸钠鉴别A、C、D
B、D、E都能与溴水反应使其褪色
a.
c.B分子中所有原子都在同一个平面上,通过加聚反应可制得塑料
b.
d.葡萄糖可由淀粉或纤维素水解制得,可用新制氢氧化铜检验葡萄糖的生成
(5)写出葡萄糖的结构简式________。
下载最新免费模拟卷,到公众号:一枚试卷君参考答案
一、选择题
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
D C B D D B B C B A C B B C D
二、填空题:
16(14分)每空2分(1)Na O、K O (各1分)
2 2
(2)SiO +2OH−=SiO2−+H O
2 3 2
(3)MgO和Fe O (各1分)
2 3
(4)向漏斗中注入蒸馏水至浸没沉淀,让水自然流下,重复操作2~3次
(5)H SiO SiO +H O 坩埚 三脚架 (或带铁圈的铁架台,答其它
2 3 2 2
仪器均没有分)
17.(15分)除标注外每空2分
I: (1) 电 (1分);负(1分); Zn−2e−=Zn2+ (1分)
(2) ZnSO 溶液 (其它的可溶性锌盐也可1分) ;2H++2e−=H ↑ (1
4 2
分)
(3) 22.4 ; 2
II(1) 释放 (1分) ;90
(2) 0.2mol/(L·min) 50% (1分)
18(15分)除标注外每空2分. (1)SO2− 或H SO
4 2 4
下载最新免费模拟卷,到公众号:一枚试卷君(2)2FeCl +SO +2H O 2FeCl +H SO +2HCl ;H SO
3 2 2 2 2 4 2 4
(3)①Fe2+、H SO (各1分,有错不得分)
2 3
步骤1:1∼2滴0.1❑mol.L−1KSCN 溶液
步骤2:另取2∼3mL样品溶液与试管中,滴入1∼2mL(或少量)品红
稀溶液预期现象和结论:若品红稀溶液红色褪去,则假设3成立;若品红稀溶液红
色不褪去,则假设3不成立,假设1或假设2成立(3分,不完整但正确得1
分)
19.(11分)除标注外每空2分
(1)羧基 (2)加成反应
(3)C H O 2CH CH OH+2CO
6 12 6 3 2 2
(4)acd (3分,对1个得1分,有错得0分) (5)CH (OH)(CHOH)
2
CHO(合理即可)
4
下载最新免费模拟卷,到公众号:一枚试卷君