文档内容
专题训练 配合物
1.将一定量的CuSO 固体溶于水后得到蓝色 溶液,再向溶液中逐滴滴
4
加氨水至过量,观察到先有蓝色沉淀Cu(OH) 生成,后蓝色沉淀溶解,得到深蓝色
2
的透明溶液。下列说法正确的是
A.1mol 含有16molσ键
B. 和 均为含有非极性键的分子晶体
C.与 形成配位键的能力: 强于
D.在 中, 中的H提供孤对电子
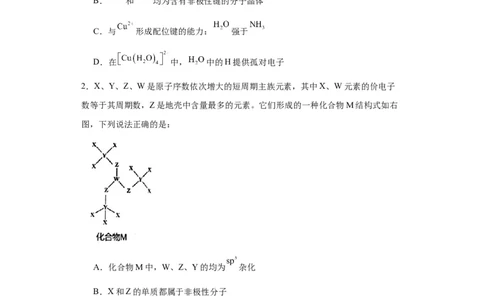
2.X、Y、Z、W是原子序数依次增大的短周期主族元素,其中X、W元素的价电子
数等于其周期数,Z是地壳中含量最多的元素。它们形成的一种化合物M结构式如右
图,下列说法正确的是:
A.化合物M中,W、Z、Y的均为 杂化
B.X和Z的单质都属于非极性分子
C.氢化物的沸点:YO>S
B.第一电离能:I(N)>I (O)>I (S)
1 1 1
C.标准大气压下沸点:HS>HO>NH
2 2 3
D.1mol[Fe(H O) ]2+含有σ键数目为12mol
2 6
6.DACP是我国科研工作者合成的一种新型起爆药,其结构简式如图所示。下列关于
该物质的说法正确的是
A.中心离子的配位数为4
B.1个DACP中含有25个σ键
2C. 和 中心原子的杂化方式相同
D.该配合物中 为中心离子, 、 为配体
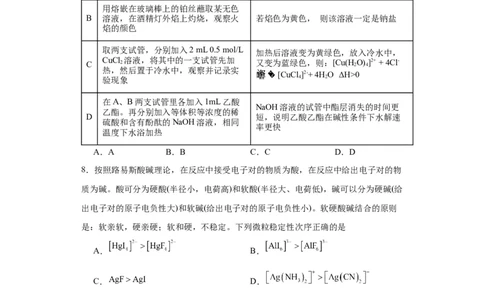
7.由下列实验内容得到的现象和结论错误的是
实验内容 现象及结论
向4mL 0.1mol/L CuSO 溶液中滴加
4
1mol/L的浓氨水至刚开始产生的沉淀 析出深蓝色的晶体,其成分是
A
溶解,再加入极性较小的溶剂,并用 [Cu(NH )]SO ·H O
3 4 4 2
玻璃棒摩擦试管壁
用熔嵌在玻璃棒上的铂丝蘸取某无色
B 溶液,在酒精灯外焰上灼烧,观察火 若焰色为黄色, 则该溶液一定是钠盐
焰的颜色
取两支试管,分别加入2 mL 0.5 mol/L
加热后溶液变为黄绿色,放入冷水中,
C CuCl 2 溶液,将其中的一支试管先加 又变为蓝绿色,则:[Cu(H 2 O) 4 ]2+ + 4Cl-
热,然后置于冷水中,观察并记录实
[CuCl ]2-+ 4H O ΔH>0
验现象 4 2
在A、B两支试管里各加入1mL乙酸
NaOH溶液的试管中酯层消失的时间更
乙酯。再分别加入等体积等浓度的稀
D 短,说明乙酸乙酯在碱性条件下水解速
硫酸和含有酚酞的NaOH溶液,相同
率更快
温度下水浴加热
A.A B.B C.C D.D
8.按照路易斯酸碱理论,在反应中接受电子对的物质为酸,在反应中给出电子对的物
质为碱。酸可分为硬酸(半径小,电荷高)和软酸(半径大、电荷低),碱可以分为硬碱(给
出电子对的原子电负性大)和软碱(给出电子对的原子电负性小)。软硬酸碱结合的原则
是:软亲软,硬亲硬;软和硬,不稳定。下列微粒稳定性次序正确的是
A. B.
C. D.
9.硼酸 主要用于玻璃生产,能改善玻璃的耐热、透明性能,提高机械强度。
硼酸是一元弱酸,其电离方程式如下,常温下,其电离常数 。下列说
法正确的是
资料收集整理【淘宝店铺:向阳百分百】 试卷第3页,共7页
学科网(北京)股份有限公司A. 电离常数的表达式为
B. 分子的空间构型为三角锥形
C. 的中心原子 的 模型为四面体形
D. 中普通共价键与配位键的个数之比为
10. 具有对称的空间结构, 中的 个 被 个 取代,
能得到 种不同结构的产物,则 的空间结构为
A.正四面体形 B.三角锥形 C.正方形 D.无法确定
11.下列说法正确的是
A.0.1 溶液中加入过量氨水:
B. 溶液中通入HCl:
C.实验室制备氢氧化铝可用可溶性铝盐加足量氨水:
D.化学式为 的配合物中,加入足量 溶液,所有
均被完全沉淀
12.Fe、Co、Ni均为第族元素,它们的化合物在生产、生活中有着广泛的应用,下列
说法错误的是
A.基态Fe原子中,电子填充的能量最高的能层符号为N
B.铁氰化钾 溶液是检验Fe2+常用的试剂。lmol 含
键的数目为12N (N 为阿伏伽德罗常数的值)
A A
C.从电子排布的角度分析,在空气中FeO稳定性大于Fe O
2 3
D.Co3+的一种配离子 中,Co3+对的配位数是6
13.由铁及其化合物可制得FeSO ·7H O、FeCl 、KFeO 等化工产品,它们在生产、生
4 2 3 2 4
4活中具有广泛应用。已知NO能被FeSO 溶液吸收生成配合物[Fe(NO)(H O) ]SO 。高
4 2 5 4
炉炼铁的反应为 Fe O(s)+3CO(g)=2Fe(s)+3CO(g) ΔH=-23.5 kJ· mol-1。下列有关说
2 3 2
法不正确的是
A.如图所示γFe的晶胞中,铁原子的配位数为12
B.配离子为[Fe(NO)(H O) ]2+,配位数为6
2 5
C.基态铁原子的核外电子排布式为1s22s22p63s23p63d74s1
D.该配合物中阴离子空间结构为正四面体形
14.下列关于超分子和配合物的叙述不正确的是
A.利用超分子的分子识别特征,可以分离 和
B.1mol 分子中含5 个配位键
C. 提供空轨道, 中氧原子提供孤对电子,从而形成配位键
D.配合物在半导体等尖端技术、医学科学、催化反应和材料化学等领域都有广泛
应用
15.近年来,光催化剂的研究是材料领域的热点。一种Ru配合物(如图所示)复合光催
化剂可将 转化为HCOOH。下列说法错误的是
A.Ru配合物中第二周期元素的电负性:O>N>C
B.吡啶( ,原子在同一平面)中C、N原子的杂化方式分别为 、
C.该配合物中Ru的配位数是6
资料收集整理【淘宝店铺:向阳百分百】 试卷第5页,共7页
学科网(北京)股份有限公司D. 中P的价层电子对数为4,空间结构为正四面体形
16.有研究称金粉溶于过氧化氢 浓盐酸也可以安全环保地制备氯金酸 ,
其化学方程式为 ,下列有关说法错误的
是
A. 有强氧化性,其中 与4个氯离子形成4个σ键
B.该反应中, 的作用是与 配合,使其更易被氧化
C.当反应中溶解 时,有 过氧化氢发生还原反应
17.利用如图装置进行 的制备及性质探究实验。下列说法不正确的是
A.使用A装置制备 时,分液漏斗中盛放浓氨水
B.装置B中盛放湿润红色石蕊试纸,打开 ,关闭 ,可证明 为碱性气体
C.利用C装置模拟候氏制碱法时,可将a和c连接
D.将a和d连接验证 与 的配位能力强于
18.乙二胺四乙酸又叫EDTA,是一种良好的配合剂,常用于测定金属离子的含量。
已知:EDTA的结构如图。下列叙述正确的是
A.EDTA中氮原子杂化方式为sp2
B.EDTA与金属离子形成配合物时,碳原子提供孤电子对
C.EDTA分子中既含有σ键又含有π键
D.EDTA是共价化合物,属于共价晶体
619. 是重要的化工原料,可用于某些配合物的制备,如 溶于氨水形成
。液氨可以微弱的电离产生 和 , 中的一个H原子若被
取代可形成 (联氨),若被 取代可形成 (羟胺)。 经过转化
可形成 、 、 、 (无色) 等。 与 反应有气体生成,同时
放出大量热。下列说法正确的是
A.第一电离能: B. 的键角比 大
C. 难溶于水 D. 中 键的数目为
20.许多配合物都是用 作配位体的,如 溶于氨水可以形成 。
下列有关 的说法正确的是
A. 中 键的数目为
B. 中 的键角小于 中的键角
C.由于 是配合物,故向其中滴加 溶液不会产生沉淀
D. 中任意两个 被两个Cl取代,只有一种产物,则
的空间结构为正四面体
资料收集整理【淘宝店铺:向阳百分百】 试卷第7页,共7页
学科网(北京)股份有限公司